布氏菌病活疫苗的生产现状与质量分析
王 楠,程君生,丁家波,蒋玉文,毛开荣
(中国兽医药品监察所,北京 100081)
布氏菌病(简称布病)是由布氏菌(Brucella)引起的一种人畜共患传染病。近年来,我国布病疫情形势严峻,对人体健康和畜牧业的发展造成了严重的危害[1-3]。目前,我国主要采取以预防为主的防疫措施,所以,布病疫苗产品质量优劣直接关系到全国布病疫情的有效控制。农业部高度重视布病类疫苗产品质量,每年安排并组织抽检计划,中国兽医药品监察所负责对该类产品实施监督检验。本文对布氏菌病活疫苗连续三年的生产现状和监督检验结果进行了统计分析,以了解目前我国广泛使用的布氏菌病活疫苗的质量状况。
1 布氏菌病活疫苗生产现状
目前,国内批准生产的布氏菌病活疫苗品种主要包括S2株、M5株和A19株。截至2012年7月,取得批准文号的企业共有14家,其中取得S2株疫苗批准文号的企业有13家,目前生产的企业有4家;取得M5株疫苗批准文号的企业有4家,目前生产的企业有2家;取得A19株疫苗批准文号的企业有6家,目前生产的企业有2家。
近三年,布病活疫苗总产量逐年增加,累计达到6.7亿头份。其中S2株疫苗的产量占总产量的94%,其产量增长也最快,2011年比2009年产量增加230%。结果见表1。
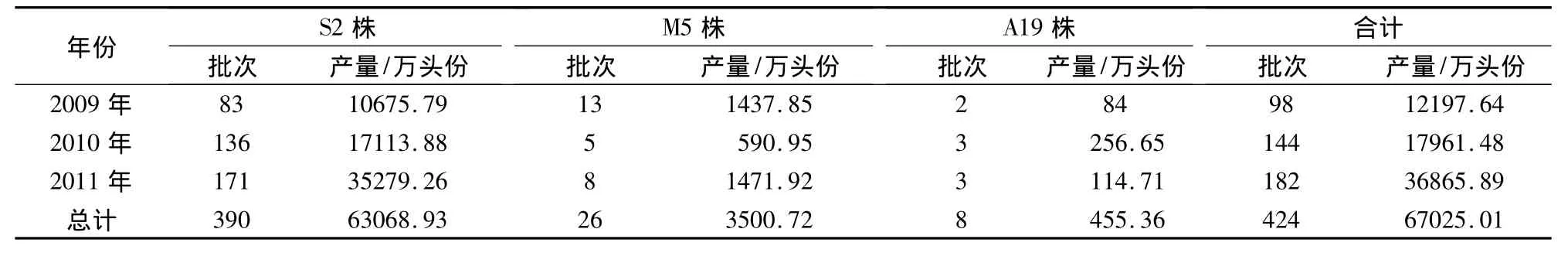
表1 2009-2011年布氏菌病活疫苗产量统计
2 布氏菌病活疫苗质量状况
布氏菌病活疫苗质量标准依据《中国兽药典》三部,其检验项目包括:性状、纯粹检验、变异检验、活菌计数、安全检验、剩余水分测定和真空度测定。活菌计数的结果是评价疫苗有效性的指标之一,所以布氏菌病活疫苗的以会检形式开展的监督检验通常选取该项检验作为主要的检验项。从2010年到2012年,监督会检的S2株疫苗活菌计数结果表明该项检验的合格率逐年上升,2012年已经达到了100%(表2)。
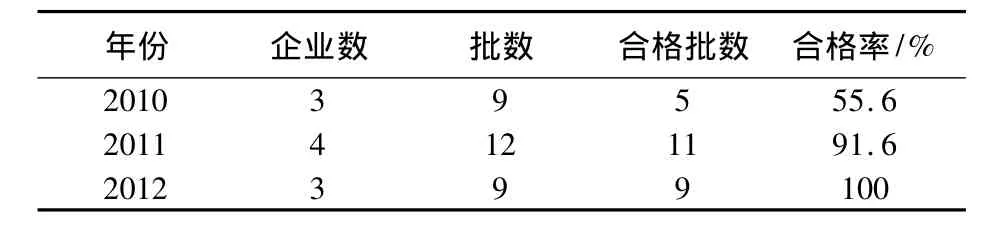
表2 2010-2012年布氏菌病活疫苗(S2株)活菌计数结果
为了能更全面的评价布氏菌病活疫苗质量,2012年的监督检验除了进行全项监督检验以外,还对疫苗菌株的纯净性、遗传稳定性和种属特异性进行了检定。各项检验结果表明,抽检的9批S2株疫苗和3批A19株疫苗的各项检验结果都符合规定,两种疫苗菌株的纯净性、遗传稳定性和种属特异性也都符合菌种的特性。但是,抽检的1批M5株疫苗的活菌计数结果不符合规定,而且该菌株的毒力检定结果也显示,该批次M5株毒力高达每克脾脏含菌量70万个,明显高于对生产用菌株每克脾脏含菌量应不超过20万个的标准规定[4](图1)。
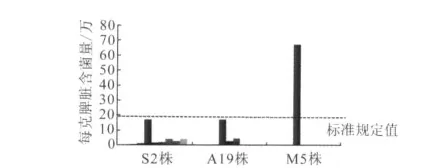
图1 2012年布氏菌病活疫苗各批次生产用菌株毒力测定结果
3 布氏菌病活疫苗生产检验存在的问题及建议
3.1 生产工艺需进一步改进 疫苗的关键是质量可控,我国兽药行业全面实行GMP管理以来,各生产企业产品质量不断提高,抽检合格率逐年提高[5-6]。但是,对于布病活疫苗仍然存在生产工艺落后影响疫苗质量的问题。一方面是培养基的成本较高且质量不稳定。布病疫苗传统生产工艺中使用的肝汤培养基在很大程度上取决于动物来源的品质和消化处理的方式,而市售的干粉培养基不同企业和不同批次之间差异较大,成为布病疫苗生产过程中影响质量的最主要问题之一。另一方面是冻干保护剂保护效果不理想,疫苗的热稳定性存在问题。实践表明,现有工艺条件下,活菌数降低和有效期时间的延长呈正相关性。建议企业积极研发提高冻干保护剂的保护效果;同时,疫苗装量应给予合理附加量、优化储藏温度并保证疫苗运输过程中冷链存储,最终确保活疫苗使用前的免疫效果不受影响。
3.2 生产企业检验能力需进一步提高 活菌计数检验项是控制疫苗质量的关键项。但是,会检中发现各企业检验人员流动性大,新上岗检验能力不足,同一批次不同人员计数结果符合性差异很大。由于活菌计数时样品的稀释液的选择、稀释方法、操作熟练程度、滴板技巧等技术细节对计数的结果都会产生较大的影响。因此各企业有必要对活菌计数方法进一步细化,并加强对检验人员的技术培训,避免由于检验技术不过关导致的疫苗质量不稳定。
3.3 开展布氏菌病活疫苗(M5株)的再评价工作
本次监督检验结果显示布氏菌病活疫苗(M5株)的菌株毒力超过了标准规定的3倍。有研究结果显示:M5株免疫后第16周仍能在小鼠脾脏内分离细菌,而S2株免疫后第6周在小鼠体内就已经分离不到活菌,M5株的毒力超过其他2个疫苗株[7]。由于2011年M5株疫苗仅生产8批,同时,监督检验受到抽检批次的限制,虽然抽检的1批疫苗不能充分说明疫苗毒株的稳定性有问题,但也给监管单位下一步的工作提供了一个方向,对M5株的安全性和质量可控性进行深入研究,掌握更多的关于M5株毒力的有关实验数据。开展对布氏菌病活疫苗(M5株)的再评价工作将对布氏菌病活疫苗的安全使用和布病的防控工作提供有利的技术支持。
[1] Seleem M N,Boyle S M,Sriranganathan N.Brucellosis:A reemerging zoonosis[J].Veterinary Microbiology,2010,140(3/4):392-398.
[2] Godfroid J,Scholz H C,Barbier T,etal.Brucellosis at the animal/ecosystem/human interface at the beginning of the 21st century[J].Preventive Veterinary Medicine,2011,102:118 -131.
[3] 崔步云.中国布鲁氏菌病疫情监测与控制[J].中国布鲁氏菌病疫情监测与控制,2007,22(10):649 -651.
[4] 中华人民共和国兽用生物制品规程[M].二〇〇〇年版.北京:化学工业出版社.154-160.
[5] 万建青,王利永,姚文生,等.2008年度兽用生物制品质量监督抽检质量分析及对策建议[J].中国畜牧兽医,2009,8:204 -207.
[6] 高艳春,赵德明.我国兽用生物制品行业现状分析与发展建议[J].中国畜牧杂志,2011,47(2):55 -59.
[7] 程君生,吴梅花,赵丽霞,等.三种布鲁氏菌病疫苗株的毒力比较[J].中国兽药杂志,2012,47(9):13 -15.

