诱导头孢噻肟钠结晶过程研究
尹永恒,鲍 颖,2*,王永莉,高振国,刘 东
(1.天津大学化工学院,天津 300072; 2. 天津市现代药物传递及功能高效化重点实验室,天津 300072; 3.华北制药集团有限责任公司,石家庄 050015)
头孢噻肟钠(CTX)是第3代头孢类抗菌素,对革兰氏阴性菌的活性较高。它的结晶过程需要严格控制以使晶体的产率、纯度、晶习和密度等性质符合商业需求。头孢噻肟钠在溶析结晶的过程中很难析出,而且极易成胶。在结晶过程中使用晶种是一种有效诱导、控制结晶方法。制作晶种的方法有很多种,包括研磨、干燥、筛分和溶剂冲洗等[1-2]。Aamir等认为在研磨过程中会出现较碎的细晶,因此不宜用研磨制备晶种[3]。Kubota等则使用冲洗方法消除了一部分研磨产生的细晶[1]。如今,纳米晶种正在被越来越多的应用,因为相对大晶体来说,纳米晶体能更好的提高结晶速率[4]。降低粒子尺寸能有效提高比表面积,进而改善晶体和溶液之间的传质[5],从这一角度来看,拥有大量小晶体的研磨晶种对诱导成核和晶体生长更加有益。
超声波作为一种有效手段被越来越多的应用到了结晶研究中,超声波影响结晶这一现象被较为广泛的认为是空化效应和声流引起。空化作用产生的气泡是均匀分散的气相,能诱导过饱和溶液中的非均相成核,从而可以替代传统的加晶种方法[6]。Lyczko等发现超声波会影响K2SO4的诱导期和介稳区[7]。此外还有大量文献表明超声具有影响产品粒度分布、提高产品纯度、影响晶型等作用[8-10]。
加入溶液的晶种一方面会在溶液中生长,另一方面,还会诱导初级成核。在有晶种存在的情况下,初级成核的速率会变缓。Saleemi等将浓度控制在介稳区以内,使用加晶种的方法来影响成核过程[11]。晶种的表面粗糙度是影响晶体成核和生长的最重要因素之一,有文献表明,晶体的表面粗糙度越大,成核越容易[12-13]。Ulrich等发现局部受损的不完整晶体其生长速率大于完整晶体[14],因为局部受损的晶体有一个更加粗糙的表面,这一观点与一些被认为是反应控制生长的物质相吻合,像K2SO4、 KAl(SO4)2·12H2O等。
本研究使用在线技术研究了3种不同晶种以及超声波对头孢噻肟钠结晶过程的影响,并通过晶种的表征研究了不同晶种的作用机理。通过使用适当的晶种,有效地避免了成胶现象,得到了较为满意的产品。本实验工作可为优化头孢噻肟钠的结晶工艺提供重要依据。
1 实验部分
1.1 实验药品及试剂
头孢噻肟酸,华北制药有限公司,质量分数≥98.5%;醋酸钠,天津科威有限公司,分析纯;去离子水,市售;头孢噻肟钠标准品,国药集团化学试剂有限公司。
1.2 实验方法
实验装置如图1所示,在混合溶剂中,将头孢噻肟酸与醋酸钠于288.00±0.05 K下进行反应得到头孢噻肟钠溶液,反应结束时溶液澄清。然后将晶种加入到溶液中,晶种质量为溶液中理论头孢噻肟钠质量的0.5%。养晶2 h后,开始滴加溶析剂。溶析结晶过程控温在283.00±0.05 K,搅拌速率为300 r/min。整个结晶过程将ATR-FTIR探头(瑞士梅特勒-托利多公司,型号:React IRTM45)和FBRM探头(瑞士梅特勒-托利多公司,型号:M400LF)插入结晶器进行监测。溶析剂滴加完毕后,过滤,滤饼取少量样品做粒度分析(英国Malvern Instruments公司,型号:Mastersizer S)后,放在313 K真空条件下干燥。干燥产品称质量用来计算产率,并使用液相色谱(美国Agilent Technologies,型号:Agilent 1260,色谱柱:Venusil MP-C18柱,150×4.6 mm, 5 μm)进行纯度分析。测试方法参照美国药典[15]。
实验分为4组,如表1所示,实验D的养晶过程在超声器(宁波新芝有限公司,型号:SB-5200DTD)中进行,超声器设置在40 kHz,300W。晶种A~C的制备过程如下。

图1 结晶实验装置图Fig.1 Setup used for crystallization
晶种A:干燥后未经任何处理的结晶产品。
晶种B:将晶种A使用球磨机(德国Retsch公司,型号:Qscillating Mill MM400)在30 Hz下研磨30 h。
晶种C:先将晶种A悬浮在10mL溶析剂中。超声器设置在40 kHz,300 W,将此悬浮液放在超声器中超声30 h,得到晶种C。

表1 四组不同条件下的头孢噻肟钠结晶实验Table 1 Four different cases of crystallization experiments of CTX
图2a)显示晶种A为粒度很大的聚结体,聚结体由大量小粒子相互紧密交织而成。需要注意的是,即便在悬浮液中是分散的晶体,经过干燥后也会聚结。因此考察晶种A对结晶过程的影响是有代表性的。图2b)显示晶种B是分散的小粒子,因为经过了球磨机研磨,这些小粒子不完整而且有大量细晶存在。图2c)中晶种C的SEM图片说明经过超声波处理后,晶种虽部分破裂,但细晶较少,晶习相对完整。

图2 不同晶种的扫描电镜图片Fig.2 SEM of different seeds
2 结果与讨论
2.1 不同晶种及超声波对结晶产品性质的影响
4组实验得到的晶体产品晶习如图3所示,均为湿样的显微镜(日本奥林巴斯公司,型号:Olympus BX51)图片。

图3 不同产品的显微镜图片Fig.3 Micrographs of different products
从图3中可以看出产品A聚结严重;产品B为分散的菱形晶体,晶习较为完整;产品C也是聚结体,但存在许多破碎的细晶;产品D则是非常细小的晶体,尺寸明显比产品A~C要小。
图4为晶体粒度分布图。

图4 产品A、B、C和D的晶体粒度分布Fig.4 CSDs of products A, B, C and D
从图4中可明显看出产品A和产品C粒度分布呈双峰,这是由实验过程中的聚结现象引起。产品B和产品D为单峰。不同产品的主粒度和计算出的C.V.值列在表2中,可以看出,产品B和产品D的C.V.值相近,但产品B比D的主粒度要大。将超声波应用在养晶过程中制备的产品粒度较小,这与超声波的强烈破碎作用、大量诱导二次成核有关。聚结现象导致产品A的主粒度最大,产品C次之。
实验A~D的产品收率及纯度也列在了表2中,数值为3次平行实验得到的平均值。产品A和产品C由于聚结严重导致包藏了富含杂质的母液,尽管多次用溶剂洗涤,也难以清除干净,所以纯度较低。从表2可以得出的结论是晶种A和C不宜作为头孢噻肟钠结晶的晶种。
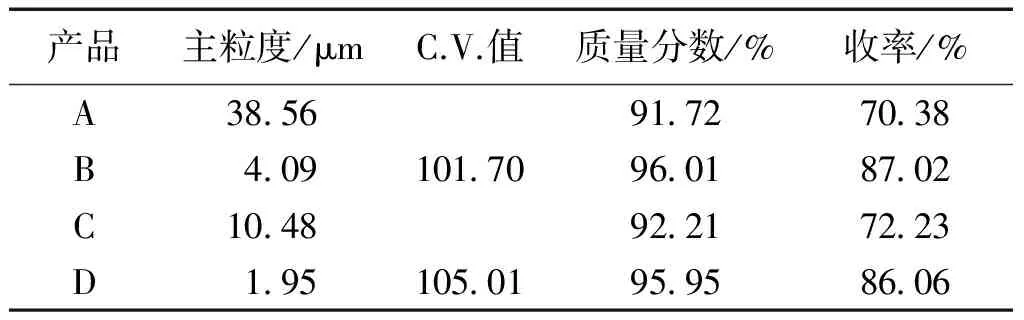
表2 四组实验产品的主粒度、C.V.值、纯度及收率Table 2 Dominant size, C.V., purity and yield of the products of four cases
2.2 不同晶种及超声波对头孢噻肟钠结晶过程的影响
2.2.1红外浓度校正模型
采用在线红外光谱数据反映结晶过程溶液中头孢噻肟钠浓度的变化。图5给出了混合溶剂以及头孢噻肟钠溶解在混合溶剂中的红外图谱。
通过比较可以发现在1 040、1 539 和1 774 cm-1处有明显的吸收峰变化,其中1 774 cm-1处为头孢
噻肟钠分子中β-内酰胺与杂环并接产生的特征峰。用1 774 cm-1处吸收峰值校正头孢噻肟钠浓度的误差最小,所以选择此处吸收值来校正头孢噻肟钠的浓度。
拟合结果证明,幂函数方程最适合作为校正模型[16],见式(1)。
A=(3.2563×10-4W+3.9570×10-3)C(6.4700×10-3W+2.2555×10-1)
R2=0.985
(1)
式(1)中,A是1 774 cm-1处的吸收值,C是头孢噻肟钠浓度,W是混合溶剂中溶析剂的质量分数,过饱和度用式(2)计算:
ΔC=C-C*
(2)
其中C*是头孢噻肟钠的溶解度[17]。
2.2.2结晶过程分析
图6是添加不同晶种及使用超声波时CTX溶析结晶的在线监测信息。
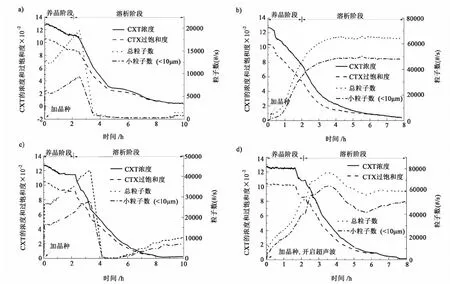
图6 结晶过程浓度,过饱和度,总粒子数和小粒子数(<10 μm)的变化Fig.6 Change of concentration, supersaturation, total counts and counts <10 μm during the crystallization process
对于实验A[图6a)],养晶期间,小粒子数(<10 μm)和总粒子数都在逐渐增加。2 h养晶结束时,小粒子数、总粒子数分别是8 109和17 213#/s,二者之比为0.47,过饱和度由初始10.56×10-2g/g溶液降低到8.85×10-2g/g溶液,降低了1.71×10-2g/g 溶液。此后,开始滴加溶析剂。滴加30 min以后,FBRM粒子数曲线陡然下降,此时肉眼可见凝胶出现,产生的凝胶黏附在结晶器壁上。此后的溶析过程中,虽然溶液过饱和度一直在减小,但析出的小粒子黏附凝胶上,所以FBRM粒子数曲线没有显著上升。直到进程为9 h左右,黏附在结晶器壁上的部分凝胶从器壁脱落,进入主体溶液后被破碎,小粒子和总粒子数才有些许增加。
对于实验B[图6b)],养晶期间,粒子总数和小粒子数大量增加,养晶结束后,小粒子数和总粒子数分别为35 799和48 420 #/s,二者之比为0.74,这说明小粒子个数的增长对总粒子的增加贡献最大。总粒子数、小粒子所占比例,都显著高于实验A。从表3中可看出粒子数在增长,又由于过饱和度在显著消耗,这表明养晶过程中晶种B有效的诱导了成核。养晶期间,过饱和度降低了5.02×10-2g/g,降幅显著大于实验A。养晶结束后,开始滴加溶析剂,CTX过饱和度继续降低,粒子数继续不断增多。表面看上去粒子数增加速率似乎变小了,其实是由于溶析剂加入后的稀释作用导致了晶浆浓度降低。加入晶种B的溶析过程没有发生胶凝,结晶过程得到控制。从表3数据来看,各区间粒子数都在增大,这说明在养晶期间晶种B有效的促进了成核和生长,使CTX不断从溶液中析出。
表3为实验B养晶期间粒子数变化情况。

表3 实验B养晶过程粒子数变化Table 3 Change of counts number in breeding of case B
实验C与实验A的过程曲线有些类似,溶析阶段开始约1 h后,出现了胶凝现象。在滴加溶析剂约4 h的时候,又开始出现晶体,这同样是由凝胶破碎造成的。值得注意的是,养晶结束后粒子总数和小粒子数分别是实验A的2倍和3倍,但是他们消耗的过饱和度基本相同,这说明晶种C与A相比,还是在一定程度上减轻了凝胶现象的发生。
实验D在养晶阶段使用了超声波,养晶阶段前1.5 h粒子数持续上升而过饱和度几乎保持不变,这说明此段时间超声波的主要作用是破碎聚结的晶种。在1.5到2.0 h之间,粒子数增加的同时消耗了相当一部分过饱和度,说明经超声波作用一段时间后,二次成核和生长开始进行。养晶结束后,总粒子数和小粒子数分别比实验B多2 508和3 197 #/s,但过饱和度消耗较实验B少了3.71×10-2g/g溶液。养晶结束后,随着溶析剂的滴加,溶液中继续析出晶体,过饱和度持续降低。从图6d)可以看出,实验约3.5 h以后粒子数曲线先下降又上升,很可能是晶体聚结后又被超声波破碎。此外,从图6中过饱和度变化值可以看出,4组实验理论析出的晶体应该相差不多,但从表2中收率来看并非如此,这是实验A和C过程中析出的胶体黏附在结晶器上造成的收率损失。
2.3 晶种诱导头孢噻肟钠结晶机理
在头孢噻肟钠的结晶过程中,过饱和度达到一定值才能发生初级成核,初级核尺寸非常小,属胶体粒子范畴,他们相互聚集、缠绕形成网状结构的凝胶。文献中提到结晶更容易发生在一些“优先位点”上[18],例如相界面、结晶器壁等。加入晶种后则为二次成核和晶体生长提供了“位点”,减少初级成核,进而避免成胶现象的发生。
如果将晶种近似考虑成球形,那么晶种的比表面积可用式(3)计算:
(3)
其中,n为粒度分析仪中的粒度通道个数;ρ为头孢噻肟钠的密度;Pi是特定半径下粒子体积分数;si和νi是具有相同半径粒子的表面积和体积。由式(3)计算出晶种A和晶种B的比表面积分别为0.61和 0.95 m2/g。这一结果表明晶种经研磨后具有更大的比表面积,这对成核和晶体生长是有益的。图7为高倍放大的晶种扫描电镜图片,从图7中可以清晰地看到晶种A晶习完整,表面更加光滑。晶种B比晶种A的表面粗糙,所以晶种B具有更低的成核能垒,从而能更好的诱导头孢噻肟钠从溶液中析出。

图7 不同晶种的高倍放大扫描电镜图片Fig.7 Magnified SEMs for surface of different seeds
3 结论
晶种的使用在控制结晶过程中起到举足轻重的作用。本研究采用PAT监测了添加3种晶种及超声波作用下的CTX结晶过程,并运用校准模型将红外吸收值转化为浓度,详细的分析了不同晶种及超声波在结晶过程中所起的作用。研究表明,研磨的晶种表面粗糙,降低了CTX的成核能垒,从而有效消耗过饱和度、促进CTX结晶。只使用超声波处理晶种虽然可以破碎晶种,但不能改变晶种本身的表面性质;将超声波应用于整个养晶阶段可起到破碎晶种、促进二次成核的作用。未处理的晶种由于比表面积小,表面光滑,很难为CTX的析出提供“位点”,因而导致胶凝现象。结晶过程使用研磨晶种或在养晶阶段使用超声波都可有效避免头孢噻肟钠的胶凝。本研究结果可为优化头孢噻肟钠的结晶工艺提供重要依据。
参考文献:
[1]Kubota N, Doki N, Yokota M,etal. Seeding policy in batch cooling crystallization[J]. Powder Technology, 2001, 121(1): 31-38
[2]Adi H, Larson I, Stewart P. Use of milling and wet sieving to produce narrow particle size distributions of lactose monohydrate in the sub-sieve range[J]. Powder Technology, 2007, 179(1/2): 95-99
[3]Aamir E, Nagy Z K, Rielly C D. Evaluation of the effect of seed preparation method on the product crystal size distribution for batch cooling crystallization processes[J]. Crystal Growth and Design, 2010,10(11): 4 728-4 740
[4]Majano G, Darwiche A, Mintova S,etal. Seed-Induced crystallization of nanosized Na-ZSM-5 crystals[J]. Industrial and Engineering Chemistry Research, 2009, 48(15): 7 084-7 091
[5]Minkov V S, Drebushchak V A, Ogienko A G,etal. Decreasing particle size helps to preserve metastable polymorphs. A case study of DL-cysteine[J]. Crystal Engineering Communication, 2011, 13: 4 417-4 426
[6]Lyczko N, Espitalier F, Louisnard O,etal. Effect of ultrasound on the induction time and the metastable zone widths of potassium sulphate[J]. Chemical Engineering Journal, 2002, 86(3): 233-241
[7]Lyczko N, Espitalier F, Louisnard O,etal. Effect of ultrasound on the induction time and the metastable zone widths of potassium sulphate[J]. Chemical Engineering Journal, 2002, 86(3): 233-241
[8]Narducci O, Jones A G. Seeding in situ the cooling crystallization of adipic acid using ultrasound[J]. Crystal Growth and Design, 2012, 12(4): 1 727-1 735
[9]Ruecroft G, Hipkiss D, Ly T,etal. Sonocrystallization: The use of ultrasound for improved industrial crystallization[J]. Organic Process Research and Development, 2005, 9(6): 923-932
[10]Chen W, Huang G. Ultrasound-Assisted crystallization of high purity of 2, 4-dinitrotoluene from spent acid[J]. Ultrasonics Sonochemistry, 2008,15(5): 909-915
[11]Saleemi A, Rielly C, Nagy Z K. Automated direct nucleation control for in situ dynamicnes removal in batch cooling crystallization[J]. Crystal Engineering Communication, 2012, 14: 2 196-2 203
[12]Gunn D J. Effect of surface roughness on the nucleation and growth of calcium sulphate on metal surfaces[J]. Journal of Crystal Growth, 1980, 50(2): 533-537
[13]Tien L C, Chen Y J. Effect of surface roughness on nucleation and growth of vanadium pentoxide nanowires[J]. Applied Surface Science, 2012, 258(8): 3 584-3 588
[14]Ulrich J. On the difference in the growth rates of fragmented (hurt) and non-fragmented (unhurt) crystals during industrial crystallization[J]. Journal of Crystal Growth, 1985, 73(2): 397-399
[15]The United States Pharmacopeial Convention. The United States Pharmacopeial Convention[M]. USP32-NF27, United States: 2009
[16]Borissova A, Dashova Z, Lai X,etal. Examination of the semi-batch crystallization of benzophenone from saturated methanol solution via aqueous antisolvent drowning-out as monitored in-process using ATR FTIR spectroscopy[J]. Crystal Growth and Design, 2004, 4(5): 1 053-1 060
[17]张海涛. 头孢噻肟钠结晶技术研究[D]. 天津:天津大学, 2008
Zhang Haitao. Research on crystallization technique of cefotaxime sodium[D]. Tianjin: Tianjin University, 2008
[18]Mullin J W. Crystallization[M]. Butterworth Heinemann: London, UK: 2001

