聚丙烯酰-6-氨基吡啶的制备及其对重金属离子的吸附
翟云会, 阮晓芳,刘 振
(西安文理学院 化学与化学工程学院,陕西 西安 710065)
吸附法是去除废水中有机或无机污染物最常用、最有效的方法之一[1]。对于吸附剂的研究一直是水处理领域的研究热点。目前应用或研究最多的吸附剂有活性炭、黏土、硅胶、沸石、壳质类物质等[2-5]。重金属是主要的水体污染物之一。重金属吸附剂分子中存在各种活性基团,可通过与金属离子形成配位键或共价键而达到分离重金属离子的目的。氨基是最常用的金属离子配位基之一,许多文献报道了以含氨基的有机试剂修饰不同的固相载体作为吸附金属离子的材料[6-8]。通常,采用聚合物表面修饰的方法得到的吸附材料具有较快的吸附速率,但因试剂修饰量有限,导致饱和吸附量不大。采用配位功能单体直接聚合得到功能吸附材料,可以增加单位聚合物中配位基团的数量,提高吸附容量。2,6-二氨基吡啶分子中含有两个氨基和一个吡啶环,可有效地与过渡重金属离子进行配位结合[9]。
本工作以2,6-二氨基吡啶为原料,合成了功能单体2-丙烯酰-6-氨基吡啶,并将其与乙二醇二甲基丙烯酸酯共聚,合成了聚合物吸附剂聚丙烯酰-6-氨基吡啶,并考察了聚合物吸附剂对重金属离子的吸附分离性能。
1 实验部分
1.1 试剂和仪器
2,6-二氨基吡啶、丙酮、三乙胺、丙烯酰氯、甲醇、乙二醇二甲基丙烯酸酯、偶氮二异丁腈、HCl:分析纯。
Cd2+,Cu2+,Zn2+,Ni2+的标准储备液:质量浓度1 g/L。
TAS-990型原子吸收分光光度计:北京普析通用仪器有限责任公司;Varian 1000型傅里叶变换红外光谱仪:美国Nicolet公司;s-3400N11型扫描电子显微镜:日本日立公司;PHS-2C型pH计:上海雷磁分析仪器厂;101-0型电热鼓风干燥箱:北京科伟永兴仪器有限公司;TGL-16C型离心机:北京维欣仪奥科技发展有限公司。
1.2 聚合物吸附剂的制备
1.2.1 功能单体的制备
将2.2 g 2,6-二氨基吡啶加入50 mL丙酮中,常温下搅拌溶解。再加入3.8 mL三乙胺,在4 ℃冰水浴条件下滴加10 mL丙酮和3 mL丙烯酰氯的混合液,滴加完毕后控温30 ℃,反应1 h。过滤,待溶剂自然挥发后用蒸馏水洗涤滤饼,再过滤后于60℃下恒温干燥,得到黄色固体——2-丙烯酰-6-氨基吡啶[10]。
1.2.2 聚合物吸附剂的制备
采用本体聚合法,在5 mL甲醇中加入0.163 g功能单体、4.2 mL交联剂乙二醇二甲基丙烯酸酯、40 mg引发剂偶氮二异丁腈,通氮气除氧后密封,置于60 ℃水浴中,聚合反应12 h。将得到的固体研磨,先醇洗,再水洗,最后烘干得聚合物吸附剂——聚丙烯酰-6-氨基吡啶[11]。
1.3 吸附实验
室温下取10 mL一定质量浓度的重金属离子混合溶液,调节溶液pH,加入5 g/L聚合物吸附剂,振荡反应一定时间,静置,离心后取上清液进行分析。
将吸附后的聚合物吸附剂用蒸馏水清洗,加入5 mL一定浓度的HCl溶液进行洗脱,离心后对洗脱液进行分析[12]。
1.4 分析方法
对聚合物吸附剂的结构和形貌进行FTIR和SEM表征;采用原子吸收分光光度计测定溶液中重金属离子的含量,计算吸附量、吸附率和洗脱率。
2 结果与讨论
2.1 表征结果
2-丙烯酰胺基-6-氨基吡啶的FTIR谱图见图1。由图1可见:3 447,3 352,3 222 cm-1处的吸收峰归属于N—H键的伸缩振动;3 028 cm-1处的吸收峰归属于C=C键的伸缩振动;1 622,1 590,1 544,1 458 cm-1处的吸收峰说明吡啶环的存在;1 675 cm-1处的吸收峰归属于酰胺键上羰基的伸缩振动;1 404 cm-1处的吸收峰归属于C—N键的伸缩振动;980 cm-1处的吸收峰归属于C H键的弯曲振动。
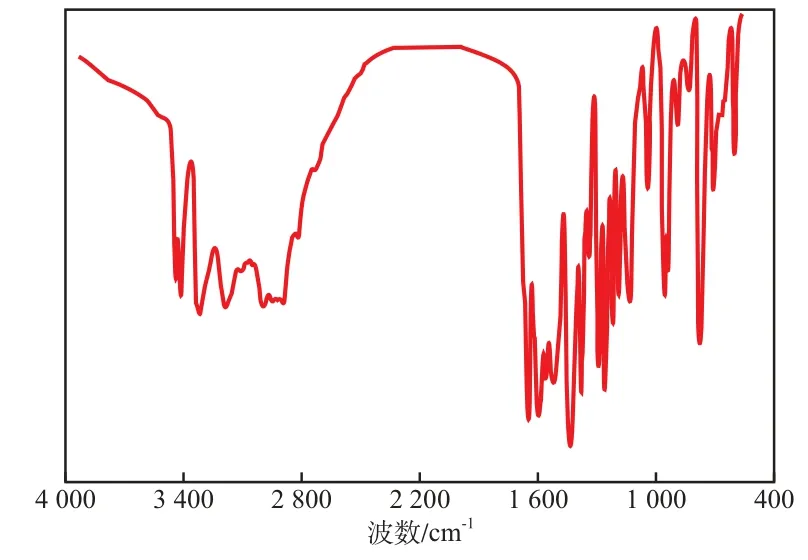
图1 2-丙烯酰胺基-6-氨基吡啶的FTIR谱图
聚合物吸附剂的SEM照片见图2。

图2 聚合物吸附剂的SEM照片
由图2可见,聚合物吸附剂为颗粒状,粒径约2~3 μm。小粒径的颗粒状材料具有较大的比表面积,因此更利于重金属离子的吸附。
2.2 溶液pH对吸附率的影响
在聚合物吸附剂加入量为5 g/L、各重金属离子的初始质量浓度均为10 mg/L、吸附时间为10 min的条件下,溶液pH对吸附率的影响见图3。由图3可见,当溶液pH>4时,4种离子的吸附率均达95%以上。聚合物吸附剂对重金属离子的吸附作用来自于氨基吡啶基团与离子的配位力。在pH<4的水溶液中,氨基易形成质子化,氢离子与其他离子竞争结合,导致其失去配位能力。因此,为保证吸附效果,选择溶液pH=5~7较适宜。
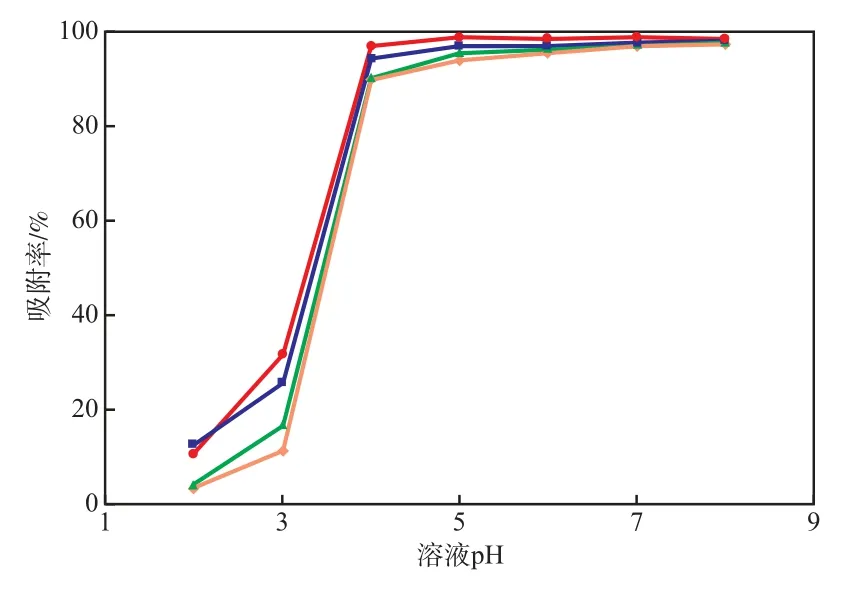
图3 溶液pH对吸附率的影响重金属离子:● Cu2+;■ Zn2+;▲ Cd2+;◆ Ni2+
2.3 初始离子质量浓度对吸附率的影响
在聚合物吸附剂加入量为5 g/L、溶液pH=7、吸附时间为10 min的条件下,初始离子质量浓度对吸附率的影响见图4。
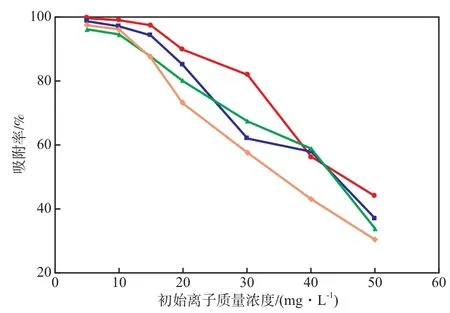
图4 初始离子质量浓度对吸附率的影响重金属离子:● Cu2+;■ Zn2+;▲ Cd2+;◆ Ni2+
由图4可见:当混合溶液中各重金属离子的初始质量浓度小于10 mg/L时,聚合物吸附剂对各离子的去除率均大于90%;当混合溶液中各重金属离子的初始质量浓度为20 mg/L时,Cd2+和Ni2+的去除率低于80%;当重金属离子的初始质量浓度大于20 mg/L时,重金属离子去除率下降明显。聚合物吸附剂对Cu2+,Zn2+,Cd2+,Ni2+的饱和吸附量分别为62,55,67,38 mg/g,与采用表面试剂修饰法制得的材料[7]相比,饱和吸附量明显增加。
2.4 吸附时间对吸附率的影响
在聚合物吸附剂加入量为5 g/L、各重金属离子的初始质量浓度均为10 mg/L、溶液pH=7的条件下,吸附时间对吸附率的影响见图5。由图5可见:聚合物吸附剂对4种重金属离子的吸附很快;当吸附时间为10 min时,各重金属离子的去除率可达90%以上。这是由于,聚合物吸附剂具有较小的颗粒粒径和较大的比表面积,增加了功能基团与目标离子接触的机会;另一方面,聚合物吸附剂以氨基吡啶为吸附作用基团,该基团具有很好的亲水性,有利于对水溶液中目标离子的吸附。
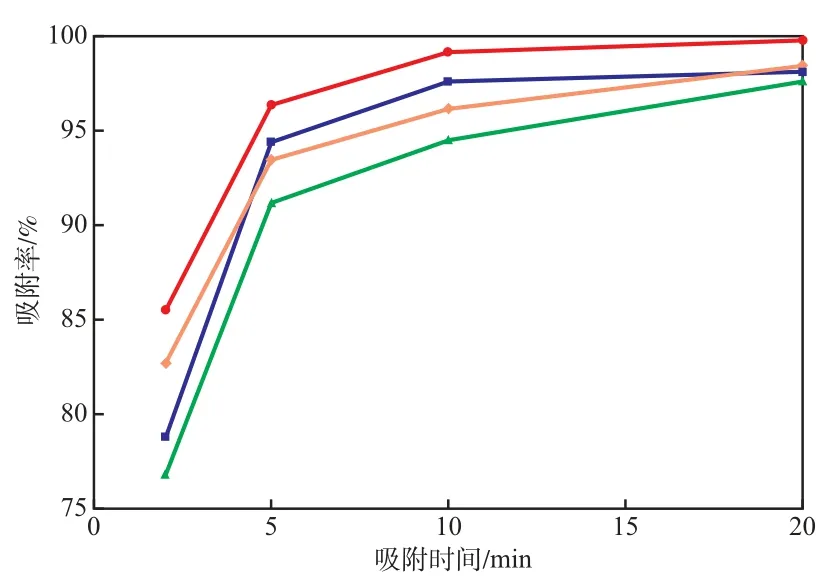
图5 吸附时间对吸附率的影响重金属离子:● Cu2+;■ Zn2+;▲ Cd2+;◆ Ni2+
2.5 洗脱实验
在各重金属离子的初始质量浓度均为10 mg/L、溶液pH=7、吸附时间10 min的条件下,对吸附重金属后的聚合物吸附剂进行脱附,HCl溶液的浓度对洗脱率的影响见图6。
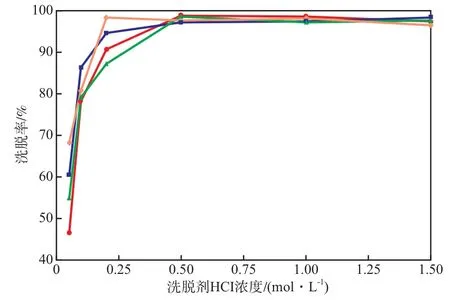
图6 HCl溶液的浓度对洗脱率的影响重金属离子:● Cu2+;■ Zn2+;▲ Cd2+;◆ Ni2+
由图6可见,当HCl溶液的浓度为0.5 mol/L时,4种重金属离子的洗脱率均可达97%以上。
对洗脱后的聚合物吸附剂进行重复实验,聚合物吸附剂的重复使用效果见图7。由图7可见,经过11次的重复使用,聚合物吸附剂对4种重金属离子的饱和吸附量均未有明显的下降。
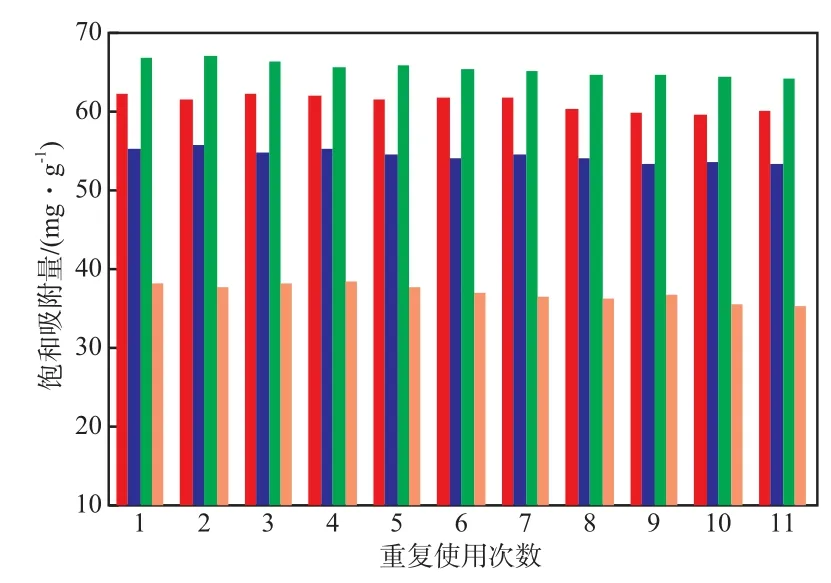
图7 聚合物吸附剂的重复使用效果重金属离子:■ Cu2+;■ Zn2+;■ Cd2+;■ Ni2+
3 结论
a)合成了一种新型吸附材料——聚丙烯酰-6-氨基吡啶,通过对重金属离子的吸附与分离实验得出该聚合物吸附剂对Cu2+,Zn2+,Cd2+,Ni2+具有很好的吸附效果,可用于处理重金属离子废水。
b)实验结果表明:在混合液中Cu2+,Zn2+,Cd2+,Ni2+的初始质量浓度均为10 mg/L、聚合物吸附剂加入量5 g/L、溶液pH=7、吸附时间10 min的条件下,各重金属离子的去除率均大于90%;采用浓度为0.5 mol/L的HCl溶液对吸附后的聚合物吸附剂进行洗脱,4种重金属离子的洗脱率均可达97%以上。
c)该吸附剂具有很好的稳定性,重复使用11次后对4种重金属离子的饱和吸附量均未有明显的下降。
[1] 董艳萍,田喜强,乔秀丽,等. 磁性粒子/介孔碳的合成及其吸附性能[J]. 化工环保,2012,32(1):94 -97.
[2] 武荣成. 表面改性Fe3O4去除水中酸性红B的研究[J].环境科学学报,2004,24(3):634-934.
[3] 向万宏,刘峥. 螯合树脂的合成及应用研究新进展[J]. 化工技术与开发,2003,32(5):19-26.
[4] 万柳,童仕唐. 中孔活性炭对水溶液中Cr3+的吸附[J].化工环保,2012,32(1):75-80.
[5] 张双圣,刘喜坤,刘倩. 纳米羟基磷灰石的制备及其对Pb2+的吸附性能[J]. 化工环保,2012,32(2):123-128.
[6] Lu Yun,Wu Cuixia,Lin Weiping,et al. Metal ion selective membrane prepared by surface molecular imprinting[J]. J Appl Polym Sci,1994,53:1461-1468.
[7] 翟云会,阮晓芳,王振,等. 2,6-二氨基吡啶修饰Fe3O4纳米粒子对Cu2+和Zn2+的吸附性能[J]. 光谱实验室,2011,28(4):2042-2046.
[8] Zhai Yunhui,He Qun,Han Quan,et al. Solid-phase extraction of trace metal ions with magnetic nanoparticles modified with 2,6-diaminopyridine[J]. Microchim Acta,2012,178:405-412.
[9] 周艳梅,童爱军. 2,6-二氨基吡啶衍生物作为过渡金属离子荧光探针的研究[J]. 光谱学与光谱分析,2007,27(12):2518-2522.
[10] 周艳梅. 新型荧光功能单体2,4-二甲基-7-丙烯酰胺基-1,8-萘啶的合成及其光谱特性[J]. 光谱学与光谱分析,2006,26(3):496-498.
[11] 刘峥. 铜离子印迹聚合物的制备及吸附性能[J]. 桂林工学院学报,2007,27(2):106-110.
[12] 朱端卫. 8-羟基喹啉螯合树脂与重金属离子作用研究[J]. 华中农业大学学报,2000,19(1):67-69.

