反相高效液相色谱法测定人尿中多种多环芳烃代谢物
杨红梅,王永生,黎俊宏,欧阳运富
(1.江苏省常州市中心血站,江苏常州 213004;2.南华大学 公共卫生学院,湖南衡阳 421001;3.江苏省常州市疾病预防控制中心,江苏常州 213022)
多环芳烃是环境中典型的持久性有机污染物[1-2]。它们经人体代谢后,可以生成多种不同的代谢物,通过对这些尿中代谢物的检测可为人体对其接触风险水平的综合评价奠定基础。目前同时检测PAHs羟基代谢物的主要方法是色谱法[3-6],但目前分析时间长达40 min左右。
研究利用反相高效液相色谱法建立同时检测人尿样中多种PAHs代谢物的新方法,其中主要包括1-羟基芘 (1-OHP)、α-萘酚 (α-NAP)、β-萘酚(β-NAP)、9-羟基菲(9-OHPe)、2-羟基芴(2-OHFlu)和9-羟基芴(9-OHFlu)。样品经过碱水解、富集及吹氮浓缩,采用高效液相检测,外标法定量,缩短了样品分析时间,在20 min内6种待测物质可完全分离。
1 实验部分
1.1 试剂与仪器
1-羟基芘、α-萘酚、β-萘酚、9-羟基菲、2-羟基芴、9-羟基芴均为分析纯;甲醇,色谱纯;实验用水为超纯水(电阻18 MΩ)。
DionexP680高效液相色谱仪(配紫外检测器);AB204-S电子分析天平;Aquapro纯水机;UV-8500紫外/可见分光光度计;BF-2000氮气吹干仪;PB-20(PB-S)酸度计。
1.2 试剂配制
1.2.1 1-OHP 标准储备液(5.00 ×10-4mol/L)准确称取 0.010 9 g 1-OHP,用 1∶1 甲醇-水(v∶v)溶解,并稀释至100.0 mL。标准工作液由标准储备液稀释至5.00 ×10-6mol/L。
1.2.2 α-NAP 和 β-NAP 标准储备溶液(5.00 ×10-3mol/L)准确称取 0.072 g α-NAP 和 0.072 g β-NAP 分别用 1∶1 甲醇-水(v∶v)溶解,并相应稀释至100.0 mL。标准工作液由标准储备液稀释至5.00 ×10-5mol/L。
1.2.3 9-OHPe标准储备液(5.00 ×10-3mol/L)准确称取 0.097 1 g 9-OHPe,用1∶1 甲醇-水(v∶v)溶解,并稀释至100.0 mL,标准工作液由标准储备液稀释至5.00 ×10-5mol/L。
1.2.4 2-OHFlu 和 9-OHFlu 标准储备液(1.00 ×10-3mol/L)分别准确称取0.018 2 g 2-OHFlu和0.018 2 g 9-OHFlu,用1∶1 甲醇-水(v∶v)将其溶解并相应稀释至100.0 mL,标准工作液由标准储备液逐级稀释至2.00 ×10-5mol/L。
1.3 色谱条件
色谱柱为 DiamonsilTMC18柱,5 μm,150 nm ×4.6 nm,等度洗脱,流速 0.95 mL/min,检测波长280 nm,流动相为甲醇/乙酸钠缓冲液,体积比为66∶34,相应的 pH=4.8,0.45 μm 滤膜过滤后当天使用,进样量20 μL,温度30℃。
2 结果与讨论
2.1 检测波长的选择
目前,PAHs液相色谱分析时大多数采用单一的254 nm作为分析PAHs组分的检测波长,但大量研究表明254 nm只是PAHs组分共有的紫外吸收带,对于某些组分并不是最佳吸收带,具有一定的普适性,即在254 nm处吸光度并非达到最高。以甲醇-水(66∶34,v∶v)为参比溶液,分别对 α-NAP(5.00 μmol/L)、β-NAP(5.00 μmol/L)、1-OHP(0.50 μmol/L)、9-OHPe(5.00 μmol/L)、2-OHFlu(4.00 μmol/L)及 9-OHFlu(4.00 μmol/L)的甲醇-水溶液在200~350 nm波长进行紫外扫描,结果见图1。

图1 6种PAHs羟基代谢物标准溶液紫外吸收光谱图Fig.1 The UV absorption spectrum of 6 kinds of PAHs metabolites standard solution
由图1可知,6种PAHs代谢物在220~300 nm有较强的吸收,由于样品中很多成分在220~240 nm范围有吸收,但各自的特征吸收波长不同,为避免干扰,实验选取280 nm作为测定波长。
2.2 流动相及流速的优化
反复比较了色谱中甲醇-水、乙腈-水两种常用流动相对待测物检测的影响。结果表明,两种流动相的灵敏度差不多,但考虑了乙腈毒性大及价格,故选择甲醇-水。
实验比较了流动相中甲醇体积含量对各待测物质保留时间及分离度的影响。结果表明,流动相中甲醇浓度<55%时,1-OHP保留时间超过40 min;流动相中甲醇浓度>75%时,待测物质的保留时间大大缩短,但同分异构体9-羟基芴、2-羟基芴及α、β-萘酚分离效果不好(r﹤1.0)。故实验中甲醇与水体积比为 66∶34。
实验过程中发现待测物峰有点拖尾现象。为了控制待测物羟基电离,加入合适pH值的乙酸钠-乙酸缓冲液,不仅能有较对称的峰形,而且方法的灵敏度也得到提高。在pH 3.0~7.0,随着酸度增加,待测物的保留时间缩短,而且峰形变窄。但流动相pH值>5.5时各组分出峰时间延长;当pH值<4.0时各组分出峰时间提前,但同分异构体分离效果不满意,综合实验结果,选择流动相pH值为4.8。流速对6种待测物分离的影响见图2。
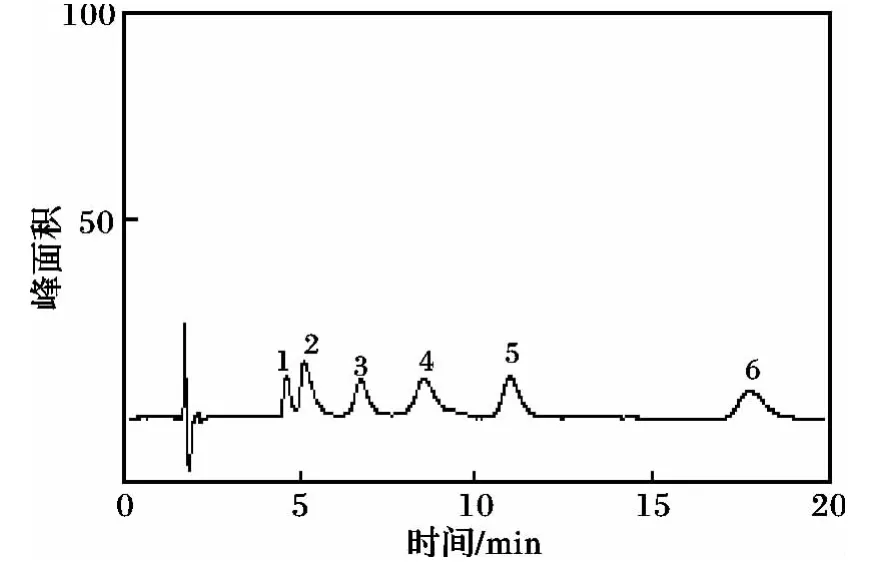
图2 6种PAHs代谢物标准溶液色谱分离图Fig.2 The chromatographic separation of 6 kinds of PAHs metabolites standard solution
由图 2可知,流速为 0.95 mL/min时,6种PAHs代谢产物有良好分离。实验条件为:流动相V(甲醇)∶V(乙酸钠-乙酸缓冲液)=66∶34,流速0.95 mL/min,进样量20 μL,紫外检测器波长为280 nm。
2.3 柱温的优化
在20~40℃每5℃进行温度实验。实验表明,保留时间与温度呈反比,即温度增加而保留时间缩短,但温度>30℃时,同分异构体分离效果不好。故实验选择柱温为30℃。
2.4 标准曲线和检出限
取不同体积的 1-羟基芘、α-萘酚、β-萘酚、9-羟基菲、2-羟基芴和9-羟基芴标准应用液,以甲醇∶乙酸钠-乙酸缓冲液(66∶34)为溶剂,配制成不同浓度系列的标准混合溶液(在-5℃冰箱内至少可以稳定15 d),在优化的色谱条件下测定,以峰面积为纵坐标,以保留时间为横坐标,得到各标准物质的定量标准曲线(见图3),表明各样品在测定范围内线性关系良好。按照S/N=2计算出各待测物的检测限,结果见表1。

图3 6种PAHs代谢物标准溶液色谱图Fig.3 The chromatographic separation of 6 kinds of PAHs metabolites standard solution
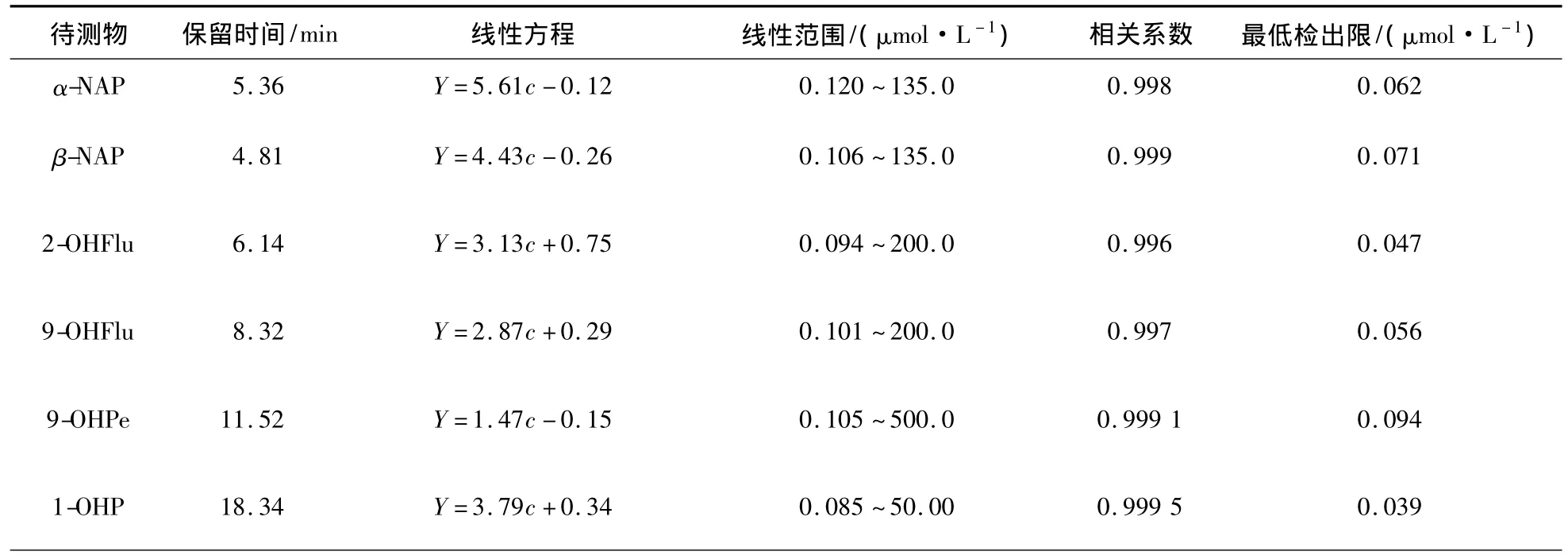
表1 线性方程与相关系数Table 1 Linear equations and correlation coefficients
2.5 精密度和重复性实验
选择在线性范围内高、低两组浓度的混合标准液进行精密度实验,取20 μL标准液连续进样7次,结果见表2。

表2 峰面积和保留时间的相对偏差Table 2 Relative standard deviation of peak area and retention time
由表2可知,在优化的色谱条件下同时测定α-萘酚、β-萘酚、2-羟基芴、9-羟基芴、9-羟基菲和 1-羟基芘具有很高的精确度和准确度。
2.6 共存物质的影响
实验考察了柠檬酸、草酸、葡萄糖、尿素、萘胺、鸟嘌呤、苯酚、对硝基苯酚和间硝基苯酚等共存物质对 1-羟基芘、α-萘酚、β-萘酚、9-羟基菲、2-羟基芴和9-羟基芴测定的影响。结果表明,这些物质对测定均无影响,由此可见该法选择性好。
2.7 样品测定
收集了开水房锅炉工和学龄前儿童尿样各1份,在-4℃冰箱冷藏过夜。参照文献[6-9]的方法,采用碱水解法处理尿样。取浓缩液20 μL注入HPLC分析,在上述条件下测定样品中的9-羟基菲、α-萘酚、β-萘酚、1-羟基芘、2-羟基芴和 9-羟基芴含量,测定6次,取其均值。结果及见表3和图4。
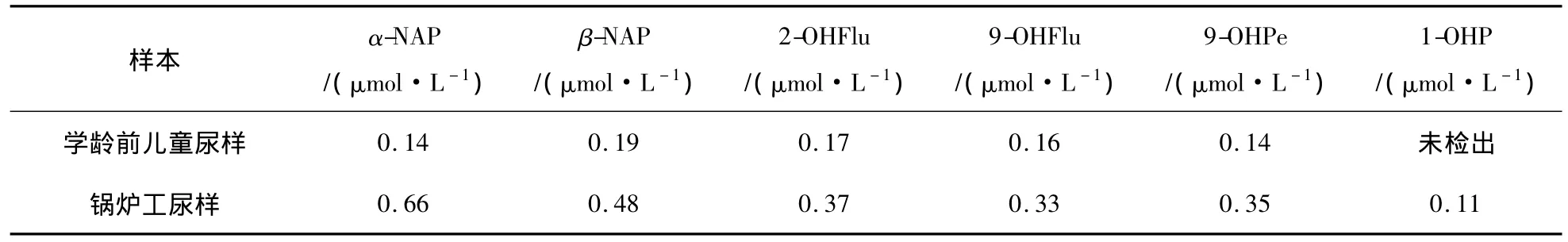
表3 样品测定结果Table 3 Determination results of samples
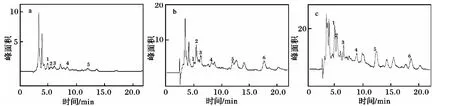
图4 小孩尿样(a)、锅炉工尿样(b)和尿样加标(c)的色谱图Fig.4 The chromatographic of the child urine sample(a)the boiler fireman sample(b)and added the boiler fireman sample(c)
2.8 尿样加标回收实验
在已知样品浓度中,分别加入低高两组浓度的9-羟基菲、α-萘酚、β-萘酚、1-羟基芘、2-羟基芴和 9-羟基芴标准混合液,在优化的实验条件下测定并计算出它们的加标回收率,结果见表4。

表4 回收率测定结果(n=6)Table 4 Determination results of recovery

续表
由表 4 可知,9-羟基菲、α-萘酚、β-萘酚、1-羟基芘、2-羟基芴和 9-羟基芴的平均回收率分别为91.0%,100.4%,101.0%,92.6%,106.7% 和95.5%。
3 结论
建立了用反相高效液相色谱同时测定尿中6种代谢产物的新方法。该方法线性范围宽,准确性好,灵敏度高,用于尿样测定,结果与文献报道相符。适用大批量的样本测定,为PAHs暴露的流行病学调查提供了快速方法。
[1]Lund M,Duedahl-Olesen L,Christensen J H.Extraction of polycyclic aromatic hydrocarbons from smoked fish using pressurized liquid extraction with integrated fat removal[J].Talanta,2009,1(70):10-15.
[2]Yan W,Chi J S,Wang Z Y,et al.Spatial and temporal distribution of polycyclic aromatic hydrocarbons(PAHs)in sediments from Daya Bay South China[J].Environ Pollut,2009,157:1823-1830.
[3]Fan R F,Dong Y,Zhang W B,et al.Fast simultaneous determination of urinary 1-hydroxypyrene and 3-hydroxybenzo[a].pyrene by liquid chromatography tandem mass spectrometry[J].J Chromatogr B,2006,836:92-97.
[4]Sancho J V,Cabanes R A,Lopes F J,et al.Direct determination of 1-naphthol in human urine by coupled-colum liquid chromatography with fluorescence detection[J].Chromatogrphia,2003,58:565-569.
[5]Kuo C T,Chen H W,Chena J L.Determination of 1-hydroxypyrene in children urine using column-switching liquid chromatography and fluorescence detection[J].J Chromatogr B,2004,805(2):187-193.
[6]杨红梅,王永生,黎俊宏,等.三维荧光法测定人尿中1-羟基芘、β-萘酚和 9-羟基菲[J].应用化工,2013(8):179-184.
[7]郭金枝,王寅淳,邢来峰.固相微萃取-气相色谱联用技术分析水相中的 α-萘酚[J].河南技师学院,2001,29(2):41-43.
[8]陈硕,韩宗勋,全燮,等.毛细管固相微萃取液相色谱法测定水中的多环芳烃[J].分析化学,2003,31(2):171-174.
[9]Yang H M,Wang Y S,Li J H,et al.Synchronous fluorescence determination of urinary 1-hydroxypyrene,β-naphthol and 9-hydroxyphenanthrene based on the sensitizing effect of β-cyclodextrin[J].Anal Chim Acta,2009,636:51-59.

