PEI联合HIFU治疗不能手术切除的中晚期原发性肝癌的临床研究
吴光平,蒲元芳,田 阗,庞 勇,曹 轲,杨 咏,徐 波,李 媛,谢 艳,何 敏
(1.重庆市南川区人民医院妇科海扶治疗中心,重庆南川408400;2.重庆医科大学生物医学工程学院,重庆400016)
目前中国肝癌患者70%以上已失去了手术机会,且约30%行手术切除术的患者3年内复发率超过了60%,其中多数患者已不愿再行手术且已不能手术切除,因此,绝大多数患者最终选择非手术治疗方式。无水乙醇注射术(percutaneous ethanol injection,PEI),肝动脉插管化疗栓塞(TACE),射频消融(RF)是临床上常用的非手术治疗方式[1];近年来,高强度聚焦超声(high intensity focused ultrasound,HIFU)消融治疗是20世纪80年代后发展的一种非侵入性治疗实体肿瘤的新技术[2],并已成功用于临床治疗肝癌,取得了较好的疗效[3-5]。但对血供丰富的原发性肝癌(primary earelnoma of the liver,PCL)行单纯HIFU 治疗,加之肋骨对声波的反射,造成了治疗靶区的能量沉积相对降低,治疗时间长,治疗效率低,并发症增多,来自患者及医生的依从性限制其在临床的应用。因此,如何安全、有效、简便、价廉地提高HIFU 治疗靶区的能量沉积,提高治疗效率一直是HIFU 治疗研究的重要课题,本研究旨在探讨PEI联合HIFU 治疗不能手术切除的PCL对其剂量的影响,现报道如下。
1 资料与方法
1.1 一般资料 2010年10月至2014年7月在重庆市南川区人民医院要求PEI联合HIFU 消融治疗不能手术切除的中晚期PCL患者36例,其中男29例,女7例;年龄38~72岁,平均(54.21±16.35)岁。其中PEI联合HIFU 治疗23 例为联合组,单纯HIFU 治疗13例为HIFU 组。入选标准:(1)所有肝癌患者均依据可靠的肝癌肿瘤标志物及影像学资料或肝穿刺病理检查确诊,且不能行手术切除;(2)有PCL 的相关症状或心理影响渴望得到治疗;(3)HIFU 治疗系统机载超声可以显示的病灶;(4)能准确地交流治疗过程中的感受;(5)同意接受镇静镇痛后实时超声引导下HIFU 消融治疗;(6)肝区无放疗病史,或有放疗病史,且剂量小于40Gy;(7)能配合执行医嘱者及能定期随访者;(8)肝功能Child-Pugh分级为A、A-B或B级。排除标准:(1)HIFU 治疗系统机载超声不能显示病灶的患者;(2)不能准确地交流治疗过程中的感受;(3)结缔组织病或接受过肝区大剂量放疗者;(4)未控制的糖尿病及肝肾功能异常者;(5)严重心、脑血管疾患。包括不稳定性心绞痛、半年内有心肌梗死、心律失常需用药物控制者,严重高血压及心力衰竭者;(6)半年内有脑梗死、脑出血者;(7)有核磁共振、钆剂、芬太尼、咪唑安定及六氟化硫微泡过敏的患者;(8)有精神病及心理疾病的患者。本研究获得重庆市南川区人民医院伦理委员会批准,并取得患者及其家属的知情同意。
1.2 方法
1.2.1 仪器设备及药品 (1)仪器设备:JC-200型聚焦超声肿瘤治疗系统由重庆海扶医疗科技有限公司研制,治疗超声换能器中心组合有超声显像探头。治疗超声换能器频率为0.80 MHz,功率0~400 W 可调,物理学焦域为1.50 mm×1.50 mm×10.00mm,循环脱气水耦合。机载显像超声参数:频率3.5 MHz。(2)药品:对比造影剂钆双胺注射液(欧乃影gadodiamid,0.50 mmol/mL),剂量为15~20 mL;镇静镇痛药物,枸橼酸芬太尼注射液(每支0.10mg)剂量为0.2~0.4mg,咪达唑仑注射液(每支2mg)剂量为4~6mg;超声造影剂,六氟化硫微泡(Sono Vue)59 mg;超声引导下高强度聚焦超声(USgHIFU)消融中用药品,格拉斯琼注射液(每支3mg)剂量为3~6mg,硫酸阿托品注射液(每支0.50 mg)剂量为0.50 mg,99.70% 无水乙醇(CH3CH2OH)每瓶500mL,碘化油每支10mL。
1.2.2 治疗前准备 两组患者均术前3d开始行流质饮食,术前1d晚上清洁灌肠,36例患者术前均行详细HIFU 治疗及PEI知情告知,并签署知情同意书。(1)常规检查:血常规、凝血分析、肝功能、肾功能、电解质、尿常规、尿-HCG,大便常规、血糖、AFP、胸片、心电图,以及肝、胆、胰、脾、肾、输尿管膀胱检查;(2)肠道准备:治疗前1d导泻,治疗当天早晨清洁灌肠;(3)皮肤准备:下腹部备皮,脱脂、脱气;(4)膀胱准备:治疗前留置导尿管;(5)镇静镇痛的实施:枸橼酸芬太尼注射液和咪达唑仑注射液联合应用,控制镇静深度达到(采用国际通用镇静镇痛Ramsey评分)Ramsey 3~4级,镇痛效果要求患者疼痛评分小于4分为佳。
1.2.3 治疗方法 (1)PCL 瘤体内穿刺注射:患者取平卧位,实施心电监护及镇静镇痛,常规消毒铺巾右上腹,联合组在彩超引导下行PEI术,于消融前30 min向瘤体内注入(99.70%无水乙醇加碘化油,9∶1)混合液10mL,HIFU 组以0.90%生理盐水10mL替代。采用国际放射介入治疗协会制定的SIR分类系统评价穿刺部位的安全性。(2)HIFU 治疗:患者取右侧卧位卧于治疗床上,右上腹部置于脱气水中的聚焦超声换能器上方,治疗前机载超声显像定位以确保有安全的声通道,避免损伤肠道等非靶区组织;根据患者对声照射引起的感觉反应和超声显像的实时灰度变化调整治疗剂量,据监测肿瘤大小和形状通过点到线到面到体的扫描方法完成治疗,36例患者均行了1次HIFU 治疗,治疗后患者在病房休息2h,可由家属陪同下床活动。
1.2.4 计算能效因子(energy-efficiency factor,EEF) EEF为单位体积所需的辐照能量。参照文献[6]计算瘤体体积,计算公式为:
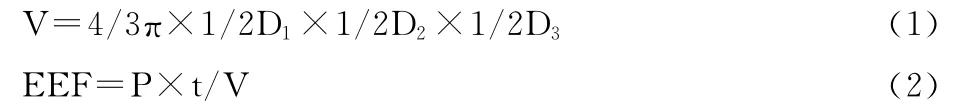
其中D1为长径,D2为前后径,D3为横径,P为输出功率,t为辐照时间,V 为瘤体体积[7-8]。
1.3 统计学处理 采用SPSS19.0 统计软件进行统计学分析,计量资料采用±s表示,组间比较采用t检验,以P<0.05为差异有统计学意义。
2 结 果
2.1 两组患者HIFU 消融参数比较 相同功率下,联合组达到治疗标准平均辐照时间及EEF 均明显低于HIFU 组,两组比较差异有统计学意义(P<0.05),见表1。
表1 两组患者HIFU 消融参数对比(±s)

表1 两组患者HIFU 消融参数对比(±s)
组别 n 辐照时间(s)总辐照能量(J)EEF(J/mm3)±6.31联合组 13 1 468.28±253.21 485 103.45±39 153.90 13.82±4.26 P<0.05 <0.05 <0.05 HFIU组 13 2 352.56±463.34 756 836.21±59 763.73 25.63
2.2 两组患者不良反应比较 36例患者在彩超引导下瘤体内穿刺,注射均一次成功,穿刺过程中联合组有19 例、HIFU组有3例出现了右上腹胀痛,均能耐受,属于SIR A 级并发症,无SIR B-F级并发症发生。
3 讨 论
3.1 HIFU 治疗特点 HIFU 治疗是保留器官、非侵入性、恢复较快的治疗方式,是在实时影像监控下,将体外低能量超声波聚焦在病灶处,通过控制焦点运动,以点-线-面-体组合的方式实行适形性消融,通过焦点区超声波产生的热效应、机械效应、空化效应致使靶区内组织发生凝固性坏死,经组织病理学证实能够有效消融靶组织并不显著损伤焦点外正常组织[9-14],从而阻止瘤体的生长使其缩小或消失,减轻或缓解瘤体引起的症状或体征。据影像引导技术不同,分为磁共振引导下高强度聚焦超声(MRIgHIFU)消融治疗和USgHIFU 治疗[15-19]。故本组研究采用USgHIFU 消融不能手术切除中晚期PCL 技术上是可行的。而单纯HIFU 治疗的不足之处在于:肋骨反射使超声波达到靶区的能量减少,HIFU 治疗的时间过长导致镇静镇痛、皮肤损伤、治疗风险增加,且不能手术切除中晚期PCL患者围术期的基本状况均不理想,均需在较短的时间内完成消融。这就需要在临床工作中提高HIFU 的治疗效率及治疗靶区的能量沉积。提高HIFU 治疗的效率主要途径有两方面:(1)增大HIFU 换能器(治疗头)的输出功率P以增强靶区的声强;(2)通过改变靶区组织的声学性质或声学环境以增强能量沉积。在镇静镇痛条件下增强HIFU 声输出功率(P),一方面会增加患者疼痛感,使治疗难以进行;另一方面可导致严重并发症产生。有研究表明,通过改变靶区组织局部的声学环境(acoustic environment in tissue,AET)就可以在HIFU 辐照其他参数不变的情况下,增加靶区能量沉积的效果,从而提高HIFU 治疗效率及能量沉积,并避免了严重并发症。EEF是HIFU 损伤单位体积组织所需的超声能量,EEF越小表明超声的能量沉积越高,在HIFU 辐照参数和靶区组织不变的情况下,EEF 与时间呈正相关。因此,辐照时间越短,EEF越小,通过一些方法使EEF 减少,从而也提高了HIFU 治疗的效率。
3.2 PEI特点 PEI是在超声引导下直接向瘤体内注入(99.70%无水乙醇加碘化油,9∶1)混合液10mL,使肿瘤细胞及其血管的内皮细胞迅速脱水、蛋白凝固、癌细胞变性坏死,癌周围血管完成闭塞,继而引起癌组织缺血坏死,由于超声引导及肿瘤包膜的限制,故对正常肝组织损伤较小。本组研究中联合组所需辐照时间及EEF均小于HIFU 组,差异有统计学意义(P<0.05),这可能是PEI术中无水乙醇与碘油混合液在肿瘤组织中的弥散改变了治疗靶区组织局部AET,从而降低了HIFU 损伤组织所需的EEF,增加能量沉积,缩短辐照时间,提高治疗效率。究其原因为可能与PEI术中无水乙醇与碘油混合液的高声阻抗有关,声阻抗差异增加了超声波在两种不同声阻抗界面间的反射,从而增加了能量沉积。
综上所述,PEI联合HIFU 治疗不能手术切除中晚期PCL,这两种方法相互联合,互补性强,可提高HIFU 治疗不能手术切除PCL的治疗效率及能量沉积。
[1] 毛羽,李浩,张立军,等.无法切除肝癌的微创治疗现况及展望[J].中华肝胆外科杂志,2005,11(11):276-278.
[2] The Haar GR.High intensity focused ultrasound for the treatment of tumors[J].Echocardiography,2001,18(4):317-325.
[3] Kennedy JE.High-intensity focused ultrasound in the treatment of solid tumours[J].Nat Rev Cancer,2005,5(4):321-327.
[4] Wu F,Wang ZB,Chen WZ,et al.Extracorporeal high intensity focused ultrasound ablation in the treatment of 1038patients with solid carcinomas in china:an overview[J].Ultrason Sonochem,2004,11(3/4):149-154.
[5] Zhang L,Zhu H,Jin C,et al.High-intensity focused ultrasound(HIFU):effective and safe therapy for hepatocellular carcinoma adjacent to major hepaticveins[J].Eur Radiol,2009,19(2):437-445
[6] Haar G,Rivens I,Chen L,et al.High intensity focused ultrasound for the treatment of rat tumors[J].Phys Med Biol,1991,36(11):1405-1501.
[7] 李发琪,王智彪,杜永洪,等.高强度聚焦超声“切除”组织的剂量学研究[J].生物医学杂志,2006,23(4):839-843
[8] 刘宝琴,熊树华,王智彪,等.体外不同频率高强度聚焦超声的生物学焦域[J].中国超声医学杂志,2002,18(6):417-420.
[9] Wulf J,Guckenberger M,Haedinger U,et al.Stereotactic radiotherapy of primary liver caner and hepatic metastases[J].Acta Oncol,2006,45(7):838-847.
[10] Wu F,Wang ZB,Chen WZ,et al.Advanced hepatocellular carcinoma:treatment with high intensity focused ultrasound ablation combined with trascatheter arterial embolization[J].Radiology,2005,235(2):659-667.
[11] 伍烽,王智彪,陈文直,等.高强度聚焦超声体外破坏原发性肝癌的病理学观察[J].中华肿瘤杂志,2011,23(3):237-239.
[12] 王月香,梁萍.肝癌热凝固治疗疗效的影像学判断[J].中华超声医学影像学杂志,2004,13(8):623-624
[13] Chan AC,Cheung TT,Fan ST,et al.Survival analysis of high-intensity focused ultrasound therapy versus radiofrequency ablation in the treatment of recurrent hepatocellular carcinoma[J].Ann Surg,2013,257(4):686-692.
[14] Leslie T,Ritchie R,Illing R,et al.High-intensity focused ultrasound treatment of liver tumours:post-treatment MRI correlates well with intra-operative estimates of treatment volume[J].Br J Radiol,2012,85(1018):1363-1370.
[15] Salomir R,Petrusca L,Auboiroux V,et al.Magnetic resonance-guided shielding of prefocal acoustic obstacles in focused ultrasound therapy:application to intercostal ablation in liver[J].Invest Radiol,2013,48(6):366-380.
[16] Ansari D,Andersson R.Radiofrequency ablation or percutaneous ethanol injection for the treatment of liver tumors[J].World J Gastroenterol,2012,18(10):1003-1008.
[17] Ng KK,Poon RT,Chan SC,et al.High-intensity focused ultrasound for hepatocellular carcinoma:a single-center experience[J].Ann Surg,2011,253(5):981-987.
[18] Zhang Y,Zhao J,Guo D,et al.Evaluation of short-term response of high intensity focused ultrasound ablation for primary hepatic carcinoma:utility of contrast-enhanced MRI and diffusion-weighted imaging[J].Eur J Radiol,2011,79(3):347-352.
[19] 黎建军,徐国良,罗广裕,等.原发性肝癌经高强度聚焦超声治疗后并发症分析[J].中华超声医学影像学杂志,2006,15(9):668-670.

