睾丸精原细胞瘤的MSCT及MRI表现
石义志,吕国士,赖丙林,刘伟,王小娟
(1.承德医学院研究生学院,河北 承德 067000;2.解放军251医院影像科,河北 张家口 075000)
睾丸精原细胞瘤的MSCT及MRI表现
石义志1,吕国士2,赖丙林1,刘伟2,王小娟2
(1.承德医学院研究生学院,河北 承德 067000;2.解放军251医院影像科,河北 张家口 075000)
目的:分析睾丸精原细胞瘤的MSCT、MRI表现,以提高对该病的认识。方法:回顾性分析9例经手术病理证实的睾丸精原细胞瘤的MSCT、MRI表现,观察病灶的形态特征、密度、信号强度及强化特点,5例行MSCT检查,2例行MRI检查,2例同时行MSCT和MRI检查。结果:精原细胞瘤MSCT主要表现为密度相对均匀,增强扫描后肿瘤轻至中度强化。MRI主要表现为卵圆状或分叶状,信号均匀,T2WI示更低信号条带状样分隔,增强扫描时分隔强化程度高于其他实质部分。结论:睾丸精原细胞瘤影像学表现有一定特征性,MSCT、MRI检查对睾丸精原细胞瘤的诊断与鉴别诊断有很大价值。
睾丸肿瘤;精原细胞瘤;体层摄影术,X线计算机;磁共振成像
精原细胞瘤是睾丸最常见的恶性生殖细胞肿瘤,起源于睾丸原始生殖细胞,多见于20~40岁青壮年,80%发生于30岁后[1]。精原细胞瘤是少数几种即使远处转移也可治愈的恶性肿瘤之一[2],不同分期患者的5年生存率达96.6%。笔者回顾性分析解放军251医院2010年3月至2015年12月收治的经手术病理证实的9例精原细胞瘤的MSCT、MRI资料,总结其影像学特点,旨在提高对该病的诊断水平。
1 资料与方法
1.1 一般资料本组9例,年龄24~65岁,平均43.6岁。发生于左侧4例,右侧5例;其中5例为患侧
睾丸肿块,有触痛感,阴囊坠涨感3例;1例睾丸无痛性肿大。HCG轻微上升3例,AFP均未见明显异常。9例均行超声检查发现占位性病变,住院后行MSCT及MRI检查,2例同时行CT、MRI平扫加增强扫描,2例仅行MRI平扫加增强扫描,5例仅行CT平扫加增强扫描,肿瘤大小4.1 cm×2.8 cm×3.0 cm~8.8cm×5.0cm×7.3 cm。
1.2 仪器与方法应用GE Lightspeed VCT型64排螺旋CT机,扫描范围从膈顶直至睾丸消失层面,常规CT平扫加动静脉双期增强扫描。扫描参数:100~120 kV,200 mA,层厚5.0 mm,螺距1.0 mm,矩阵512×512。使用非离子型对比剂碘海醇80~100 mL,使用高压注射器经肘静脉注射,流率3.5 mL/ s,对病变区行动脉期、静脉期扫描(延迟时间分别为注射开始后25、60 s)。重建间隔1.5 mm,采用标准算法进行重建。将重建后的图像传输至AW 4.5后处理工作站,行MPR、CPR MIP。MRI检查采用GE Signa HDx 3.0T MRI扫描仪,均采用体线圈。扫描序列及参数、平扫常规轴位T1WI同反相位、DWI,轴位、冠状位和矢状位FSE T2WI,层厚3 mm,层距0.5 mm,矩阵256×256,回波链12~14,2~4次激发。增强扫描于静脉注射对比剂Gd-DTPA(剂量0.2 mmol/kg体质量)后扫描,采用矢状位LAVA扫描及轴位脂肪抑制T1WI。
2 结果
2.1 CT表现7例中,病灶均呈椭圆形,5例肿瘤边缘清晰锐利,2例边缘不清,周围结构受压移位。5例密度均匀(图1a,1b),2例密度不均匀,以软组织密度为主,周边伴不同程度的低密度坏死区;1例瘤体见斑点状钙化灶;病灶均有轻至中等均匀或不均匀强化,CT值上升18~34 HU。仅1例出现肝脏、双肺、纵隔及腹膜后淋巴结多发转移。
2.2 MRI表现4例MRI检查中,3例呈卵圆状,1例呈轻度分叶状;边界清楚3例,不清楚1例。T1WI呈均匀等或稍低信号,其中1例病灶内见小点状短T1信号,T2WI呈均匀低信号(图2a~2c)。DWI上明显扩散受限,呈高信号(图2d),其中2例信号均匀(图1c),2例信号欠均匀,欠均匀者边缘见小斑片状T1WI低信号,T2WI高信号区。4例病变T2WI均可见条带状更低信号薄分隔,增强扫描强化程度高于肿瘤其他实质部分(图2e),其中2例分隔较多,部分分隔相交。
2.3 其他表现9例中,伴鞘膜积液4例,附睾受侵1例,白膜穿破1例,其中较大者压迫同侧精索致使精索静脉曲张。
3 讨论
精原细胞瘤占睾丸生殖细胞瘤的50%[1],青壮年男性多见,绝大多数单侧发病。其发病可能与隐睾、种族、家族史、微钙化、不育及环境等因素有关,隐睾是最常见的危险因素之一,未经手术更正或青春期后更正的隐睾发生睾丸肿瘤的危险上升8倍[3]。本组24~65岁,平均43.6岁,均单侧发病,其中左侧4例,右侧5例,均位于睾丸,无发生于隐睾基础上病例。
3.1 病理学特点精原细胞瘤典型的组织学表现为均一的肉质性肿块,呈局限性,边界清楚,常伴随小的中心性出血坏死和(或)囊变等。精原细胞瘤一般生长在细胞巢内,其内见薄的纤维隔膜分隔,隔膜内可见显著易变的淋巴细胞,细胞形态单一,具有丰富的透明胞浆,细胞核较大(一般不具有多型性),多呈圆形,内常包括明显渗出的核仁,此外常有淋巴细胞炎症。免疫组化染色显示SALL4和约50%的患者c-kit阳性,NUT、GAGE7及NY-ESO-1发现具有更高的敏感度及特异性[4]。
3.2 CT表现CT平扫呈相对均匀等或稍低密度,边界多清晰,这可能与睾丸坚韧的白膜包裹起到限制肿瘤向周围侵犯的作用有关[5],肿块内可出现囊变、坏死,钙化较少见,增强扫描病变呈轻至中度强化。本组7例CT检查示5例肿瘤边缘清晰锐利,2例边缘不清;5例密度均匀,2例不均匀,以软组织密度为主,周边伴不同程度的低密度坏死囊变区;1例瘤体内见斑点状钙化灶,密度不均肿块的囊变坏死区位于病灶外周,而实质区密度较均匀。增强扫描示肿瘤均呈轻中度强化,与文献[6]报道一致,但未见明显分隔样强化。笔者认为可能与本组例数较少、CT对软组织分辨力较MRI低或与扫描层距、病灶中分隔的走行方向相关。
3.3 MRI表现MRI对精原细胞瘤内部薄分隔的显示较CT有明显优势,MRI主要表现为肿瘤呈卵圆状或浅分叶状实性肿块,边界多清晰,较大者可伴出血、囊变或坏死等。肿瘤实质T1WI常呈等或稍低信号,低于健侧正常睾丸组织,伴出血时可呈小点状短T1高信号;T2WI呈均匀低信号,与正常睾丸组织高信号形成明显对比;DWI上明显扩散受限,呈高信号。增强扫描肿瘤轻度强化,内薄的纤维血管分隔强化程度高于其他实质部分[7]。Tsili等[8]指出,精原细
胞瘤T2WI常表现为均匀低信号,而其内纤维血管分隔呈带状更低信号;增强扫描纤维血管分隔强化程度高于肿瘤其他实质部分是其特征性表现。本组4例MRI表现与文献[7-8]报道一致,纤维血管分隔的显示具有特征性表现,均准确诊断。
3.3 鉴别诊断需与以下疾病鉴别:①睾丸淋巴瘤,好发于60岁以上的老年人,MRI表现为患侧睾丸肿大、类圆形肿块,T1WI、T2WI呈均匀稍低信号,增强扫描呈轻度均匀强化[9],内无分隔,坏死囊变较少;精原细胞瘤则好发于青壮年,常发生于隐睾基础上,内见带状分隔,增强扫描强化程度较前者稍高。②睾丸良恶性畸胎瘤,常可见脂肪、钙化等混杂信号或密度,与睾丸精原细胞瘤明显不同。③睾丸胚胎癌侵袭性更强,肿瘤边界往往不清,睾丸包膜多有侵犯,增强扫描呈明显不均匀强化。④睾丸转移瘤,常有原发病灶病史。⑤表皮样囊肿,呈椭圆形边界清楚的低密度影,增强扫描无强化,MRI信号均匀,T1WI呈稍低信号,T2WI呈高信号,增强扫描无强化。⑥睾丸炎症,常伴明显的泌尿系感染症状,影像学表现为睾丸弥漫性肿大,伴鞘膜积液。⑦若睾丸、附睾病变伴钙化或肾、输尿管结核,则有助于睾丸结核的诊断。
总之,睾丸肿块如密度或信号均匀,边界清楚,尤其MRI显示卵圆状或浅分叶状肿块,T2WI呈均匀低信号,DWI呈高信号,内见条带状更低信号分隔,增强扫描时其强化程度高于肿瘤其他实质部分,AFP阴性时,高度提示睾丸精原细胞瘤可能。
[1]Howitt BE,Berney DM,Daniel M,et al.Tumors of the testis:morphologic features and molecular alterations[J].Surg Pathol Clin,2015,8:687-716.
[2]SEER Cancer Statistics review,1975-2011[ED/OL].[2014-12-17]. http://Seer.cancer.gov/archive/csr/1975-2016.
[3]Wood HM,Elder JS.Cryptorchidism and testicular cancer:separating fact from fiction[J].J Urol,2009,181:452-461.
[4]Kao CS,Badve SS,Ulbright TM.The utility of immunostaining for NUT,GAGE7 and NY-ESO-1 in the diagnosis of spermatocytic seminoma[J].Histopathology,2014,65:35-44.
[5]Pohl HG,Shukla AR,Metcalf PD,et al.Prepubertal testis tumors:actual prevalence rate of histological types[J].J Urol,2004,172:2370-2372.
[6]王亮,张雪峰,王琦.睾丸精原细胞瘤的MRI诊断与鉴别诊断[J].中国中西医结合影像学杂志,2015,13(2):126-128,131.
[7]郭本树,吴耀贤,杨长俊,等.睾丸精原细胞瘤的低场MR诊断[J].临床放射学杂志,2008,27(11):1520-1522.
[8]Tsili AC,Tsampoulas C,Giannakopoulos X,et al.MRI in the histologic characterization of testicular neoplasms[J].AJR Am J Roentgenol,2007,189:331-337.
[9]王夕富,张贵祥,李康安,等.睾丸原发性淋巴瘤的CT及MRI表现(附5例报告)[J].实用放射学杂志,2010,26(8):1144-1147.
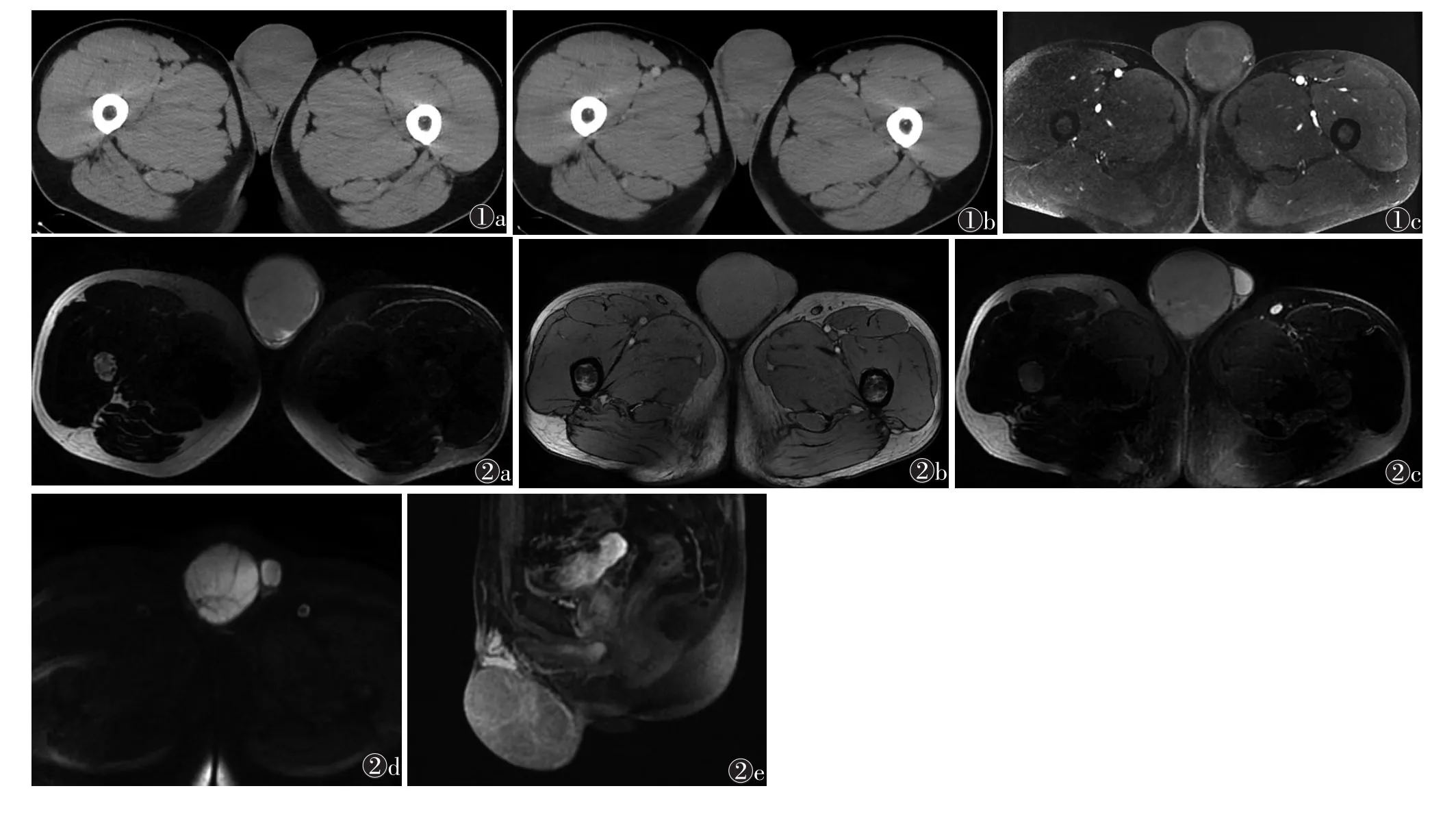
图1 男,40岁,左侧睾丸精原细胞瘤图1aCT平扫示左侧睾丸见卵圆形软组织密度影,边界清晰,密度均匀图1bCT增强扫描动脉期示睾丸卵圆形软组织密度影轻度均匀强化图1c MRI增强扫描示睾丸肿块边界清晰,轻度强化,内见分隔明显强化图2男,50岁,右侧睾丸精原细胞瘤图2aT1WI同相位示右侧睾丸卵圆形等信号肿块(与健侧对比),信号欠均匀,边界清楚,内似可见更低信号分隔图2bT1WI反相位示睾丸信号未见明显改变图2cT2WI示睾丸肿块呈低信号(明显低于健侧)图2d DWI示肿块弥散受限呈高信号,内较多分隔呈低信号图2e压脂矢状位增强扫描示睾丸轻中度强化,其内分隔明显强化
2016-01-10)
10.3969/j.issn.1672-0512.2016.06.034
吕国士,E-mail:lament-378@163.com。

