替米考星微囊的体外释放特性考察
梁劲康,吴志玲,黎乃添,吴广辉,张桂君
(广东温氏大华农生物科技有限公司,广东云浮,527400)
替米考星微囊的体外释放特性考察
梁劲康,吴志玲,黎乃添,吴广辉,张桂君*
(广东温氏大华农生物科技有限公司,广东云浮,527400)
为考察替米考星微囊在磷酸盐缓冲液(pH=6.8)中的释放特性,采用篮法进行替米考星微囊的体外释放试验,并与市售制剂进行比较,进而对替米考星微囊的释药模型进行拟合。结果表明,市售替米考星微囊中的药物在1 h时几近释放完全;而自制替米考星微囊样品1和样品2药物可缓释至4 h,样品3的药物累积释放率在4 h时才达到50%。模型拟合结果表明,自制替米考星微囊的体外释药曲线与Ritger-Peppas方程拟合度最好。自制的替米考星微囊表现出一定的缓释作用,而且药物释放符合Ritger-Peppas方程,为后续的临床试验研究和临床上药物的使用提供了一定的参考价值。
替米考星;微囊;缓释;体外释放
替米考星(Tilmicosin)是美国礼来公司于20世纪80年代开发的大环内酯类抗生素,具有同其他大环内酯类药物相似的抗菌活性,对所有的革兰阳性菌、部分革兰阴性菌和螺旋体等均有一定的抑制作用,对胸膜肺炎放线杆菌、巴氏杆菌及畜禽支原体的抗菌效果甚至优于泰乐菌素[1]。临床上主要用于治疗山羊、奶牛、猪、鸡等动物的感染性疾病,尤其在治疗畜禽呼吸道疾病方面效果尤为显著[2]。但是,替米考星味道极苦,适口性差,对猪的采食量影响极大,难以保证动物体内的药物浓度,影响用药效果[3]。因此,如何提高替米考星的适口性和延长替米考星的药效成为了目前急需解决的难题。本课题组在前期的研究中通过微囊技术将替米考星与相应的药用辅料制得替米考星微囊。该替米考星微囊不仅能够在很大程度上掩盖替米考星的苦味,而且还能够延缓替米考星的释放,显著延长其药效并使其血药浓度能够趋于稳定,从而提高其生物利用度。在上述研究的基础上,为考察替米考星微囊的体外释药特性,参照《中国兽药典》(2015年版)第一部附录溶出度测定法的第一法[4]进行替米考星微囊的体外释放试验,并对其释药曲线进行模型拟合,以期为后续替米考星微囊的临床试验研究和临床使用提供一定的参考价值。
1 材料与方法
1.1 仪器 Waters e2695高效液相色谱系统配置2489 UV/Vis检测器(美国Waters公司);CPA225D型电子天平(德国Sartorius公司);Milli-Q超纯水仪(美国Millipore公司);基本型磁力搅拌器(德国IKA公司);ZRS-8GD智能溶出试验仪(天津天大天发科技有限公司);PHS-3C pH计(上海雷磁仪器厂);SHZ-D(Ⅲ)循环式真空泵(巩义市予华仪器有限责任公司);KQ-100E型超声波清洗器(昆山市超声仪器有限公司)。
1.2 试药 磷酸替米考星(含量为80.9%,宁夏泰瑞制药有限公司);磷酸替米考星对照品(含量为93.9%,中国兽医药品监察所,批号:K0311407);替米考星预混剂A(市售替米考星微囊A,A公司产品,批号:20150123);替米考星预混剂B(市售替米考星微囊B,B公司产品,批号:16012801);三种自制替米考星微囊(批号分别为20161005-1、20161005-2和20161005-3);乙腈和四氢呋喃(色谱纯,德国Merck公司);其余试剂均为分析纯。
1.3 分析方法的建立
1.3.1 色谱条件 参考《中国兽药典》(2015年版)第一部替米考星预混剂的含量测定方法[5],选择Waters XBridge TMC18(4.6 mm×150 mm,5 μm)为色谱柱;以水-乙腈-磷酸二丁胺溶液-四氢呋喃(805∶115∶25∶55)为流动相;流速1.0 mL/min;柱温为25 ℃;检测波长为280 nm;进样量为10 μL。理论塔板数按替米考星顺式峰计算不得低于3000,而且替米考星的顺式和反式异构体峰的分离度应满足要求,两种异构体峰的相对保留时间应分别为1.0、0.9 min。
1.3.2 专属性试验 分别取空白磷酸盐缓冲液(pH=6.8)、磷酸替米考星对照品溶液(0.5 mg/mL)以及替米考星微囊提取液(0.5 mg/mL),按1.3.1项下的色谱条件进样分析,记录色谱图。
1.3.3 标准曲线的制备 精密称取0.01258 g磷酸替米考星对照品,置于25 mL棕量瓶中,加入5 mL 乙腈,超声处理使药物全部溶解。待溶液冷却至室温后,用磷酸溶液(pH=2.5)稀释至刻度,摇匀,作为对照品母液。精密移取一定体积的磷酸替米考星对照品母液于10 mL的棕量瓶中,磷酸溶液稀释定容,摇匀,配得一系列质量浓度的混合对照品溶液后,按1.3.1项下的色谱条件进样,测定替米考星顺式和反式异构体的峰面积。
1.3.4 精密度试验 分别精密移取一定体积的1.3.3项下的对照品母液,用磷酸溶液稀释成低、中、高3种浓度。该3种溶液按1.3.1项下的色谱条件连续重复进样5针,记录替米考星两种异构体的峰面积之和。
1.3.5 稳定性试验 取同一磷酸替米考星对照品溶液,分别于0、2、4、6、8、12、16、18、24 h按1.3.1项下的色谱条件进样,记录替米考星两种异构体的峰面积之和。
1.3.6 回收率试验 精密移取一定体积的低、中、高3种磷酸替米考星对照品溶液于一定体积的已知浓度的替米考星微囊提取液中,每一浓度平行制备三份,混合均匀后,按1.3.1项下的色谱条件进样,记录峰面积,依据标准曲线计算加样回收率。
1.3.7 最低检测限和定量限 分别精密移取一定体积的磷酸替米考星对照品溶液,利用磷酸溶液进行逐级稀释。稀释液按1.3.1项下的色谱条件进样分析。以信噪比(S/N)≥3的检测量为最低检测限,以信噪比(S/N)≥10的检测量为定量限。
1.4 替米考星微囊的含量测定 利用不同比例的相同辅料与替米考星原料药制备三种规格为20%(W/W)的替米考星微囊。参考《中国兽药典》(2015年版)第一部中替米考星预混剂的含量测定方法[5],对市售及自制替米考星微囊的药物含量进行测定:精密称定约1.25 g替米考星微囊,置于50 mL棕量瓶中,加入40 mL提取溶液后,进行超声处理10 min。待冷却至室温,提取液定容至刻度。上述溶液用滤纸滤过,精密移取1 mL续滤液于10 mL棕量瓶中,磷酸溶液定容至刻度,摇匀。稀释液经0.45 μm的滤膜滤过后,按1.3.1项下的色谱条件进样分析。
1.5 替米考星微囊的体外释放试验 参考《中国兽药典》(2015年版)第一部附录溶出度测定法[4],考察替米考星微囊在磷酸盐缓冲液(pH=6.8)中的体外释放行为。为了保持漏槽条件,精密称取2.25 g替米考星微囊,置于溶出篮中,在以900 mL磷酸盐缓冲液(pH=6.8)为释放介质、温度为(37±0.5)℃、转速为75 r/min的条件下进行实验。分别于5 min、10 min、15 min、 30 min、45 min、1 h、1.5 h、2 h和4 h时,精密移取1 mL样品溶液,并补加同体积同温度的释放介质。样品溶液经0.45 μm的滤膜滤过,取适量续滤液按1.3.1项下的色谱条件进样分析,记录峰面积,根据1.3.3项下的标准曲线计算替米考星的浓度,然后按下式计算各时间点的累积释放率Q,并绘制体外释药曲线。
式中,Q:替米考星微囊的累积释放率,%;Vs:取样体积(1mL);V0:释放介质体积(900mL);Ci:第i次取样时释放液中替米考星的药物浓度,μg/mL;Md:替米考星微囊中药物的质量,μg;n:取样次数。
2 结果与分析
2.1 专属性试验 替米考星专属性试验结果见图1~图3。由图中可以看出,空白溶液在该色谱条件下并不会干扰替米考星的色谱峰,而且替米考星的顺式和反式异构体的出峰时间分别为6.0min和5.2min,两种异构体峰分离度良好,均符合要求。
2.2 标准曲线的制备 利用1.3.1项下的高效液相色谱方法测得磷酸替米考星对照品顺式和反式异构体的峰面积后,以替米考星的质量浓度C为纵坐标,顺式和反式异构体的峰面积之和A为横坐标,进行线性回归,结果表明替米考星在5~500μg/mL范围内线性关系良好,回归方程为A=10498C-4128.5(R2=1)。
2.3 精密度试验 以低、中和高三种浓度替米考星顺式和反式异构体的峰面积之和计算,RSD分别为0.03%、0.08%和0.19%,符合方法学要求。
2.4 稳定性试验 同一浓度替米考星对照品溶液在不同时间点进样,以顺式和反式异构体的峰面积之和计算,RSD为1.39%,表明替米考星溶液在24h内稳定性良好,符合方法学要求。
2.5 回收率试验 低、中和高三种浓度的加样回收率分别为101.33%±0.42%、102.02%±0.34%和98.77%±0.10%,RSD分别为0.34%、0.27%和0.09%,均符合方法学要求。
2.6 检测限和定量限 通过实验测得,以替米考星顺式异构体峰的信噪比计算,替米考星的最低检测限可达1.0μg/mL,定量限可达3.0μg/mL。
2.7 替米考星微囊的含量测定结果 替米考星微囊的含量测定结果可见表1。由表中结果可知,该方法能够将市售及自制替米考星微囊中的药物提取完全。除了自制样品1 的药物含量稍高外,市售及自制替米考星微囊中的药物含量均符合要求,而且市售及自制替米考星微囊中的药物分布也比较均匀。

图1 空白溶液高效液相色谱图Fig 1 HPLC of blank solution

图2 磷酸替米考星对照品溶液高效液相色谱图Fig 2 HPLC of Tilmicosin phosphate standard solution
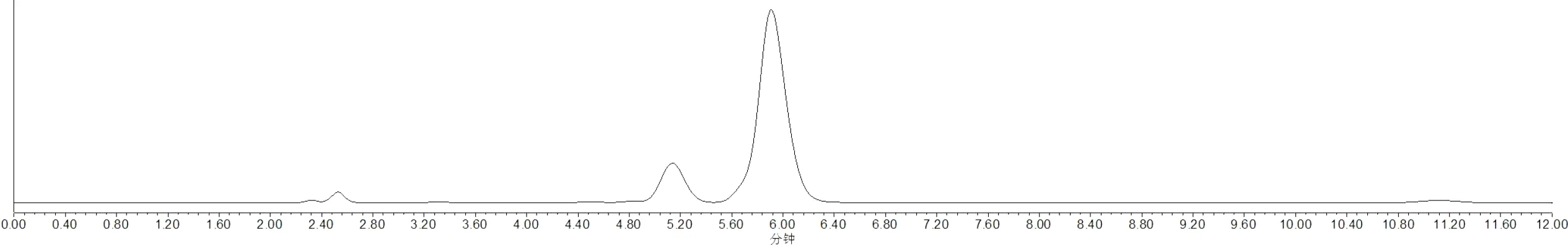
图3 替米考星微囊提取液高效液相色谱图Fig 3 HPLC of the Tilmicosin microcapsule extract
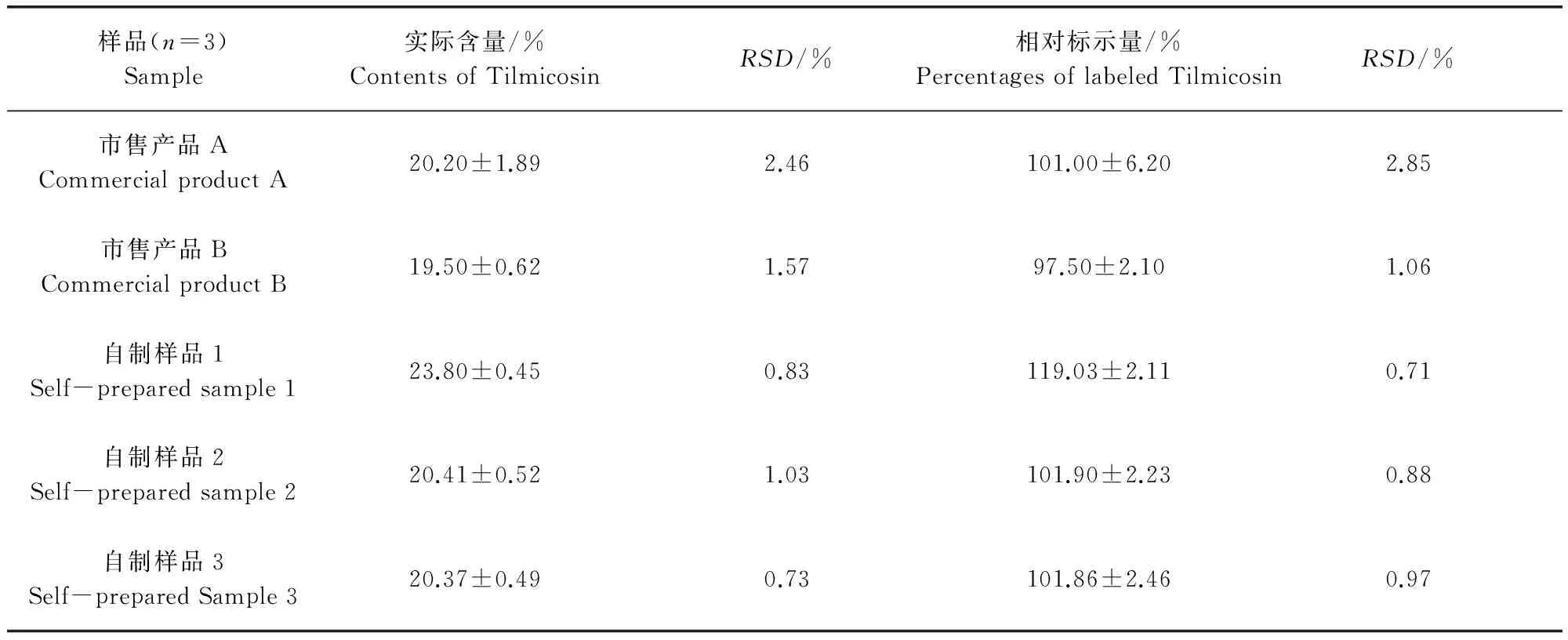
样品(n=3)Sample实际含量/%ContentsofTilmicosinRSD/%相对标示量/%PercentagesoflabeledTilmicosinRSD/%市售产品ACommercialproductA20.20±1.892.46101.00±6.202.85市售产品BCommercialproductB19.50±0.621.5797.50±2.101.06自制样品1Self-preparedsample123.80±0.450.83119.03±2.110.71自制样品2Self-preparedsample220.41±0.521.03101.90±2.230.88自制样品3Self-preparedSample320.37±0.490.73101.86±2.460.97
2.8 替米考星微囊的体外释放试验测定结果
替米考星微囊的体外释放曲线可见图4。由图可知,两种市售替米考星微囊在开始阶段迅速释放至介质中,30 min时两种替米考星微囊的累积释放率已经达到80%以上,并没有表现出明显的缓释作用;此后药物的释放趋于平缓,至1 h时基本释放完全。而自制替米考星微囊样品则均表现出了一定的缓释效果:样品2在前1 h内药物释放相对较快,在1 h时累积释放率已经达到了50%;而样品1和样品3的药物释放相对较缓慢,累积释放率分别为35%和26%。随后,样品1和样品2的药物释放曲线开始趋于一致。在4 h时,样品1和样品2的药物也已经基本释放完全,累积释放率达到90%左右。而样品3中的药物在1 h后仍能保持缓慢释放的效果,至4 h时,累积释放率才达到50%,表现出良好的缓释效果。
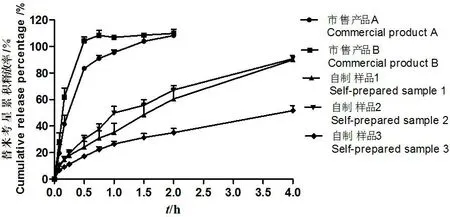
图4 替米考星微囊的药物体外释放曲线Fig 4 In-vitro release profile of Tilmicosin from Tilmicosin microcapsules
为了进一步阐明自制替米考星微囊的体外释药特性,在上述结果的基础上继续对样品1和样品3的体外释药曲线进行拟合。分别采用零级模型、一级模型、Higuchi方程、Ritger-Peppas方程、Hixson-Crowell方程和Neibergull方程进行模型拟合,计算残差平方和(sum of squares of residues,SSR)及调整决定系数(adjusted coefficient of determination,R2adjusted),作为模型拟合相似度的判据(表2)。SSR越小,R2adjusted越接近1,药物释放曲线与对应方程的拟合效果越佳[6]。由表2可见,样品1和样品3替米考星微囊的体外释药曲线均与Ritger-Peppas方程拟合度最好,其拟合方程分别为lnQ=0.5436lnt-0.9494(R2=0.9991)和lnQ=0.5391lnt-1.3876(R2=0.9973)。
3 讨论与小结
除了改善替米考星的适口性外,延缓替米考星的释放从而延长其药效也是替米考星制剂的研究目标之一,也是难点之一。目前已有报道的替米考星制剂包括纳米乳[2]、肠溶微囊[3,7]和纳米粒[8]等,这些制剂均能够在一定程度上延缓替米考星的释放而提高其生物利用度,但纳米粒和纳米乳等制剂工艺繁琐复杂,难以规模化生产。市售的两种替米考星微囊虽然能够在很大程度上掩盖替米考星的苦味,然而其也仍未能达到理想的缓释效果。因此,在上述基础上对替米考星缓释微囊开展了一系列研究工作,优化了替米考星微囊的制备工艺。与市售替米考星微囊相比,自制的替米考星微囊表现出了较好的缓释效果。
药物的释放模型有零级方程、一级方程、Higuchi方程和Ritger-Peppas方程等多种。其中,Ritger-Peppas方程是可降解体系药物释放规律的经验方程,符合Ritger-Peppas方程的释放也是比较常见的缓释模式。在Ritger-Peppas方程(lnQ=nlnt+k,k为常数项)中,n作为释放常数,是表征释放机制的特征参数,而且也与制剂的形状密切相关。对于球体制剂,当n<0.43时,药物的释放主要是Fick 扩散;当0.43
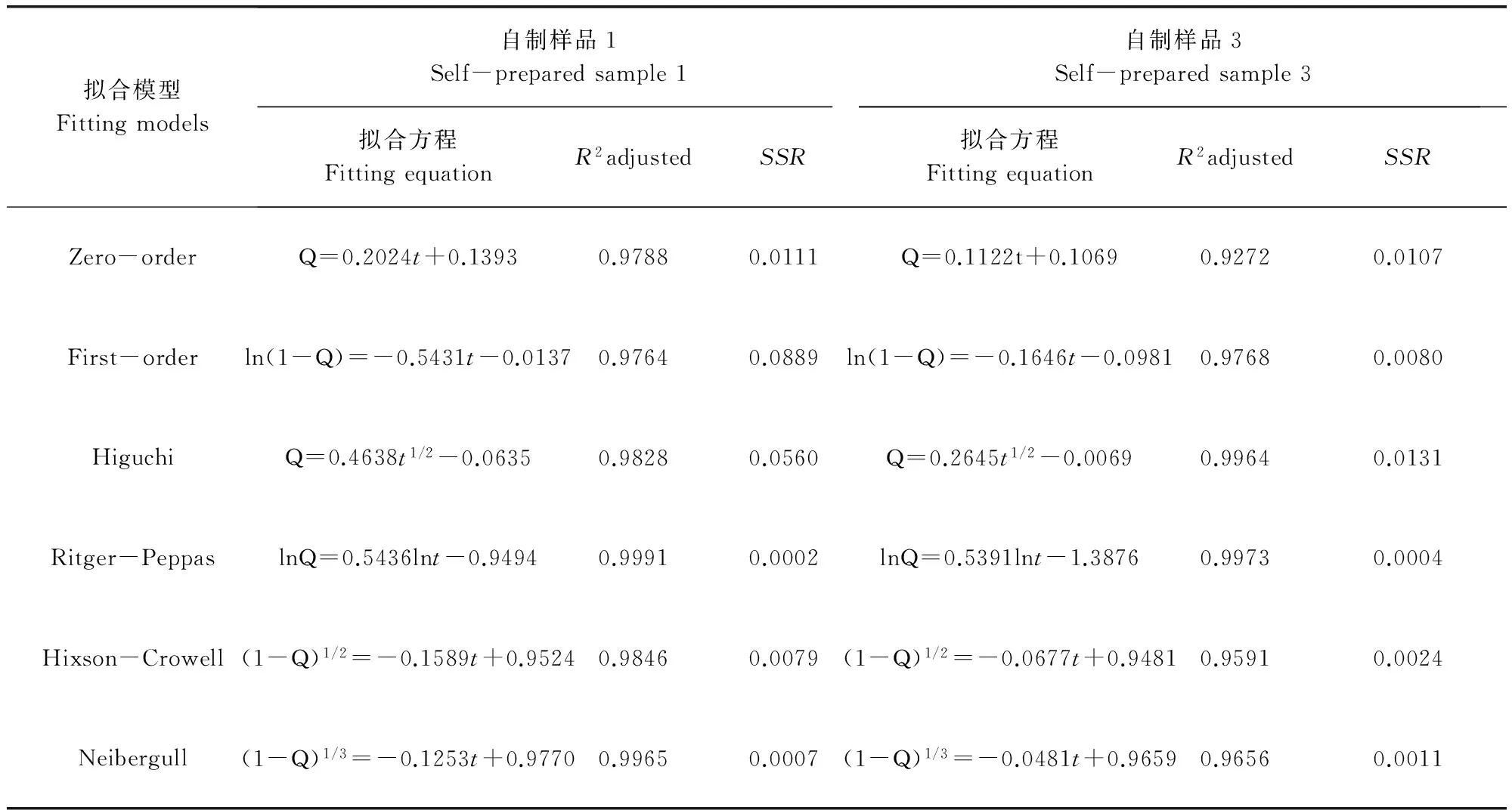
表2 替米考星微囊药物体外释放性能拟合方程Tab 2 Fitting equations of in-vitro release of Tilmicosin from Tilmicosin microcapsules
在释放度的试验中,由于包封于微囊浅表层的药物分子可以较快地脱离微囊而扩散进入释放介质中,因此,自制替米考星微囊在前1 h出现较快释放。随后的过程中,药物的释放较1 h前稍缓慢,这主要是因为载体材料在释放介质中被溶蚀,载体包载的药物分子游离出来并溶解于溶剂后再扩散进入介质中,而这一过程相对缓慢。虽然三种自制替米考星微囊使用了相同的两种辅料,但是不同比例的两种辅料对替米考星的溶出特性也表现出了较明显的差异:当该两种辅料以制剂1和2的比例使用时,其组成的载体体系更易于发生溶蚀而利于药物扩散进入介质;而当该两种辅料以制剂3的比例使用时,其组成的载体体系在水溶液中更稳定,能够有效延缓替米考星的释放而提高其生物利用度。
本文采用篮法考察了替米考星微囊的体外释药特性,证实了替米考星微囊具有一定的缓释效果,且其释药过程符合Ritger-Peppas释放模型,从而为后续的临床试验研究和使用奠定了基础。
[1] 江海洋,沈建忠,胡顶飞. 兽用抗菌药物替米考星[J]. 中国兽药杂志,2002,36(8):28-31.
Jiang H Y, Shen J Z, Hu D F. Veterinary Antibiotics of Tilmicosin[J]. Chinese Journal of Veterinary Drug, 2002, 36(8): 28-31.
[2] 胡帅. 复方替米考星纳米乳的制备及其药效学研究[D]. 陕西:西北农林科技大学,2010.
Hu S. Preparation of Compound Tilmicosin and Trimethoprim Lactate Nanoemulsion and Its Pharmacodynamics[D]. ShanXi: Northwest Agriculture and Forestry University, 2010.
[3] 陈宝妮,冯宝仪,李美娣,等. 替米考星肠溶微丸的质量评价[J]. 中国兽药杂志,2010,44(5):18-20.
Chen B N, Feng B Y, Li M T,etal. Quality Evaluation of Enteric Pellets of Tilmicosin[J]. Chinese Journal of Veterinary Drug, 2010, 44(5): 18-20.
[4] 中国兽药典委员会. 中华人民共和国兽药典 2015年版第一部附录[S].
Commission of Chinese Veterinary Pharmacopoeia. People's Republic of China Veterinary Pharmacopoeia 2015 Appendix of the First Edition[S].
[5] 中国兽药典委员会. 中华人民共和国兽药典 2015年版第一部[S].
Commission of Chinese Veterinary Pharmacopoeia. People's Republic of China Veterinary Pharmacopoeia 2015 the First Edition[S].
[6] 吴得天,梁劲康,胡巧红. 羟基喜树碱/GA-PEI-PLGA纳米粒的体外释放特性考察[J]. 食品与药品,2016,18(1):30-34.
Wu D T, Liang J K, Hu Q H. Study oninvitroRelease Behavior of Hydroxycampothecin Loaded GA-PEI-PLGA Nanoparticles[J]. Food and Drug, 2016, 18(1): 30-34.
[7] 韩萌萌,李沙沙,孙朋超,等. 替米考星肠溶微丸的制备及其评价[J]. 中国兽药杂志,2014,48(2):34-38.
Han M M, Li S S, Sun P C,etal. Preparation and Evaluation of Tilmicosin Enteric Coated Pellets[J]. Chinese Journal of Veterinary Drug, 2014, 48(2): 34-38.
[8] 杜昌余,王洪光,林卫瑞,等. 替米考星Eudragit L100纳米粒的制备及体外评价[J]. 中国抗生素杂志,2013,38(11):848-852.
Du C Y, Wang H G, Lin W R,etal. Preparation of Tilmicosin-Eudragit L 100-Nanoparticles and Its Characteristicsinvitro[J]. Chinese Journal of Antibiotics, 2013, 38(11): 848-852.
[9] 刘洪泽,齐民,魏志勇,等. 本体溶蚀型药物传输系统的数学模型[J]. 中国组织工程研究与临床康复,2009,13(52):10340-10344.
Liu H Z, Qi M, Wei Z Y,etal. Mathematical models for bulk erosion type drug delivery systems[J]. Journal of Clinical Rehabilitative Tissue Engineering Research, 2009, 13(52): 10340-10344.
(编辑:侯向辉)
Study oninvitroRelease Behavior of Tilmicosin Microcapsules
LIANG Jing-kang, WU Zhi-ling, LI Nai-tian, WU Guang-hui, ZHANG Gui-jun*
(Guangdong Wenshi Dahuanong Biotechnological Co Ltd., Yunfu, Guangdong 527400, China)
ZHANG Gui-jun, E-mail: lczgj1987@163.com
Theinvitrorelease behavior of tilmicosin microcapsules was investigated in phosphate buffer solution (pH=6.8) and compared with that of two kinds of commercial tilmicosin microcapsules. The release model of tilmicosin microcapsules was also fitted. The drug of commercial tilmicosin microcapsules was almost totally released at 1 h. But the drug release of sample 1 and 2 of self-prepared tilmicosin microcapsules could sustained to 4 h, and the cumulative release percentage of sample 3 was about 50% after 4 h. And the release profile of self-prepared tilmicosin microcapsules conformed to Ritger-Peppas equations. In conclusion, the self-prepared tilmicosin microcapsules exhibited sustained release effect, and the release profile conformed to Ritger-Peppas equation. These results can provide a reference to the future clinical study and use of the self-prepared tilmicosin microcapsules.
tilmicosin;microcapsule;sustained-release;invitrorelease
10.11751/ISSN.1002-1280.2017.5.09
广东省战略性新兴产业核心技术攻关项目(20120214)
梁劲康,硕士,从事兽药新剂型与新技术研究。
张桂君,E-mail: lczgj1987@163.com
2016-12-08
A
1002-1280 (2017) 05-0041-07
S859.796

