高效液相色谱法测定头花蓼冻干粉中槲皮素和槲皮苷的含量*
曹 芳,段 萍,王洪平,张友波,谭 辉,杨秀伟△
(1.黔南州民族医学高等专科学校基础医学部,贵州都匀 558000; 2.黔南州食品药品检验所,贵州都匀 558000;3.北京大学药学院天然药物及仿生药物国家重点实验室,北京 100191;4.黔南州中医医院普外科,贵州都匀 558000)
高效液相色谱法测定头花蓼冻干粉中槲皮素和槲皮苷的含量*
曹 芳1,段 萍2,王洪平3,张友波3,谭 辉4,杨秀伟3△
(1.黔南州民族医学高等专科学校基础医学部,贵州都匀 558000; 2.黔南州食品药品检验所,贵州都匀 558000;3.北京大学药学院天然药物及仿生药物国家重点实验室,北京 100191;4.黔南州中医医院普外科,贵州都匀 558000)
目的 建立测定头花蓼冻干粉中槲皮素、槲皮苷的含量测定方法。方法 采用高效液相色谱(HPLC)法测定头花蓼冻干粉中槲皮素、槲皮苷的含量。结果 槲皮素在0.020 9~0.157 0 μg内呈良好的线性关系,r=1.000 0,平均回收率为101.49%,RSD为1.93%;槲皮苷在0.368~2.760 μg内呈良好的线性关系,r=0.999 9;平均回收率为98.87%,RSD为2.46%。结论 该方法测定头花蓼冻干粉中槲皮素、槲皮苷的含量,结果准确,重复性、稳定性较好。
蓼科;色谱法,高压液相;头花蓼;槲皮素;槲皮苷;高效液相色谱
头花蓼又名石莽草、四季红、红酸杆等,属于蓼科、蓼属、头状蓼组多年生草本植物,全草入药[1]。多用于治疗泌尿系统疾病[2]。有关头花蓼的化学成分主要有黄酮类、酚酸类、挥发油、有机酸等[3-9]。自李勇军等[3]从头花蓼中分离鉴定了槲皮素、槲皮苷、陆地棉苷、槲皮素-3-o-(2′′-没食子酰基)-鼠李糖苷后,多位学者相继从头花蓼中也分离得到了黄酮类化合物[4-6]。其中黄酮类化合物是蓼属植物中普遍存在的一种成分,具有各种生物活性[10]。本研究旨在通过建立同一条件下同时分离头花蓼药材中两种黄酮类化合物槲皮素、槲皮苷的高效液相色谱(HPLC)法,并测定其在药材中的含量,为今后研究其在动物体内的药代动力学特点提供实验依据。
1 材料与方法
1.1 材料
1.1.1 实验仪器 岛津2401紫外分光光度计,HPLC仪(Agilent1260,岛津LC-2010A),SK250LHC超声波清洗器(上海科导仪器有限公司),电子天平(梅特勒AG135、AL204)。
1.1.2 实验药物 乙腈(色谱纯),水为娃哈哈纯净水;槲皮苷(对照品批号为111538-201105,含量92.7%)、槲皮素对照品(批号为111538-200301,含量97.3%),均由中国药品生物制品检定所提供。头花蓼冻干粉由头花蓼全草的70%的醇提液冷冻干燥而得,作为供试样品。头花蓼全草采于贵州省黔东南州施秉县,由北京大学医学部药学院天然药物与仿生药物国家重点实验室杨秀伟教授鉴定为头花蓼(polygonum capitatum Buch.-Ham.ex D.Don)。
1.2 方法
1.2.1 色谱柱 Agilent ODS C18(250.0 mm×4.6 mm,5 μm);迪马Diamonsil ODS C18(250.0 mm×4.6 mm,5 μm) ,流动相为0.3%醋酸溶液(A)-乙腈(B),梯度洗脱, 0~5 min,92%~90% A;5~20 min,90%~75% A;20~40 min,75%~50% A,40~41 min,50%~92% A,41~50 min,92%A。检测波长254 nm,进样量10 μL,流 速1.0 mL/min,柱温30 ℃。理论板数以槲皮苷峰计算应不低于5 000。
1.2.2 对照品溶液 精密称取槲皮苷、槲皮素适量,加甲醇制成每毫升约含槲皮素8 μg,槲皮苷0.18 mg的溶液。
1.2.3 混合对照品溶液 精密称取槲皮素对照品10.32 mg,置50 mL量瓶中,精密量取5 mL置200 mL量瓶中,另精密称取槲皮苷对照品15.23 mg置同1个200 mL量瓶中,加甲醇溶解并稀释至刻度,制得槲皮素、槲皮苷混合对照品溶液(5.020 7、70.591 1 μg/mL)。
1.2.4 供试品溶液 取样品约0.5 g,精密称定,置具塞锥形瓶中,精密加入甲醇25 mL,玻璃珠数粒,称质量,超声0.5 h,再加热回流1.0 h,放冷,再称质量,减失的重量用甲醇补足,摇匀,滤过,取续滤液。
2 结 果
2.1 专属性考察 槲皮苷、槲皮素的紫外扫描图均在254 nm处有最大吸收。取供试品、对照品溶液各10 μL,分别注入色谱仪,按色谱条件测定,结果见图1。供试品图谱中,槲皮苷、槲皮素的保留时间与对照品图谱一致,与其相邻色谱峰的分离度均大于1.5。
2.2 线性关系的实验 精密吸取槲皮苷、槲皮素混合对照品溶液2、5、8、10、15 μL,注入液相色谱仪,按色谱条件测定,以峰面积为纵坐标,质量数为横坐标进行线性回归计算,槲皮素、槲皮苷线性回归方程为:槲皮素 A=4 247.968C+2.680,r=1.000 0;槲皮苷 A=2 981.723C+44.992,r=0.999 9。结果表明槲皮苷在0.368~2.760 μg内有良好的线性关系;槲皮素在0.020 9~0.157 0 μg内有良好的线性关系。
2.3 精密度实验 精密吸取混合对照品溶液10 μL,连续进样6次,槲皮素、槲皮苷峰面积的相对标准偏差(RSD)分别为0.74%、0.35%,结果表明此法精密度良好。
2.4 稳定性实验 取供试品溶液分别于0、4、8、12、16、24 h进样,进样量10 μL,槲皮素、槲皮苷峰面积的RSD分别为1.02%、0.71%,说明供试品溶液在24 h内具有良好的稳定性。
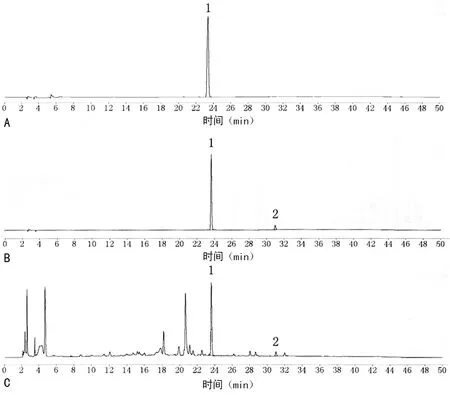
A:槲皮苷;B:槲皮苷、槲皮素混合对照品溶液;C:供试品溶液。1:槲皮苷;2:槲皮素。
图1 头花蓼冻干粉中槲皮苷、槲皮素的HPLC图谱
2.5 重复性实验 按供试品溶液制备法制备6份供试品溶液,精密吸取槲皮素、槲皮苷混合对照品溶液及供试品溶液各10 μL,按色谱条件分别测定峰面积。槲皮素、槲皮苷的平均含量分别为0.401 5、8.856 3 mg/g,RSD分别为2.75%、0.91%。
2.6 回收率实验 精密称取0.25 g样品(槲皮素、槲皮苷的平均含量分别为0.401 5、8.856 3 mg/g)6份,置具塞锥形瓶中,精密加入槲皮素、槲皮苷混合对照品溶液25 mL,玻璃珠数粒,称质量,超声0.5 h,再水浴回流1.0 h,放冷,再称质量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,进样10 μL;另取槲皮素、槲皮苷混合对照品溶液10 μL,同法测定。平均回收率分别为101.50%、98.87%;RSD分别为1.93%、2.46%,见表1。
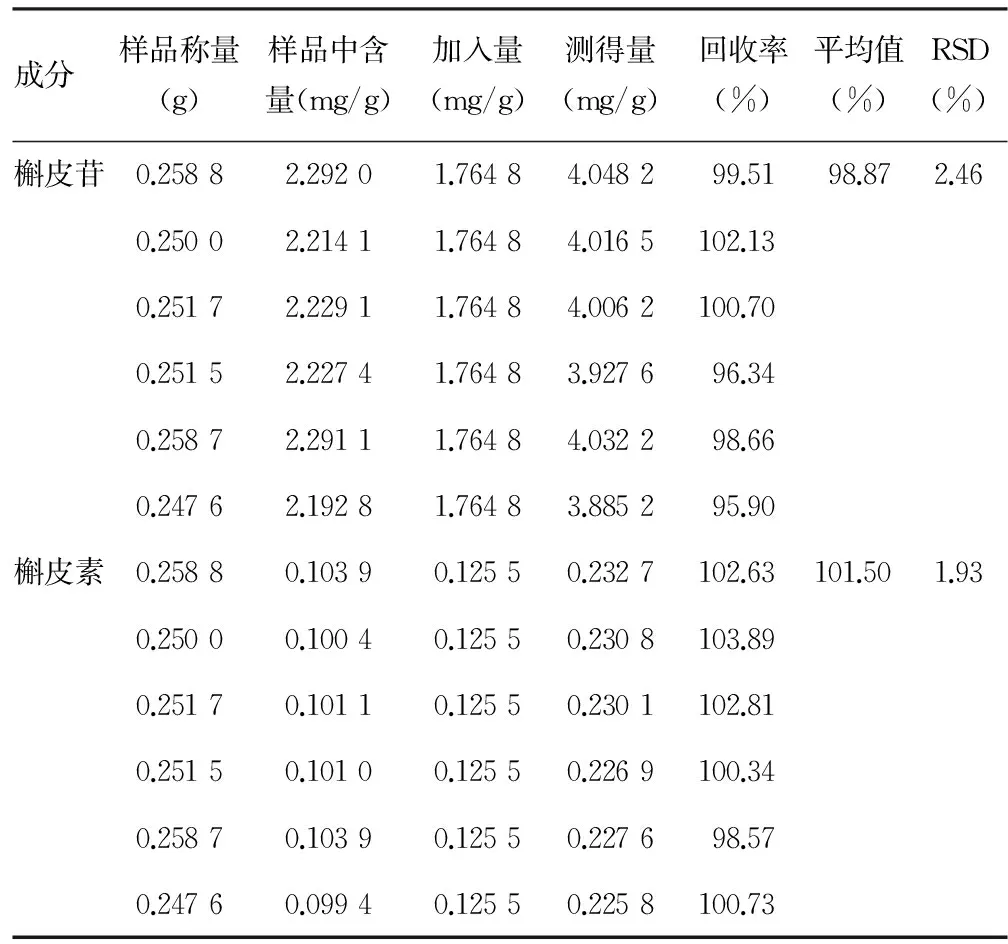
表1 头花蓼冻干粉中槲皮素、槲皮苷的回收率实验结果
2.7 样品含量测定 取不同采择时间制备的头花蓼冻干粉,编号分别为20130321、20130518,按供试品溶液制备方法制得供试品溶液,精密吸取槲皮素、槲皮苷对照品溶液及供试品溶液各10 μL,按色谱条件进行测定,分别记录峰面积。结果,20130321的样品中槲皮素、槲皮苷的含量分别为0.401 5、8.856 3 mg/g(n=3);20130518的样品中槲皮素、槲皮苷的含量分别为0.387 7、8.825 8mg/g(n=3)。
3 讨 论
头花蓼化学成分中含黄酮类化合物,黄酮类化合物有各种生物活性,它们在蓼属植物中是普遍存在的一种成分[10]。国内多位学者采用不同的方法对头花蓼中黄酮类化合物的含量进行了测定[11]。本课题组以头花蓼中的槲皮素、槲皮苷两种黄酮类化合物为指标,通过反复实验,建立了同一条件下分离测定这两种化合物含量的HPLC法。
本研究以0.3%醋酸溶液(A)-乙腈(B)为流动相梯度洗脱,使槲皮素、槲皮苷与其他组分、槲皮素、槲皮苷两者之间色谱峰均分离良好。
比较甲醇作溶剂,加热回流1.0 h、超声1.0 h及先超声0.5 h,再加热回流1.0 h,以超声0.5 h,再加热回流1.0 h所测槲皮素、槲皮苷的含量较高。
此方法的建立,对今后开展头花蓼中部分黄酮类化合物对动物体内的药代动力学特点的研究有重要意义。
[1]南京中医药大学.中药大辞典(上册)[M].2版.上海:上海科技出版社,2006:850.
[2]贾敏如,李星炜.中国民族药志要[M].北京:中国医药科技出版社,2005:479.
[3]李勇军,骆宏丰,王永林,等.头花蓼黄酮类化学成分的研究[J].中国药学杂志,2000,35(5):300-302.
[4]Xian Li,Ming Yu,Meng D,et al.A new chromone glycoside from polygonum capitatum[J].Fitoterapia,2007,78(7/8):506-509.
[5]刘志军,戚进,朱丹妮,等.头花蓼化学成分及抗氧化活性研究[J].中药材,2008,31(7):995-998.
[6]于明,李占林,李宁,等.头花蓼的化学成分[J].沈阳药科大学学报,2008,25(8):633-635.
[7]杨阳,蔡飞,杨琦,等.头花蓼化学成分的研究[J].第二军医大学学报,2009,30(8):937-940.
[8]王祥培,万德光,吴红梅.川产野生与栽培头花蓼挥发油的GC-MS分析[J].贵阳中医学院学报,2007,29(5):61-62.
[9]高玉琼,代泽琴,刘建华,等.头花蓼挥发性成分的研究[J].生物技术,2005,15(3):55-56.
[10]王开金,张颖君,杨崇仁.蓼属植物的化学成分与生物活性成分研究进展[J].天然产物研究与开发,2006,18(1):151-164.
[11]曹芳,谭辉,邓先扩.头花蓼化学成分及其黄酮类化合物含量的研究进展[J].黔南民族医专学报,2012,25(2):121-125.
10.3969/j.issn.1671-8348.2017.14.034
贵州省卫生厅科学技术基金资助(gzwkj2012-1-074)。 作者简介:曹芳(1971-),副教授,本科,主要从事中草药药效学及药动学方面研究。△
,E-mail:xwyang@bjmu.edu.cn。
R917
B
1671-8348(2017)14-1972-02
2016-11-27
2017-01-15)
——黔南州老年大学校歌

