二甲双胍与吡格列酮对多囊卵巢综合征患者性激素及代谢水平的影响▲
(陕西省延安市人民医院妇产科,延安市 716000,电子邮箱:yanliangnaa@163.com)
多囊卵巢综合征(polycystic ovary syndrome,PCOS)是一种常见的内分泌疾病,胰岛素抵抗和高胰岛素血症在PCOS的发病机制中起重要作用[1]。有研究显示,胰岛素抵抗和高胰岛素血症通过直接(诱导卵泡膜细胞产生雄激素)和间接[增加黄体生成素(luteinizing hormone,LH)分泌,降低胰岛素样生长因子结合蛋白以及激素结合球蛋白的肝脏合成]的方式升高雄激素水平[2]。胰岛素抵抗会对妊娠和生育造成不良影响,而PCOS也会增加子宫内膜癌的风险[3-4]。二甲双胍能够抑制肝脏葡萄糖的产生和脂肪生成,并增加外周葡萄糖的摄取,同时减少脂肪酸氧化。研究表明二甲双胍能降低PCOS患者的胰岛素抵抗和内分泌参数水平,是治疗PCOS最常用的药物[5]。但单独使用二甲双胍无法完全恢复PCOS患者正常的生殖功能,且许多PCOS患者对胰岛素增敏剂反应不佳。吡格列酮为过氧化物酶体增殖物激活受体γ激动剂,能够降低肝脏和外周组织的胰岛素抵抗,具有抗动脉粥样硬化和抗炎作用[6]。鉴于二甲双胍和吡格列酮在治疗胰岛素抵抗方面的具有“叠加效应”,本研究探讨二甲双胍与吡格列酮对PCOS患者性激素以及血糖、胰岛素、血脂代谢水平的影响,以期为临床PCOS的治疗用药提供参考。
1 资料与方法
1.1 临床资料 选择2015年7月至2016年12月间我院妇产科收治的66例PCOS患者,年龄(29.1±5.82)岁。纳入标准:(1)所有患者性发育正常,没有口服避孕药或抗雄激素。(2)符合PCOS诊断标准:① 月经稀发或闭经,其中月经稀发为月经周期间隔≥35 d,继发性闭经为至少6个月没有月经;② 高雄性激素血症的表现,如多毛症,痤疮和(或)血清总睾酮>0.7 μg/L;③ 超声检查显示多囊卵巢,即至少1个卵巢存在12个以上的包膜下卵泡,直径2~9 mm不等,或卵巢体积增加(>10 cm3);至少符合两种症状即可诊断为PCOS。(3)研究开始前3个月内未接受任何影响激素水平、脂蛋白或糖代谢或食欲的药物。排除标准:甲状腺功能障碍、高泌乳素血症、库欣氏综合征、雄激素分泌肿瘤、糖尿病、非经典型21-羟化酶缺乏症、自身免疫性疾病、中枢神经系统疾病、严重高血压、接受过子宫切除术、肝或肾功能异常、活动性肝病、已知患有心脏病、妊娠和哺乳期的女性。将患者按照随机数字表法分为二甲双胍组22例、吡格列酮组21例及联合用药组23例,3组一般资料差异均无统计学意义(均P>0.05),具有可比性,见表1。所有研究对象均签署书面知情同意,研究方案经我院伦理委员会批准。

表1 3组患者一般资料比较(x±s)
注:FIN为空腹胰岛素;空腹G/I比值为空腹血糖/胰岛素比值;DHEAS为硫酸脱氢表雄酮;FSH为促卵泡激素。
1.2 用药方法 二甲双胍组给予进餐时口服二甲双胍(商品名:格华止;厂家:中美上海施贵宝制药有限公司,批号:72H203003)500 mg,3次/d。吡格列酮组给予进餐时口服吡格列酮(商品名:艾可拓;厂家:武田制药,批号:0B025)30 mg,3次/d。联合用药组同时给予口服吡格列酮及二甲双胍,用法同上。3组疗程均为3个月。
1.3 观察指标 (1)治疗前及治疗后3个月,于自发性出血的早期卵泡期(第3~5天)或孕激素诱发的撤退性出血10~12 h后(隔夜)采集空腹静脉血标本5 ml,常温下1 500 r/min离心15 min,取上层血浆,用于检测LH、FSH、FBG、FIN、DHEAS、总睾酮、TC、TG、HDL-C、LDL-C水平。采用BT-3000PLUS型分析仪(意大利Biotemcnica公司)根据葡萄糖氧化酶法测定FBG;采用DiaSorin公司LIAISON®型分析仪根据化学发光免疫分析法测定空腹血清胰岛素、LH、FSH、总睾酮及DHEAS;采用BT-3000PLUS型分析仪(意大利Biotemcnica公司)根据分光光度法测定TC、TG、HDL-C及LDL-C。(2)比较3组患者治疗前及治疗后3个月的体重、体质指数(body mass index,BMI)、腰臀比及痤疮评分[7]。(3)比较3组治疗前及治疗后3个月的稳态模型评估-胰岛素抵抗(homeostatic model assessment-insulin resistance,HOMA-IR)指数及胰岛素敏感性定量检查指数(quantitative insulin sensitivity check index,QUICKI),计算公式:HOMA-IR=FIN×FBG/22.5,其中FIN、FBG的单位分别采用μU/ml、mmol/L;QUICKI=1/(FIN×FBG),FIN、FBG的单位分别采用μU/ml、mg/dl。(4)比较3组患者治疗后3个月的月经周期改善率,其中根据月经周期是否稳定判断改善情况。
1.4 统计学分析 采用SPSS 17.0软件进行统计学分析。计量资料用(x±s)表示,两组间采用配对t检验,多组间比较采用方差分析;计数资料比较采用χ2检验。P<0.05表示差异统计学有意义。
2 结 果
2.1 3组患者治疗前后体重、BMI、腰臀比比较 3组患治疗前后体重、BMI及腰臀比比较,差异均无统计学意义(均P>0.05),见表2。

表2 3组患者治疗前后体重、BMI和腰臀比比较(x±s)
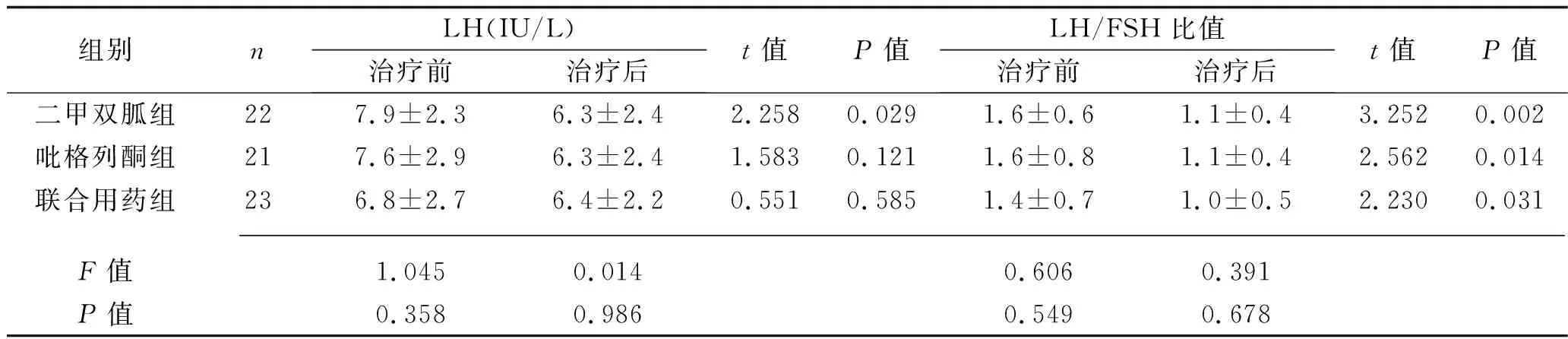
2.2 3组患者治疗前后生化指标比较 治疗后,3组FIN、HOMA-IR指数均较治疗前降低,QUICKI及空腹G/I比值均较治疗前升高(均P<0.05);吡格列酮组、联合用药组、二甲双胍组FBG依次升高,联合用药组、吡格列酮组、二甲双胍组HOMA-IR指数依次升高(均P<0.05),但3组FIN、QUICKI及空腹G/I比值比较,差异均无统计学意义(均P>0.05)。治疗前后,3组的TC、TG、HDL-C、LDL-C、DHEAS水平比较,差异均无统计学意义(均P>0.05)。治疗后,二甲双胍组总睾酮水平低于治疗前,吡格列酮组总睾酮水平均高于其他两组(均P<0.05)。治疗后,3组LH/FSH比值均低于治疗前,联合用药组FSH水平高于治疗前,二甲双胍组治疗后LH水平低于治疗前(均P<0.05);二甲双胍组、吡格列酮组、联合用药组FSH水平依次升高(均P<0.05),但3组LH/FSH比值及LH水平比较,差异均无统计学意义(均P>0.05)。见表3。

表3 3组患者治疗前后激素水平比较(x±s)

续表3

组别nHDL-C(mg/dl)治疗前治疗后t值P值TC(mg/dl)治疗前治疗后t值P值TG(mg/dl)治疗前治疗后t值P值二甲双胍组2251.1±12.152.9±11.00.5160.608215.0±36.5209.7±37.20.4770.636140.3±58.2147.0±78.90.3210.750吡格列酮组2151.1±12.552.8±12.50.4410.662185.6±51.6177.7±53.30.4880.628111.6±76.0100.9±61.80.5010.619联合用药组2352.2±12.255.7±13.20.9340.355196.0±36.6197.0±35.60.0940.926131.0±59.3114.3±78.50.8140.420 F值0.0600.4042.7353.0821.0962.242P值0.9420.6700.0730.0530.3410.118

组别nDHEAS(mg/L)治疗前治疗后t值P值总睾酮(μg/L)治疗前治疗后t值P值FSH(IU/L)治疗前治疗后t值P值二甲双胍组221.5±0.71.4±0.50.5450.5880.7±0.20.6±0.12.0980.0425.2±1.75.5±1.40.6390.526吡格列酮组211.4±0.71.6±0.60.9940.3260.7±0.10.7±0.2*0.0001.0004.7±1.25.6±2.1*1.7050.096联合用药组231.4±0.71.5±0.80.4510.6540.6±0.20.6±0.1#0.0001.0005.6±2.27.0±2.2*#2.1580.036 F值0.1500.5102.4583.6671.4314.229P值0.8610.6030.0940.0310.2470.019
组别nLH(IU/L)治疗前治疗后t值P值LH/FSH比值治疗前治疗后t值P值二甲双胍组227.9±2.36.3±2.42.2580.0291.6±0.61.1±0.43.2520.002吡格列酮组217.6±2.96.3±2.41.5830.1211.6±0.81.1±0.42.5620.014联合用药组236.8±2.76.4±2.20.5510.5851.4±0.71.0±0.52.2300.031 F值1.0450.0140.6060.391P值0.3580.9860.5490.678
注:与二甲双胍组比较,*P<0.05;与吡格列酮组比较,#P<0.05。
2.3 3组患者月经改善率及痤疮评分比较 治疗3个月后,二甲双胍组月经周期改善率为36.4%(8/22),吡格列酮组月经周期改善率为71.4%(15/21),联合用药组月经周期改善率为73.9%(17/23),3组月经周期改善率比较差异有统计学意义(χ2=8.150,P=0.017),其中联合用药组、吡格列酮组、二甲双胍组月经周期改善率依次降低(均P<0.05)。3组治疗前痤疮评分比较,差异无统计学意义(P>0.05);治疗后3组患者痤疮评分均低于治疗前,且联合用药组痤疮评分低于二甲双胍组及吡格列酮组(P<0.05),见表4。

表4 3组患者痤疮评分比较(x±s,分)
注:与二甲双胍组比较,*P<0.05;与吡格列酮组比较,#P<0.05。
3 讨 论
研究表明,二甲双胍与吡格列酮均能够明显改善PCOS患者的卵巢功能、临床特征、激素和代谢指标[8-9]。本研究结果显示,治疗后3组FIN、HOMA-IR指数均较治疗前降低,QUICKI及空腹G/I比值均较治疗前升高(均P<0.05),说明二甲双胍、吡格列酮单独或联合治疗均能改善PCOS患者的胰岛素抵抗及高胰岛素血症,而这有助于降低PCOS患者因胰岛素抵抗可能诱发的代谢综合征和心血管疾病的风险。研究表明,吡格列酮或其他类型噻唑烷二酮(thiazolidinedione,TZD)治疗能够改善PCOS患者胰岛素作用和胰岛素抵抗,但会增加体重、腰臀比和BMI,其原因可能是TZD引起胰岛素从内脏到皮下脂肪的优势转移,以及改善肝、外周组织的胰岛素敏感性[10-11]。但本研究结果显示,3组治疗前后体重、BMI及腰臀比比较,差异均无统计学意义(均P>0.05),可能与研究例数较少、观察时间较短有关。治疗后,3组患者月经周期均不同程度改善,而联合用药组与吡格列酮组月经周期改善率均高于二甲双胍组(均P<0.05),与以往研究结果相似[12-14]。因此,经TZD治疗后PCOS患者月经周期的改善可能并不是通过减轻体重来实现的。
有研究表明,PCOS患者雄激素水平升高可能是外周胰岛素抵抗所致高胰岛素血症引起的[14-15]。本研究结果显示,二甲双胍组治疗后总睾酮水平低于治疗前(P<0.05),而联合治疗组与吡格列酮组治疗前后总睾酮水平差异并无统计学意义(P>0.05),且治疗后吡格列酮组T水平均高于二甲双胍组与联合用药组(均P<0.05),这与以往的研究结果[16-17]不一致,可能是选取患者的种族及标本量有所不同导致。研究表明,二甲双胍能更有效地降低PCOS患者雄性激素水平,而吡格列酮能够更好地降低PCOS患者血清胰岛素和胰岛素抵抗[17]。在本研究中,接受吡格列酮与二甲双胍联合治疗后的PCOS患者总睾酮水平改变不明显的原因可能为:(1)二甲双胍对雄激素的产生有抑制作用;(2)吡格列酮剂量不足。Valsamakis等[18]研究发现,PCOS患者在怀孕期间继续使用二甲双胍可降低流产、妊娠糖尿病和胎儿生长受限的发生率。但罗格列酮和吡格列酮为妊娠C类药物,因此,服用这些药物的PCOS患者应采取避孕措施,并在怀孕后立即停止服用。本研究结果显示,二甲双胍组、吡格列酮组、联合用药组治疗后FSH水平依次升高(P<0.05)。
Negrotto等[19]研究发现,对二甲双胍反应不佳的PCOS患者接受吡格列酮和二甲双胍联合治疗后,胰岛素抵抗、空腹血糖、胰岛素水平和DHEAS水平显著降低,HDL-C和性激素结合球蛋白水平显著增加,月经周期改善。但Wysham等[20]的研究结果显示,对于胰岛素敏感性正常的非肥胖PCOS患者,二甲双胍与吡格列酮联合治疗的疗效并未明显优于单一药物治疗。本研究结果也显示,3组治疗前后的TC、TG、HDL-C、LDL-C、DHEAS水平比较,差异均无统计学意义(均P>0.05),说明二甲双胍与吡格列酮联合治疗对POCS患者性激素及血脂代谢的调节并不一定优于单一药物治疗。
此外,治疗后3组患者痤疮评分均低于治疗前,且联合用药组痤疮评分低于二甲双胍组及吡格列酮组(均P<0.05),提示联合用药组患者机体激素紊乱得到较大改善。
总之,二甲双胍与吡格列酮联合治疗能更好地改善PCOS患者胰岛素抵抗及月经周期;但与单一药物治疗相比,二甲双胍与吡格列酮联合治疗对PCOS患者的性激素及血脂代谢调节并无优势。本研究中存在一些缺陷,如样本量过小、药物治疗时间及随访时间短,在下一步研究中需扩大样本量,延长药物治疗时间和随访期,以评估二甲双胍和吡格列酮在PCOS患者中作用。

