纤维蛋白胶对骨再生作用的影响
吴怡蓉,谢志刚,鲍济波
(昆明医科大学附属口腔医院种植科,昆明 650000)
纤维蛋白胶(fibrin glue,FG)是在凝血级联的最后一步由凝血酶对纤维蛋白原作用后形成的天然生物聚合物。1909年,Bergel[1]首次提出了纤维蛋白可以作为止血剂使用。1940年,纤维蛋白原被Young和Medawar[2]用作周围神经吻合的黏合剂。1944年,Cronkite等[3]将牛纤维蛋白原和凝血酶混合成FG,用于皮肤移植,这是第一次提到牛凝血酶作为欧洲商业产品。到了20世纪70年代,大多数欧洲产品中都使用了病毒灭活的人凝血酶,1972年,Matras等[4]报道了用含有浓缩纤维蛋白原的FG进行神经吻合。1985年,Dresdale等[5]首次描述了用新鲜冰冻血浆和牛凝血酶混合制造FG。20世纪90年代,非商业形式的FG在美国应用广泛,直到1998年,商用FG产品第一次被美国食品药品管理局批准使用[6]。FG生物相容性、生物可降解性良好,可喷洒或滴注,且具有成胶速度快、易于操作以及粘合力中等的特性。目前,FG除在各类外科手术中用于局部止血、防止渗透、防止粘连和促进愈合外,还可作为缓释载体和骨移植材料的支架应用于骨组织工程[7-11]。现就FG对骨再生作用的影响予以综述。
1 FG的活性成分和成胶机制
1.1活性成分 FG主要由纤维蛋白原、凝血酶、凝血因子ⅩⅢ和钙离子等活性成分组成。纤维蛋白原是一种由肝脏合成的具有凝血功能的蛋白质,能够溶解于水,是凝血过程、血栓形成过程中的重要物质,相对分子量约为340 000,呈三联球形,由α、β、γ三对不同的多肽链组成,两端为D区,中间为E区,D区与E区通过3条呈α螺旋的肽链相连(图1);凝血酶是从人体或动物血液中提取的凝血酶原的蛋白水解酶,直接作用于血液凝固过程的最后一步,促使血浆中的可溶性纤维蛋白原转变为不溶的纤维蛋白,加速伤口表面血液凝固,达到速效止血的目的,而且还能促进上皮细胞的有丝分裂,加速创伤愈合,是一种速效的局部止血药[12]。凝血因子ⅩⅢ是血纤维蛋白稳定因子,在钙离子存在的情况下允许纤维蛋白交联并形成稳定不易碎的凝块,还可帮助未分化的间充质干细胞在胶的高度交联结构上向外迁移,并促进间充质干细胞增殖[13]。
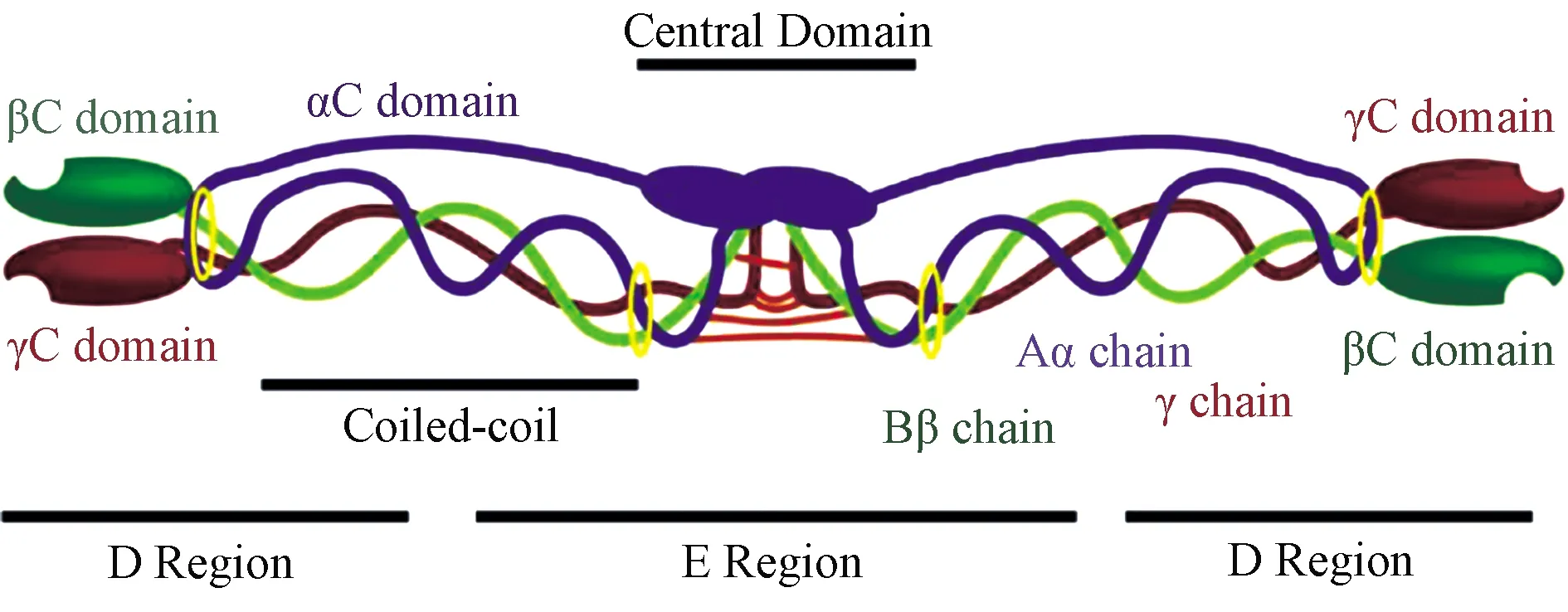
Aα chain:Aα链;Bβ chain:Bβ链;γ chain:γ链;Central Domain:中心结构域;αC domain:αC 结构域;βC domain:βC 结构域;γC domain:γC 结构域;D Region:D区;E Region:E区;Coiled-coil:卷曲螺旋
1.2成胶机制 将纤维蛋白原、凝血因子ⅩⅢ、凝血酶和钙离子等混合,模拟血液凝固过程的最后一个阶段,凝血酶断裂纤维蛋白原的2链(Aα,Bβ)而释放酸性多肽A和B,使纤维蛋白原转化为纤维蛋白单体,而各单体自发聚集成无桥键相连的多聚体;同时凝血酶激活凝血因子ⅩⅢ,激活的凝血因子ⅩⅢ在钙离子的作用下催化各纤维蛋白单体间两条γ链的谷氨酰胺残基和赖氨酸的ε-氨基形成共价键,最终形成稳定的纤维蛋白多聚体,呈一种十字交叉、多层、均匀的三维网状结构,能够网罗住红细胞及有效成分,同时也为成纤维细胞和毛细血管的爬行及生长提供了生物支架[14]。
2 FG对成骨作用的影响
骨组织工程的三大重要组成包括合适的支架、种子细胞以及生长因子等活性成分。FG具有良好的生物相容性和生物可降解性,在骨再生修复中得到广泛应用,可以用作支架材料、复合材料的涂层剂以及细胞、生长因子、基因、药物或其他生物活性分子的载体[15-17]。FG中的生长因子可以刺激和促进组织修复,与其他成分(如骨移植材料、成骨细胞和生物活性分子)联合应用时,可以改善单一材料的物理性能,提高其生物性能,对骨再生修复有积极作用。
2.1FG对细胞成骨作用的影响 FG可促进成骨过程中的成骨细胞或有成骨潜能的干细胞增殖、迁移、分化和矿化,为细胞提供初始基质,促进骨再生。Rao等[18]用纤维蛋白原和纤维蛋白处理钛植入物表面,并在体外与人成骨细胞共培养,结果发现,经处理的钛植入物的表面可促进更多的细胞增殖、黏附、基因表达和矿化。可能是纤维蛋白原和纤维蛋白的加入增强了亲水性和细胞相容性,使它们具有加速骨整合的能力。同时,有研究表明,在同样成骨诱导条件下,与骨髓间充质干细胞和磷酸盐缓冲液混合相比,骨髓间充质干细胞和FG混合诱导了更多的骨髓间充质干细胞向成骨细胞分化,获得了更好的骨再生[19]。另一方面,Woo等[20]观察到,与未添加FG相比,在硫酸钙骨水泥中添加FG可促进成骨细胞的增殖和分化,且进一步提高了硫酸钙骨水泥作为骨移植材料的可行性。另外,FG在骨再生中作为支架、载体或缓释系统,具有修复组织的能力。Perumcherry等[21]首次将纤维蛋白均匀电纺成纳米纤维,扫描电镜图像显示形成了尺寸为50~500 nm的纤维支架,且该支架支持人脐血间充质干细胞的黏附、扩散和增殖。除纤维蛋白纳米支架外,还有纤维蛋白纳米管和纤维蛋白纳米颗粒,可以通过水-肌醇乳化-扩散法制备[22]。这些结构表现出优异的抗聚集性和高温稳定性,并具有以可控方式传递生长因子和缓慢释放药物的能力。Fujioka-Kobayashi等[23]将生长因子人骨形态发生蛋白(bone morphogenetic protein,BMP)-9加入FG中与成骨细胞共培养,结果显示,FG有极好的保留人BMP-9的能力,使人BMP-9在10 d内逐渐释放,FG单一成分对成骨细胞分化的影响很小,但与人BMP-9联合运用后,碱性磷酸酶活性增强,茜素红染色增多,并且成骨细胞分化标志物碱性磷酸酶、骨唾液蛋白和骨钙素的信使RNA水平均显著升高。此外,FG还可作为药物的缓释剂。Kim等[24]利用牛骨粉和FG制备了一种载血管紧张素的支架,评估支架的结构、形态和力学性能以及血管紧张素的体外释放曲线,结果显示,骨粉在支架内均匀分布,血管紧张素在25 d内持续释放,且释放的血管紧张素可刺激细胞增殖和黏附,无细胞毒性。综上,FG与细胞混合培养时表现出良好的生物相容性,不会引起炎症反应,与细胞、骨移植材料和(或)生物活性分子联合运用,能够促进有成骨潜能的细胞黏附、增殖、迁移和分化,使生物活性分子缓慢释放,延长作用时间,促进骨再生。
2.2FG植入动物体内后对成骨作用的影响 FG具有良好的生物学性能,常与细胞、骨移植材料和生长因子等复合后植入骨缺损的动物模型,作为细胞和生长因子的载体,提高细胞接种效率,减少颗粒状骨移植材料的移位,加速骨组织的愈合。Park等[25]将包埋人骨髓间充质干细胞或牙囊间充质干细胞的FG注入脱钙骨基质支架中,然后植入裸鼠皮下进行体内成骨实验,证实了骨髓间充质干细胞和牙囊间充质干细胞的成骨能力以及FG作为细胞载体的可行性。同样,Seebach等[26]的研究证实了FG对大鼠股骨缺损植入间充质干细胞的早期作用,如宿主细胞的募集、早期炎症反应的调节、新血管的形成和骨组织再生等,FG可作为一种良好的载体用于组织工程。研究人员还将骨移植材料和(或)生物活性分子与FG混合,以达到加速骨修复的目的。例如,Cassaro等[27]研究了FG、双相磷酸钙和间充质干细胞在大鼠股骨缺损中的联合再生能力,结果表明,FG有利于优化手术过程,并且可以促进细胞黏附和增殖,是一种适合于骨缺损的支架材料。van der Stok等[28]用负载BMP-2的FG填充多孔钛植入物,并将该生物材料用于修复大鼠股骨节段性骨缺损,结果发现,在单纯钛植入物及FG填充的钛植入物填充缺损的对照组中骨再生没有发生,换言之,FG本身并不能提高钛植入物的骨再生潜能,而是作为BMP-2的载体,改善了骨修复过程。而Zhang等[29]则发现,将血管内皮生长因子/聚乳酸-乙醇酸/FG输送到犬股骨缺损处,可以显著改善血管重建以及骨愈合的质量和速度。同样,Vila等[30]将纤维蛋白与血小板衍生生长因子和BMP-2混合后植入小鼠颅骨缺损处,结果显示,与对照组相比,纤维蛋白介导的血小板衍生生长因子和BMP-2可改善血管生成,使血管更加丰富和粗大,可诱导更多的骨形成。还有学者发现,将以FG/纤维连接蛋白/肝素为基础的BMP-2给药系统植入大鼠颅骨缺损处后,BMP-2可稳定释放,给药系统可显著促进大鼠颅骨缺损模型的骨再生,表明FG可作为理想的缓释剂应用于组织工程[31]。此外,FG还可用于基因治疗,Li等[32]将聚丙交酯-乙交酯/FG负载脂质体/pDNA-转化生长因子-β1与间充质干细胞复合组作为实验组,将无纤维蛋白组作为对照组,其中聚丙交酯-乙交酯/FG复合物充当软骨形成的支架,基因复合物脂质体/pDNA-转化生长因子-β1均匀地分布于复合支架中,FG使基因缓慢释放,且FG包裹骨髓间充质干细胞,有助于提高复合支架中的细胞负载密度;体内实验结果表明,实验组转化生长因子-β1的表达水平显著高于对照组,实验组治疗12周后,与正常软骨组织相似的新组织修复软骨全层缺损。这些研究均证实了FG植入动物体内后对成骨作用的积极影响。
但也有少量研究报道了FG在骨再生方面的负面影响。例如,Gerngross等[33]发现,在自体松质骨移植上添加FG,对绵羊模型胫骨皮质骨重建有负面影响。Lappalainen等[34]也发现,FG与自体颗粒骨在修复兔颅骨缺损中可延迟骨矿化,但愈合情况仍优于未植入任何材料的阴性空白对照组。分析副作用的原因可能是FG限制了血管在移植骨中的生长方面的潜在作用,或者FG作为一种空隙填充物阻止了天然纤维蛋白的形成。同样,Carmagnola等[35]指出,在Bio-Oss颗粒中添加FG可使犬下颌骨缺损的骨与生物材料之间的组织接触减少,与Bio-Oss单独治疗组相比,在Bio-Oss/FG治疗组的骨缺损中未观察到新骨形成,FG破坏了生物骨颗粒与骨组织的结合。还有学者指出,高浓度的纤维蛋白原(35~55 mg/mL)可能会阻碍细胞长入骨缺损处,导致骨愈合延迟[36]。
综上,FG用于动物体内成骨时延迟骨愈合的原因,可能是FG用量不恰当或各组分的浓度不合适,导致骨组织与生物材料间的接触减少,妨碍了生物骨颗粒与骨组织的结合或者限制了新生血管的长入。但是,FG联合其他骨移植材料植入骨缺损区,并选择合适的用量及配比,可以改善新生血管形成、提高骨愈合能力。因此,需要进一步研究FG的最适用量及各组分的浓度后,再植入FG与骨移植材料复合物,才能改善骨再生,加速骨愈合,否则可能适得其反。
3 FG对人口腔颌面部骨再生的影响
虽然FG植入动物体内改善骨愈合的观点尚无定论,但仍有FG作为黏合剂、缓释剂和支架与不同骨移植材料联合应用于骨增量手术的报道。单独运用FG时,由于机械强度较差以及降解速度与骨再生速度不完全匹配,故不足以维持骨再生过程中所需的空间。临床上多将FG加入其他骨移植材料用于骨增量手术,这样既保持了骨移植材料的骨传导和空间维持作用,又能使FG充分发挥缓慢释放生长因子及促进细胞迁移的作用,进而改善骨愈合,增强骨再生。将FG与骨移植材料联合运用,证实了加入FG后的骨移植材料更易于临床操作,且不容易移位[37-38]。FG作为颗粒状骨移植材料之间的生物连接物,将颗粒黏合在一起,可提高临床操作效率,而且纤维蛋白网络能促进细胞迁移,这是新生血管形成、血管化和移植材料成骨所必需的。Giannini等[39]将5例使用自体骨碎片和纤维蛋白血小板胶混合物行骨重建手术患者的结果与20例具有相同手术指征未使用纤维蛋白血小板胶患者的结果进行比较,结果表明,自体骨碎片和纤维蛋白血小板胶的混合物有利于改善骨再生,减少感染,且可缩短住院时间。Tayapongsak等[40]指出,使用自体FG治疗人下颌骨缺损,加速了血运重建,并刺激了成纤维细胞和成骨细胞的生长。Segura-Castillo等[41]也发现,在治疗牙槽裂时使用FG,移植骨吸收显著减少,FG在移植材料与正常骨之间形成桥,通过促进细胞迁移改善移植材料的整合。因自体骨移植应用具有局限性,出现了其他骨替代材料与FG联合应用的情况。例如,Reppenhagen等[42]使用双相陶瓷(60%羟基磷灰石和40%β-磷酸三钙)结合FG,对51例良性骨肿瘤或肿瘤样病变刮除后的缺损进行修复,结果50例患者在56个月后骨缺损均完全愈合,且术后未见骨折,组织学分析显示新骨形成,表明植入材料具有良好的生物相容性和骨整合性,双相陶瓷结合FG是一种有效的骨移植替代物,可降低供区并发症的发生率。同时,有学者将自体细胞加载到FG复合的陶瓷颗粒上,治疗8例低位肱骨近端骨折患者,治疗期间无不良反应,12个月后对修复组织进行活检,发现骨形成,表明复合材料有良好的生物相容性[43]。此外,FG还可将抗生素高效输送至所需位置。Tofuku等[44]报道指出,使用FG包裹的抗生素,可显著降低接受骨科手术患者深部手术部位感染的发生率,在未使用FG治疗的188例患者中有11例患者深部手术部位感染,而在196例使用FG包裹抗生素的患者中无一例深部手术部位感染。这可能是由于FG作为缓释系统使抗生素缓慢释放,延长了抗生素的作用时间。
近年来,将黏性骨应用于临床骨增量手术,并取得了良好的成骨效果。黏性骨是自体FG和骨移植材料的混合物,术中易于操作,可以塑造成所需的形状,防止骨移植材料分散,而且自体FG富含各种生长因子,十分有利于骨再生;另外,黏性骨还可以在不使用任何骨钉或钛网的情况下,将移植材料稳定到骨缺损处,从而加速骨组织愈合[45]。Joshi等[46]用异体牙颗粒联合自体FG治疗上颌右尖牙区牙槽嵴缺损,临床和放射学结果均证实,牙槽骨宽度和高度有显著增加。在另一项研究中,Dhanaraj[47]用自体FG和异质骨混合成黏性骨,并将黏性骨置于去除的旧种植体与新植入种植体之间的骨缺损处,治疗期间因植入物压迫引起了下颌神经疼痛,结果术后1个月疼痛完全消失,6个月后行种植义齿修复效果良好,表明黏性骨可以促进新骨的形成,对组织愈合产生积极作用。因此,临床上可将FG与其他骨移植材料联合应用于骨增量手术,既可缩短临床操作时间,稳定骨移植材料,又可为细胞迁移提供支架,使生长因子缓慢释放,加速新生血管形成的同时促进骨再生,为骨组织工程提供了一种更有效的骨移植材料。
4 小 结
FG在骨形成过程中具有促进细胞迁移、增殖、分化和矿化的作用。然而,FG单一成分对成骨作用不显著,往往需要联合其他骨移植材料和(或)生物活性分子,作为支架、传递系统和(或)缓释剂运用于骨组织工程。这种组合可以改善单一材料的物理性能,使生长因子缓慢释放,促进新生血管的形成和骨组织的愈合。临床应用时还能将骨移植材料稳定在骨缺损处,缩短操作时间,获得良好的成骨效果。在未来,FG还有很大的发掘空间,纤维蛋白原和凝血酶作为FG的重要活性成分,其最佳作用浓度以及FG与其他生物材料或生物活性分子的最佳运用配比,仍需深入研究。

