正己烷与正十二烷在硝酸体系中的化学行为
周春俐,王 墨,唐洪彬,李星彦,于 婷,唐双凌,*
1.南京理工大学 化学化工学院和环境与生物工程学院,江苏 南京 210000;2.中国原子能科学研究院 放射化学研究所,北京102413
乏燃料的后处理对于核能生产中铀和钚的经济使用是必不可少的[1],其中以磷酸三丁酯(TBP)为萃取剂、直链烷烃为稀释剂的PUREX流程是目前世界上工业广泛应用的水法流程。添加稀释剂的目的是为了改变TBP的物理性质并降低有机溶剂的粘度和密度,这是改善两相分离的关键步骤,也是大规模溶剂萃取过程所必需的。由于后处理过程中溶剂与硝酸接触并长时间暴露在高温与辐射环境中,因此会导致TBP和稀释剂烷烃发生降解,降解产物会降低溶剂性能使萃取分离效果变差[2]。同时在蒸发浓缩工艺过程中,痕量有机溶剂在硝酸浓度过高以及重金属硝酸盐存在下会形成红油,一旦形成红油,就会在合适的条件下产生热失控分解,释放大量气体引发剧烈的爆炸事故[3]。到目前为止,全球已发生6次所谓的红油爆炸事故[4-8],造成了不同程度的设备损坏以及环境污染。
目前针对TBP与硝酸反应体系下的研究成果较多[9-13],稀释剂对TBP降解过程的影响也略有涉及[14-17],而围绕稀释剂烷烃单独与硝酸反应体系的研究则较少。关于稀释剂辐射降解的研究成果表明,降解产物主要包括硝基烷烃、硝酸酯(亚硝酸酯)、羧酸、酮等[2,18-19],最近有文献[20]分析了稀释剂在γ射线辐射下的反应产物,包括十二烷醇异构体和硝基十二烷异构体的混合物。由于正己烷、正十二烷均为直链烷烃且均不溶于水,化学性质也十分相似。因此,结合实际操作环境,本工作选择正己烷作为稀释剂在强辐射条件下的一个代表性降解产物。本工作拟将正己烷和正十二烷作为研究对象,确定其在硝酸环境中的反应产物以及温度、硝酸浓度、反应时间等因素与硝化产物的关系。另外,拟通过高压密闭反应釜中压力的监测来研究“红油”爆炸反应的前兆。
1 实验部分
1.1 主要试剂及仪器
正己烷、硝酸,分析纯,南京化学试剂公司;正十二烷,分析纯,上海迈瑞尔化学公司;其它试剂均为市售分析纯。
50 mL水热反应釜,南京大卫仪器公司;NICOLET IS10型红外光谱仪、ISQ型气相色谱-质谱联用仪,美国赛默飞世尔公司;GC-2014C型气相色谱仪,日本岛津公司;AVANCE Ⅲ 500 MHz核磁共振谱仪,瑞士布鲁克公司;高压反应釜,由某仪器公司按照南京理工大学要求定制。
1.2 实验方法
1.2.1合成方法 准确移取一定体积的烷烃和已知浓度的硝酸溶液于聚四氟乙烯内衬中,将装有物料的内衬放入不锈钢釜中拧紧,接着放入烘箱中进行反应,反应结束后取出反应釜冷却至室温,开釜取出物料。将反应液置于分液漏斗中静置分层,取上层有机相加入饱和碳酸氢钠水溶液洗涤3遍,分液,然后用无水硫酸钠干燥有机相,将预处理后的有机相用于后面的分析测定。图1为正十二烷-硝酸体系反应得到的红色油状物。

θ=150 ℃,t=12 h,c(HNO3)=6 mol/L
1.2.2气相色谱-质谱联用分析条件 色谱分析条件:溶剂,正己烷;色谱柱型号,DB-5HT 15 m×φ0.25 mm;柱温,50 ℃下保持3 min,以20 ℃/min升温至100 ℃,保持3 min,以12 ℃/min升温至230 ℃,保持4 min,以5 ℃/min升温至260 ℃,以10 ℃/min升温至300 ℃,再保持14 min;进样不分流;进样口温度,285 ℃。质谱条件(EI):离子源温度,230 ℃;电子能量,70 eV;扫描范围,m/z=30~650。
1.2.3反应过程中的压力探究 正己烷和正十二烷与HNO3反应过程中的压力探究是在密闭高压反应釜中进行的,装置示意图示于图2。如图2所示,该仪器釜体材料为锆材,体积容量为0.5 L,反应体系工作温度为室温~250 ℃,工作压力为0~10 MPa。同时仪器设有故障处理装置可以保障反应过程安全进行,反应过程中的压力及温度数据可通过电脑远程操控实时记录并导出。
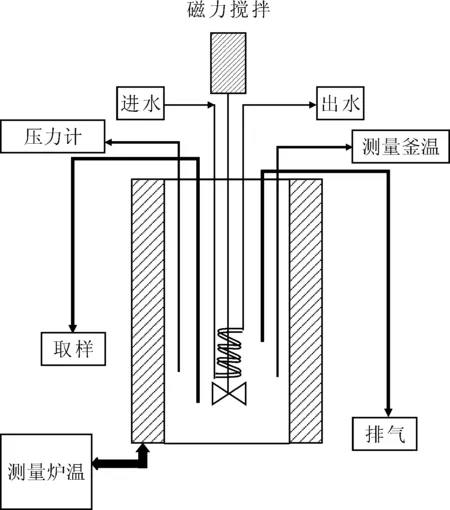
图2 高压反应釜示意图
2 结果与讨论
2.1 烷烃-硝酸体系产物的红外分析
图3为正己烷和正十二烷在硝酸体系中产物的IR光谱图。如图3曲线Ⅰ所示,1 546.56 cm-1处的吸收峰为硝基烷(-NO2)的反对称伸缩吸收峰,1 388.82 cm-1处为对称伸缩吸收峰;另外2 962.86 cm-1、2 876.07 cm-1、1 459.69 cm-1处的吸收峰为烷基链上的伸缩振动。类似地,图3曲线Ⅱ也存在硝基烷(-NO2)的吸收峰,即1 549.83 cm-1和1 377.46 cm-1。说明烷烃-硝酸体系反应产物含有硝基烷烃。
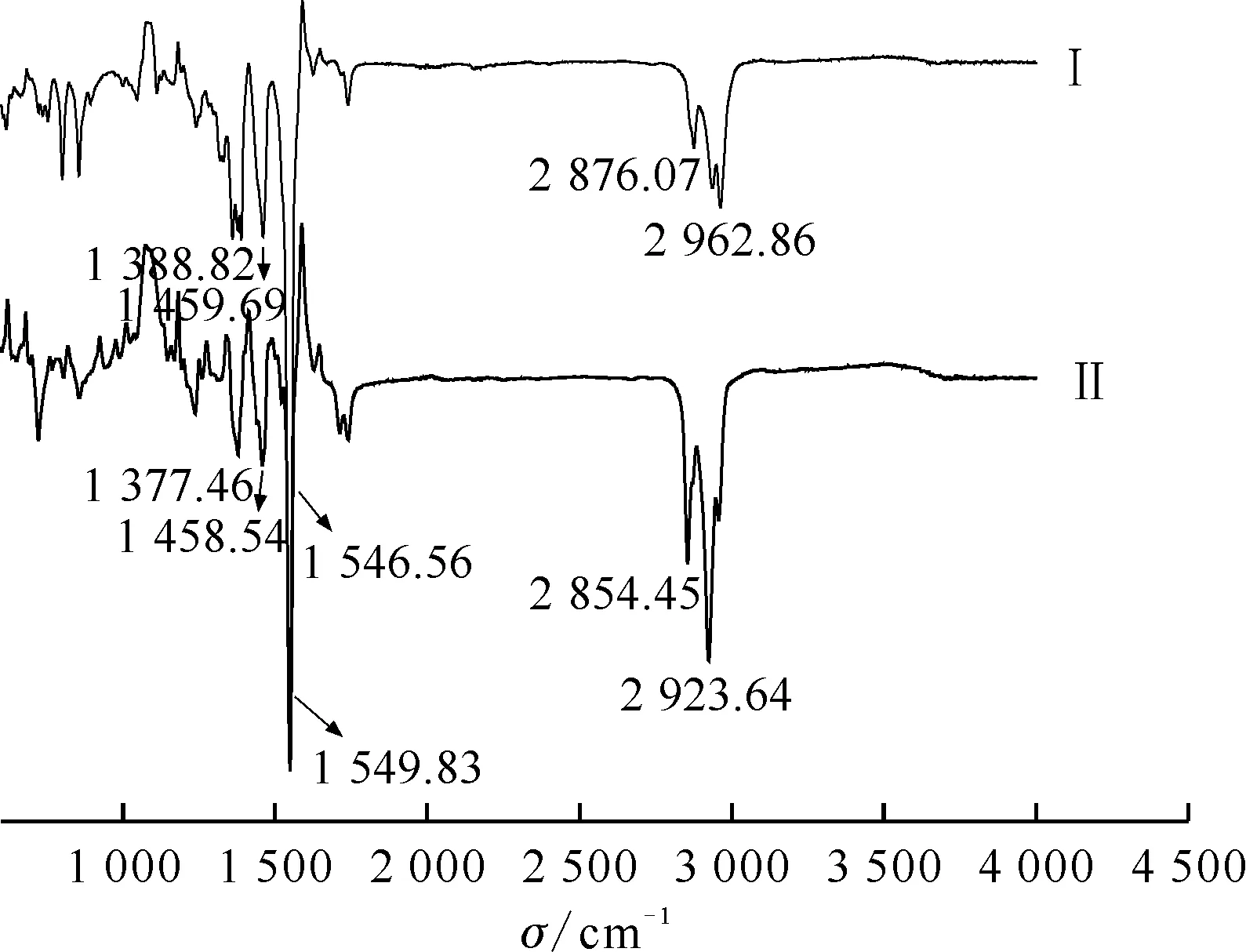
Ⅰ——正己烷,Ⅱ——正十二烷
2.2 烷烃-硝酸体系产物的GC-MS分析
正己烷-硝酸体系产物的GC图示于图4。由图4发现有两组气相峰,两个峰的质谱图示于图5。通过谱图库检索,保留时间为5.69 min时的物质为2-硝基己烷,保留时间为5.97 min时的物质为3-硝基己烷。由图5两个质谱图可以明显地看到相对分子质量为85.10的碎片峰,猜测其为硝基己烷打掉一个硝基而得到的—C6H13。

图4 正己烷-硝酸体系产物的GC图
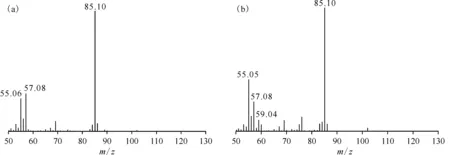
tR,min:(a)——5.69,(b)——5.97
正十二烷-硝酸体系产物的GC图示于图6。由图6可知,保留时间为9.80 min的峰为原料正十二烷,通过数据库检索可知保留时间14.79、14.81、14.87、15.05、15.32 min时的物质为硝基十二烷的5种异构体(2-硝基十二烷、3-硝基十二烷、4-硝基十二烷、5-硝基十二烷和6-硝基十二烷),其中保留时间为14.87 min时的质谱图示于图7。由图7可以看到,硝基十二烷未能像硝基己烷一样观测到特征性的分子裂片峰,这可能是由于十二烷产物的碳链太长,其烷基链的分子离子峰强度掩盖了硝基峰。
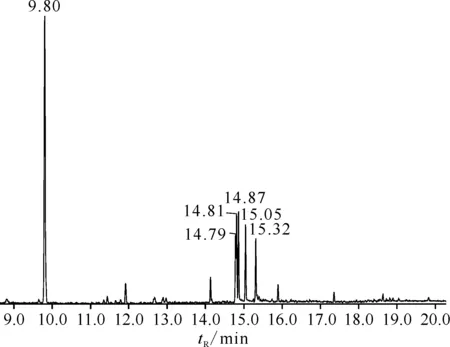
图6 正十二烷-硝酸体系产物的GC图
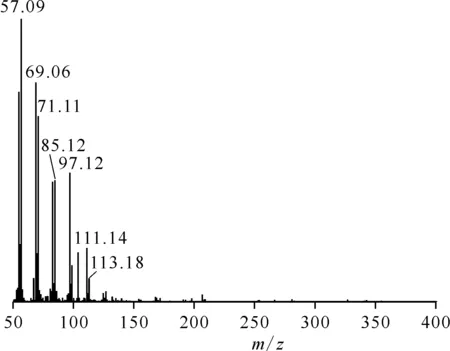
图7 正十二烷-硝酸体系产物GC图中tR=14.87 min对应物质的质谱图
2.3 烷烃-硝酸体系产物的核磁碳谱分析
正己烷-硝酸和正十二烷-硝酸体系产物的核磁碳谱示于图8,根据文献[21]数据从图8(a)中可以判断化学位移83.31 ppm和89.94 ppm的两组峰分别为2-位和3-位硝基所连碳的化学位移,即确定了正己烷-硝酸体系下的产物有2-硝基己烷和3-硝基己烷,该结果与GC-MS分析一致。由正十二烷-硝酸产物的13C NMR谱(图8(b))显示了四组碳信号,化学位移分别为83.38、88.61、88.89、90.29 ppm,仔细分析发现化学位移为88.89 ppm处是未分裂的两个峰,结合GC的分析结果可知化学位移在83.38~90.29 ppm之间有5组峰。根据文献[19]碳谱数据推测产物包括2-硝基十二烷、3-硝基十二烷、4-硝基十二烷、5-硝基十二烷和6-硝基十二烷。
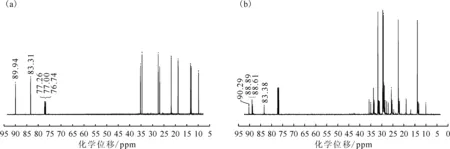
(a)——正己烷,(b)——正十二烷
2.4 各因素对直链烷烃硝化反应的影响
利用气相色谱对产物定量分析,分别探究了温度、硝酸浓度、反应时间等因素对直链烷烃硝化反应的影响,结果示于图9。其中当硝酸浓度为6 mol/L、反应时间为4 h、烷烃与硝酸摩尔比为1∶1时,不同温度下正己烷和正十二烷在硝酸溶液中硝化产物产率变化示于图9(a)。如图9(a)所示,当反应温度由110 ℃升高到150 ℃时,正己烷和正十二烷硝化产物的产率显著增加,而当温度升高到160 ℃时,产率有所下降,主要因为高温可能会引起烷烃稀释剂及产物发生碳化。
当反应温度为150 ℃、反应时间为4 h、烷烃与硝酸摩尔比为1∶1时,研究了硝酸浓度对硝化产物形成的影响,其结果示于图9(b)。如图9(b)所示,当硝酸浓度范围为2~10 mol/L时,正己烷的硝化产率呈现先增加后降低的趋势,当硝酸浓度为6 mol/L时,正己烷的硝化产率达到最大值。对于正十二烷,硝化产率随着硝酸浓度的增加而逐渐增加,当硝酸浓度为10 mol/L时,硝化产率最大。当温度、时间和摩尔比一定的情况下,硝酸浓度越高,越容易分解生成NO2,产生的NO2浓度越高,烷烃与硝酸的硝化反应越容易发生。由于正己烷沸点低,当硝酸溶液在150 ℃下分解生成NO2时,正己烷与硝酸的反应过程为均匀的气相反应;而正十二烷沸点高,在该温度下反应为气-液相界面反应,此时反应体系为两相。因此正己烷比正十二烷更容易与硝酸反应,达到最大反应产率时所对应的硝酸浓度也就更低。
当反应温度为150 ℃、硝酸浓度为6 mol/L、烷烃与硝酸的摩尔比为1∶1时,反应时间对硝化产物产率的影响情况示于图9(c)。对于正己烷-硝酸体系分别探究了反应时间为2、4、6、8、10、12 h的产率变化,由图9(c)可以看出,正己烷硝化反应产率在4 h时达到最大,随着时间的继续增加而减小之后反应产率基本不变。对于正十二烷-硝酸体系探究了反应时间在2~20 h范围内的产率变化,当反应时间为12 h时,正十二烷硝化反应产率达到最大值,且随着时间的继续增加有微弱减小。从上述结论可以看出,反应一段时间后烷烃硝化产率受反应时间的影响较小。
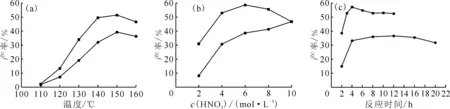
■——正己烷,●——正十二烷
2.5 烷烃-硝酸体系下的压力探究
正己烷-硝酸体系及正十二烷-硝酸体系反应过程中压力随时间的变化曲线示于图10,其中硝酸浓度为6 mol/L,反应釜内部温度设为150 ℃。
从图10(a)可以看出,单独稀硝酸水溶液产生的最大压力为0.38 MPa,正己烷产生的最大压力为0.64 MPa,而正己烷/HNO3摩尔比1∶1时产生的最大压力为2.90 MPa,正己烷/HNO3摩尔比1∶2时产生的最大压力为3.44 MPa。因此,正己烷-硝酸的反应体系与正己烷或稀硝酸相比,压力显著升高,这意味着当硝酸和有机物接触时可促进硝酸的分解,系统压力也瞬间增加。根据文献[22],萃取剂和稀释剂与硝酸在高温下接触可以产生大量气体,如NO2、NO、CO2、N2等。另外,系统压力也会随着硝酸含量的增加而显著增加,且反应过程中放热更加剧烈。
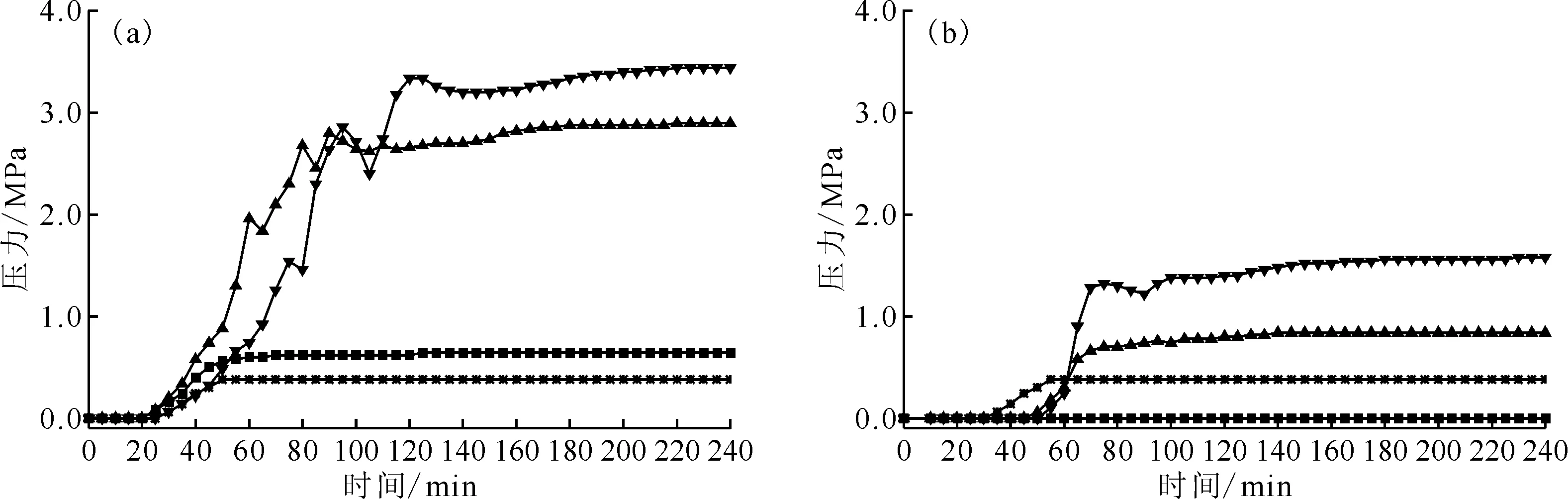
c(HNO3)=6 mol/L,反应釜内部温度150 ℃
同时探究了正十二烷-硝酸体系反应过程中的压力变化,如图10(b)所示,单独稀硝酸水溶液产生的最大压力为0.38 MPa,正十二烷产生的最大压力为0 MPa(因为正十二烷的沸点为217 ℃),而正十二烷/HNO3摩尔比为1∶1时产生的最大压力为0.84 MPa,正十二烷/HNO3摩尔比1∶2时产生的最大压力为1.58 MPa。该结果与正己烷-硝酸体系的情况类似,即当硝酸的比例增加时,反应体系的压力将显著增加。
猜测烷烃与硝酸在一定条件下可发生剧烈的氧化还原反应,生成大量的气体产物,从而使反应体系压力迅速增加。基于正己烷与正十二烷的上述结果可以看到,正十二烷-硝酸反应体系产生的压力远低于正己烷-硝酸体系,也就是说,与长链烷烃-硝酸体系相比,短链烷烃-硝酸体系提供了更高的压力并且放热更加剧烈。主要因为正己烷在150 ℃下与硝酸的反应为气相反应,反应分子亲密接触,反应过程中产生的压力更大;而正十二烷在该条件下为液相反应,反应分子接触少,相应的产生的气体量少,压力也更小。根据以上分析,产物中未检测到醇或硝酸酯,怀疑硝酸酯发生了快速氧化分解,这可能是导致体系压力迅速增加的关键。可能的反应机理如下:
3 结 论
(1)正己烷和正十二烷在硝酸中的化学行为研究表明长链或短链烷烃均可形成硝基化合物。红外光谱、GC-MS和13C NMR等分析方法确定了正己烷-硝酸体系下的产物是2-硝基己烷和3-硝基己烷的混合物;正十二烷-硝酸体系下的产物是2-硝基十二烷、3-硝基十二烷、4-硝基十二烷、5-硝基十二烷和6-硝基十二烷的混合物。
(2)气相色谱定量分析结果表明,硝基化合物的形成受温度及硝酸浓度的影响较大,反应时间影响较小。
(3)根据高压反应釜测得正己烷-硝酸及正十二烷-硝酸反应体系下的时间-压力曲线,结果表明:与正十二烷-硝酸体系相比,正己烷-硝酸体系产生的压力更大;随着硝酸比例的增加,烷烃与硝酸反应过程中产生的压力和反应程度均有所增加。
(4)根据产物定性分析及时间-压力曲线,推测反应体系压力迅速增加与硝酸酯的快速氧化分解密切相关,提出了可能的反应机理。

