二氧化氮制取实验装置和除气操作的改进
张婉枫(中核四0四有限公司第三分公司,甘肃 兰州 732850)
0 引言
氮气作为空气中占有比例最大的气体,拥有众多的氧化物,因此往往也会涉及到许多的复杂问题。二氧化氮呈现红棕色,并且在二氧化氮气体当中往往存在着一定量的四氧化二氮,并且彼此之间往往存在着平衡制约的关系,维持这种关系会具有显著的颜色变化,并且正反应是一种放热反应,随着反应的进行气体的体积会减小。因此二氧化氮与四氧化二氮二者之间的转化因为温度、压强的变化会导致化学反应平衡呈现出显著的颜色变化,参与实验的学生可以显著感受到气体温度、压强的变化导致化学平衡出现移动。所以说在一般教材当中,二氧化氮制备实验都会出现在化学平衡移动条件教学当中,而二氧化氮就是这一实验当中的重要气体。二氧化氮本身是一种有毒性、有害性气体,并且在二氧化氮制备实验当中,常常不可避免地会有一定量的二氧化氮出现在空气当中。所以在制备二氧化氮实验、平衡实验结束以后,需要将余气去除,如果这些气体释放出来就会对环境造成污染。为了最大程度上减少二氧化氮对环境造成的污染,教学实验中将二氧化氮制备与平衡实验作为重点研究课题。
1 二氧化氮制取实验
1.1 常用制取装置存在的一系列缺陷
在化学实验教学过程中,往往使用铜、浓硝酸制备二氧化氮气体。对于少量的二氧化氮气体制备往往在试管当中进行。不过对于气体平衡实验而言,往往需要制备大量的气体,因此需要在大容量烧瓶当中进行。需要将制备气体的烧瓶和玻璃导管实现连接,随后在烧瓶当中插入玻璃导管。制备二氧化氮实验装置如图1所示。制备二氧化氮的过程中,需要将铜、浓硝酸进行充分混合,并且反应处于持续进行的状态,同时导管当中排出气体也是处于持续进行的状态,由此导致排出气体的过程和收集气体的过程并没有实现密切结合:

图1 制备二氧化氮实验装置
(1)在集气瓶更换过程中难免会将瓶中气体释放出来,如果更换集气瓶数量多,释放出的气体也就越多。(2)收集气体结束以后,烧瓶内部剩余的铜、浓硝酸之间还需要继续产生反应,继续产生二氧化氮,这些后来产生的二氧化氮就会释放到空气当中[1]。虽然将导管插入NaOH溶液当中,但是在气体排出较快的条件下,还是会有很多气泡从溶液当中的气泡释放出来对空气造成污染。(3)生成物与对应的现象:气体制备烧瓶内部,铜和硝酸反应生成硝酸铜、二氧化氮、一氧化氮,经过电离产生二氧化氮离子,与铜离子反应生成Cu(NO2)2,液体呈现绿色。其中加入大量的氢氧化钠溶液以后,会很大程度上降低硝酸铜浓度,液体呈现绿色,主要是亚硝酸铜溶液的颜色[2]。通过倒吸使氢氧化钠溶液进入到烧瓶内部,溶液当中形成Cu(OH)2、Cu(OH)2·Cu(NO3)2。当二氧化氮等气体和已经进入烧瓶当中的下落氢氧化钠溶液在运动过程中由于充分接触而发生反应:
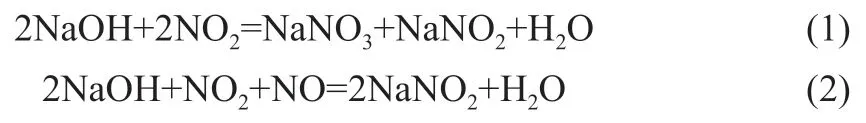
少量的水当中会形成大量的NaNO2沉淀,和铜离子发生反应,产生具有可溶性的Cu(NO2)2黄绿色固体。受到多种因素影响,在氢氧化钠溶液当中会掺杂一定量的碳酸钠,正因如此在酸性区域当中才会产生二氧化氮气体,并且红棕色消失。二氧化氮和氢氧化钠溶液在实际反应过程中,产生的气体会转化成为液体或固体,从而气压下降,这样才能保证倒吸可以持续进行。因为浓度过高,在倒吸过程中会产生竞争反应,浓度不同会形成不同的物质,部分物质因为不稳定性,会产生转化现象。
1.2 去除烧瓶中的气体
去除气体的过程中,烧瓶需要和气球之间使用T形管进行连接,随后将T形管与玻璃导管实现连接,在氢氧化钠溶液当中插入玻璃导管。随后将K2关闭,将K1打开,使用热毛巾捂住烧瓶,气体在加热条件下会出现膨胀,气压增加,此时气体会进入到气球当中。一段时间后,将K1关闭,拿掉热毛巾,将K2打开,换用冷毛巾捂住烧瓶,气体受冷就会收缩,气压下降,由此产生倒吸现象,氢氧化钠溶液进入烧瓶中,此时再将K1打开。集气瓶当中有氢氧化钠溶液进入以后会和瓶内的气体发生反应,产生多种氧化物,包括NaNO3、NaNO2、H2O,去除NO2、N2O4、NO,原本呈现红棕色的气体最终变为浅黄色的溶液。
2 实验改进
2.1 在实际教学当中的应用
实验经过改进以后,制取、去除二氧化氮的方法、内容、操作细节都会在实际教学活动中成为一种优质的教学资源,并且在教学过程中可以结合实际需求进行灵活的变动,包括适当的拓展与压缩。气体制备装置改进以后,在倒吸的作用下,往往烧瓶中会呈现出多种多样的现象,在一定程度上吸引学生的学习兴趣,通过具有趣味性的方法掌握去除二氧化氮的方式,并且这在很大程度上可以加深学生的学习印象。关于二氧化氮制备实验不仅可以在课堂上进行,在课外的化学活动小组、化学兴趣小组同样可以进行,这样可以提升学生们学习化学的积极性。对于已经学习过关于二氧化氮知识的学生,这一实验可以帮助学生巩固知识,对于还没有学习过二氧化氮知识的学生,可以激发其求知欲、探索欲、趣味性。并且在整个学习过程中,通过一个实验涉及到了多方面的知识,包括化学式、化合价、化学平衡等等。在实验过程中可以实现对这些方法、内容的归纳、分类,并且在实际教学过程中,还可以从多角度提升学生的化学核心素养。
2.2 推广应用倒吸法
制备二氧化氮气体的装置,无论是否加热,在有必要的条件下,使用这一套装置与方法均可以产生倒吸现象,通过倒吸法可以将多种有毒气体去除。在中学化学教学中,不仅是二氧化氮,包括二氧化硫、氯气、盐酸、氨气均可以使用倒吸法进行去除。二氧化硫、氯气、盐酸等气体可以使用氢氧化钠进行去除,氨气需要使用盐酸溶液进行吸收。由于不同的气体具有不同的性质,因此在制备气体时往往也具有不同的特点。对于一些气体制备反应,有时需要加热,而有些气体并不需要加热,有些气体在反应过程中放热多,有些气体则放热少。有些气体在特定的液体中具有相对较大的溶解度,而有些气体在液体中具有较小的溶解度,而溶解度会在根本上决定倒吸的速度。在去除残留气体的过程中往往气体需要一定的冷却时间,冷却完成后,才可以用手去触碰烧瓶,通过气球的舒张程度对气压大小进行判断,以此来选择正确的倒吸方法与时间。在去除气体的过程中,气球当中往往不能含有过多的气体。
3 改进后实验设计
结合以往的实验数据分析,烧瓶内部二氧化氮气体压力、吸收剂的实际温度、料填充度均是对吸收二氧化氮气体产生影响的主要因素。鉴于此,需要在正交设计法实验原则的基础上对上述三因素进行分析,并在此基础上探索吸收二氧化氮。
3.1 二氧化氮的产生
铜和浓硝酸之间发生剧烈的反应,反应释放出大量的红棕色二氧化氮气体,反应式:

3.2 二氧化氮与水的反应
集气管当中收集满二氧化氮气体以后,集气管下口就会放出已经形成的二氧化氮,反应瓶当中用于液封的水会吸收二氧化氮。反应式:

3.3 一氧化氮与氧气之间的反应
铜与浓硝酸剧烈反应停止以后,因为铜已经完全消耗完毕,因此反应停止,整个反应大约持续4 s时间,并且集气管内部的水位迅速上升,同时红棕色气体不断淡化。二氧化氮与水之间发生反应生成硝酸、一氧化氮。生成的一氧化氮在氧气的作用下很容易被氧化,反应式:

3.4 集气管水面上升
二氧化氮与水之间发生反应,由此集气管内部的气体体积减少,造成负压,水被向上吸,水面最终停止在集气管的2/3~3/4位置。
4 特点与用途
4.1 特点
在对实验仪器进行清洗之前,需要将内管罩向上轻轻提起,脱离水面持续几秒钟,使空气进入,这样就可以将残留在内部的一氧化氮被反应掉,氧气含量大约为40 mL。结合反应理论,产生的一氧化氮会转化为二氧化氮,此时需要消耗大约10 mL的氧气,反应结束后,往往实验器内部会剩余大量的氧气,而一氧化氮几乎没有剩余,此时对实验器进行冲洗可以确保安全性。
4.2 用途
因为二氧化氮气体易溶于水,由此制备二氧化氮以及二氧化氮和水之间发生的反应可以实现在反应器内连续进行,改进后的实验装置可以很大程度上解决实验进行的时间以及实验试剂的使用量,并且确保实验的环保。
5 结语
通过改进二氧化氮制备实验,可以有效防止气体制备过程中出现二氧化氮泄漏的情况。实验进行的过程中,受到多种因素的影响,溶液会呈现出多种颜色的变化现象。对二氧化氮制备实验改进以后可以有效提升二氧化氮气体的吸收率,并且实验过程中涉及到多项知识点,可以帮助学生进行预习、巩固。

