CdS纳米线的溶剂热合成及其光催化产氢性能
王广崎,吴邦昊,毕艺洋*,张 钰
(1.吉林化工学院 材料科学与工程学院,吉林 吉林 132022;2.吉林化工学院 石油化工学院,吉林 吉林 132022)
城市化的快速发展在消耗能源资源的同时也带来了环境污染问题[1].为解决能源短缺和环境危机,光催化技术作为太阳能转换领域的有效策略,得到了广泛的研究[2].在众多半导体材料中,CdS因具有合适的导带位置(-0.9 eV)和带隙(2.4 eV),已被证明是一种优良的光催化剂,在可见光催化产氢领域受到了极大关注[3].然而,CdS严重的光腐蚀作用和电子-空穴对的快速复合限制了它的实际应用[4].
几何形貌和表面结构直接影响着CdS的光催化产氢活性和稳定性.通过改变CdS的形貌、尺寸和比表面积等可以有效缩短传输距离、促进电荷的转移和分离,从而提高光催化产氢活性[5].近年来,颗粒状[6]、棒状[7]、片状[8]和球状[9]等多种形貌的CdS已被开发用于光催化分解水产氢.如Wu等人[10]基于异质结工程与共催化剂改性相结合的思想,合成一种高效的Ni2P-CdS/g-C3N4纳米棒复合材料,产氢速率高达44.45 mmol·g-1·h-1,g-C3N4包覆在CdS纳米棒上可以有效促进电子-空穴对在空间上分离,同时,Ni2P降低了H+还原的过电位.与纳米棒相比,具有更小的径向尺寸、更大的长径比的CdS纳米线将更有利于发挥其促进电荷转移和分离的优势.但CdS纳米线在制备过程中极易集结成束状,降低了材料的比表面积和分散性,不利于获得更好的光催化活性,也限制了纳米线为基体的进一步改性修饰.
基于上述问题,采用简单可控的乙二胺(EDA)溶剂热法制备了高长径比、分散良好的一维CdS NWs,探究了EDA含量及溶剂热晶化条件对CdS NWs的组成、形貌、电化学性能及光催化产氢活性的影响.
1 实验部分
1.1 试剂与仪器
四水硝酸镉(Cd(NO3)2·4H2O)、硫脲(NH2CSNH2)、乙二胺(EDA,C2H8N2)和无水乙醇(EtOH),以上试剂均为分析纯,购自中国阿拉丁公司.
Bruke-AXS(D8)X射线衍射仪(X-ray Diffractometer(XRD));JEOL JSM-6490LV扫描电子显微镜(Scanning Electron Microscope(SEM));3H-2000PM1 比表面积及孔径分析仪(Specific surface area and porosity analyzer(BET));PerkinElmer Lambda750 紫外可见吸收光谱仪(Ultraviolet visible absorption spectrometer);CHI-760E 电化学工作站(Electrochemical workstation);Shimadzu GC-2014气相色谱仪(Gas Chromatograph(GC));Perfectlight Labsolar-6A全玻璃自动在线微量气体分析系统.
1.2 CdS NWs的制备
分别称取0.641 g Cd(NO3)2·4H2O和0.474 g硫脲,放置于干燥的带聚四氟乙烯内胆的20 mL水热合成釜中.分别注入0、4、8、12、16 mL EDA后密封,于180 ℃下分别晶化6、12和18 h.溶剂热反应后快速淬火至室温.将得到的黄色沉淀物离心,用乙醇和蒸馏水依次洗涤3次,最后在60 ℃的真空烘箱中干燥过夜得到CdS NWs.将所得样品分别记为CdS NWs-x-y,其中x,y分别代表EDA体积用量和晶化时间.
1.3 光催化活性测试
所有的光催化测试都是在真空条件下进行的,采用带有滤光片的氙灯(λ≥420 nm)来模拟可见光光源.产氢实验是在密闭系统中进行的,称取50 mg光催化剂于50 mL Na2S(0.35 mol/L)和Na2SO3(0.25 mol/L)的混合水溶液中,经超声分散后转移至Pyrex石英顶照式光催化反应器中.同时开启真空泵、色谱、气体进样系统、低温循环水等装置并对系统抽真空排除干扰.调整氙灯光源与Pyrex石英顶照式光催化反应器的距离保持在3 cm后开启300 W氙灯光源,在磁力搅拌的条件下进行液固相光催化反应,开始实验.设置反应过程中每间隔1 h由气体进样装置将系统产生的气体注入气相色谱仪中进行定量分析,反应持续3 h.
2 结果与讨论
2.1 结构物相分析
不同EDA用量制备CdS样品的XRD谱图如图1所示.所制备的样品均为六方纤锌矿结构CdS,XRD谱图与标准卡片(JCPDS No.65-3414)一致.在2θ=24.9°、26.5°、28.2°、36.6°、43.8°和47.8°处特征峰分别代表六方CdS(100)、(002)、(101)、(102)、(110)和(103)晶面的衍射峰,且没有其他的杂峰出现,说明获得纯度较高的六方硫化镉[11].样品的XRD衍射峰相对强度随着EDA用量的增加而提高,在加入12 mL EDA时所合成的CdS NWs具有最高的峰强度,表明该样品具有更好的结晶度[12].进一步增加EDA的用量(16 mL),XRD相对强度有所下降,这可能与过量EDA导致样品结晶度下降有关.
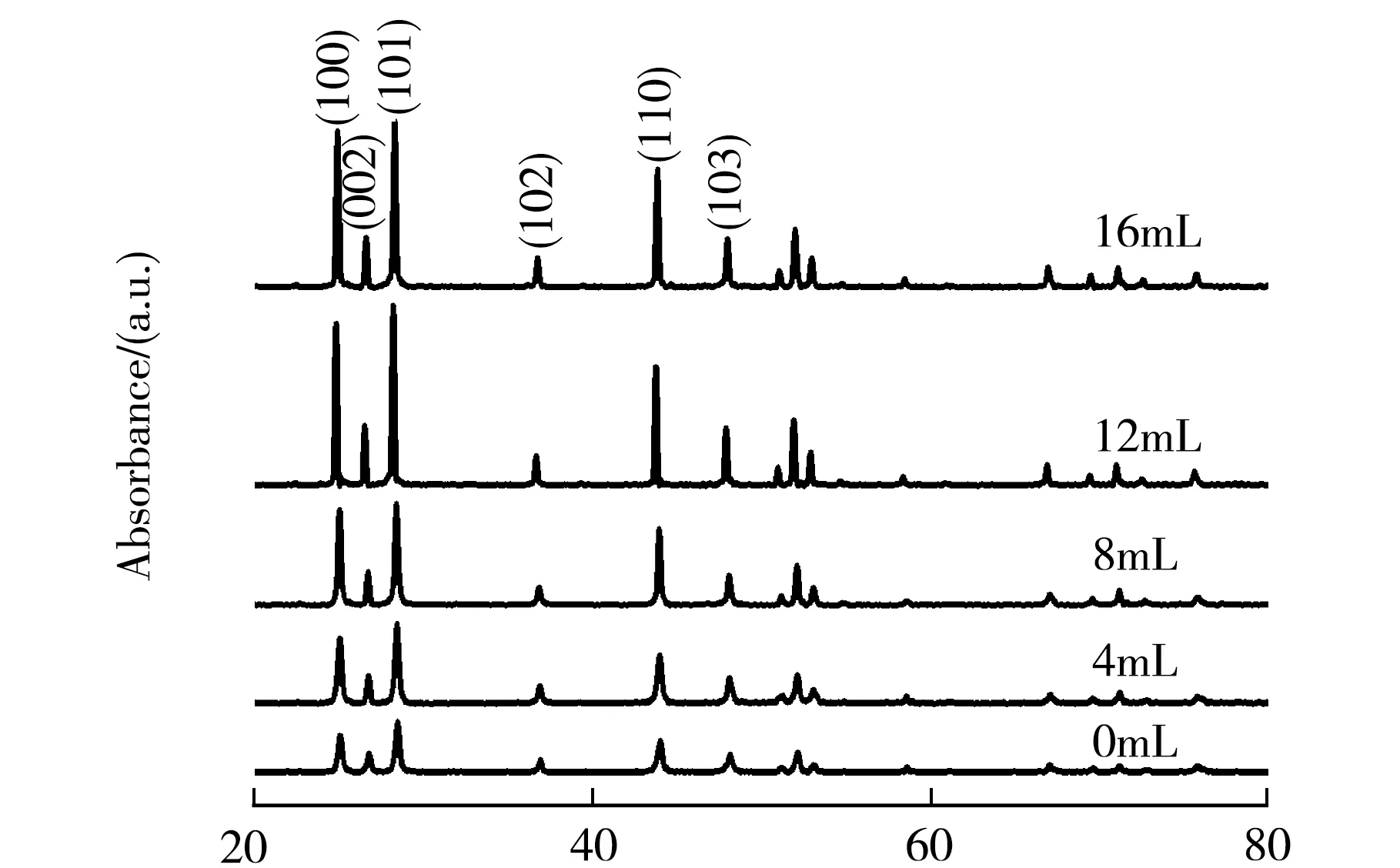
2θ/°
图2给出溶剂热晶化时间对CdS NWs结构和晶型的影响.随着晶化时间的延长,样品XRD衍射峰相对强度逐渐增大.在18 h时所合成的CdS NWs具有最高峰值强度,表明该样品具有最佳结晶度.
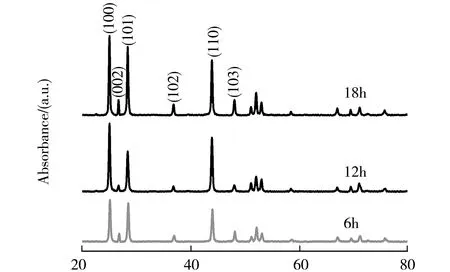
2θ/°
2.2 表观形貌分析
图3为采用不同EDA用量制备CdS NWs的扫描电子显微镜照片.采用水热合成法时(不加EDA,CdS主要由粗大的棒状晶、不规则的块状晶和极少量的线状晶构成,见图2(a).其中棒状晶的径向尺寸为1.5~4 μm,块状晶大小在0.5~4.8 μm,而线状晶的长径比约为100、径向尺寸约为10 nm.当EDA用量为4~8 mL时,CdS线状晶占比明显增加,长径比增加至300,但仍残留部分棒状晶及块状晶,见图2(b)~(c).继续增加EDA用量至12 mL时,CdS表现出纳米线形貌,径向尺寸约为30 nm,长径比明显提高至400.SEM中未见棒状晶、块状经或颗粒存在,见图2(d).进一步增加EDA的用量为16 mL,CdS纳米线发生了部分团聚,局部出现线束相貌,见图2(e).

(a)CdS-0mL-18h
通常,晶体的形貌受形核速率和生长速率的共同影响,当晶体形核速率大于晶体生长速率时,晶体尺寸和长径比将变小[13].适量的乙二胺作为CdS生长的表面配体,加快了CdS的晶体生长速度使其晶粒尺寸变大,且沿择优生长方向具有较大的长径比,促进了一维CdS NWs的生长,而过量的乙二胺由于电荷堆积的影响导致团聚现象的发生.
保持12 mL EDA用量不变,探究了CdS NWs形貌随溶剂热晶化时间的演变过程(图4).晶化时间为6 h时,CdS由纳米颗粒和纳米线共同构成,见图4(a).而且纳米线有聚集现象发生,整体变为束状形貌.提高晶化时间至12 h,纳米线的聚集程度显著降低,同时长径比有所提高,但SEM中仍然可见大量纳米颗粒,见图4(b).18 h时,SEM中未见CdS纳米颗粒,纳米线长径比增加至550,径向直径约为50 nm且表面光滑、尺寸分布均匀,具有最佳形貌,见图4(c).

(a)CdS-12mL-6 h
在EDA溶剂热法合成体系中,EDA作为络合剂与Cd2+发生配位形成络合物[Cd(en)2]2+,S2-则来自硫脲的溶解.随着温度的升高,[Cd(en)2]2+与S2-缓慢结合生成CdS.六方纤锌矿结构的CdS各向异性生长是由表面原子相对于内部原子的过剩能量所驱动[14].(001)晶面在纤锌矿结构中具有较高的堆积密度和大量的配位原子,其过剩能量远低于(100)和(110)晶面.随着晶化时间的延长,Cd2+可以充分地与EDA进行配位,选择性地择向生长,即沿着生长速率最快的方向逐渐伸长,最终形成一维纳米线结构.
2.3 比表面积及孔结构分析
为了对比EDA溶剂热合成和水热合成所得样品的区别,对样品进行了N2-吸附脱附实验(图5).
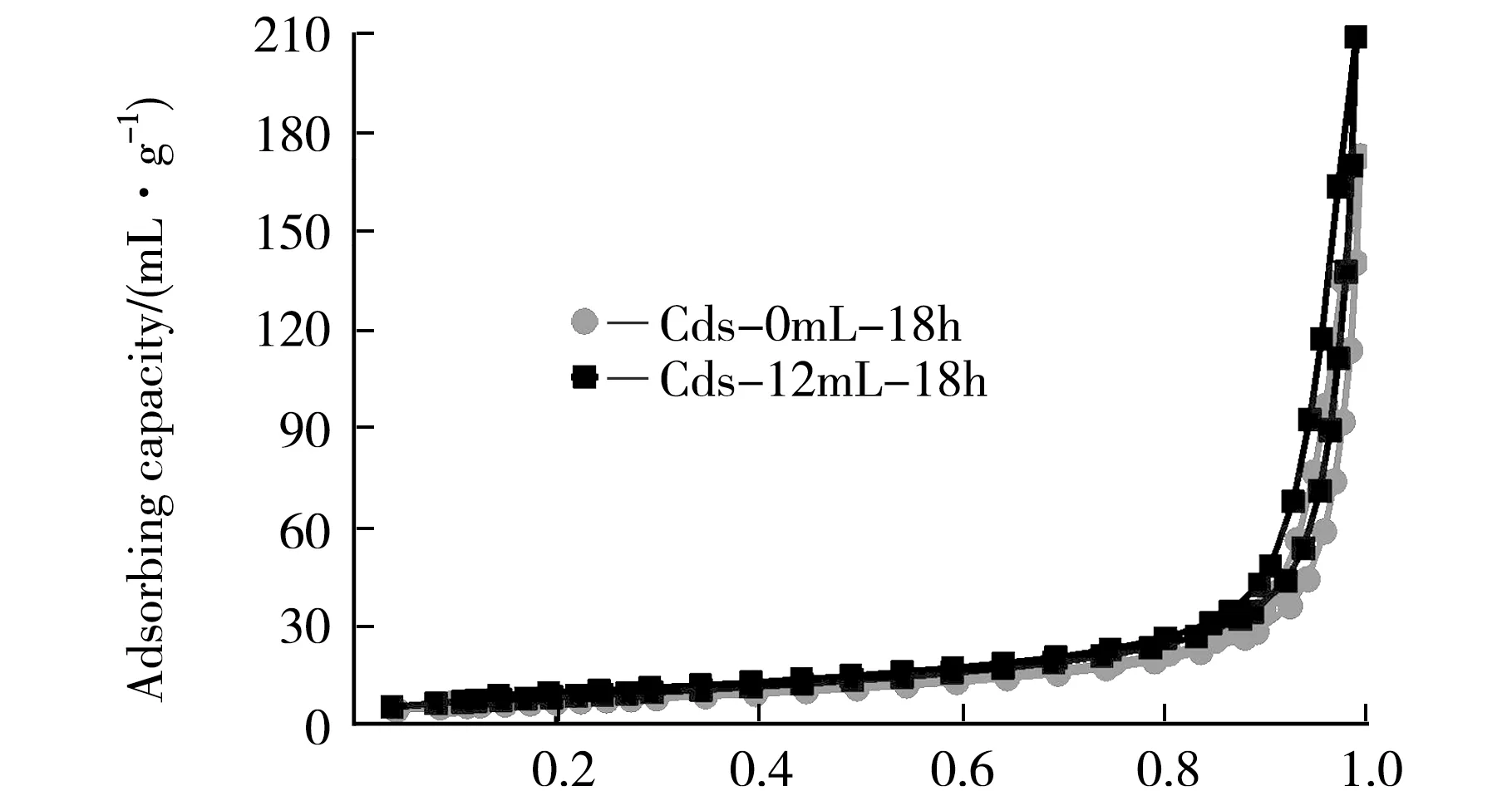
Relative pressure(P/P0)
图5(a)显示两者都是带有滞后环的Ⅲ型吸附等温线,结合图5(b)给出的孔径分布图,可见两个样品皆包含部分介孔[15].样品的比表面积及孔结构参数如表1所示,采用EDA溶剂热法制备的CdS纳米线表现出更高的比表面积(31.92 m2·g-1),而总孔容和平均孔直径有所下降.

表1 样品的比表面积及孔结构参数
2.4 CdS NWs的光学性能
采用紫外可见漫反射吸收光谱研究CdS-0mL-18h和CdS-12 mL-18 h的光吸收特性.如图6(a)所示,样品的吸收带边皆约为525 nm,CdS-12 mL-18 h表现出更高的光吸收强度.此外,如图6(b)所示,由Kubelka-Munk函数得到样品的禁带宽度也基本一致.这说明,分散良好的硫化镉纳米线有助于提高硫化镉的光吸收性,但不改变材料的禁带宽度和吸收带边.
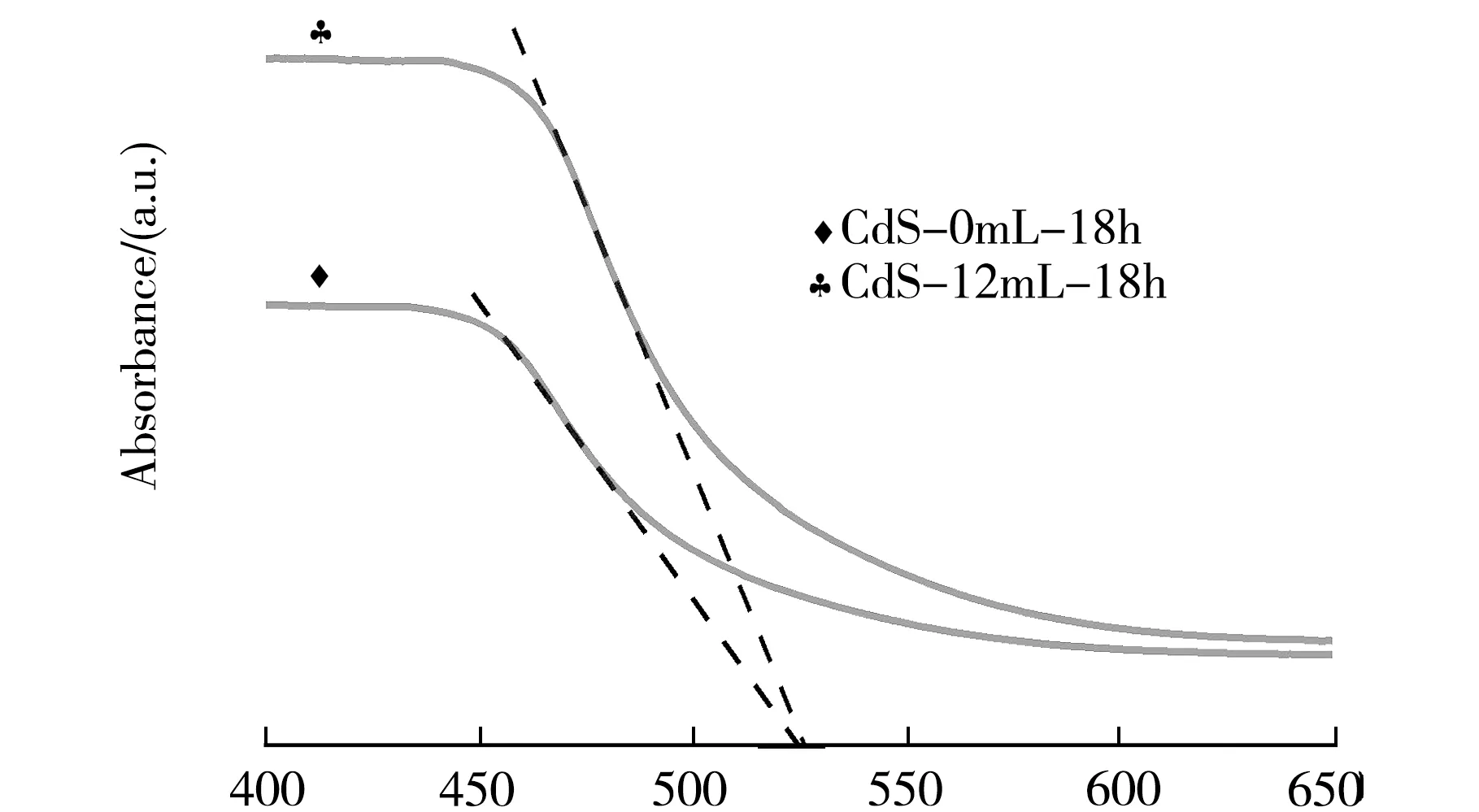
Wavelength/nm
2.5 CdS NWs的光催化性能
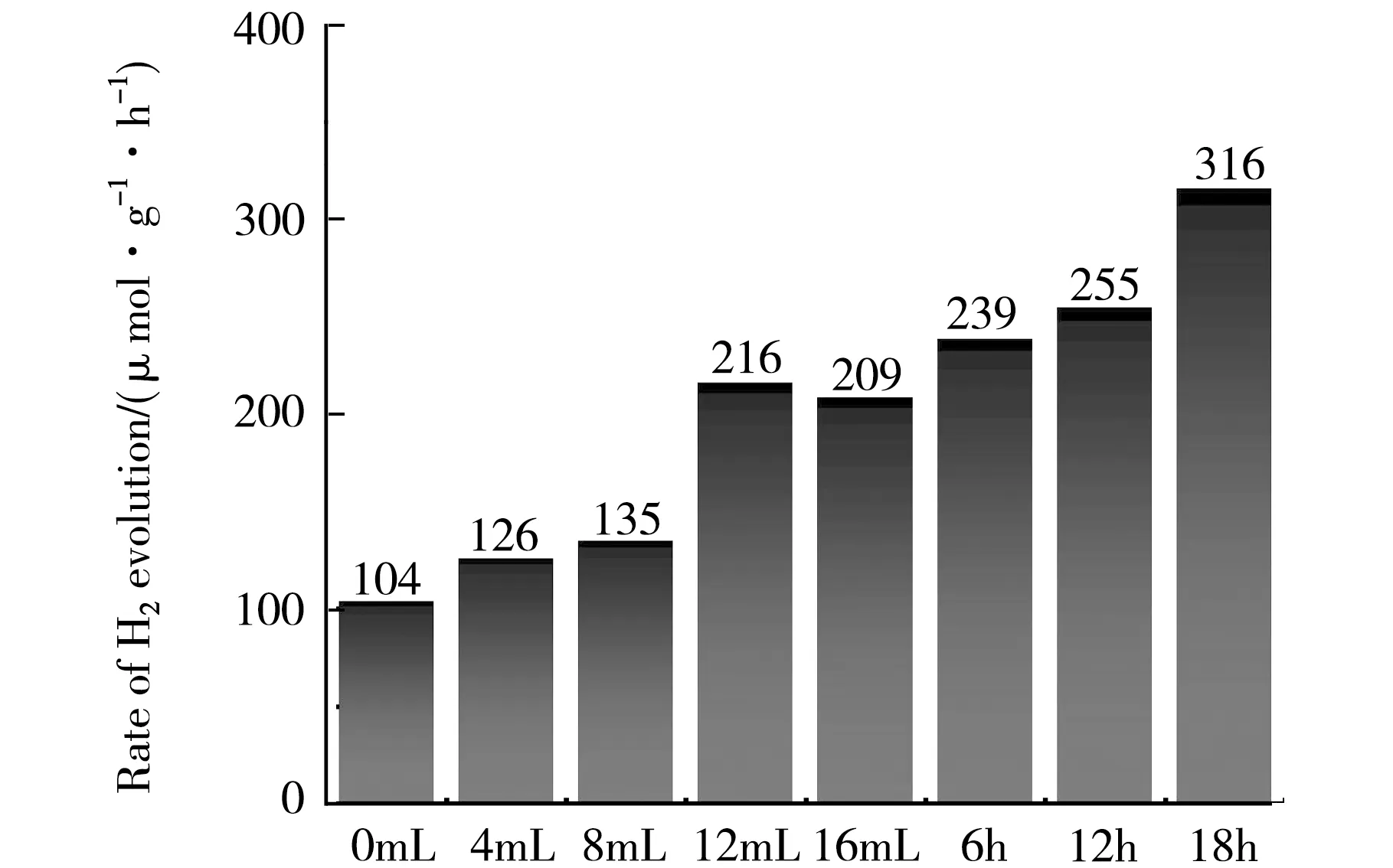
以Na2S-Na2SO3为牺牲剂,在可见光(λ≥420 nm)照射下,对比研究了样品的光催化产氢活性.如图6(a)所示,随着EDA含量的增加,CdS NWs的产氢速率呈现递增的趋势.当EDA加入量为12 mL时,光催化产氢速率在该系列样品中达到最大216 μmol·g-1·h-1,约为不加EDA的样品的2.1倍.进一步增加EDA用量后,产氢速率有所下降,这是由于团聚现象阻碍了光生载流子的迁移和分离.此外,在加入12 mL EDA的情况下,随着溶剂热时间的延长光催化产氢速率逐渐提高,见图6(b).当延长晶化时间至18 h,具有最佳纳米线形貌的CdS产氢速率达到316 μmol·g-1·h-1,约为不加EDA时样品产氢速率的3.0倍.
进一步,对样品(CdS-12mL-18h)进行了产氢循环实验,用以研究其光催化稳定性.因为光催化剂的耐久性和稳定性直接决定了其能否应用于实际生产的需要[16].如图6(c),在可见光照射12 h的重复实验中,应进行到第4个循环时的产氢速率约为初始值的 81%,仍具有良好的光催化产氢速率,表明所制得的CdS NWs是一种性能比较稳定的光催化剂.
2.6 CdS NWs的电化学性能
为了验证CdS维度对光生载流子转移和分离情况的影响,分别对水热合成制备的CdS颗粒、EDA溶剂热制备的CdS纳米线进行了电化学阻抗(EIS)和瞬态光电流响应(I-t)测试[17].如图7所示,CdS-12 mL-18h的半圆半径更小、光电流密度更高,这和其更高的光催化产氢速率一致.这可以归因于纳米线所具有的更高的长径比和比表面积,有效缩短了光生电子和空穴从体相向表面的移动距离,抑制了体相内的复合,加速了电子-空穴对的转移和分离,从而促进了光催化产氢速率的提高[18].
CdsNWs
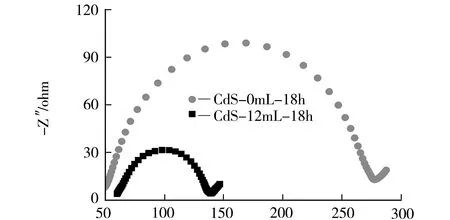
Z′/ohm
3 结 论
利用简单可控的EDA溶剂热法成功制备了具有较高长径比、分散均匀的一维CdS纳米线.EDA的用量在CdS纳米线的形成过程中具有重要作用.优化条件下制备的高结晶度、纯净的CdS NWs由于存在大的比表面积/体积比,缩短了光生电子和空穴的迁移距离,有效抑制了光生载流子的复合,使光催化产氢速率达到316 μmol·g-1·h-1.且该光催化剂在12 h的光催化产氢循环实验中还具有81%的初始产氢速率,表现出良好的稳定性.这为以一维线状形貌CdS的进一步改性修饰奠定了基础.

