硅/铝掺杂对针铁矿的表面性质和吸附磷的影响
刘 鑫,吕青檐,魏世勇
(湖北民族大学 化学与环境工程学院,湖北 恩施 445000)
磷是植物生长必需的主要营养元素之一,也是引起水体富营养化的主要因素.磷在土壤中的赋存形态决定着磷的有效性和流失状况.土壤中的磷素主要是无机磷酸盐,它可与土壤黏粒矿物发生多种作用,从而影响土壤磷的赋存形态、生物有效性及环境效应[1-2].吸附作用是土壤中磷素与黏粒矿物之间常见的作用方式.土壤中黏粒矿物可吸附溶解态磷于土壤固相表面,减少土壤磷的流失和环境污染;吸附态磷是一种潜在有效磷,可解吸进入土壤溶液供作物吸收利用[1,3-4].可见,深入认识黏粒矿物对磷的吸附特性,可为调控土壤磷的利用率、有效性和环境污染提供科学依据.
氧化铁广泛分布于各类土壤中,是土壤中重要的活性黏粒矿物,对土壤结构和性质有显著影响[1-2,5].针铁矿是土壤中最常见的晶质氧化铁,其颗粒尺寸一般在几百纳米到数微米之间,表面功能团主要是两性铁羟基(≡Fe-OH)和边缘不饱和的铁原子,表面通常带可变正电荷[4-7].针铁矿对溶液中磷酸盐的吸附能力较强,最大吸附量可达50 mg/g左右,吸附机制主要有表面配位和静电引力[5-6,8-9].红壤去铁后表面正电荷减少,导致样品对磷的吸附量明显降低[8,10].在悬浮液体系中,针铁矿对磷酸盐的静电吸附与溶液的酸碱度和离子强度相关.升高介质溶液的离子强度会导致氧化铁矿物表面的可变电荷量也随之增加,在高pH值条件下不利于矿物表面对磷酸盐的静电吸附,而低pH时可促进对磷的吸附[3,5-6,11].磷酸盐与针铁矿表面羟基通常以配位形式键合,双基配位的磷比单基配位更稳定;当反应体系的pH较低时,H2PO4-的相对含量较高有利于单基配位,pH高时有利于双基配位;磷酸盐的浓度影响着针铁矿对磷的吸附结合方式,高浓度时易形成单核配合物,低浓度时则形成双核配合物[9-14].可见,针铁矿对磷的吸附特性与介质溶液的pH值、离子强度、磷浓度等因素密切相关.此外,针铁矿对磷酸盐的吸附机制还包括离子交换、表面沉淀等作用[5-6,13-14].
土壤中的氧化铁普遍存在硅、铝掺杂现象,土壤发育的程度越深,氧化铁中硅、铝掺杂的比例往往越高[15-16].研究表明,硅、铝掺杂后氧化铁的结晶度变差,产物的颗粒尺寸、比表面积和表面吸附能力都有明显变化[15-17].方敦等[18]报道,硅、铝掺杂降低了纤铁矿的结晶度,升高了其比表面积;与纤铁矿比较,硅、铝掺杂产物对氟的吸附量升高,但吸附速率有所降低.纤铁矿和针铁矿都属于含羟基的晶质氧化铁,但它们的形成条件、晶体结构、表面特性等方面有较大差异[9,15,18].因此,在合成针铁矿的体系中掺杂硅或铝,掺杂产物的结构与性质将发生怎样的改变、表面吸附特性如何等问题还需进一步研究.本研究在合成针铁矿的水热体系中分别添加少量的硅或铝,分析了针铁矿及硅、铝掺杂产物的微观结构和表面性质,并研究了不同形态氧化铁对磷酸盐的吸附特性.这些研究有助于深入理解土壤中硅、铝掺杂氧化铁与无机磷酸盐的界面作用特性,其结果可丰富土壤磷的地球化学循环理论,为合理调控土壤磷的有效性和环境污染提供基础数据.
1 实验方法
1.1 样品制备
针铁矿(Goe)的制备:磁力搅拌状态下,向100 mL 1 mol/L Fe(NO3)3溶液中加入5 mol/L KOH溶液至悬浮液的pH=12.0,用蒸馏水将反应悬浮液的总体积稀释至2 L,然后密闭塑料烧杯,置于70 ℃油浴中静置老化60 h.悬浮液冷却至室温后离心分离,沉淀物用超纯水清洗,样品60 ℃烘干、碾磨过筛、保存备用.
硅掺杂针铁矿(Goe-Si)的制备:磁力搅拌状态下,将1.14 g硅酸钠(Na2SiO3·9H2O)加入到100 mL 1 mol/L Fe(NO3)3溶液中,然后加入5 mol/L KOH溶液至悬浮液的pH=12.0,用蒸馏水将反应悬浮液的总体积稀释至2 L,然后密闭塑料烧杯,置于70 ℃油浴中静置老化60 h.悬浮液冷却至室温后离心分离,沉淀物用超纯水清洗,样品60 ℃烘干、碾磨过筛、保存备用.
铝掺杂针铁矿(Goe-Al)的制备:磁力搅拌状态下,将0.96 g氯化铝(AlCl3·6H2O)加入到100 mL 1 mol/L Fe(NO3)3溶液中,然后加入5 mol/L KOH溶液至悬浮液的pH=12.0,用蒸馏水将反应悬浮液的总体积稀释至2 L,然后密闭塑料烧杯,置于70 ℃油浴中静置老化60 h.悬浮液冷却至室温后离心分离,沉淀物用超纯水清洗,样品60 ℃烘干、碾磨过筛、保存备用.
1.2 样品分析
样品中铁、铝和硅含量的测定:用电感耦合等离子体(ICP)法测定样品中Fe、Al和Si的质量分数,称取粉末样品20 mg于50 mL聚乙烯离心管中,消解以后在12 000 r/min的转速下离心,上清液中Fe、Al和Si的质量分数在Varian Vista-MPX ICP-OES上测定.
X-射线衍射(XRD)分析的仪器型号为德国布鲁克公司D8 ADVANCE型,CuKα(λ=0.154 06 nm)辐射.扫描电镜(SEM)分析的仪器型号为日本电子JSM-6700F,粉末样品于导电胶表面真空镀碳后观察样品表面形貌.样品的比表面积及孔隙状况分析在全自动比表面和孔径分布分析仪(Quantachrome Autosorb-1型)上进行,分别用BET(Brunauer-Emmett-Teller)、HK(Horvath-Kawazoe)、FHH(Frenkel-Halsey-Hill)方法分析样品的比表面积、孔径分布和表面分形度,根据N2吸附总量计算样品的总孔体积.酸碱滴定法分析样品的表面质子电荷量(qH),参照文献[5]中的方法进行.
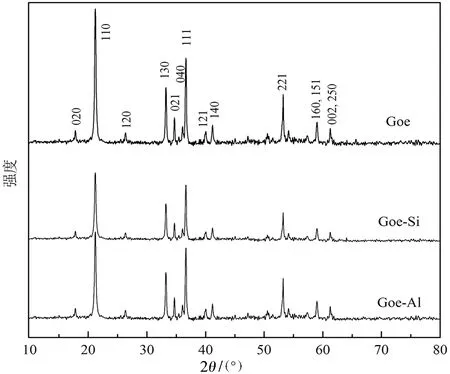
图1 样品的X-射线衍射(XRD)分析Fig.1 X-ray diffraction (XRD) images of the samples
1.3 吸附实验
配制含磷400 mg/L的磷酸盐(KH2PO4)储备溶液以及2.0 g/L矿物样品悬浮液,用0.01 mol/L KOH或HCl溶液将其pH调至5.0.
动力学吸附实验:吸附体系的矿物样品浓度为1.0 g/L,磷初始浓度为100 mg/L,250 r/min条件下持续振荡.在设定的时间及时取样,10 000 r/min离心10 min得到上清液,用钼锑抗分光光度法检测磷的浓度,计算样品对磷的吸附量.
等温吸附实验:吸附体系中磷初始浓度为2~200 mg/L,矿物样品浓度均为1.0 g/L,在25 ℃、转速为250 r/min条件下振荡24 h.其余步骤参照动力学吸附实验.
热力学吸附实验:吸附体系的温度分别控制为10、20、30 ℃和40 ℃,矿物样品浓度均为1 g/L,磷初始浓度为100 mg/L,在250 r/min条件下振荡24 h.其余步骤参照动力学吸附实验.
2 结果与讨论
2.1 样品的表征
2.1.1 样品的结构与形貌 3种矿物样品的X-射线衍射(XRD)分析见图1.Goe的XRD图谱中出现了一系列强度较高、峰形尖锐的衍射峰,它们都可归属为针铁矿晶体(PDF#29-0713)各晶面的衍射峰,这表明Goe结晶度良好且纯度较高[5,15].Goe-Si和Goe-Al的XRD图谱中也出现了明显的针铁矿特征峰,且没有其它晶体衍射峰出现.可见,在形成针铁矿的水热体系中,掺杂少量的硅、铝没有改变产物的晶体类型.与Goe相比,Goe-Si和Goe-Al的衍射峰强度减弱且宽化,这说明Goe-Si和Goe-Al的结晶度降低.样品的扫描电镜(SEM)结果见图2.3种样品都为棒状颗粒,Goe的颗粒长度大多在1~2 μm之间,Goe-Si和Goe-Al的颗粒长度主要在1 μm左右.可见,相对Goe而言,Goe-Si和Goe-Al的结晶度降低因而颗粒尺寸变小.

(a) Goe (b) Goe-Si (c) Goe-Al图2 样品的扫描电镜(SEM)图Fig.2 Scanning electron microscope (SEM) images of the samples
2.1.2 样品的组成及表面性质 Goe中Fe的质量分数为54.64%,Goe-Si中Fe和Si的质量分数分别为47.52%和1.31%,Goe-Al中Fe和Al分别为50.26%和1.07%.可见,Goe-Si和Goe-Al中铁的质量分数都低于Goe,其中Goe-Si中铁含量最低;Goe-Si和Goe-Al中分别含有少量的Si和Al.3种样品的表面孔性参数及表面分形度列于表1.与Goe相比,Goe-Si和Goe-Al的BET表面积和孔体积均明显增大,而平均孔径减小,其中Goe-Si的这些参数变化更大.3种样品的表面分形度略有差异,大小关系为Goe 表1 样品的孔性结构参数及表面分形度Tab.1 Pore structure parameters and surface fractal degree of the samples 图4 样品对磷的吸附动力学曲线Fig.4 Kinetic curves of phosphate adsorption on the samples 图3为样品的质子电位滴定曲线.Goe、Goe-Si和Goe-Al的表面质子电荷量qH均随pH升高而持续下降,它们的表面电荷零点pHZPC分别为7.5、7.5和6.8.当悬浮液的pH=5.0时,3种样品的表面都带正电荷,Goe、Goe-Si和Goe-Al的qH分别为0.21、0.30和0.27 mmol/g.根据文献[5,16],在一定的pH范围内矿物悬浮液的质子缓冲容量(即质子消耗量,ΔqH)与其表面羟基含量有高度的正相关性.当电解质为0.01 mol/L KCl时,Goe、Goe-Si和Goe-Al的悬浮液从pH=10.0降低到pH=4.0消耗的质子量分别为0.60、0.74和0.73 mmol/g,表明硅、铝掺杂导致样品的表面羟基含量明显增大. (a) Goe(b) Goe-Si (c) Goe-Al图3 样品的质子滴定曲线Fig.3 Proton titration curves of the samples 表2 样品对磷的动力学吸附方程拟合参数Tab.2 Fitting parameters of the kinetic models of the samples adsorbing phosphate 2.2.1 动力学吸附 图4为样品对磷酸盐的动力学吸附曲线.在吸附最初的70 min内,Goe的吸附量随着时间的延长明显增加,之后吸附逐渐达到平衡.Goe-Si的吸附量在前70 min内随着时间的延长明显增加,在70~150 min时吸附量仍然不断增加,150 min以后吸附量逐渐趋于平稳.Goe-Al的吸附量在前50 min内随着时间的延长明显增加,在50~150 min时吸附量缓慢增加,150 min以后吸附达到平衡状态.可见,铝、硅掺杂产物对磷酸盐的吸附需要更长的时间才能达到平衡状态.相对Goe而言,Goe-Si和Goe-Al的平均孔径减小、表面异质性增加(表1);这导致吸附体系中磷酸根离子在掺杂产物表面的分配过程更复杂,且孔间传递速率减缓,因而吸附达到平衡状态需要更长时间. 用准一级动力学方程和准二级动力学方程对样品吸附磷的动力学数据进行拟合分析,2个方程的表达式分别见式(1)和(2): (1) (2) 式中,qt为时间t(min)时样品对磷的吸附量,mg/g;qe为样品对磷的平衡吸附量,mg/g;k1(L/min)和k2[g/(mg·min)]分别为准一级、准二级动力学速率常数[7,16,19]. 动力学方程拟合参数列于表2.拟合结果中,动力学吸附速率常数都表现为Goe-Si 图5 样品对磷的等温吸附曲线Fig.5 Isothermal adsorption curves of phosphate on the samples 表3 样品对磷的等温吸附模型拟合参数Tab.3 Fitting parameters of isothermal adsorption models for phosphate by the samples 图6 样品对磷的热力学吸附曲线Fig.6 Thermodynamic adsorption curves of phosphate by the sample 2.2.2 等温吸附 图5为样品对磷酸盐的等温吸附曲线.磷的质量平衡浓度ce从0升高到180 mg/L,3种样品的吸附量qe逐渐增加直至趋于饱和状态.吸附达到平衡状态时,3种样品对磷的最大吸附量qe差异较大,大小关系表现为Goe-Si>Goe-Al>Goe.根据文献[2-3,5-6,21],样品的比表面积和孔体积增加有利于表面物理吸附,表面金属羟基含量增多将促使样品表面与磷酸根离子之间的表面配位及离子交换作用,表面正电荷量升高可加强样品表面对磷酸根离子的静电引力.比较3种样品的表面性质(表1和图3),它们的比表面积、孔体积、表面羟基含量和pH=5.0时表面正电荷量都表现为Goe-Si>Goe-Al>Goe,因此其表面最大吸附量也有同样的变化趋势. 选用Langmuir和Freundlich等温吸附模型拟合分析样品对磷的等温吸附数据,两种模型分别见式(3)和(4): (3) (4) 式中,qe和qm分别为样品对磷的吸附量和饱和吸附容量,mg/g;ce为吸附体系中磷的质量平衡浓度,mg/L;b为表示吸附亲和力的参数,L/mg;k为与吸附容量相关的参数,(mg1-(1/n)·L1/n)/g;1/n为表示吸附强度的参数;Langmuir模型适合描述吸附剂表面均匀位点的单层吸附,而Freundlich模型适合描述异质性表面的多层吸附[6-7,10,21-23]. 两种等温吸附模型的拟合参数列于表3.3种样品对磷酸盐的等温吸附过程适合用Langmuir模型拟合(R2=0.980 4~0.989 0).这说明3种样品对磷的吸附主要属于匀质性单层模式.Goe、Goe-Si和Goe-Al对磷的饱和吸附容量(qm)分别为21.96、38.48和30.26 mg/g.3种样品的吸附亲和力参数b的大小关系为Goe>Goe-Al>Goe-Si,其相对大小关系与样品的吸附容量qm相反.这表明硅、铝掺杂样品对磷的吸附容量明显增加,但吸附亲和力却有所减小.Freundlich模型对3种样品吸附磷的拟合度都较低(R2=0.860 2~0.918 4),说明吸附作用中异质性表面的多层吸附贡献较小;与Goe比较,Goe-Si和Goe-Al的拟合相关系数R2略高,说明硅、铝掺杂增加了样品的表面异质性,致使多层吸附有所增加,这也是导致Goe-Si和Goe-Al的最大吸附量增加的原因之一. 2.2.3 热力学吸附 图6为Goe、Goe-Si和Goe-Al对磷酸盐的热力学吸附数据.3种样品对磷的吸附受温度的影响情况较为类似.在10~40 ℃范围内,3种样品对磷的吸附量qe均随温度的升高而不断增加,这种增加趋势在10~20 ℃范围内更明显.可见,升温有利于样品对磷的吸附. 用吉布斯自由能变、修正后的吸附体系分布系数和Van’t Hoff 3种热力学方程对热力学吸附数据进行拟合,3种方程分别见式(5)(6)(7). ΔGθ=-RTln(Kc), (5) (6) (7) 式中,Kc、R和T分别为无量纲的分布系数、理想状态气体常数(8.314 J/(mol·K))和吸附体系的温度(K);ΔGθ、ΔHθ和ΔSθ分别为吸附的标准自由能变(kJ/mol)、焓变(kJ/mol)和熵变[J/(mol·K)];Qe和Ce分别为平衡吸附量(mmol/g)和吸附质的摩尔平衡浓度(mmol/L)[7,11,14].根据文献[11,20,22],ΔGθ的正负可判断吸附是自发/非自发过程,ΔHθ的正负可判断吸附作用是吸热/放热过程,ΔSθ的正负可判断吸附剂表面的无序度增加/减小. 表4 样品对磷的热力学吸附参数Tab.4 Thermodynamic parameters of phosphate adsorption on the samples 拟合的热力学参数列于表4.吸附温度在10~40 ℃范围内,3种样品吸附磷的ΔGθ均为负值,且ΔGθ随着温度的升高而降低.这说明3种样品对磷的吸附均属于自发过程,且升高温度有利于提高样品对磷的吸附自发性.当温度从10 ℃升高到40 ℃时,3种样品的ΔGθ分别减小了2.01、2.20和1.99 kJ/mol,表明3种样品对磷的吸附受温度影响的差异较小.3种样品的ΔHθ和ΔSθ均为正值,表明样品对磷的吸附均为吸热过程,且吸附反应导致样品表面的无序度增加.当温度从10 ℃升高到40 ℃时,3种样品吸附磷的热力学参数比较接近,表明铝、硅掺杂对针铁矿吸附磷的热力学特性影响较小. 水热条件下成功制备了针铁矿(Goe)和硅、铝掺杂针铁矿(Goe-Si、Goe-Al).在合成针铁矿的体系中掺杂少量的硅或铝都没有改变产物的晶体类型,但掺杂产物的结晶度降低、颗粒尺寸减小.3种样品的比表面积和pH=5.0时的表面质子电荷量都表现为Goe-Si>Goe-Al>Goe,表面分形度表现为Goe-Al>Goe-Si>Goe.相对Goe而言,Goe-Si和Goe-Al对磷酸盐的吸附需要更长的时间才能达到吸附平衡;准二级动力学方程适合描述Goe和Goe-Al对磷的动力学吸附过程,而Goe-Si的吸附数据更适合用准一级动力学方程拟合.3种样品对磷的等温吸附数据都适合用Langmuir模型拟合,饱和吸附容量表现为Goe-Si>Goe-Al>Goe.吸附热力学参数表明,3种样品对磷酸盐的吸附均为自发的吸热过程,吸附以后样品表面的无序度增加.
2.2 样品对磷的吸附

3 结论

