水溶性含氮杯芳烃的合成
张亚洲, 刘丽梅, 臧树良, 陈 平
(辽宁石油化工大学化学与材料科学学院,辽宁抚顺113001)
杯芳烃作为继冠醚与环糊精后发现的“第三代”大分子化合物,具有独特的空腔大环结构,能通过静电作用、氢键作用、疏水作用、π-π 作用及包结作用等识别离子和分子客体,还可以和金属元素配合[1-5]、分子识别[6-7]、作相转移催化剂[8-9]等,因此引起了超分子化学研究者的极大关注,并已经成为该领域的研究热点。但是由于它的特殊结构,使其具有较强的疏水性,而它的水溶性较差,使杯芳烃优良的功能远没有发挥其作用,限制了杯芳烃在涉及生命领域—水溶液体系中的研究,所以开发水溶性的杯芳烃及其衍生物成为研究的一大热点。本文经一系列化学反应合成了水溶性的杯芳烃偶氮类化合物及杯芳烃铵盐。
1 实验部分
1.1 仪器及试剂
热重分析仪TGA 型,美国Perkin-Elmer公司;傅里叶变换红外光谱仪Spetrum GX 型,美国Perkin-Elmer公司;超导核磁共振仪AV-600型,美国Brucker公司;X-6显微熔点测定仪,北京泰克仪器有限公司;气相色谱仪GC-7890Ⅱ型,上海天美科学仪器厂。
对叔丁基苯酚,工业纯;37%(质量分数)的甲醛、二苯醚、乙酸乙酯、二甲苯、对氨基苯磺酸、浓盐酸、丙酮均为分析纯试剂。以上试剂使用时按标准无水干燥方法处理。
1.2 对叔丁基杯[4]芳烃的合成
将对叔丁基苯酚和37%的甲醛溶液在碱性条件下反应,经过后处理得白色固体对叔丁基杯[4]芳烃粗产物[10],收率达到70%。
1.3 脱叔丁基杯[4]芳烃(1)的合成
将叔丁基杯[4]芳烃、苯酚、三氯化铝加入装有温度计的250mL的三口瓶中,加热至30~40 ℃恒温搅拌5h经过后处理得到白色粗产品。粗产品用氯仿和甲醇重结晶,得到无色晶体,收率达64%。
1.4 5,11,17,23-四[(对磺酸基苯基)偶氮]-杯[4]芳烃(2)的合成
制备方法参考文献[11-12],在100 mL 烧杯中,将3.51g对氨基苯磺酸加入到17.6mL 质量分数5% 氢氧化钠溶液中,微热,使对氨基苯磺酸溶解,然后用冰盐浴冷却到0 ℃以下;将1.41g亚硝酸钠用10.5 mL 水溶解,也维持温度在0~5 ℃。在搅拌下,慢慢用滴管滴入5.3 mL 浓盐酸和17.6 mL水溶液,并用淀粉碘化钾试纸检测直到变蓝色为止,此为重氮组分。继续冰盐浴15 min左右,使反应完全。将2g脱叔丁基杯[4]芳烃用DMF 溶解,加入6.46g 无水Na2CO3,加无水甲醇(V(甲醇)/V(DMF)=5∶8,共65 mL)使之成为澄清溶液,冰盐浴冷却至-5 ℃,此为偶合组分。将上述重氮组分和偶合组分两种反应液混合在一起,控制反应温度在0℃以下,冰盐浴下反应4h。此时溶液变为血红色。反应完毕加入质量分数0.25%盐酸150 mL,加热至60 ℃,继续搅拌反应1.5h 有固体生成。过滤、水洗、甲醇洗,最终得到血红色产物,收率达80%。
1.5 5,11,17,23-四氨基盐酸盐-杯[4]芳烃(3)的合成
制备方法参考文献[13],将0.371g杯四偶氮化合物加入到30 mL 质量分数为37% 盐酸中,成为悬浊液,然后向其中加入1g 锡粉,磁力搅拌,加热回流5h。反应液颜色不断发生变化,由最初的深红色逐渐变为紫红色,最后变为乳白色悬浊液。反应结束后,冰水浴中冷却,析出沉淀。抽滤,用浓HCl和丙酮、乙醚洗,得到白色固体,收率达78%。
2 结果与讨论
2.1 反应方程式
反应方程式如下所示:

2.2 产物表征分析
2.2.1 热分析 对叔丁基杯[4]芳烃的表征与分析见参考文献[10]。化合物(1)、(2)、(3)的热分析谱图见图1。
图1(a)中热失重曲线在低于100 ℃时有很小的失重,可能有少量的溶剂或H2O 未除净,而差热曲线在314 ℃左右出现一个比较强的吸热峰,说明此时有相态的变化,应该是该物质的熔化温度,与其熔点比较接近,可认为是熔化温度,同时在热失重曲线上有明显的失重,说明该化合物在高温下将发生分解,与文献[14]报道一致。

图1 化合物(1)、(2)、(3)的热分析谱图Fig.1 Thermal analysis spectrum of the compound(1),(2),(3)
图1(b)、(c)分别是化合物(2)和化合物(3)的热分析谱图。两者共同的特点是,DTA 差热曲线在低于100 ℃以下都有个小的吸热峰,同时有较小的失重,说明都有溶剂或水分子存在;随后的失重曲线也都有逐渐失重现象出现;但两者不同的是,图1(b)中差热曲线在325 ℃左右时出现了比较强的放热峰,同时热失重曲线有一拐点,这有可能是化合物(2)有明显的分解所致。而图1(c)中,在300 ℃和330 ℃左右,DTA 差热曲线上有两个明显的吸热峰,可能有相态变化或分解,同时热失重曲线有明显的失重拐点,说明化合物(3)在该温度范围内有相态的变化并伴随有明显的分解现象。
2.2.2 红外光谱 图2(a)是化合物(1)的红外光谱图。其吸收峰归属如下:3 147cm-1为—OH 伸缩振动峰;2 934cm-1为—CH2伸缩振动峰;2 867 cm-1为—CH3伸缩振动峰;1 608cm-1为苯骨架振动峰;1 145cm-1为C—O 伸缩振动峰;谱图中没有叔丁基对应的峰,可认为叔丁基已经脱除,与合成的目标产物相符。化合物(2)的红外光谱见图2(b)。其吸收峰归属 为:3 3 2 6~2 9 2 6cm-1为—OH伸 缩 振 动 峰;1 274cm-1为C—N伸缩振动峰;1 630cm-1为N-N伸缩振动峰;1190cm-1为—SO3H 伸缩振动峰;1 608cm-1为苯骨架振动峰;说明—SO3H 已引入分子中,可以认为所合成的物质为目标产物。
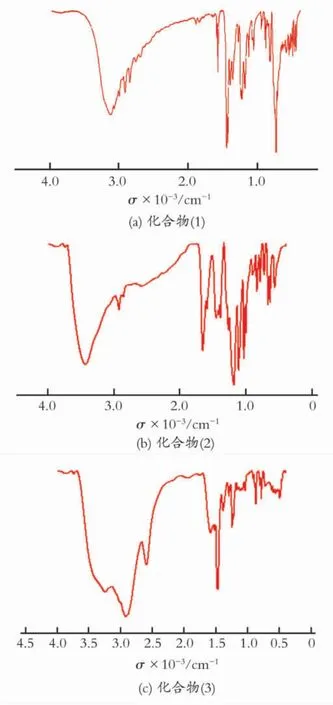
图2 化合物(1)、(2)、(3)的红外光谱图Fig.2 IR spectra of the compound(1),(2),(3)
图2(c)为化合物(3)的红外光谱图。图2(c)中,2 923cm-1为—OH 伸缩振动峰;1 248cm-1为C—N伸缩振动峰;1 608cm-1为苯骨架振动峰;2 597cm-1为—NH+3伸缩振动峰;说明已经有NH+3生成,可以认为所合成的物质为目标产物。
2.2.3 紫外光谱 图3是化合物(2)和(3)的紫外光谱图。图3(a)中共存在3个明显的吸收峰,其中在220nm 和265nm 处的2个吸收带为苯环的第2和第3吸收谱带;而在356nm 左右出现一个比较宽而强的吸收带则对应的是偶氮基的n→π*跃迁。图3(b)中化合物(3)只在220nm 和282nm 左右有吸收带,356nm 处的吸收带消失,说明偶氮基团已经不存在,也进一步证明了化合物(2)中的偶氮基团已经被还原了。

图3 化合物(2)和(3)的紫外光谱图Fig.3 UV spectrum of the compound(2)and(3)
2.2.4 核磁共振 化合物(3)的结构式为:

其化学式为C28H32C14N4O4,对应 的1H-NMR 谱 图如图4所示(以D2O 为溶剂)。在图4中各峰的归属如下:a,3.894(8H,单峰,CH2);b,7.062(8H,单峰,ArH)。—OH 和—NH+3两者的峰在谱图中并未显示出来,可能是溶剂D2O 有质子交换所致,δ=3.424(2H,四重峰,CH2)和δ=0.921(3H,三重峰,CH3)应是溶剂乙醚的峰。所以与结构式比较符合。

图4 化合物(3)的核磁共振谱图Fig.4 The nuclear magnetic resonance spectrogram of the compound(3)
2.3 实验方法的改进
2.3.1 化合物(3)的合成方法的改进 在杯芳烃分子中引入—NH2从而转变成铵盐(NH+3),可以增加杯芳烃的水溶性,实现其在水溶液中使用的目的。一般的—NH2大都是通过—NO2还原得到的,即

但是这条路线很难实现,原因是四硝基杯四芳烃(b)中由于羟基的活性较高,导致四个硝基很难同时被还原,可以还原部分硝基[15-17]。有可能其中一个、两个、三个硝基被还原,生成的是几种混合物。文献[18-19]报道,羟基醚化后再硝化还原,可同时还原4个硝基,即

在实验室中尝试着用各种方法还原硝基,效果均不理想,其实验结果列于表1。

表1 不同方法还原四硝基杯四芳烃对比Table 1 Different methods for four aromatic nitro cup contrast reduction
文献[12]通过偶氮化合物在酸性条件下还原合成铵盐的方法值得借鉴。以对氨基苯甲酸与杯四芳烃为原料,采取下列方法得到了杯芳烃铵盐。效果较好,收率较高。

但是对氨基苯甲酸比较贵,而对氨基苯磺酸的结构与对氨基苯甲酸相似,都有利于重氮化并与杯芳烃发生偶合反应,而且对氨基苯磺酸价廉、易得、反应活性高,因此实验中以对氨基苯磺酸代替对氨基苯甲酸,取得了良好的效果。合成结果见表2。
从表2中可以看出,两种药品的价格相差很大,虽然用两种原料合成产品收率相差无几,但原料成本几乎是近5倍的差距,所以实验方案改进合理。

表2 杯四芳烃偶氮化合物合成对比Table 2 Cup four aromatic azo compound synthesis contrast
2.3.2 化合物(2)合成中实验条件的影响 化合物(2)合成中,体系的酸碱性对该反应的影响比较大,文献[13]以无水醋酸钠溶液来调节体系的pH,这样可以和体系中存在的酸形成缓冲溶液,维持体系稳定的酸碱环境。实验中对此也做了改进,以廉价的无水碳酸钠代替无水醋酸钠,也达到了相同的结果。另外,化合物(2)在不同的条件下处理,得到的产物物理性质略有区别,对比如下:
酸性条件:产物结构为

物理化学性质为桔黄色粉末状固体,溶于DMSO和DMF,适度溶于甲醇,微溶于水、乙醇和丙酮,但不溶于氯仿、乙醚等非极性有机溶剂。

碱性条件:产物结构为物理化学性质为橙红色粉末状固体,易溶于水、碱和酸性水溶液、DMSO 和DMF,适度溶于甲醇,微溶于乙醇和丙酮,但不溶于氯仿、乙醚等非极性有机溶剂。
3 结论
以对氨基苯磺酸和杯[4]芳烃为原料合成杯[4]芳烃偶氮化合物,经杯[4]芳烃偶氮化合物还原得到结构比较单一的杯[4]芳烃铵盐,改进后的方法大大降低了成本,合成方法简单,产品比较单一。
[1] 王勇平,郑利民,咸春颖.对叔丁基杯[4]芳烃衍生物对K+的液膜传输规律的研究[J].化学工程与装备,2009,1:34-37.
[2] 陈雪梅,李海冰.硫(硒)杂多酸杯[4]芳烃合成及其络合物性能研究[J].有机化学,2008,28:11-15.
[3] 刘芳,罗欣,贺启环.杯[4]芳烃及其酯类衍生物对贵金属离子Ag+的回收研究[J].云南环境科学,2005,24:1-3.
[4] Tran H A,Ashram M,Mizyed S,et al.O-Ethoxy carbonyl methoxy esters of homo calix[n]naphthalenes:synthesis and recognition behaviour towards alkali cations[J].J.Incl.Phenom Macrocycl Chem.,2008,60:43-49.
[5] Makrlík E,Vaura P,Budka J.Extraction of H+,NH+4,Ag+and Tl+into nitrobenzene by using sodiumdicarbollyl cobaltate in the presence of tetramethyl p-tert-butylcalix[4]arene[J].Journal of Radio Analytical and Nuclear Chemistry,2008,275(2):459-461.
[6] 王建红,曹端林,胡志勇,等.杯芳烃对中性分子识别的最新研究进展[J].天津化工,2007,21(5):9-12.
[7] 吕鉴泉,陈朗星,郭洪声,等.杯芳烃的功能化修饰及其在分子识别中的应用[J].化学进展,2001,13(3):209-213.
[8] 赵芳,梁斌,刘道杰.杯芳烃催化剂的研究进展[J].信阳师范学院学报:自然科学版,2006,19(3):364-366.
[9] 孟祥启,冯亚青,孟舒献,等.杯芳烃作为相转移催化剂用于四氟对苯二甲酸二甲酯的合成[J].化学试剂,2006,28(1):5-7.
[10] 武秋朋,赵群力,陈平,等.对叔丁基杯[4]芳烃及其醚类衍生物的合成[J].石油化工高等学校学报,2011,24(5):48-52.
[11] 刘爱林,傅崇岗,张立云,等.新型水溶有色主体分子对磺酸基苯偶氮杯[n]芳烃衍生物的合成及特性[J].化学试剂,2002,24(6):331-334.
[12] Lu L L,Zhu Sh F,Liu X Z,et al.Highly selective chromogenic ionophores for the recognition of chromium(III)based on a water-soluble azocalixarene derivative[J].Anal.Chim.Aeta,2005,535(1-2):183-187.
[13] 卢欢欢.杯[4]芳经衍生物的合成及性质的初步研究[D].长春:东北师范大学,2010.
[14] 胡小安,陈栋华,沈玉芳,等.对叔丁基杯[4]的热力学和热分析动力学[J].中南民族大学学报:自然科学版,2002,2:12-15.
[15] Jogani S K,Menon S K,Agrawal Y K.Synthesis and characterization of a calix[4]arene shiff base and its complexation studies with transition metal ions[J].Synth React Inorg Met-Org Chem.,2002,32(3):603-615.
[16] Beer P D,Drew M G B,Hesek D,et al.Anion recognition properties of new upper-rim bis[rhenium (I)bipyridyl,ruthenium(ⅱ)bis(bipyridyi),cobaltocenium receptors dictated by lower-rim substituents[J].Chem.Commun.,1996:2161-2162.
[17] Seiji Shinkai,Takashi Arimura,Koji Araki,et al.Syntheses and aggregation properties of new water-soluble calixarenes[J].Chem.Soc.Perkin Trans I,1989:2039-2045.
[18] Seiji Shinkai,Yoshiharu Shirahama,Takayuki Tsubaki,et al.Calixarene-catalyzed basic hydrolysis of p-nitrophenyl dodecanoate:A possible change in the mechanism from“deshielding”to“host-guest”[J].J.Am.Chem.Soc.,1989,111:5477-5478.
[19] Li Lei,Lv Ping,Xian Chunying,et al.Synthesis of novel calix[4]arene containing one and two substituents on the“upper rim”[J].Indian Jonural of Chemistry,2006,45:2118-2122.

