乙炔氢氯化反应体系热力学分析
王雷,沈本贤,程晓光,任若凡,肖卫国,赵基钢
(1华东理工大学化学工程联合国家重点实验室,上海 200237;2天津大沽化工股份有限公司,天津 300455)
氯乙烯单体(VCM)主要用来合成聚氯乙烯,而聚氯乙烯(PVC)是世界五大工程塑料之一,在各行各业具有非常广泛的应用。目前我国约70%以上的VCM采用乙炔氢氯化法制取,但该路线一直主要以剧毒的氯化汞/活性炭为催化剂,存在严重的环境污染问题。现在,寻找一种绿色环保的非汞催化剂已成为研究热点,已有多名学者作了非汞催化剂活性组分[1-4]及载体[5-6]方面的研究,但对其反应体系的热力学研究未见系统报道。热力学的平衡问题是化工反应过程开发的第一条线,所以对反应体系各产物的平衡转化率进行研究具有一定的理论和现实意义。
化工流程模拟软件中的Gibbs反应器模块,采用反应系统总 Gibbs自由能在平衡时取得极小[7]这个判据可以确定平衡组分。在Gibbs自由能极小、质量平衡、能量平衡的条件约束下,根据输入计算输出物质组分和物性,避开了复杂的反应方程式,可以计算在给定的温度、压力下一个化学反应体系的极限,即平衡转化率的大小。本文以Aspen软件对乙炔氢氯化反应体系热力学进行了研究。
1 乙炔氢氯化反应过程分析
乙炔氢氯化反应过程较为复杂,主要涉及的反应过程如式(1)~式(6)。
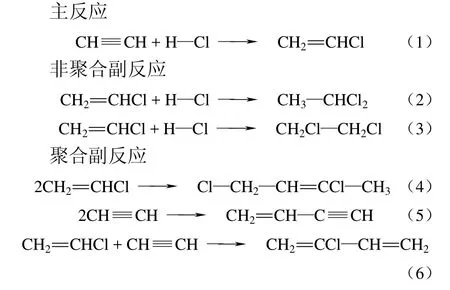
乙炔和氯化氢在催化剂的作用下主要加成生成氯乙烯[反应式(1)]。当氯化氢过量时,生成的氯乙烯会继续与氯化氢加成生成 1,1-二氯乙烷[反应式(2)]、1,2-二氯乙烷[反应式(3)]等物质,在实际的反应过程中,也检测到了该副产物[8],该反应的发生会降低氯乙烯产物的选择性。另外,反应生成的氯乙烯也可能发生自身的聚合[反应式(4)]或与乙炔发生聚合[反应式(6)];未能及时反应的乙炔之间也可能发生自身聚合[反应式(5)]。聚合产物可能会沉积在催化剂表面,形成积炭。由于多分子聚合较复杂,故在本文中仅考察双分子间聚合。
2 热力学参数与反应体系计算方法
2.1 标准状态下热力学参数
各组分在298 K、0.1 MPa下的标准熵和标准摩尔生成焓如表1所示,其中,乙炔、氯化氢、氯乙烯、1,1-二氯乙烷、1,2-二氯乙烷、乙烯基乙炔均能从手册中直接查到[9],而 1,3-二氯丁烯与氯丁二烯无直接数据可查。本文中这两种产物的热力学数据通过 Benson法[10]进行估算,该方法应用广泛,已有多篇文献[11-14]对其可靠性进行了研究,准确度高,误差在2%以下。
2.2 标准状态下反应可行性热力学分析

2.3 模拟计算
在Aspen11.1中建立反应流程,如图1所示。C2H2与HCl的摩尔流量均为1 mol/min,30 ℃常压下进行混合。混合后的气体进入Gibbs反应器反应,反应器压力为0.1 MPa,出口物流即为反应所能达到的平衡状态。
表2列出了各产物的沸点参数,仅计算90 ℃以上(其中涉及 1,3-二氯-2-丁烯的计算时产物的Valid phase采用Mixed相态,其他物质均采用Vapor相态)反应温度的平衡转化率。选用RK-SOAVE物性方程,以反应器反应温度为自变量,产物中目标组分的摩尔流量为因变量,采用 Model Analysis Tools中的灵敏度分析Sensitivity工具,分别求解了单一产物时乙炔的平衡转化率,以及不考虑聚合反应和考虑聚合反应两种理想反应情况下 90~420 ℃时各产物的平衡收率。
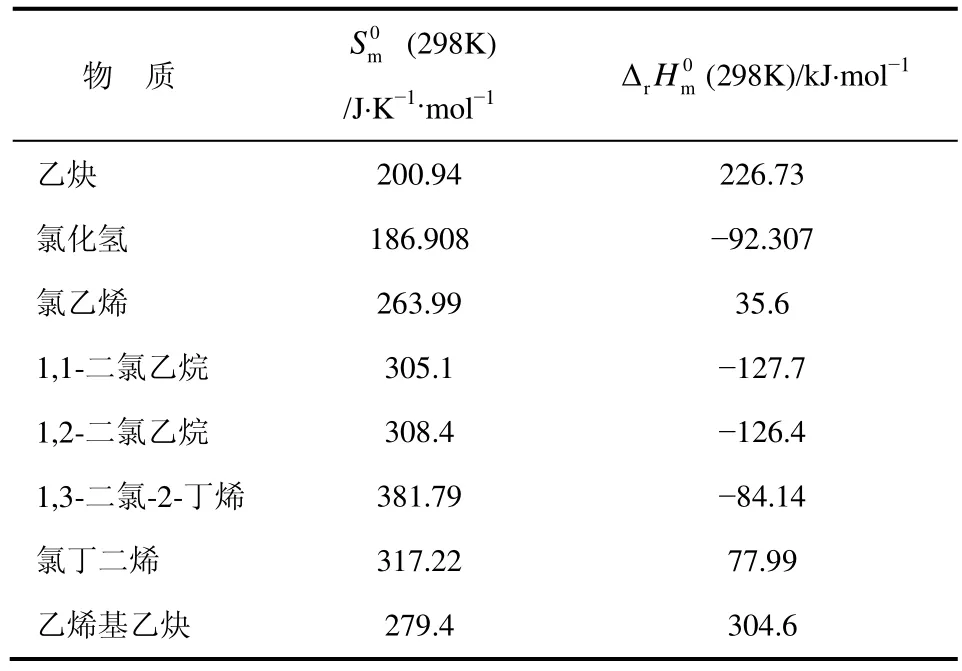
表1 标准热力学性质表
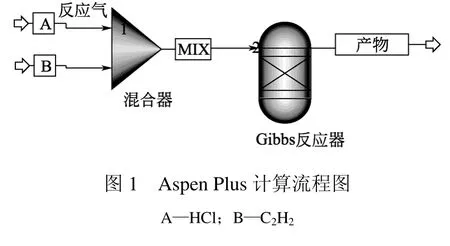

表2 产物沸点
3 结果与讨论
3.1 标准状态下反应可行性分析
由表3可知,在标准状态下主、副反应的标准吉布斯自由能均为负值,表明主、副反应均为不可逆反应。从热力学角度分析,各反应在室温下均可自发进行。还可看出,聚合反应的Gibbs自由能绝对值较大,说明聚合反应很容易发生;另外,主、副反应的标准摩尔反应焓均为负值且绝对值较大,表明主、副反应均为强放热反应。因此,有效地移除反应热和避免催化剂床层过热是反应器设计和控制中必须考虑的问题。化工热力学理论表明,对于放热反应,低温有利于反应进行,转化率较高,所以在相对较温和的工艺条件下进行乙炔氢氯化反应理论上是可行的。此外,聚合反应的热效应较主反应大,因此选择适当较高的温度又有利于抑制积炭副反应的进行,提高主反应的选择性,理论上存在一个最优的反应温度,这与Nkosi等[15]报道的实验结果相符。
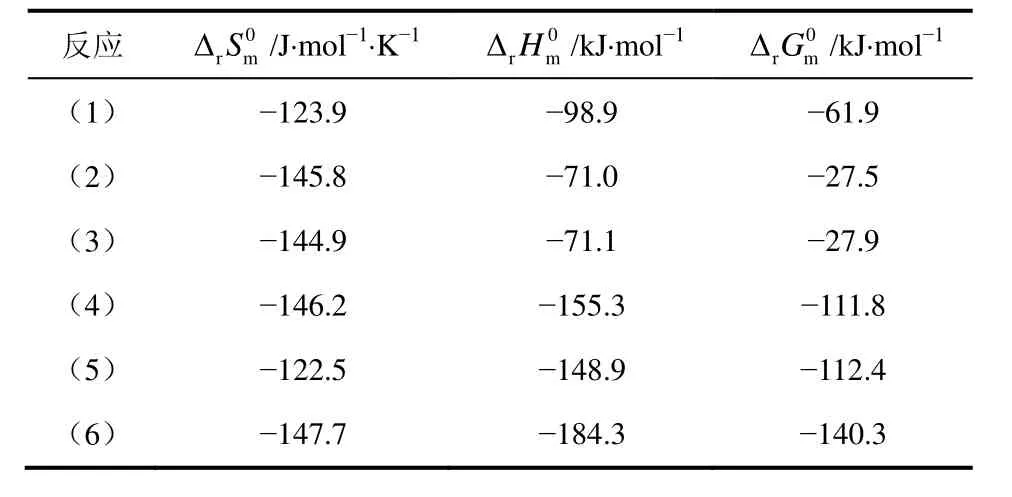
表3 298 K时反应热力学计算结果
3.2 Gibbs反应器模拟结果分析
3.2.1 单一产物时各反应乙炔平衡转化率随温度的变化
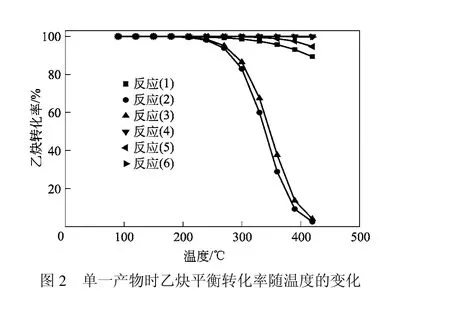
仅考虑单一产物时各反应的乙炔平衡转化率随温度变化情况如图2所示。由图2可知,在210 ℃以下时,各个反应均有很高的乙炔平衡转化率,表明各个反应均能自发进行,且反应程度大,可以认为是不可逆反应。灵敏度分析表明,低温时乙炔的平衡转化率受温度影响不大。当反应温度大于210 ℃时,主反应与聚合副反应仍保持很高的平衡转化率。随着温度的升高,主反应的平衡转化率相对于聚合副反应下降更快,表明仅提高反应温度不能达到抑制聚合副反应发生的目的。另外,对于非聚合副反应,即生成 1,1-二氯乙烷与 1,2-二氯乙烷的平衡转化率有下降趋势,表明高温不利于这两个副反应的发生。灵敏度分析表明,较高温度时,对于主反应与聚合副反应,乙炔的平衡转化率受反应温度的影响不大,但是对于非聚合副反应,反应温度对乙炔转化率影响很大,随着温度的升高,其乙炔转化率急剧下降。
3.2.2 不考虑聚合副反应时各产物平衡收率随温度的变化
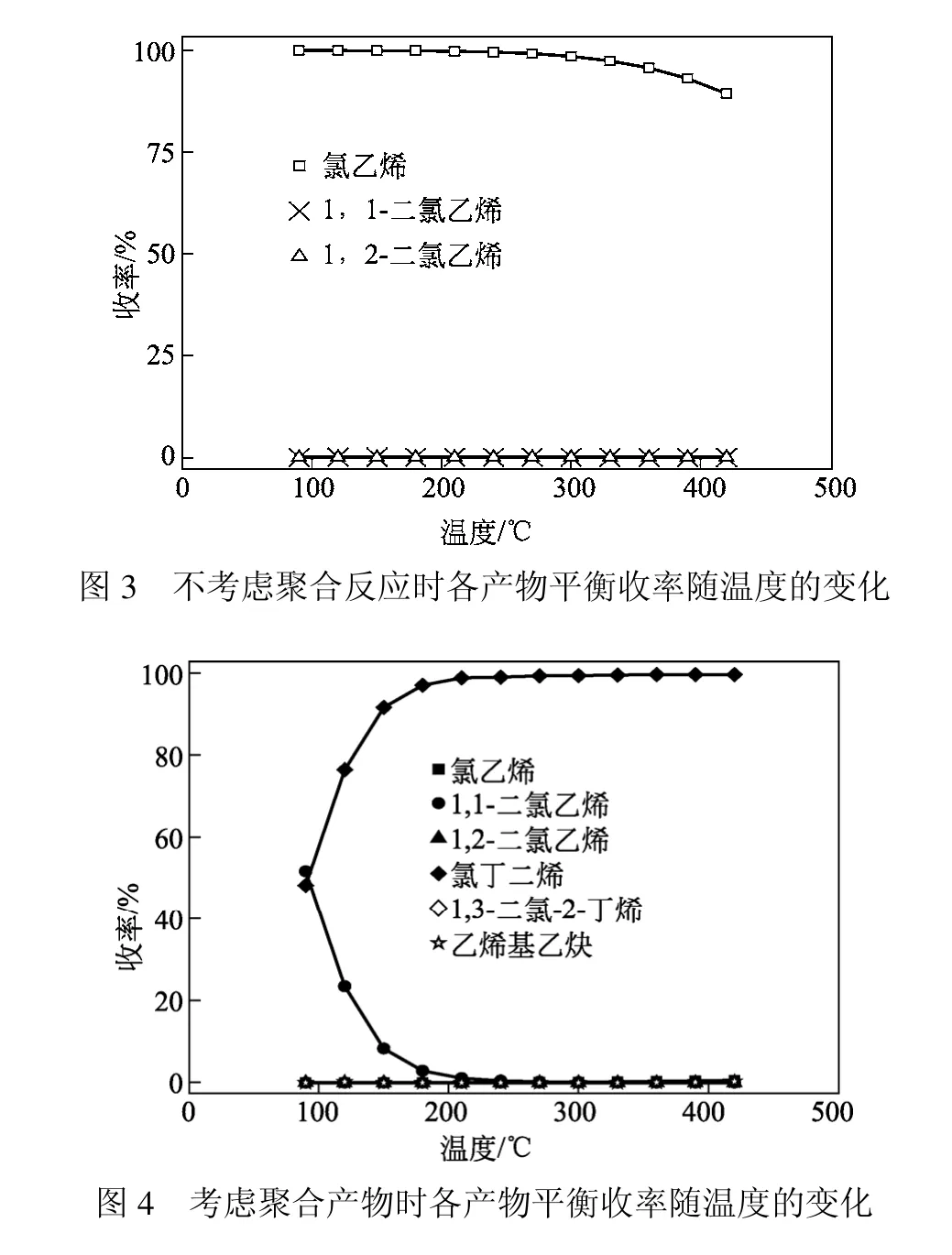
不考虑聚合反应时不同反应温度下各产物的平衡收率见图3。由图3可知,90~420 ℃范围内,氯乙烯的收率都很高。表明在不考虑聚合反应情况下,当体系达到平衡时,主要发生的是乙炔氢氯化主反应,1,1-二氯乙烷与1,2-二氯乙烷收率极低,最高时仅为0.02%,这与宋庆雷[16]报道的实验结果一致,也表明了非聚合副反应对主反应的影响很小。
3.2.3 考虑聚合反应时各产物平衡收率随温度的变化
图4为考虑聚合反应时各产物在不同温度下的平衡收率,由图4可知,90~420 ℃温度范围内,主产物氯乙烯的收率都很低,最高仅为 0.6%。180 ℃以下,主要发生的是副反应(4)和副反应(6),即生成1,3-二氯-2-丁烯与氯丁二烯的反应,而且随着温度的升高,副反应(4)逐渐占主导地位,在180 ℃以上时已成为主要反应,表明乙炔氢氯化反应生成的氯乙烯单体很容易与未反应的乙炔发生聚合生成副产物聚合物。另外,灵敏度分析表明,180 ℃以下时,1,3-二氯-2-丁烯与氯丁二烯的收率受温度影响较大;180 ℃以上时几乎不受温度影响。其他产物的收率在考察的温度范围内不受温度影响。
4 结 论
(1)热力学上主反应与副反应标况下均能自发进行,且为强放热反应,各反应的乙炔平衡转化率随温度升高而降低,且非聚合副反应下降得更快。高温不利于主反应的进行,所以实际反应过程中应及时移走反应热。
(2)当只考虑非聚合副反应时,该副反应对主反应影响不大,氯乙烯的平衡收率仍能达到 97%以上。
(3)当考虑聚合反应时,聚合反应比主反应更容易发生,尤其是氯乙烯与乙炔的反应产物氯丁二烯,平衡收率能达到99%以上,说明主反应产物很容易与未反应的乙炔发生聚合,实际反应中应避免乙炔过量。
(4)实际反应中的聚合副产物可能会沉积在催化剂表面引起积炭失活,所以在反应过程中应考虑积炭失活因素,降低积炭。
[1]HutchingsG J.Vapor phase hydrochlorination of acetylene:Correlation of catalytic activity of supported metal chloride catalysts[J].J.Catal,1985,9(1):292-295.
[2]Conte M,Carley A F,Hutchings G J.Reactivation of a carbon-supported gold catalyst for the hydrochlorination of acetylene[J].Catal.Lett.,2008,124(3-4):165-167.
[3]Mitchenko S A,Khomutov E V,Shubin A A,et al.Catalytic hydrochlorination of acetylene by gaseous HCl on the surface of mechanically pre-activated K2PtCl6salt[J].J.Mol.Catal.A:Chem.,2004,212(1-2):345-352.
[4]王声洁,沈本贤,肖卫国,等.乙炔氢氯化反应高分散载金催化剂的制备及催化性能[J].石油学报:石油加工,2010,26(2):201-207.
[5]王芳超,高官俊,胡瑞生,等.炭载体对乙炔氢氯化反应金催化剂催化性能的影响[J].化工进展,2010,29(12):2304-2308.
[6]徐龙龙,王绪根,张海洋,等.一种新型炭载体在乙炔氢氯化反应中的应用[J].化工进展,2011,30(3):536-541.
[7]黄河,李政,倪维斗.Gibbs反应器模型及其计算机实现[J].动力工程,2004,26(4):902-907.
[8]王声洁.乙炔氢氯化非汞催化反应制取氯乙烯单体研究[D].上海:华东理工大学,2010.
[9]卢焕章.石油化工基础数据手册[M].北京:化学工业出版社,1982.
[10]马沛生.化工数据[M].北京:中国石化出版社,2003.
[11]王洪波,祁增忠,夏代宽.尿素和甲醇制备碳酸二甲酯的热力学分析[J].天然气化工,2006,31(1):75-78.
[12]张立庆,赵晓辉,赵立明.催化合成丙烯酸酯的热力学分析与计算[J].精细石油化工,2006,23(6):45-49.
[13]黄荣生,莫婉林,李光兴.氧化羰基化法合成碳酸甲乙酯热力学及催化性能的研究[J].燃料化学学报,2004,32(2):129-134.
[14]张旭,王保伟.草酸二乙酯和草酸二甲酯加氢反应热力学对比分析[J].石油化工,2011,40(4):403-407.
[15]Nkosi B,Adams M D,Coville N J,et al.Hydrochlorination of acetylene using carbon-supported gold catalyst:A study of catalyst reactivation[J].J.Catal.,1991,128(2):378-386.
[16]宋庆雷.乙炔氢氯化反应新工艺及动力学研究[D].上海:华东理工大学,2011.

