NaCl-HCl体系浸出铅渣中铅的动力学分析
杨利姣,陈南春,钟夏平,解庆林,高 军,郎耀秀,刘长淼,吴照洋
(1. 桂林理工大学 材料科学与工程学院 省部共建广西有色金属及特色材料加工国家重点实验室培育基地 广西矿冶与环境科学实验中心,桂林 541004; 2. 广西科学院 应用物理研究所,南宁 530000; 3. 桂林理工大学 环境科学与工程学院,桂林 541004; 4. 广西金山铟锗冶金化工有限公司,河池 547200; 5. 河池学院 化学与生物工程学院,宜州 546300; 6. 中国地质调查局 郑州矿产综合利用研究所,郑州 450000)
随着铅消耗量增长,铅矿资源日益枯竭,从二次含铅物料中回收铅引起世界各国广泛关注。含铅物料包括含铅浸出渣、含铅烟尘和铅蓄电池废渣等,既是污染环境的有害物质,同时又是综合回收有价金属的二次资源[1]。目前,从含铅物料中湿法回收铅的方法主要有氯盐法[2-4]、碱浸法[5-6]和碳酸化转化法[7-8]等。张亚莉等[9]采用氯盐一步法浸出氧化锌贫矿提锌渣中铅和银,铅的浸出率达到95%左右。韦岩松等[10]研究硝酸浸出法从锑精矿除铅渣中回收铅,铅的浸出率达到94%。刘清等[11]提出氢氧化钠浸出-两步沉淀法从贫杂氧化锌矿中制备铅锌精矿新工艺,得到铅含量为78%(质量分数)的铅精矿,达到行业标准。ZHU等[12]研究化学转化法用碳酸铵和碳酸钠从废铅渣中回收铅,然后用过热分解法得到铅氧化物,铅回收率达98%。
有关铅回收的研究已经很多,但是关于含铅浸出渣浸出动力学的研究较少。DRAGAN等[13]研究发现,硫酸铅在氯化钙-氯化镁体系中浸出同时受扩散和化学反应控制;齐美富等[14]研究废铅酸蓄电池中铅膏在HCl-NaCl-CaCl2体系中浸取铅的动力学,发现其属于固膜扩散控制过程。本文作者在大量试验研究基础上,对比其他浸出方法,发现NaCl-HCl体系对湿法炼锌过程中产生的铅渣具有很好的浸出效果;通过考察各因素对铅浸出率的影响,发现可以用液-固多相反应的收缩核模型来分析其浸出过程动力学,以寻找强化浸出过程的措施。
1 实验
1.1 实验原料
实验原料为广西某炼锌厂的冶锌酸浸渣,又称为铅渣,其主要化学成分和XRD谱分别见表1和图1。由表1可知,铅渣含铅量较高,而图1物相分析结果表明,铅的存在形式主要为硫酸铅。
1.2 实验方法
本实验中进行温度、氯盐浓度、粒度和液固比4个因素实验。实验在500 mL圆底烧瓶中进行,按一定液固体积质量比加入NaCl溶液,在磁力搅拌器上加热搅拌,达到预热温度后,加入实验原料,用15%盐酸溶液调节pH值为1.0~1.5。反应结束后,进行热过滤,滤饼用热NaCl溶液洗涤2~3次。采用EDTA滴定法测定浸出液中铅离子质量浓度。
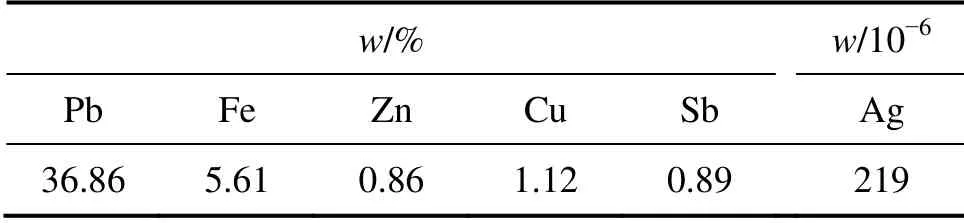
表1 铅渣主要成分分析 Table1 Main composition of lead slag
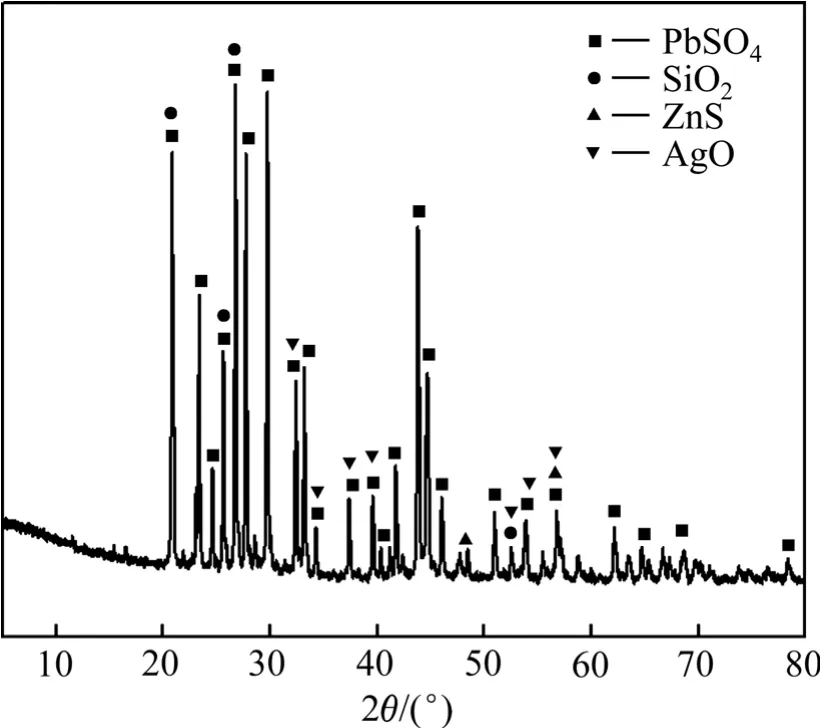
图1 铅渣XRD谱 Fig.1 XRD pattern of lead slag
1.3 动力学分析
铅渣中的铅主要以PbSO4形式存在,氯盐浸出铅的反应为
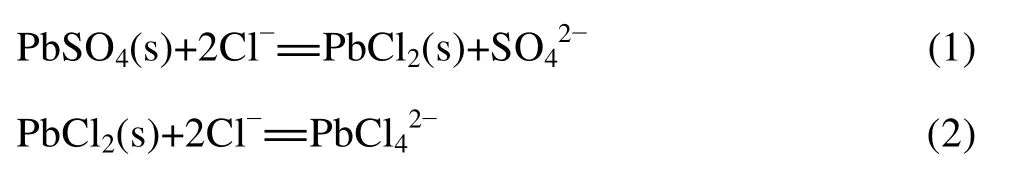
PbSO4在NaCl-HCl体系中浸出是复杂的液-固多相反应过程,浸出反应首先在固体颗粒表面发生,随着反应进行,反应逐渐向固体颗粒中心收缩,未反应核缩小。因此,氯化钠浸出铅渣过程可由未反应核收缩模型来描述。浸出过程主要由液相传质、固膜扩散以及表面化学反应3个步骤组成,在控制高速搅拌条件下,可以忽略液相传质(外扩散)对浸出速率的影响,浸出速率取决于固膜扩散或表面化学反应[15]。根据未反应核收缩模型[16],如果表面化学反应是整个浸出过程的控制步骤,那么反应速率遵循以下方程:

式中:α为铅浸出率,kr为化学反应速率常数,t为反应时间。
如果固膜扩散是整个浸出过程的控制步骤,那么反应速率遵循以下方程:

式中:α为铅浸出率,kd为扩散速率常数,t为反应时间。
式(3)和(4)中左边与反应时间t呈线性关系,直线的斜率为反应速率常数kr或kd,而反应速率常数与温度的关系,可根据阿累尼乌斯公式来表示:

式中:k为不同温度下反应速率常数,A为频率因子(s-1),Ea为活化能(J/mol),R 为摩尔气体常数[J/(mol·K)],T为绝对温度(K)。
2 结果与讨论
2.1 温度变化对铅浸出过程的影响
固定条件为:NaCl溶液300 g/L,铅渣粒度0.106~ 0.075 mm,液固比10:1,用HCl溶液调节pH值为1.0~1.5。考察浸出温度变化对Pb浸出率的影响,其结果如图2所示。
温度对铅浸出率有很大影响,在同一温度下Pb浸出率随时间延长明显增大,最后趋于不变;在同一时间下,温度越高,铅浸出率越大。当温度从60 ℃升高到90 ℃时,铅平衡浸出率由60.50%增大为90.10%。温度升高,浸出剂向固体颗粒表面扩散速度加大,化学反应速率加快[9];PbSO4在NaCl溶液中溶解度迅速增加,避免PbCl2结晶析出,降低浸出黏度,进一步加快化学反应速率[17]。
将不同温度下铅浸出率数据分别代入式(3)、(4)进行拟合(见图3),发现1-(1-α)1/3与时间t的线性关系明显优于1-2/3α-(1-α)2/3,因此,可以认为铅在NaCl-HCl体系中的浸出受表面化学反应控制,而非固膜扩散控制。
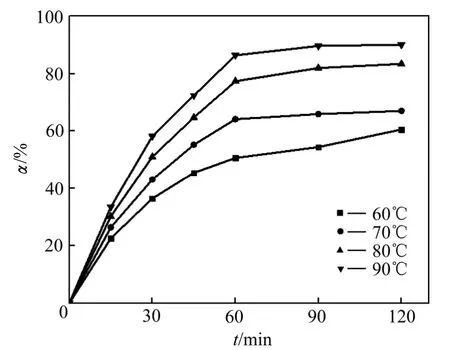
图2 温度变化对铅浸出率影响 Fig.2 Effect of temperature on leaching rate of lead
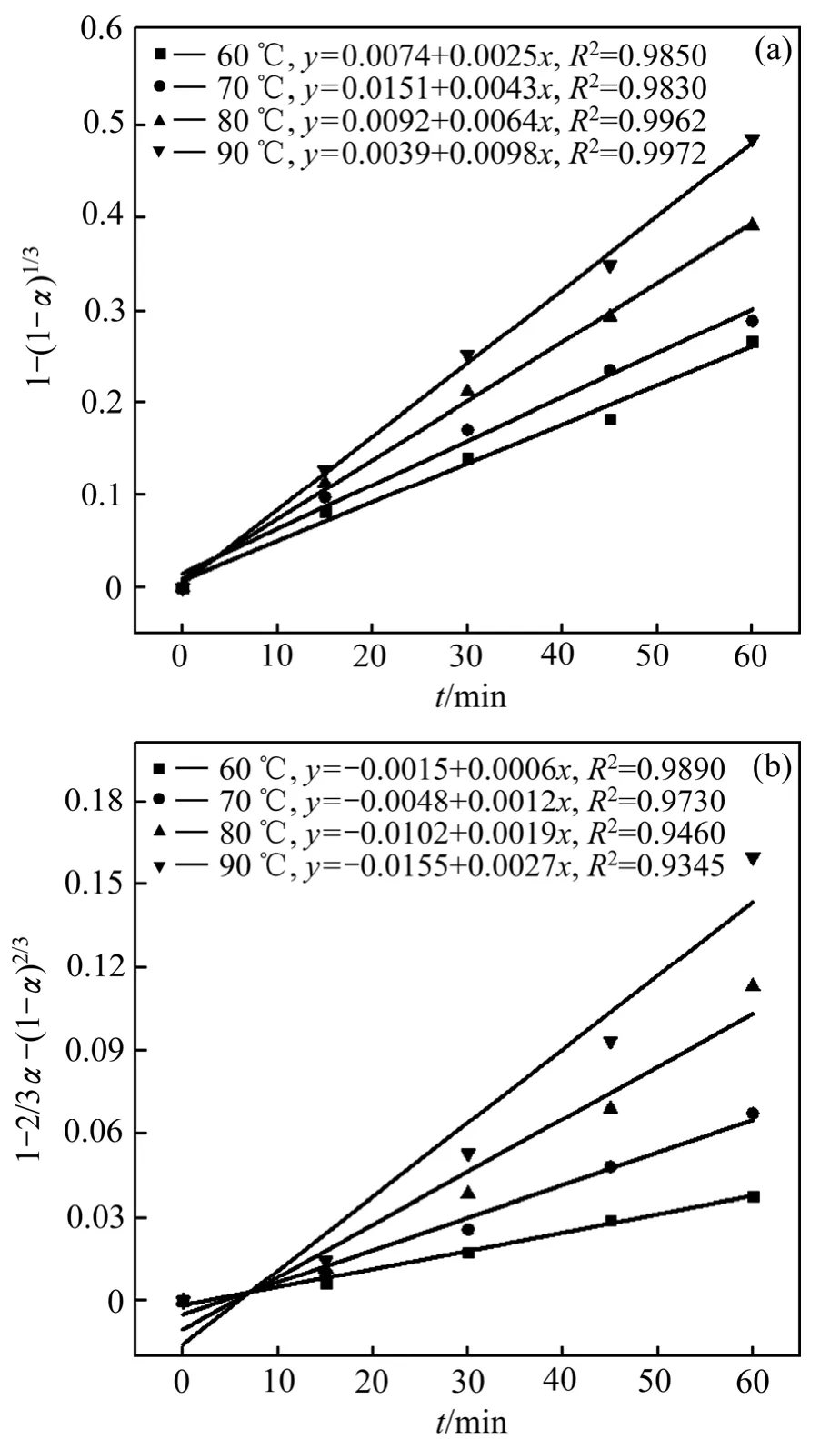
图3 不同温度下1-(1-α)1/3和1-2/3α-(1-α)2/3与t关系 Fig. 3 Relationships between 1-(1-α)1/3(a) and 1-2/3α-(1-α)2/3(b) and time at different temperatures
以ln k对T-1作图(见图4)得到一条直线,直线的斜率为(-Ea/R)。由此直线方程求出浸出反应的表观活 化能为Ea=45.293 kJ/mol,Ea>42 kJ/mol,进一步验证浸出铅的过程为表面化学反应控制过程[18]。
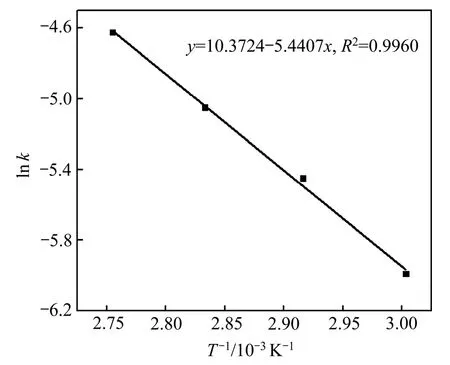
图4 浸出铅Arrhenius图Fig.4 Arrhenius plot of reaction rate against reciprocal of temperature
2.2 NaCl浓度变化对铅浸出过程的影响
固定条件为:铅渣粒度0.106~0.075 mm,液固比10:1,温度90 ℃,用HCl溶液调节pH值为1.0~1.5。考察了NaCl浓度变化对Pb浸出率的影响,其结果如图5所示。
在同一NaCl浓度下,铅浸出率随浸出时间延长而增大;在同一浸出时间下,NaCl浓度越大铅浸出率越高,NaCl浓度从150 g/L升到300 g/L时,铅的平衡浸出率由47.54%增大到91.14%。这是由于络合剂Cl-1浓度越大,越有利于反应(2)向生成络合物[PbCl4]2-的方向进行,铅浸出率越大[19]。将不同NaCl浓度下铅浸出率数据代入式(3)进行线性拟合(见图6),其结果与表面化学反应控制模型相吻合。
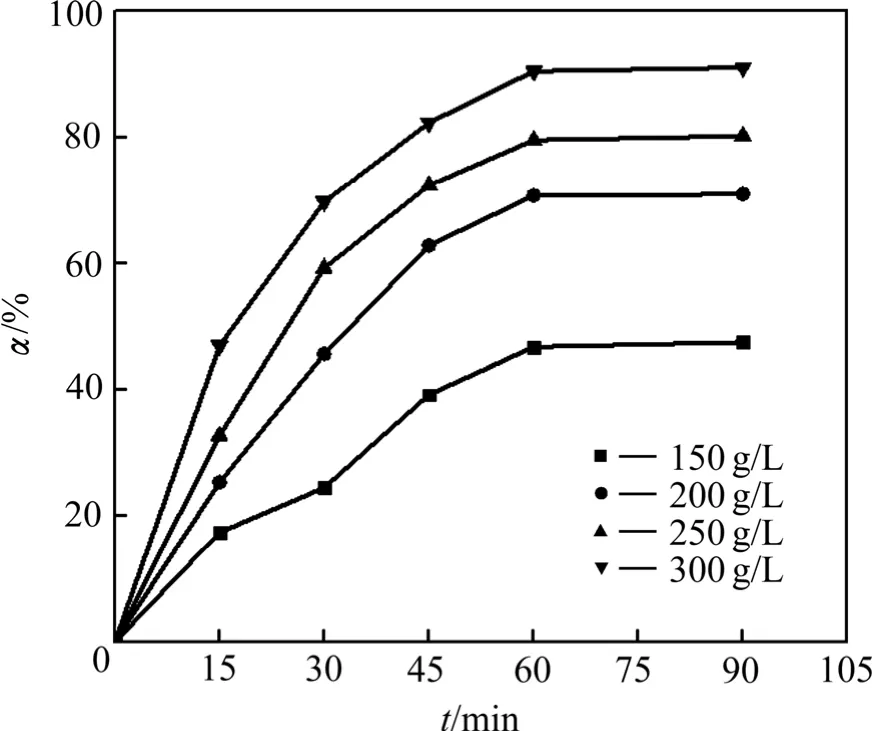
图5 NaCl浓度变化对Pb浸出率影响 Fig.5 Effect of NaCl concentration on leaching rate of lead
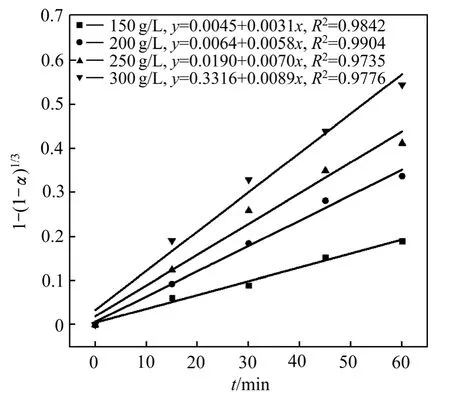
图6 不同NaCl浓度下1-(1-α)1/3与时间关系 Fig.6 Relationship between 1-(1-α)1/3 and time at different NaCl concentrations
2.3 铅渣粒度变化对铅渣浸出过程的影响
固定条件为:NaCl溶液300 g/L,液固比10:1,温度90 ℃,用HCl溶液调节pH值为1.0~1.5。考察铅渣粒度变化对Pb浸出率(α)的影响,结果如图7所示。
在同一粒度下,随着浸出时间延长,铅浸出率逐渐增大;在同一浸出时间下,粒度越小铅浸出率越高,当粒度从180~250 μm减小至75~106 μm时,铅的平衡浸出率由70.79%升高到91.14%。这是因为浸出速率与原料比表面积成正比[20],颗粒越小,比较面积越大,铅的反应速率和浸出率越大。将不同NaCl浓度下铅浸出率数据代入式(3)进行线性拟合(见图8),1-(1-α)1/3与时间t呈很好的线性关系。
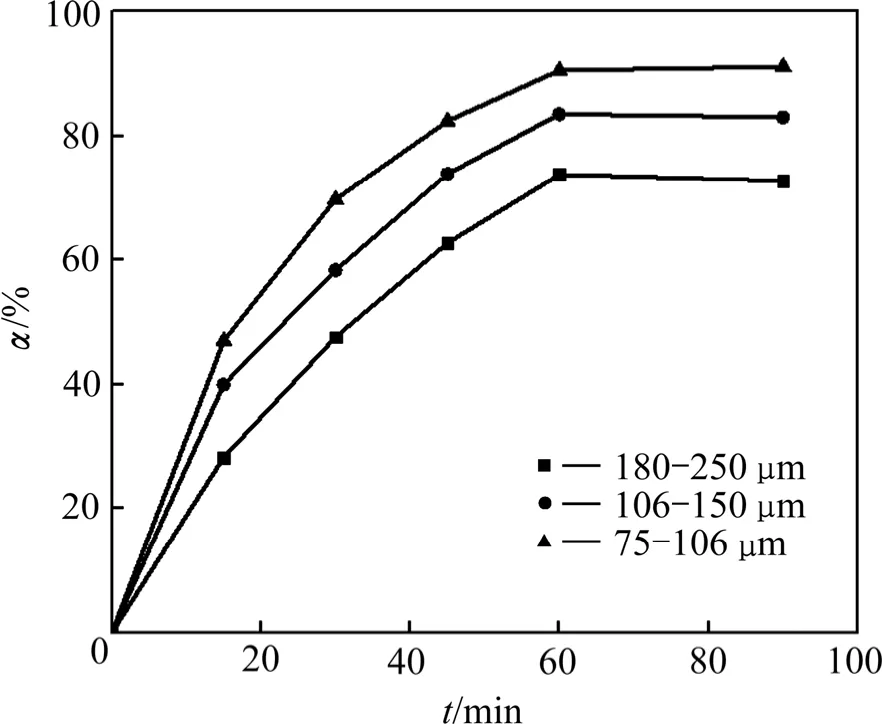
图7 铅渣粒度变化对Pb浸出率影响 Fig.7 Effect of particle size on leaching rate of lead
2.4 液固比变化对铅渣浸出过程的影响
固定条件为:NaCl溶液300g/L,铅渣粒度75~106 μm,温度90 ℃,用HCl溶液调节pH值为1.0~1.5。考察了液固比变化对Pb浸出率的影响,其结果如图9所示。

图8 不同粒度下1-(1-α)1/3与时间关系 Fig.8 Relationship between 1-(1-α)1/3 and time at different particle sizes

图9 不同时间下液固比变化对Pb浸出率影响 Fig.9 Effect of liquid-solid ratio on leaching rate of lead at different time
在同一液固比下随着浸出时间延长铅的浸出率逐渐增大;在同一浸出时间下,液固比越大,铅的浸出率越高,液固比从5:1增大至10:1时,铅的平衡浸出率由56.23%升高到91.14%。液固比较大时,可以减小溶液黏度和溶剂扩散阻力,铅浸出率较高且易于过滤;而液固比较小时,因不能满足反应的化学计量比,铅浸出率较低。将不同液固比下铅浸出率数据代入式(3)进行线性拟合(见图10),1-(1-α)1/3与时间t呈很好的线性关系,验证了铅在NaCl-HCl体系中的浸出受未反应收缩核表面化学反应控制。
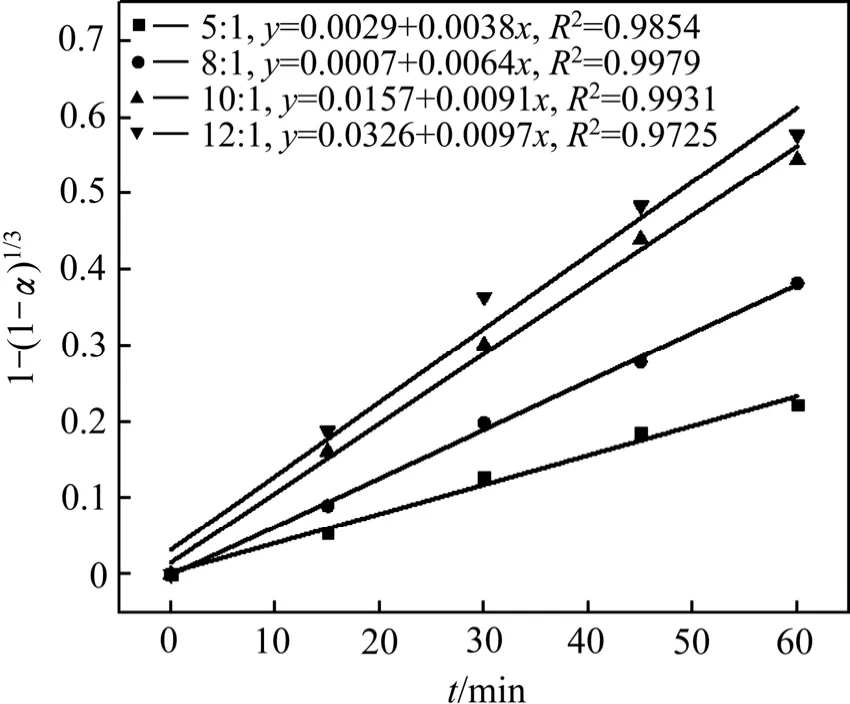
图10 不同液固比下1-(1-α)1/3与时间关系 Fig.10 Relationship between 1-(1-α)1/3 and time at different liquid-solid ratios
2.5 浸出前后渣样物相组成和表面特征
图11 所示为铅渣和浸出渣的XRD谱。从图11的XRD测试结果可以看出,浸出前铅渣主要物相为PbSO4、SiO2、ZnS,浸出后PbSO4相消失,表明大部分硫酸铅已被浸出。图12所示为浸出前后铅渣和浸出渣的SEM像。由图12可看出,浸出前铅渣颗粒表面较光滑、棱角分明[21];浸出后,渣样颗粒表面粗糙,且棱角被侵蚀消失,样品表面反应是表面化学反应过程,这与动力学分析结果一致。
2.6 浸出动力学方程的确定
根据上述各影响因素的研究结果,对于所研究的体系,其动力学方程可表示为式(3),式中kr可以表示为[22]
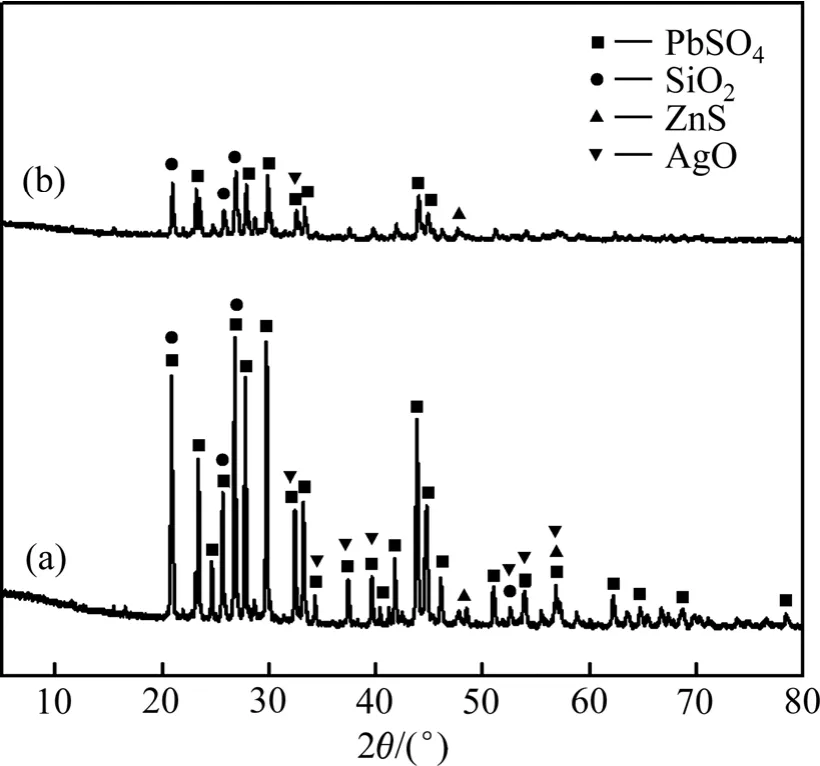
图11 铅渣和浸出渣的XRD谱 Fig.11 XRD patterns of lead residue(a) and leaching residue(b)

图12 铅渣和浸出渣的SEM像 Fig.12 SEM images of lead residue(a) and leaching residue(b)
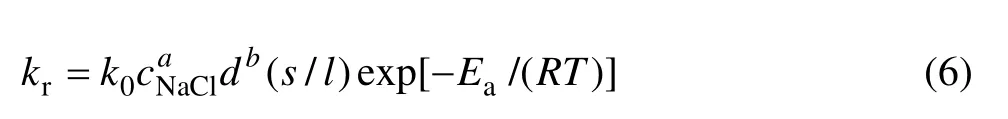
将上式代入式(3),得到半经验公式
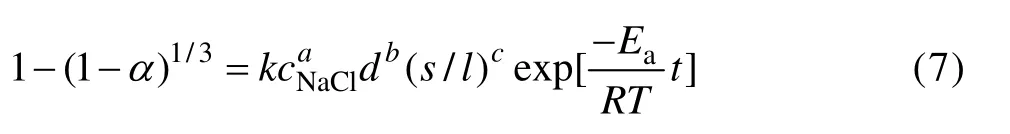
就不同的NaCl浓度而言,当其他条件固定时,式(7)可以改写成式(8)所示形式。

对式(8)两边进行微分并取对数可得
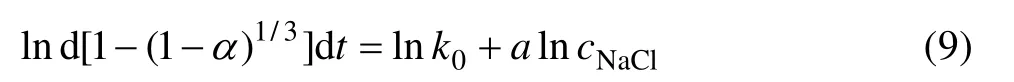
以ln cNaCl为横坐标,ln d[1-(1-α)1/3]/dt为纵坐标作线性拟合,如图13所示,该直线斜率即为NaCl的反应级数a,a=1.469。同理,分别以lnd、ln(s/l)为横坐标,ln d[1-(1-α)1/3]/dt为纵坐标作线性拟合(见图14和15),可分别求出铅渣粒度的反应级数b=-0.469,液固比的反应级数c=-2.112。
将上述求出的a、b、c和Ea代入式(7),再用式(7)拟合图3、5、7、8中各直线,可求得k0的统计值为1.73×10-2。由以上可以确定在NaCl-HCl体系中铅渣中铅的浸出动力学方程可表示为

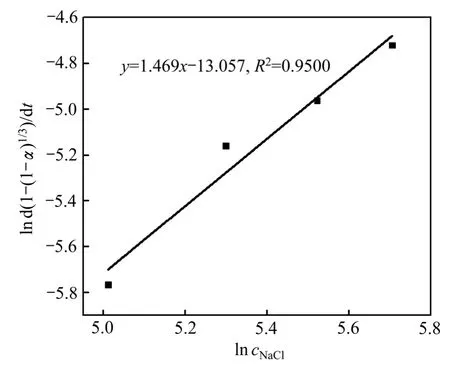
图13 ln d[1-(1-α)1/3]/dt与ln cNaCl关系图Fig.13 Plot of ln d[1-(1-α)1/3]/dt against ln cNaCl
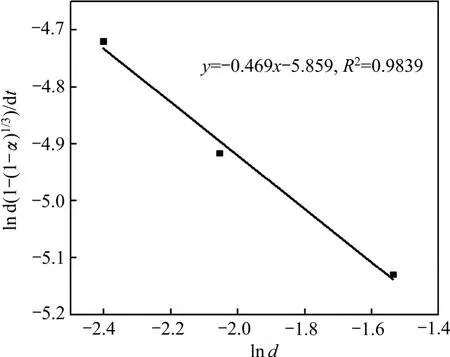
图14 ln d[1-(1-α)1/3]/dt与ln d关系图Fig.14 Plot of ln d[1-(1-α)1/3]/dt against ln d
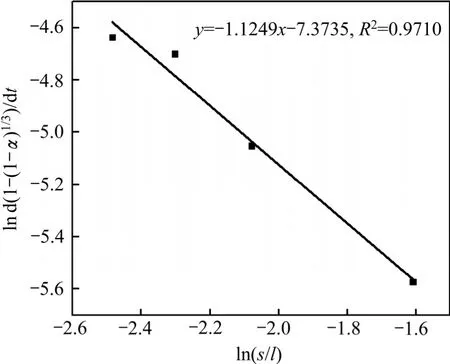
图15 ln d[1-(1-α)1/3]/dt与ln (s/l)关系图Fig.15 Plot of ln d[1-(1-α)1/3]/dt against ln (s/l)
3 结论
1) 在NaCl浓度300 g/L、液固比10:1、浸出温度80 ℃条件下,浸出反应60 min,铅浸出率达到91.14%。在实验选取的参数范围内,增大NaCl浓度、提高浸出温度、增大液固比、减小铅渣粒度和延长浸出时间均有利于提高铅的浸出率。
2) 在NaCl-HCl体系中,铅渣中铅的浸出过程可用未反应收缩核模型来表示,反应速率受表面化学反应控制,表观活化能为45.293 kJ/mol,其宏观动力学方程可表示为 1-(1-α)1/3=1.73×10-2cNaCl1.469d-0.469· (s/l)-2.112exp{[-45293E/(RT)] t}。
[1] 焦志良,陈为亮,张旭. 从二次含铅物料中湿法回收铅的研究现状[J]. 湿法冶金,2014,33(2): 90-93.
JIAO Zhi-liang,CHEN Wei-liang,ZHANG Xu. Current situation of recovery lead from secondary lead-containing materials by hydrometallurgical technology[J]. Hydrometallurgy of China,2014,33(2): 90-93.
[2] 唐秋香. 从锌烟灰中浸出锌和铅的试验研究[J]. 湿法冶金,2013,32(5): 302-304.
TANG Qiu-xiang. Test study on leaching of zinc and lead from zinc fume dust[J]. Hydrometallurgy of China,2013,32(5): 302-304.
[3] 徐 辉,颜文斌,张传宝,高 峰,易 静,华 骏. 从冶锌酸浸渣中回收铅、锌的工艺研究[J]. 矿冶工程,2012,32(6): 78-81.
XU Hui,YAN Wen-bin,ZHANG Chuan-bao,GAO Feng,YI Jing,HUA Jun. Study on recovery of Pb and Zn from acid-leaching residue[J]. Mining and Metallurgical Engineering,2012,32(6): 78-81.
[4] 彭国敏,俎小凤,张福元. 酸浸渣综合回收浸铅工艺研究[J]. 无机盐工业,2012,44(1): 52-54.
PENG Guo-min,ZU Xiao-feng,ZHANG Fu-yuan. Study on leaching process of lead from acid residue [J]. Inorganic Chemicals Industry,2012,44(1): 52-54.
[5] AMIN A S,ABDALLAH M,OMAR A A. Hydrometallurgical treatment of Egyptian zinc-lead oxide ore[J]. Modelling,Measurement & Control,1995,49(1/3): 1-12.
[6] FERRACIN L C,CHACON-SANHUEZA A E,DAVOGLIO R A,ROCHA L O,CAFFEU D J,FONTANETTI A R,ROCHA-FILHO R C,BIAGGIO S R,BOCCHI N. Lead recovery from a typical Brazilian sludge of exhausted lead-acid batteries using an electro hydrometallurgical process[J]. Hydrometallurgy,2002,65(2/3): 137-144.
[7] 张福元,俎小凤,彭国敏. 沉淀转化法综合回收酸浸渣中铅的工艺研究[J]. 无机盐工业,2013,45(1): 40-59.
ZHANG Fu-yuan,ZU Xiao-feng,PENG Guo-min. Study on process of recovering lead from acid leaching residue by precipitation transformation method[J]. Inorganic Chemicals Industry,2013,45(1): 40-59.
[8] 任兴丽,蒋兴荣,朱复跃. 回收铅渣中碳酸铅工艺条件研究[J]. 河北化工,2012,35(9): 43-44. REN Xing-li,JIANG Xing-rong,ZHU Fu-yue. Research on process conditions of recovering lead carbonate from lead slag[J]. Hebei Chemical Engineering and Industry,2012,35(9): 43-44.
[9] 张亚莉,于先进,李小斌. 氧化锌贫矿提锌渣中铅和银的氯盐一步浸出[J]. 中国有色金属学报,2012,22(1): 296-330.
ZHANG Ya-li,YU Xian-jin,LI Xiao-bin. Leaching of silver and lead by chloride simultaneously from residue after zinc extraction of low-grade zinc oxide ores[J]. The Chinese Journal of Nonferrous Metals,2012,22(1): 296-330.
[10] 韦岩松,黎铉海,马 宸. 硫化铟氧化酸浸与常规酸浸的动力学比较[J]. 金属矿山,2014,43(3): 165-170.
WEI Yan-song,LI Xuan-hai,MA Chen. Kinetics comparison of oxidizing acid leading and conventional acid leading of indium sulfide[J]. Metal Mine,2014,43(3): 165-170.
[11] 刘 清,赵由才,招国栋. 氢氧化钠浸出-两步沉淀法制备铅锌精矿新工艺[J]. 湿法冶金,2010,29(1): 32-36.
LIU Qing,ZHAO You-cai,ZHAO Guo-dong. A novel process for preparation of zinc and lead concentrates by alkaline leaching and precipitation[J]. Hydrometallurgy of China,2010,29(1): 32-36.
[12] ZHU X F,YANG J K,GAO L X,LIU J W,YANG D N,SUN X J,ZHANG W,WANG Q,LI L,HE D S,KUMAR R V. Preparation of lead carbonate from spent lead paste via chemical conversion[J]. Hydrometallurgy,2013,134: 47-53.
[13] DRAGAN S,ZELJKO K,ALEKSANDAR S. Leaching kinetics of lead from lead (Ⅱ) sulphate in aqueous calcium chloride and magnesium chloride solutions[J]. Hydrometallurgy,1997,47: 137-147.
[14] 齐美富,郑园芳,桂双林. 废铅酸蓄电池中铅膏氯盐体系浸取铅的动力学研究[J]. 矿冶工程,2010,30(6): 61-64.
QI Mei-fu,ZHENG Guo-fang,GUI Shuang-lin. Kinetic study on leaching lead from waste lead-acid batteries for lead plaster chloride system[J]. Mining and Metallurgical Engineering,2010,30(6): 61-64.
[15] 朱炳辰. 化学反应工程[M]. 北京: 化学工业出版社,2001: 360-364.
ZHU Bing-chen. Chemical reaction engineering[M]. Beijing: Chemistry Industry Press,2001: 360-364.
[16] MOHAMMAD S S,DAVOOD M,MEHDI O I. Kinetics of sulfuric acid leaching of cadmium from Cd-Ni zinc plant residues[J]. Journal of Hazardous Materials,2009,163: 880-890.
[17] 张传宝,颜文斌,徐 辉,高 峰,华 骏. 难处理铅锌矿酸浸渣回收硫酸铅的工艺研究[J]. 应用化工,2012,41(7): 1188-1192.
ZHANG Chuan-bao,YAN Wen-bin,XU Hui,GAO Feng,HUA Jun. Study on recovery lead sulfate from complex acid leaching residue of lead-zinc mine[J]. Applied Chemical Industry,2012,41(7): 1188-1192.
[18] 李洪桂. 冶金原理[M]. 北京: 科学出版社,2005: 191-316.
LI Hong-gui. Principles of metallurgy[M]. Beijing: Science Press,2005: 191-316.
[19] RUSEN A,SUNKAR A S,TOPKAYA Y A. Zinc and lead extraction from Çinkur leach residues by using hydrometallurgical method[J]. Hydrometallurgy,2008,93: 45-50.
[20] LI Q,ZHANG B,MIN X B,SHEN W Q. Acid leaching kinetics of zinc plant purification residue[J]. Transaction of Nonferrous Metals Society of China,2013,23(9): 2786-2791.
[21] 徐志峰,朱 辉,王成彦. 富氧硫酸体系中硫化锌精矿的常压直接浸出动力学[J]. 中国有色金属学报,2013,23(12): 3440-3447.
XU Zhi-feng,ZHU Hui,WANG Cheng-yan. Atmospheric direct leaching kinetics of zinc sulfide concentrate in oxygen-rich sulfuric acid system[J]. The Chinese Journal of Nonferrous Metals,2013,23(12): 3440-3447.
[22] 何 静,王小能,刘明海,王继民,唐谟堂,鲁君乐,王 涛,罗 超,郭 瑞,蓝明艳. 含锗真空炉渣在HCl-CaCl2-H2O体系中浸出锗的动力学研究[J]. 稀有金属材料与工程,2013,42(6): 1258-1263.
HE Jing,WANG Xiao-neng,LIU Ming-hai,WANG Ji-min,TANG Mo-tang,LU Jun-le,WANG Tao,LUO Chao,GUO Rui,LAN Ming-yan. Leaching kinetics of germanium in vacuum slag in HCl-CaCl2-H2O solution[J]. Rare Metal Materials and Engineering,2013,42(6): 1258-1263.

