共沉淀法制备暖白光LED用Na2TiF6∶M n4+红色荧光粉及其发光性能研究
罗 洋,江建青,侯得健,游维雄,叶信宇,2*
(1.江西理工大学冶金与化学工程学院,江西赣州 341000;
2.国家离子型稀土资源高效开发利用工程技术研究中心,江西赣州 341000)
共沉淀法制备暖白光LED用Na2TiF6∶M n4+红色荧光粉及其发光性能研究
罗 洋1,江建青1,侯得健1,游维雄1,叶信宇1,2*
(1.江西理工大学冶金与化学工程学院,江西赣州 341000;
2.国家离子型稀土资源高效开发利用工程技术研究中心,江西赣州 341000)
采用简便的共沉淀法制备了不同Mn4+掺杂摩尔分数的Na2TiF6∶Mn4+红色荧光粉。通过X射线衍射仪、扫描电子显微镜、红外光谱仪、荧光光谱仪对荧光粉的结构、形貌、傅立叶红外光谱、激发和发射光谱及荧光寿命曲线进行了表征。结果表明,Mn4+的掺杂没有改变Na2TiF6的晶格结构,样品具有六方结构。Mn4+最佳掺杂摩尔分数为4.77%,量子效率为74%。在460 nm激发下,最强窄带发射峰位于628 nm处(2Eg-4A2),色坐标为(0.681,0.317)。2Eg能级的荧光寿命曲线遵循双指数衰减,其荧光寿命值为3.148 ms。
Na2TiF6∶Mn4+;红色荧光粉;白光LEDs;共沉淀法
1 引 言
白光发光二极管(Light emitting diodes, LEDs)具有高亮度、长寿命、节能、环保等特点[1-3]。目前,白光LEDs主要由蓝光芯片和YAG∶Ce3+黄色荧光粉组合而成[4-5]。然而,这种白光实现方式由于缺乏红光成分而导致显色性低、色温偏高的缺点逐渐显现,阻碍了其在暖白光LEDs (色温4 000~8 000 K)中的发展,限制了其在室内照明中的应用[6-7]。
随着稀土离子激活的红色荧光粉的发展,氮化物[8-9]、硫化物[10]、钛酸盐[11]、钨酸盐以及钼酸盐[12]红色荧光粉在暖白光LEDs有了一定应用。这些物质多以Eu3+掺杂为主,而Eu3+的激发归属于宇称禁阻的4f-4f跃迁,在蓝光区域吸收较低,不适用于蓝光GaN芯片[13-14]。Eu2+/Ce3+掺杂的氮化物荧光粉依靠量子效率高、稳定性强、温度特性好的优点得到了广泛的商业化应用,但过宽的发射带引起的重吸收现象以及苛刻合成条件带来的高生产成本限制了其在高效暖白光LEDs中的应用[15-16]。因此,急需寻找一种能在蓝光激发下,适用于暖LEDs的高光效、高显指、稳定廉价的红色荧光粉。
近年来,Mn4+掺杂的氟化物红色荧光粉因具有红光窄带发射、能被紫外和蓝光激发以及原料便宜的特点,成为一个新的研究热点[17]。目前,对于Na2TiF6∶Mn4+荧光粉的研究尚罕有报道。Adachi等采用湿化学腐蚀法在室温下合成了Na2TiF6∶Mn4+荧光粉[18],但并未对这种荧光粉的形貌和不同Mn4+掺杂浓度下的结构和发光特性进行表述。同时,这种合成方式存在着制备工艺复杂、周期长、产率低等问题[19]。为了在室温下短时间内得到目标产物,Zhu等[20]采用离子交换法,通过K2TiF6和K2MnF6在HF溶液中发生离子交换作用,短时间内制备了K2TiF6∶Mn4+,其量子效率可达98%。Liao等[21]采用氧化还原法,在HF/KMnO4溶液中制备了K2SiF6∶Mn4+,其反应时间只需20min。而江先禹等[17]采用水热合成法制备了结晶度好、发光强度高的BaTiF6∶Mn4+和BaSiF6∶Mn4+,但其反应时间一般需要20 h。Sekiguchi等[22]采用共沉淀法合成了长度5μm,直径小于1μm的棒状BaGeF6∶Mn4+,其反应时间需要6 h。
本文采用简便的共沉淀法制备了不同Mn4+浓度下Na2TiF6∶Mn4+红色荧光粉,通过滴加H2O2加快了反应时间,并将Mn7+还原成Mn4+。利用Na2TiF6和K2TiF6在40%HF溶液中溶解度的差异,得到了Na2TiF6∶Mn4+沉淀。由于制备方式简便、周期短、光学性质优异,所制备的Na2TiF6∶Mn4+有望应用于暖白光LED用红色荧光粉。
2 实 验
采用简便的共沉淀法制备了不同Mn4+浓度掺杂的Na2TiF6∶Mn4+红色荧光粉。首先,按照质量比20∶1将KHF2和KMnO4加入至40 mL的40%HF中,搅拌0.5 h后,向溶液中缓慢滴加H2O2(30%),可观察到溶液由深紫色逐渐变为黄色,最终产生黄色沉淀。所得沉淀用丙酮(99.9%)清洗后置于烘箱中在70℃下干燥2 h,即得到K2MnF6粉末。
随后,将0.8 g TiO2(99.9%)置于15 mL的40%HF中,在60℃下搅拌2 h,得到H2TiF6。.再向溶液中加入适量K2MnF6(0.05~0.5 g),搅拌15 min后,缓慢加入2 g Na2SO4,所得黄色沉淀用去离子水清洗,再用无水乙醇(99.9%)清洗3次,最后在70℃下干燥5 h即得所需样品。
样品采用PANalytical X'Pert Pro型X射线粉末衍射仪进行物相表征,辐射源为Cu靶(λ= 0.154 187 nm);样品形貌采用扫描电镜(Hitachi TM-3030)进行表征。Mn4+实际掺杂量采用美国热电公司生产的IRIS INTREPID II型全谱直读光谱仪进行测定。傅立叶红外光谱采用德国布鲁克公司的ALPHA红外光谱仪测定,分辨率为0.8 cm-1。荧光寿命测定采用英国爱丁堡公司的FLS980型荧光光谱仪,激发光源为450 W氙灯,激发波长为460 nm,狭缝为0.5 nm;发射波长为628 nm,狭缝为1.5 nm。激发光谱、发射光谱测定采用日本日立公司的F-7000荧光光谱仪,激发光源是150 W氙灯,测试狭缝为2.5 nm,光电倍增管电压为400 V。量子效率测定采用北京卓立汉光仪器公司的SENS-9000稳态荧光光谱仪,激发光源是500W氙灯;色坐标及相对亮度采用杭州远方公司的PMS-80型光谱分析系统测定。
3 结果与讨论
3.1 样品合成
制备过程中的化学反应如下:
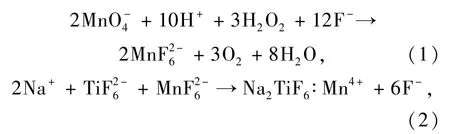
室温下,H2O2在反应过程中起到了增加反应速率的作用[23],同时将Mn7+还原成Mn4+。值得注意的是,过量的H2O2会直接将Mn7+还原成Mn2+:
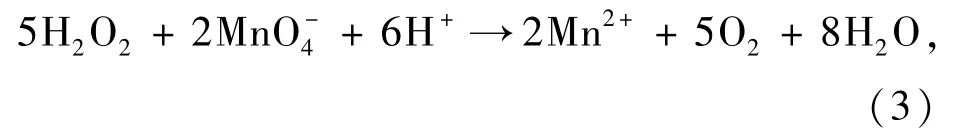
利用Na2TiF6和K2TiF6在40%HF溶液中溶解度的差异,通过增加溶液中Na+的浓度,得到Na2TiF6∶Mn4+沉淀。因此,控制H2O2的滴加速率以及沉淀剂Na2SO4的加入量是合成纯相Na2TiF6∶Mn4+的重要因素。
3.2 结构与形态表征
采用共沉淀法合成了6个不同Mn4+掺杂浓度的Na2TiF6∶Mn4+样品,通过ICP-AES进行成分分析,得出样品Mn4+掺杂摩尔分数分别为0.83%, 1.93%、4.77%、6.94%、8.57%、10.93%,对应的Mn4+理论掺杂摩尔分数分别为2.01%、4.01%、7.96%、11.81%、15.63%、19.4%。图1为不同Mn4+掺杂摩尔分数的Na2TiF6∶Mn4+样品和中间产物K2MnF6的XRD谱。所有样品谱图中没有多余的杂相峰出现,均为纯相。Na2TiF6∶Mn4+样品的衍射峰与相应的标准六方晶相Na2TiF6(JCPDS No.00-043-0522)相匹配,空间群为-Pm1。通过Diamand软件模拟了(110)方向上Na2TiF6的晶体结构模型(图2)。可以发现,每一个Ti4+由6个F-包围形成规律的Ti八面体结构,每个Na+都位于12个相邻的F-中心而与F-形成近乎规则的多面体结构。而Mn4+处于八面体晶格中可以稳定存在,并发出红光[17,24],这有利于Mn4+对Ti4+的替换。
为了确认Mn4+是否掺入Na2TiF6主晶格中,我们选取18.5°~20°下不同Mn4+掺杂摩尔分数Na2TiF6∶Mn4+的XRD谱放大图(图3),可以发现随着掺杂浓度的不断增加,衍射峰逐渐向高角度偏移。同时,通过JADE软件分析发现,10.93%样品的晶胞体积相比纯物质Na2TiF6的0.375 94 nm3减少到了0.375 75 nm3。这是因为Mn4+的半径(0.053 0 nm)小于Ti4+的半径(0.060 5 nm)且价态相同,Mn4+易于进入Na2TiF6主晶格占据Ti4+格位。

图1 中间产物K2MnF6和不同Mn4+掺杂摩尔分数的Na2TiF6∶Mn4+样品的XRD谱Fig.1 XRD patterns of K2MnF6and Na2TiF6samples with different Mn4+mole fraction
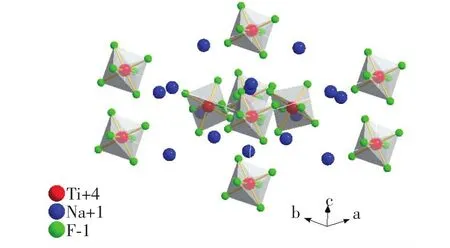
图2 (110)方向上的Na2TiF6∶Mn4+的晶体结构模型Fig.2 Crystal structure of K2TiF6∶Mn4+depicted in(110) direction
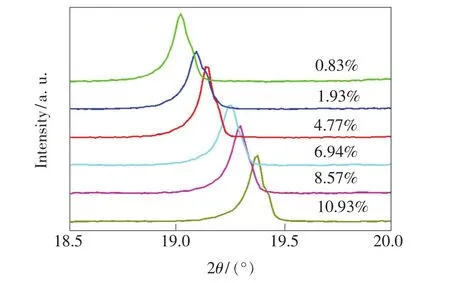
图3 18.5°~20°之间的不同Mn4+掺杂摩尔分数的Na2TiF6∶Mn4+的XRD谱Fig.3 XRD patterns of Na2TiF6∶Mn4+samples with different Mn4+mole fraction from 18.5°to 20°
图4(a)为Na2TiF6∶4.77%Mn4+样品的扫描电镜图像,粒径大小约为5μm,具有较规则的形貌,未发生明显的团聚现象。样品在自然光下为均一的亮黄色粉末(图4(b)),在紫外光(365 nm)和蓝光(460 nm)激发下,发出了明亮的红光(图4(c)、(d))。

图4 Na2TiF6∶4.77%Mn4+的扫描电镜图(a)以及分别在自然光(b)、365 nm(c)和460 nm(d)照射下的效果图。Fig.4 Scanning electron microscope image(a),and photographs under natural light(b),UV light(365 nm) (c),and blue light(460 nm)(d)of Na2TiF6∶4.77%Mn4+sample,respectively.
3.3 红外光谱
图5显示,不同Mn4+掺杂摩尔分数(0.83%~10.93%)的Na2TiF6∶Mn4+荧光粉具有相似峰形的红外光谱。位于3 448 cm-1左右的宽峰和1 631 cm-1处的弱峰分别是由水分子内的O—H键的伸缩和弯曲振动造成的[25],而在570 cm-1处的峰远远强于其他峰,应属于Ti—F键的振动形成的[26]。
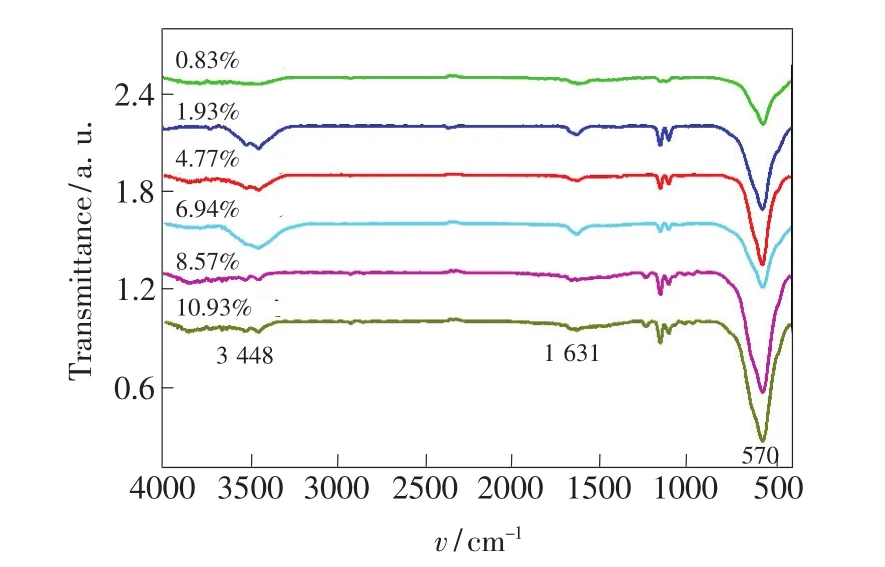
图5 不同Mn4+掺杂摩尔分数的Na2TiF6∶Mn4+荧光粉的红外光谱Fig.5 IR spectra of Na2TiF6∶Mn4+phosphorswith different Mn4+dopingmole fraction
3.4 发光性质
图6为628 nm波长监控下,不同Mn4+摩尔分数的Na2TiF6∶Mn4+样品的激发光谱。样品在320~500 nm具有很宽的激发谱带,在360 nm和467 nm处出现的两个宽吸收带分别归属于自旋允许的4A2-4T1和4A2-4T2电子跃迁[17],其能级跃迁如图7所示。样品的最强激发带位于467 nm,其中4.77%样品的半峰宽约为60 nm,宽于蓝光芯片的发射带(约20 nm),这使得Na2TiF6∶Mn4+能很好地与蓝光芯片相匹配。
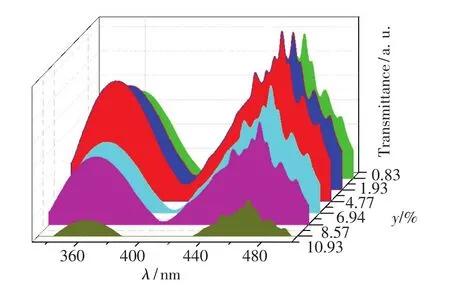
图6 628 nm波长监控下,不同Mn4+掺杂摩尔分数的Na2TiF6∶Mn4+样品的激发光谱。Fig.6 Excitation spectra of Na2TiF6∶Mn4+with differentMn4+mole fraction(λem=628 nm)
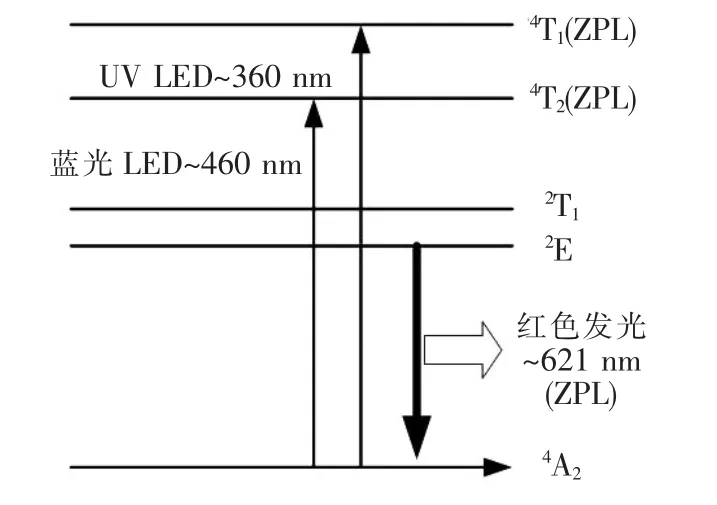
图7 Mn4+的能级跃迁示意图Fig.7 Transition diagram of energy level for Mn4+ions
图8为365 nm激发下,不同Mn4+摩尔分数的Na2TiF6∶Mn4+样品的发射光谱和相对强度图。样品的3个强烈的尖锐发射带位于610,618,628 nm处,来自于Mn4+自旋禁阻的2Eg-4A2电子跃迁[20],如图8所示。其中最强峰位于628 nm。发射峰强度随着Mn4+掺杂摩尔分数的增加而先增大后减小,这归因于浓度猝灭的发生[27]。当Mn4+掺杂摩尔分数为4.77%时,发射强度达到最大,量子效率为74%。
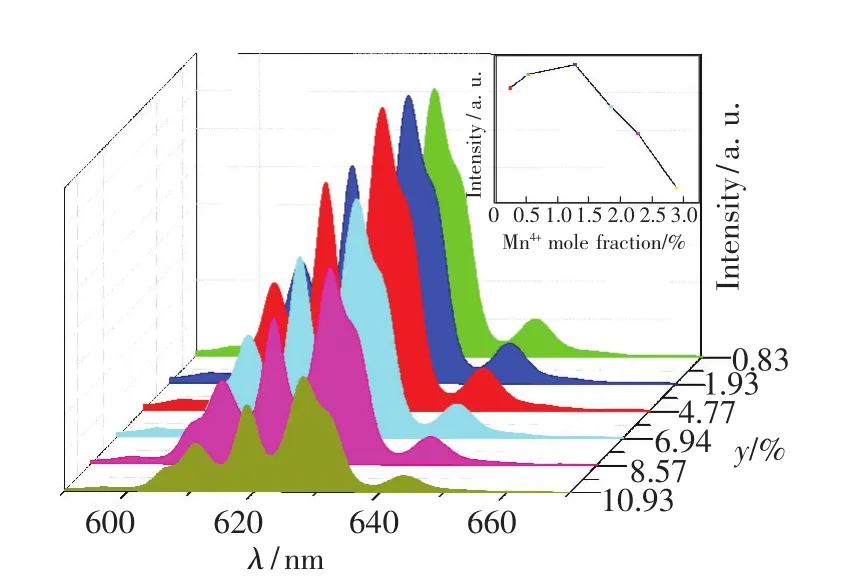
图8 460 nm波长激发下,不同Mn4+掺杂摩尔分数的Na2TiF6∶Mn4+样品的发光光谱。Fig.8 Emissson spectra of Na2TiF6∶Mn4+with different Mn4+mole fraction(λex=460 nm)
图9为460 nm激发下,Na2TiF6∶Mn4+荧光粉的CIE(国际发光照明委员会)色度图,其色坐标(0.681,0.317)(图9(b))处于深红区域,与其他Mn4+掺杂氧化物红色荧光粉如Mg2TiO4∶Mn4+(0.73,0.26)[28](图9(c))、Sr4Al14O25∶Mn4+(0.722,0.278)[29](图9(d))相比,更加接近于美国国家电视标准委员会(NTSC,National TV Standard Committee)标准值(0.67,0.33) (图9(a))。因此,Na2TiF6∶Mn4+是非常适合于蓝光激发的白光LED用红色荧光粉。
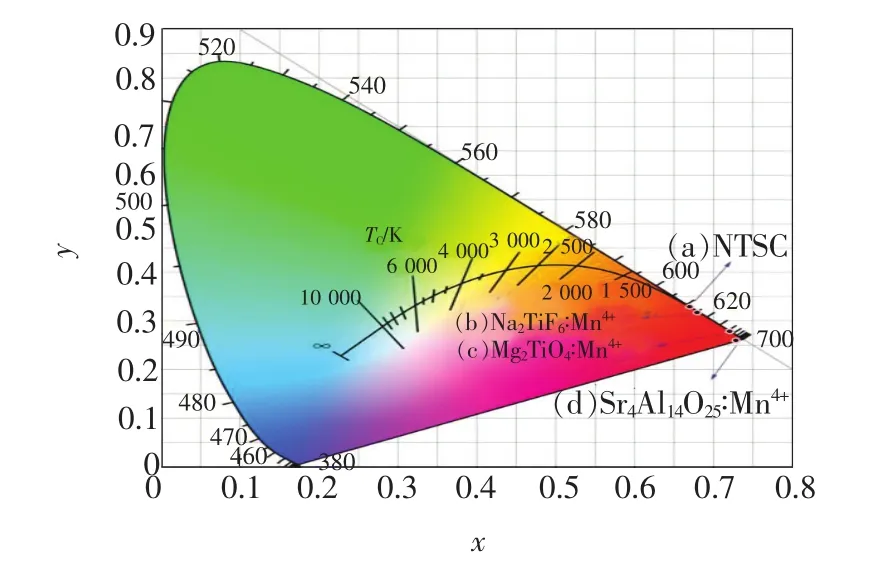
图9 460 nm激发下,Na2TiF6∶Mn4+荧光粉的CIE色度图。Fig.9 CIE chromaticity diagram of K2TiF6∶Mn4+phosphors (λex=460 nm)
3.5 荧光寿命
图10为Na2TiF6∶4.77%Mn4+样品的光寿命衰减曲线,激发波长为460 nm,监控波长为628 nm。通过对Mn4+衰减的时间曲线进行拟合发现, Mn4+在该基质中满足双指数衰减规律,公式如下:
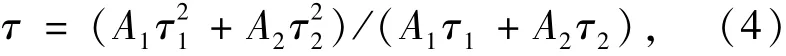
虽然Mn4+在Na2TiF6结构中只有一种晶格存在,但高浓度下的Mn4+掺杂会引起荧光粉表面缺陷,从而增加非辐射跃迁渠道,最终部分Mn4+无法进入主格,并吸附在荧光粉的表面,致使Na2TiF6∶4.77%Mn4+的荧光寿命符合双指数方式衰减。通过拟合,得出Na2TiF6∶Mn4+样品中的2Eg能级的荧光寿命值τ=3.148 ms。Mn4+的毫秒级荧光寿命与其跃迁类型和离子价态相符。

图10 室温下Na2TiF6∶4.77%Mn4+的荧光寿命衰减曲线Fig.10 Decay curve of Na2TiF6∶4.77%Mn4+at room tempurature
4 结 论
采用简便的共沉淀法制备了不同Mn4+掺杂摩尔分数(0.83%~10.93%)的六方晶相Na2TiF6∶Mn4+微米(约5μm)荧光粉,未发现有杂质相生成。Na2TiF6∶Mn4+红色荧光粉在蓝光区域有着强烈吸收,在460 nm激发下,在628 nm处产生强窄带红色发射峰(2Eg-4A2)。不同浓度样品的发射和激发光谱表明,Mn4+的最佳掺杂摩尔分数为4.77%。Na2TiF6∶Mn4+荧光粉色坐标为(0.681, 0.317),更接近于标准红光(0.67,0.33)。荧光粉的荧光寿命符合双指数方程,2Eg能级的荧光寿命值约为3.148 ms。Na2TiF6∶Mn4+荧光粉优异的光学性质和简便的合成方式,使其成为极具发展潜力的暖白光LED用红色荧光粉。
参 考 文 献:
[1]Nizamoglu S,Erdem T,Demir H V.High scotopic/photopic ratiowhite-light-emitting diodes integrated with semiconductor nanophosphors of colloidal quantum dots[J].Opt.Lett.,2011,36(10):1893-1895.
[2]Chang M H,Das D,Varde P V,et al.Light emitting diodes reliability review[J].Microelectron.Reliab.,2012, 52(5):762-782.
[3]Daicho H,Iwasaki T,Enomoto K,etal.A novel phosphor for glarelesswhite light-emitting diodes[J].Nat.Commun., 2012,3:1132-1136.
[4]Ahemen I,De D K,Amah A N.A review of solid state white light emitting diode and its potentials for replacing conventional lighting technologies in developing countries[J].Appl.Phys.Res.,2014,6(2):95-99.
[5]Lin C C,Liu R S.Advances in phosphors for light-emitting diodes[J].J.Phys.Chem.Lett.,2011,2(11): 1268-1277.
[6]Humphreys C J.Solid-state lighting[J].MRSBull.,2008,33:459-470.
[7]Sun L,Zhang Y,Hu X K,et al.Synthesis and photoluminescence properties of KZn4(BO3)∶Eu3+red-emitting phosphor [J].Chin.J.Liq.Cryst.Disp.(液晶与显示),2014,29(6):893-900(in Chinese).
[8]Li Y Q,Van Steen JE J,Van Krevel JW H,et al.Luminescence properties of red-emitting M2Si5N8∶Eu2+(M=Ca, Sr,Ba)LED conversion phosphors[J].J.Alloys Compd.,2006,417(1):273-279.
[9]Zhang Y P.Patent review on synthesis of Red-M2Si5N8(M=Ca,Sr,Ba)phosphors[J].Chin.J.Lumin.(发光学报),2015,36(2):135-140(in Chinese).
[10]Poelman D,Van Haecke JE,Smet P F.Advances in sulfide phosphors for displays and lighting[J].J.Mater.Sci., 2009,20(1):134-138.
[11]Wu Y B,Sun Z,Ruan K B,etal.Structural and optical properties of Ca0.88TiO3∶0.12Eu3+red phosphors[J].Chin.J. Lumin.(发光学报),2014,35(8):932-938(in Chinese).
[12]Dutta P S,Khanna A.Eu3+activated molybdate and tungstate based red phosphorswith charge transfer band in blue region[J].ECS J.Solid State Sci.Technol.,2013,2(2):R3153-R3167.
[13]Xu Z,Gao Y,Liu T,et al.General and facilemethod to fabricate uniform Y2O3∶Ln3+(Ln3+=Eu3+,Tb3+)hollow microspheres using polystyrene spheres as templates[J].J.Mater.Chem.,2012,22(40):21695-21703.
[14]Zhang L,Lu Z,Han P,et al.Synthesis and photoluminescence of Eu3+-activated double perovskite NaGdMg(W, Mo)O6—A potential red phosphor for solid state lighting[J].J.Mater.Chem.C,2013,1(1):54-57.
[15]Yamada S,Emoto H,Ibukiyama M,et al.Properties of SiAlON powder phosphors forwhite LEDs[J].J.Eur.Ceram. Soc.,2012,32(7):1355-1358.
[16]George N C,Denault K A,SeshadriR.Phosphors for solid-statewhite lighting[J].Ann.Rev.Mater.Res.,2013,43: 481-501.
[17]Jiang X Y.Research on Synthesis and Luminescent Properties of Mn4+-doped Fluoride Phosphors[D].Wenzhou: Wenzhou University,2014(in Chinese).
[18]Xu Y K,Adachi S.Properties of Mn4+-activated hexafluorotitanate phosphors[J].J.Electrochem.Soc.,2011,158(3): J58-J65.
[19]Nguyen H D,Lin CC,Fang M H,etal.Synthesis of Na2SiF6∶Mn4+red phosphors forwhite LED-applications by co-precipitation[J].J.Mater.Chem.C,2014,2(48):10268-10272.
[20]Zhu H,Lin C C,LuoW,et al.Highly efficientnon-rare-earth red emitting phosphor forwarm white light-emitting diodes [J].Nat.Commun.,2014,5:4312-1-5.
[21]Liao C,Cao R,Ma Z,et al.Synthesis of K2SiF6∶Mn4+phosphor from SiO2powders via redox reaction in HF/KMnO4solution and their application in warm-white LED[J].J.Am.Ceram.Soc.,2013,96(11):3552-3556.
[22]Sekiguchi D,Adachi S.Synthesis and photoluminescence spectroscopy of BaGeF6∶Mn4+red phosphor[J].Opt.Mater., 2015,42:417-422.
[23]Lee M J,Song Y H,Song Y L,etal.Enhanced luminous efficiency of deep red emitting K2SiF6∶Mn4+phosphor dependent on KF ratio for warm-white LED[J].Mater.Lett.,2015,141:27-30.
[24]SekiguchiD,AdachiS.Synthesis and optical properties of BaTiF6∶Mn4+red phosphor[J].ECSJ.Solid State Sci.Technol.,2014,3(4):R60-R64.
[25]Farmer V C.The Infrared Spectra ofMinerals[M].London:The Mineralogical Society,1974:46-47.
[26]Choudhury P,Ghosh B,Lamba O P,etal.Phase transitions in MnTiF6·6H2O and ZnTiF6·6H2O observed by IR spectroscopy[J].J.Phys.C:Solid State Phys.,1983,16:1609-1613.
[27]Plant A L.Mechanism of concentration quenching of a xanthene dye encapsulated in phospholipid vesicles[J].Photochem.Photobiol.,1986,44(4):453-459.
[28]Kubus M,Enseling D,Jöstel T,et al.Synthesis and luminescent properties of red-emitting phosphors:ZnSiF6·6H2O and ZnGeF6·6H2O doped with Mn4+[J].J.Lumin.,2013,137:88-92.
[29]Peng M,Yin X,Tanner P A,et al.Orderly-layered tetravalentmanganese-doped strontium aluminate Sr4Al14O25∶Mn4+: An efficient red phosphor for warm white light emitting diodes[J].J.Am.Ceram.Soc.,2013,96(9):2870-2876.
Co-precipitation Synthesis and Lum inescence Properties of Na2TiF6∶M n4+Red Phosphors for W arm W hite Light Em itting Diodes
LUO Yang1,JIANG Jian-qing1,HOU De-jian1,YOUWei-xiong1,YE Xin-yu1,2*
(1.School ofMetallurgy and Chemistry Engineering,Jiangxi University of Science and Technology,Ganzhou 341000,China; 2.National Engineering Research Center for Ionic Rare Earth,Ganzhou 341000,China))
*Corresponding Author,E-mail:xinyye@yahoo.com
Na2TiF6∶Mn4+red phosphors with different Mn4+dopingmole fraction were synthesized by the co-precipitation method.Structure,morphology,photoluminescence excitation and emission spectra as well as decay curve of Na2TiF6∶Mn4+phosphors were studied by X-ray diffraction (XRD),scanning electron microscope(SEM),Fourier transform infrared spectroscopy(FT-IR) and fluorescence spectrometer.As-prepared Na2TiF6∶Mn4+phosphors have hexagonal structures. Under 460 nm excitation,intense red emissions corresponding to2Eg-4A2transitions of Mn4+are observed.The optimum dopingmole fraction ofMn4+is4.77%and the quantum efficiency is74%for this phosphor.The chromaticity coordinates of the Na2TiF6∶Mn4+phosphors are(0.681,0.317). Decay curve of2Egstate for as-prepared Na2TiF6∶Mn4+sample fits the second order exponential behavior,and the average lifetime is 3.148 ms.
Na2TiF6∶Mn4+;red phosphor;white LEDs;co-precipitation.

罗洋(1991-),男,江西吉安人,硕士研究生,2014年于江西理工大学获得学士学位,主要从事发光材料的研究。E-mail:18146691397@163.com

叶信宇(1980-),男,安徽桐城人,博士,副教授,2008年于北京有色金属研究总院获得博士学位,主要从事稀土发光材料及相图热力学的研究。E-mail:xinyye@yahoo.com
O482.31
A
10.3788/fgxb20153612.1402
1000-7032(2015)12-1402-07
2015-09-10;
2015-09-30
江西省自然科学基金(20132BAB206020);江西省高等学校科技落地计划(KJLD14045);江西省教育厅科学技术研究项目(GJJ14408);国家自然科学基金(51304086)资助项目

