抗癫痫药物的分类、作用机制与不良反应
抗癫痫药物的分类、作用机制与不良反应
吴冬燕*朱国行**
(复旦大学附属华山医院神经内科 上海 200040)
摘 要抗癫痫药物按作用机制可分为膜稳定剂、减少神经递质释放的药物、提高γ-氨基丁酸能的药物和其他4类。许多抗癫痫药物的作用机制复杂,致使临床中治疗药物的选择及其不良反应均存在不确定性。有些抗癫痫药物有肝酶诱导或抑制作用,故在多药联合治疗或与其他药物合并使用时的代谢速率发生改变。临床上应注意抗癫痫药物的非特异性不良反应,如困倦、头晕等;也应注意各种抗癫痫药物治疗的比较严重的特异性不良反应,如拉莫三嗪可引起严重皮疹、卡马西平会引起白细胞计数降低等。
关键词癫痫 抗癫痫药物 作用机制 不良反应
Classification, mechanism and adverse effects of antiepileptic drugs
WU Dongyan*, ZHU Guoxing**
(Department of Neurology, Huashan Hospital, Fudan University, Shanghai 200040, China)
ABSTRACTAccording to drug mechanism, antiepileptic drugs can be divided into four groups: membrane stabilization, reducing neurotransmitters release, increasing γ-aminobutyric acid mediated inhibition, and the others. Many antiepileptic drugs have more than one mechanism, leading to the uncertainty of drug selection and adverse effects. Some antiepileptic drugs are liver enzyme inducers or inhibitors, resulting in changes in the metabolism, when used in multiple treatment or in combination with other drugs. Antiepileptic drugs have not only non-specific side effects such as drowsiness and dizziness, but also a variety of specific serious adverse effects such as severe rashes caused by lamotrigine and leukopenia caused by carbamazepine.
KEY WORDSepilepsy; antiepileptic drugs; mechanism; adverse effects
抗癫痫药物的化学结构和作用机制各异,且人们对其临床效用和作用机制之间的相互关系还不完全了解,有些作用机制相似的抗癫痫药物的临床效用却存在着较大的差异。额外的作用机制虽可增强抗癫痫药物的疗效,但同时也可能增加不良反应。
1 作用机制与分类
依据作用机制,抗癫痫药物可分为:①膜稳定剂,如钠、钾通道阻滞剂;②减少神经递质释放的药物,如N/P/Q型钙通道阻滞剂和突触囊泡蛋白2A(synaptic vesicle protein 2A, SV2A)配体;③提高γ-氨基丁酸(γ-aminobutyric acid, GABA)介导的兴奋性抑制的药物,如GABA类似物;④其他,如N-甲基-D-天冬氨酸(N-methyl-D-aspartate, NMDA)受体阻滞剂等。各种抗癫痫药物的作用机制归纳见表1。
2 药理学与药代动力学
已发现有些抗癫痫药物作用于目标通道或受体,如钠、钾通道或GABA受体复合体。这些通道或受体的基因变异会引起遗传性癫痫,但与癫痫类型或治疗首选的抗癫痫药物之间并无直接关联[9-10]。编码钠通道α亚单位的SCN1A基因的多态性与耐卡马西平癫痫相关[11]。
年龄增长不影响抗癫痫药物的吸收,但药物的分布会有所改变且消除速率减慢[12]。通过对肝酶的诱导或抑制作用,许多抗癫痫药物存在明显的药代动力学相互作用。遗传因素也会影响抗癫痫药物的药代动力学以及不良反应的发生。对存在2种细胞色素P450(cytochrome P450, CYP)2C9酶等位基因的患者(白种人占10% ~ 20%、亚洲人和非洲人占1% ~ 5%),苯妥英的疗效将降低20% ~ 40%[10]。人白细胞抗原(human leukocyte antigen, HLA)基因与服用卡马西平或苯妥英后出现Stevens-Johnson综合征的风险相关[13-14]。因此,美国FDA推荐亚洲人服用卡马西平和苯妥英前应先监测HLA B*1502基因[15]。抗癫痫药物的药代动力学数据归纳见表2。

表1 抗癫痫药物的作用机制[1-8]
3 临床用药时的注意事项
考虑到氨乙烯酸(可致视野缺失)和非氨酯(可致再生障碍性贫血)的安全性,只有在使用其他所有的抗癫痫药物治疗都失败后才能在专家的监督下谨慎使用这2种药物治疗难治性癫痫。
3.1 驾驶
各个国家的法律、法规各异。多数国家规定癫痫患者如要获得驾照不得服用苯二氮䓬类抗癫痫药物(困倦易诱发车祸)[24]。我国的有关法规更严,所有被诊断为癫痫的患者均不能获得驾照。
3.2 皮疹及交叉反应性超敏反应
各种抗癫痫药物治疗均可能发生皮疹及交叉反应性超敏反应[25]。
1)先前使用抗癫痫药物(尤其是苯妥英、苯巴比妥或奥卡西平)或三环类抗抑郁药物后发生过皮疹的患者,他们使用卡马西平治疗的皮疹发生风险增加。因此,如果可能,这些患者应避免使用卡马西平。
2)先前使用抗癫痫药物(尤其是卡马西平或苯巴比妥)后发生过皮疹的患者,他们使用苯妥英治疗的皮疹发生风险增加。因此,如果可能,这些患者应避免使用苯妥英。
3)奥卡西平与卡马西平治疗有25% ~ 30%的过敏交叉反应风险。
4)对磺胺类药物过敏患者应避免使用唑尼沙胺。
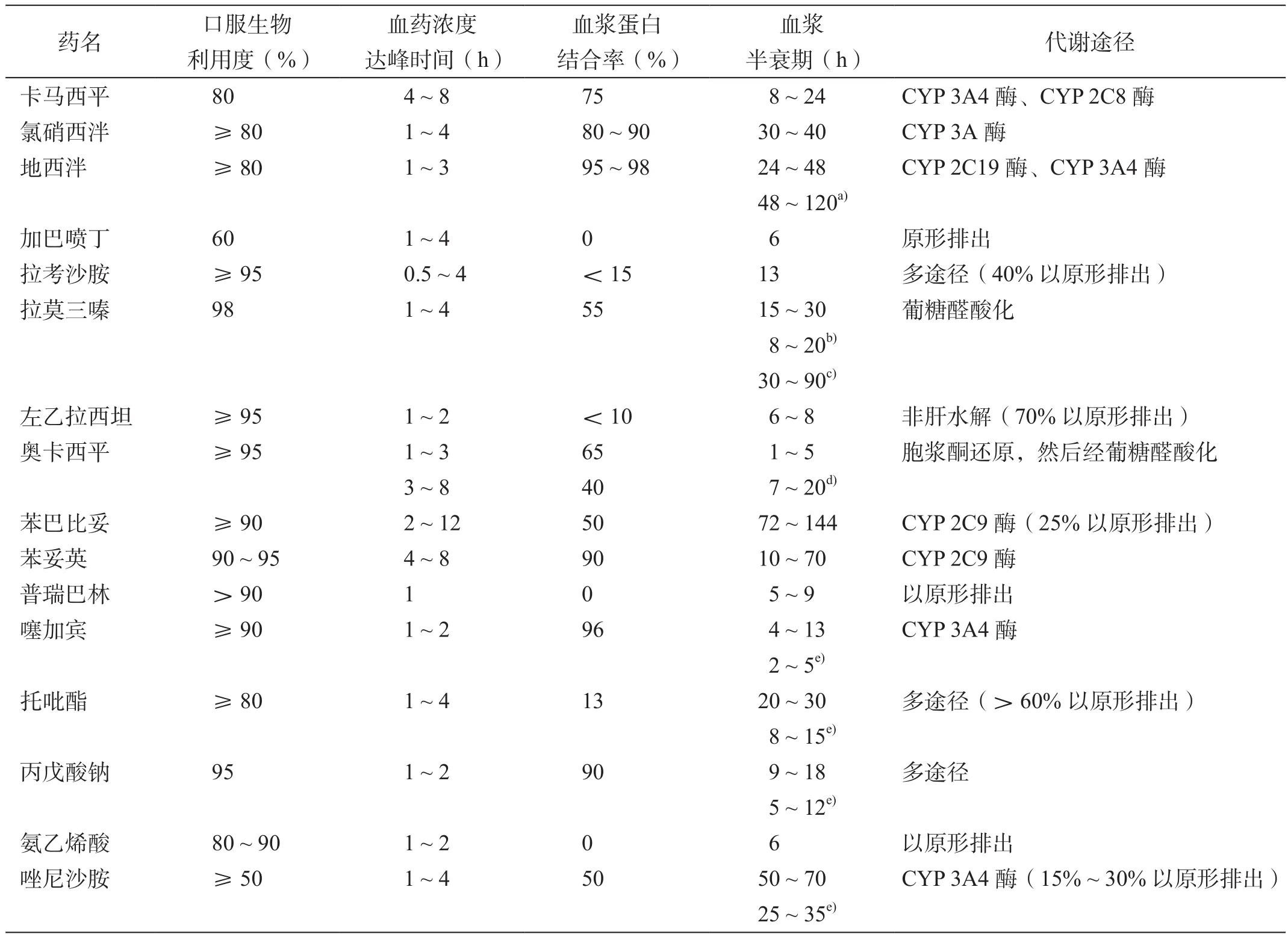
表2 抗癫痫药物的药代动力学数据[16-23]
5)儿童、先前使用抗癫痫药物后发生过皮疹、快速加量或同时服用丙戊酸钠都会增加拉莫三嗪治疗的皮疹发生风险。
3.3 肝功能损害患者用药
对肝功能损害患者,除加巴喷丁、普瑞巴林和氨乙烯酸外,药厂均建议应谨慎使用其他所有抗癫痫药物(从小剂量开始用药,缓慢加量并谨慎监测),尤其是左乙拉西坦(可能同时存在肾功能损害作用,严重肝功能损害患者宜半量使用)、拉考沙胺和奥卡西平(轻、中度肝功能损害患者仍使用常规剂量,重度肝功能损害患者如何使用还无依据)、苯妥英(监测血药浓度)、噻加宾(轻度肝功能损害患者减量用药、重度肝功能损害患者避免使用)和唑尼沙胺(尽可能避免使用)。
尽管先前或现有的肝病会增加丙戊酸钠和卡马西平治疗导致肝功能衰竭的风险,但并不影响肝脏对药物的代谢,除非已肝衰竭[26](此时使用需要谨慎监测)。
3.4 肾功能损害患者用药
对肾功能损害患者,除苯妥英和噻加宾外,药厂均建议应谨慎使用其他所有抗癫痫药物(从小剂量开始用药,缓慢加量并谨慎监测)。对拉考沙胺,如患者肌酐清除率<30 ml/min,最大使用剂量为250 mg/d;如患者肌酐清除率≥30 ml/min,使用剂量不变。对加巴喷丁、左乙拉西坦和普瑞巴林,肾功能损害患者使用都需要作剂量调整。此外,有使用普瑞巴林后发生肾衰竭、停药后回复的病例报告。
3.5 育龄期妇女用药
对育龄期妇女,如要使用有肝酶诱导作用的拉莫三
嗪、卡马西平等抗癫痫药物,需仔细询问口服避孕药的使用情况。考虑到抗癫痫药物的致畸作用,怀孕前应避免使用丙戊酸钠。苯二氮䓬类抗癫痫药物和苯巴比妥有增加“软盘婴儿综合征”的发生风险,临分娩时应避免使用。
3.6 特定抗癫痫药物的特定注意事项
1)卡马西平治疗可能导致房室传导阻滞,拉考沙胺和奥卡西平治疗可能导致完全阻滞。
2)卡马西平治疗有增加骨髓毒性的可能,处方前应询问患者是否有骨髓抑制的病史。
3)奥卡西平和普瑞巴林治疗可导致体液潴留,处方前须仔细询问患者是否有心力衰竭的病史。
3.7 药物相互作用
苯巴比妥、卡马西平和苯妥英有肝酶诱导作用,药物相互作用复杂。相反,加巴喷丁、左乙拉西坦和普瑞巴林几乎没有药物相互作用。
4 不良反应
尽管不同抗癫痫药物的化学结构和作用机制不同,但有很多一致的不良反应。
抗癫痫药物治疗均可导致精神症状和中枢神经系统抑制反应,包括困倦、共济失调、认知损害、激惹、复视和头晕。苯巴比妥导致认知损害的发生率最高,程度也最严重,而新一代抗癫痫药物和丙戊酸钠较少导致认知障碍,且程度也较轻[19]。抗癫痫药物治疗会导致约1/500的用药者产生自杀意向。
所有抗癫痫药物治疗均可导致人格改变、行为障碍和好斗,尤以左乙拉西坦最为常见(一些随机、对照临床试验报告的发生率为≤15%)[27]。通过筛查既往好斗史并且小心、缓慢加量可以降低这种不良反应发生的风险,但有时候需要换用抗癫痫药物。使用左乙拉西坦的儿童加用吡哆醛可以改善行为障碍[28]。
很多抗癫痫药物治疗可导致血液系统紊乱,其中大部分是无症状、也可能不需要停用该抗癫痫药物的。非氨酯(已限制其使用)和卡马西平(需要监测骨髓抑制的症状和全血细胞计数)可能导致严重的血液系统紊乱(如再生障碍性贫血和粒细胞缺乏症),对许多新一代的抗癫痫药物也需注意这方面的问题。有肝酶诱导作用的抗癫痫药物(如苯妥英)还可导致叶酸缺乏。
抗癫痫药物治疗导致生化指标(尤其是肝功能)紊乱也很常见,但通常无症状。许多抗癫痫药物、尤其是非氨酯(已限制其使用)和卡马西平(需监测肝脏疾病和肝功能)治疗可导致肝功能损害。新一代抗癫痫药物治疗的生化指标紊乱发生率未知。约1/3 000的丙戊酸钠用药者会发生胰腺炎[29];使用新一代抗癫痫药物的患者也可能发生胰腺炎(发生率未知)。丙戊酸钠治疗还可导致高氨血症(肝功能可以正常),但除非出现呕吐、共济失调和困倦等症状,一般不需停药。
拉莫三嗪、卡马西平和奥卡西平治疗可导致皮疹,危险因素包括先前使用抗癫痫药物后发生过皮疹、起始剂量大和加量快(儿童患者联合使用拉莫三嗪和丙戊酸钠)。各种抗癫痫药物治疗都会导致发生严重皮疹如Stevens-Johnson综合征等,但以使用拉莫三嗪后的发生率最高(对成人患者为1/1 000)。使用卡马西平和苯妥英会使某些HLA基因型患者更易发生Stevens-Johnson综合征。
有些抗癫痫药物有特殊的不良反应,如托吡酯和唑尼沙胺治疗可导致尿路结石,苯妥英治疗可导致面容粗鄙、痤疮、多毛和牙龈增生。
参考文献
[1] Perucca E. An introduction to antiepileptic drugs [J]. Epilepsia, 2005, 46(suppl 4): 31-37.
[2] Klitgaard H, Verdru P. Levetiracetam: the first SV2A ligand for the treatment of epilepsy [J]. Expert Opin Drug Discov, 2007, 2(11): 1537-1545.
[3] Jevtovic-Todorovic V, Todorovic SM. The role of peripheral T-type calcium channels in pain transmission [J]. Cell Calcium, 2006, 40(2): 197-203.
[4] Kochegarov AA. Pharmacological modulators of voltagegated calcium channels and their therapeutical application [J]. Cell Calcium, 2003, 33(3): 145-162.
[5] Shin HS. T-type Ca2+channels and absence epilepsy [J]. Cell Calcium, 2006, 40(2): 191-196.
[6] Loscher W. Basic pharmacology of valproate: a review after 35 years of clinical use for the treatment of epilepsy [J]. CNS Drugs, 2002, 16(10): 669-694.
[7] Lee CH, Tsai TS, Liou HH. Gabapentin activates ROMK1 channels by a protein kinase A (PKA)-dependent mechanism [J]. Br J Pharmacol, 2008, 154(1): 216-225.
[8] Sheets PL, Heers C, Stoehr T, et al. Differential block of sensory neuronal voltage-gated sodium channels by lacosamide [(2R)-2-(acetylamino)-N-benzyl-3-methoxypropanamide], lidocaine, and carbamazepine [J]. J Pharmacol Exp Ther, 2008, 326(1): 89-99.
[9] Mann MW, Pons G. Various pharmacogenetic aspects of antiepileptic drug therapy: a review [J]. CNS Drugs, 2007, 21(2): 143-164.
[10] Loscher W, Klotz U, Zimprich F, et al. The clinical impact of pharmacogenetics on the treatment of epilepsy [J]. Epilepsia, 2009, 50(1): 1-23.
[11] Abe T, Seo T, Ishitsu T, et al. Association between SCN1A polymorphism and carbamazepine-resistant epilepsy [J]. Br J Clin Pharmacol, 2008, 66(2): 304-307.
[12] Perucca E. Clinical pharmacokinetics of new-generation antiepileptic drugs at the extremes of age [J]. Clin Pharmacokinet, 2006, 45(4): 351-363.
[13] Chung WH, Hung SI, Hong HS, et al. Medical genetics: a marker for Stevens-Johnson syndrome [J]. Nature, 2004, 428(6982): 486.
[14] Locharernkul C, Loplumlert J, Limotai C, et al. Carbamazepine and phenytoin induced Stevens-Johnson syndrome is associated with HLA-B*1502 allele in Thai population [J]. Epilepsia, 2008, 49(12): 2087-2091.
[15] U.S. Food and Drug Administration. Information for healthcare professionals: dangerous or even fatal skin reactions — carbamazepine (marketed as Carbatrol, Equetro, Tegretol and generics). 2007 [EB/OL]. [2011-10-12]. http:// www.fda.gov/Drugs/DrugSafety/PostmarketDrugSafetyInfor mationforPatientsandProviders/ucm124718.htm.
[16] Perucca E. The clinical pharmacokinetics of the new antiepileptic drugs [J]. Epilepsia, 1999, 40(Suppl 9): S7-S13.
[17] Garnett WR. Clinical pharmacology of topiramate: a review [J]. Epilepsia, 2000, 41(Suppl 1): S61-S65.
[18] Anderson PO, Knoben JE, Troutman WG. Handbook of clinical drug data [M]. 10th Ed. New York, USA: McGraw Hill, 2002.
[19] Perucca E. Pharmacological and therapeutic properties of valproate: a summary after 35 years of clinical experience [J]. CNS Drugs, 2002, 16(10): 695-714.
[20] May TW, Korn-Merker E, Rambeck B. Clinical pharmacokinetics of oxcarbazepine [J]. Clin Pharmacokinet, 2003, 42(12): 1023-1042.
[21] Bang LM, Goa KL. Spotlight on oxcarbazepine in epilepsy [J]. CNS Drugs, 2004, 18(1): 57-61.
[22] Kwan P, Brodie MJ. Phenobarbital for the treatment of epilepsy in the 21st century: a critical review [J]. Epilepsia, 2004, 45(9): 1141-1149.
[23] Patsalos PN. Clinical pharmacokinetics of levetiracetam [J]. Clin Pharmacokinet, 2004, 43(11): 707-724.
[24] Twycross RG, Wilcock A. Hospice and palliative care formulary USA [M]. 2nd Ed. Nottingham, USA: Palliativedrugs.com Ltd., 2008: 493-496.
[25] Hirsch LJ, Arif H, Nahm EA. Cross-sensitivity of skin rashes with antiepileptic drug use [J]. Neurology, 2008, 71(19): 1527-1534.
[26] Ford-Dunn S. Managing patients with cancer and advanced liver disease [J]. Palliat Med, 2005, 19(7): 563-565.
[27] Dinkelacker V, Dietl T, Widman G, et al. Aggressive behavior of epilepsy patients in the course of levetiracetam add-on therapy: report of 33 mild to severe cases [J]. Epilepsy Behav, 2003, 4(5): 537-547.
[28] Major P, Greenberg E, Khan A, et al. Pyridoxine supplementation for the treatment of levetiracetam-induced behavior side effects in children: preliminary results [J]. Epilepsy Behav, 2008, 13(3): 557-559.
[29] French JA. First-choice drug for newly diagnosed epilepsy [J]. Lancet, 2007, 369(9566): 970-971.
收稿日期:(2013-11-26)
通讯作者:**朱国行,教授,主要从事癫痫的临床及基础研究。E-mail: guoxingyj@hotmail.com
作者简介:*吴冬燕,女,主治医师,主要从事癫痫的临床及基础研究。E-mail: walkwinter@163.com
文章编号:1006-1533(2015)09-0003-05
文献标识码:C
中图分类号:R971.6

