HPLC梯度洗脱法同时测定银黄软胶囊中绿原酸和黄芩苷的含量
艾光丽,王维,曾桢,蒲旭峰
·炮制制剂·
HPLC梯度洗脱法同时测定银黄软胶囊中绿原酸和黄芩苷的含量
艾光丽1,王维1,曾桢2,蒲旭峰2
目的:建立银黄软胶囊中绿原酸和黄芩苷含量同时测定的高效液相色谱法。方法:采用Symmetry-C18柱(4.6 mm × 250 mm,5 μm),乙腈-0.4%磷酸水溶液为流动相梯度洗脱,检测波长319 nm,柱温35℃,流速1.0 mL.min-1,进样量10 μL。结果:绿原酸在范围1.67 μg.mL-1~16.7 μg.mL-1内呈良好的线性关系,平均回收率为99%,RSD为2.1%(n=6);黄芩苷在范围3.32 μg.mL-1~33.2 μg.mL-1内呈良好的线性关系,平均回收率为97%,RSD为1.1%(n=6)。结论:本实验所建立的色谱分析方法能够简单、快速、准确地测定银黄软胶囊中黄芩苷和绿原酸的含量。不同厂家的银黄软胶囊中绿原酸和黄芩苷含有量具有显著差异,建立黄芩苷和绿原酸的定量控制方法具有重要意义。
银黄软胶囊;高效液相色谱法;绿原酸;黄芩苷;梯度洗脱
银黄软胶囊收载于国家食品药品监督管理总局新药转正标准[1],由金银花提取物和黄芩提取物两种物质加工而成,具有清热疏风、利咽解毒的功效。银黄制剂中含有多种有效成分,但指标成分分别为金银花提取物中的绿原酸和黄芩提取物中的黄芩苷;不同银黄制剂的含量测定均是以指标成分绿原酸和黄芩苷的含量为标准,文献中多采用HPLC法、毛细管电泳法、UV法等分别或同时测定银黄制剂中绿原酸和黄芩苷的含量[2-14]。目前,对银黄软胶囊制剂中的有效成分同时进行测定的研究较少,为更好地控制该产品的质量,本实验采用HPLC梯度洗脱法,在同一波长下同时测定银黄软胶囊中绿原酸和黄芩苷的含量,同时研究了提取银黄软胶囊中绿原酸和黄芩苷成分的相关条件。并利用建立的分析方法对不同厂家银黄软胶囊中指标成分的含量进行了比较,更有利于控制银黄软胶囊的质量。
1 仪器与试药
仪器:Agilent 1200高效液相色谱仪,Agilent1200DAD二极管阵列检测器,AUX220电子天平(日本岛津),AE240电子天平(梅特勒-托利多,上海),SK25OH型超声波清洗器(上海科导超声仪器有限公司)。
对照品:绿原酸(110715-201016,96.2%,供含量测定用),黄芩苷(110753-201415,94%,供含量测定用),均由中国食品药品检定研究院提供。
试剂:乙腈、甲醇为色谱纯(北京百灵威科技有限公司),水为超纯水,其余试剂均为分析纯。
药品:银黄软胶囊(贵州世仁堂制药有限公司,批号:151107;石药集团欧意药业有限公司,批号:359160115、359160113;桂林集琦药业有限公司,批号:20151002、20150704)。
2 方法学考察
2.1 色谱条件
色谱柱:Symmetry-C18柱( 4.6 mm×250 mm,5μm); 以0.4%磷酸水溶液为流动相A,乙腈为流动相B,梯度洗脱,0~30 min,5%→40%B, 30~40 min,40%→80% B; 检测波长319 nm; 柱温35℃; 流速1.0 mL. min-1; 进样量10 μL。
2.2 溶液的制备
2.2.1 混合对照品溶液的制备 精密称取黄芩苷和绿原酸对照品适量,制成重量浓度分别为33.2 µg.mL-1黄芩苷,16.7 µg.mL-1绿原酸的混合对照品溶液。
2.2.2 供试品溶液的制备 取装量差异下的银黄软胶囊约0.3 g,研匀,精密称定,置25 mL棕色容量瓶中,加入适量70%甲醇水溶液,超声处理30 min,冷却至室温,加70%甲醇溶液至刻度线,摇匀,即得。
2.2.3 阴性对照溶液的制备 取按银黄软胶囊工艺方法制备的缺黄芩提取物、缺金银花提取物的阴性对照样品,按供试品溶液制备方法制备阴性对照品溶液。
2.3 线性关系的考察
精密量取“2.2.1”项下的混合对照品溶液0.5、2、4、6、8、10 mL,分别放于10 mL的棕色容量瓶中,加70%甲醇水溶液至刻度线。精密吸取系列对照液各10 μL,注入液相色谱仪,以质量浓度为横坐标(X),峰面积为纵坐标(Y)进行线性回归,绿原酸和黄芩苷的回归方程分别为Y=21.102X+0.4024(r=1),Y=15.784X +0.5212 (r=1)。结果表明绿原酸在8.35 µg.mL-1~167µg.mL-1,黄芩苷在16.6 µg.mL-1~332 µg.mL-1内峰面积与质量浓度呈良好的线性关系。
2.4 专属性试验
按上述色谱条件分别将对照品溶液、阴性对照溶液和供试品溶液注入液相色谱仪中,记录色谱图(见图1)。试验结果表明各阴性样品溶液的色谱图中,在绿原酸及黄芩苷相应的位置无干扰,表明该法专属性良好。
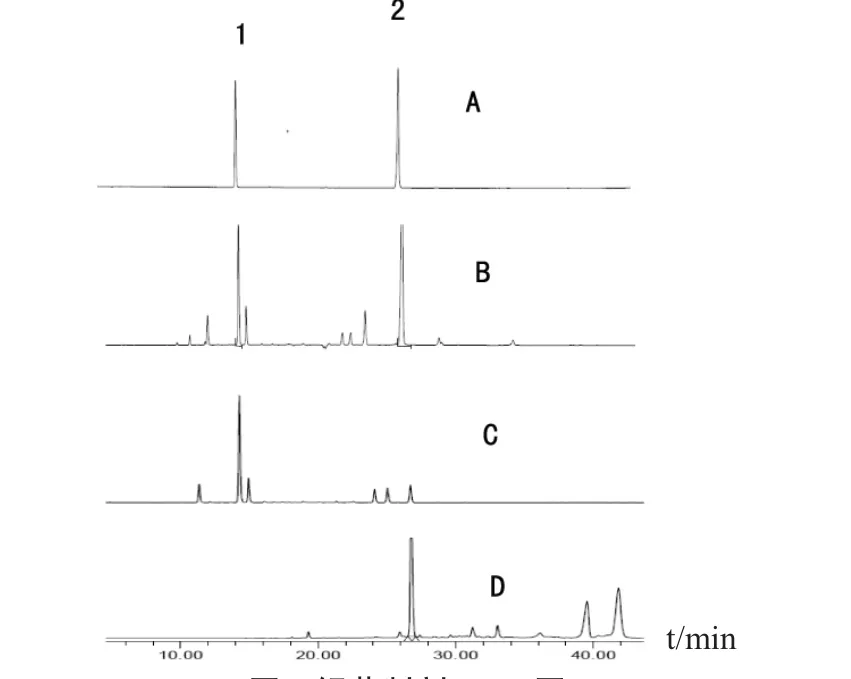
图1 银黄制剂HPLC图
2.5 精密度试验
精密吸取“2.2.1”项下的混合对照品溶液10 µL,连续进样6次并测定黄芩苷和绿原酸峰面积,黄芩苷RSD为0.4%,绿原酸RSD为0.3%,表明仪器精密度良好。
2.6 稳定性试验
取同一批供试品(151107),按正文含量测定项方法制备供试品溶液,分别于0,4,8,12,16,24 h测定黄芩苷和绿原酸峰面积,结果黄芩苷RSD为0.6%,绿原酸RSD为1.5%,表明供试品溶液中的绿原酸和黄芩苷成分在室温放置24 h内基本稳定。
2.7 重复性试验
取同一批供试品(151107),研细,取0.3 g,按“正文含量测定方法平行测定6份,黄芩苷和绿原酸的质量分数RSD分别为1.6%、2.0%,试验结果表明本法的精密度良好。
2.8 范围试验
取同一批供试品(151107)6份,其中3份取0.15 g,另3份取0.6 g,精密称定,按正文含量测定项下方法制备供试品溶液并进样测定,结果绿原酸和黄芩苷的质量分数RSD分别为1.78%、1.86%,表明供试品在限度的50%~200%之间,可满足含量测定需要。
2.9 回收率试验
取已知含量(151107)的同一批样品6份,每份0.01 g,精密称定,分别加入相同量的绿原酸、黄芩苷对照品,按正文含量测定项下方法处理并进行测定,计算回收率,结果见表1。绿原酸平均回收率为99%,RSD为2.1%;黄芩苷平均回收率为97%,RSD为1.1%。表明该方法准确可靠。
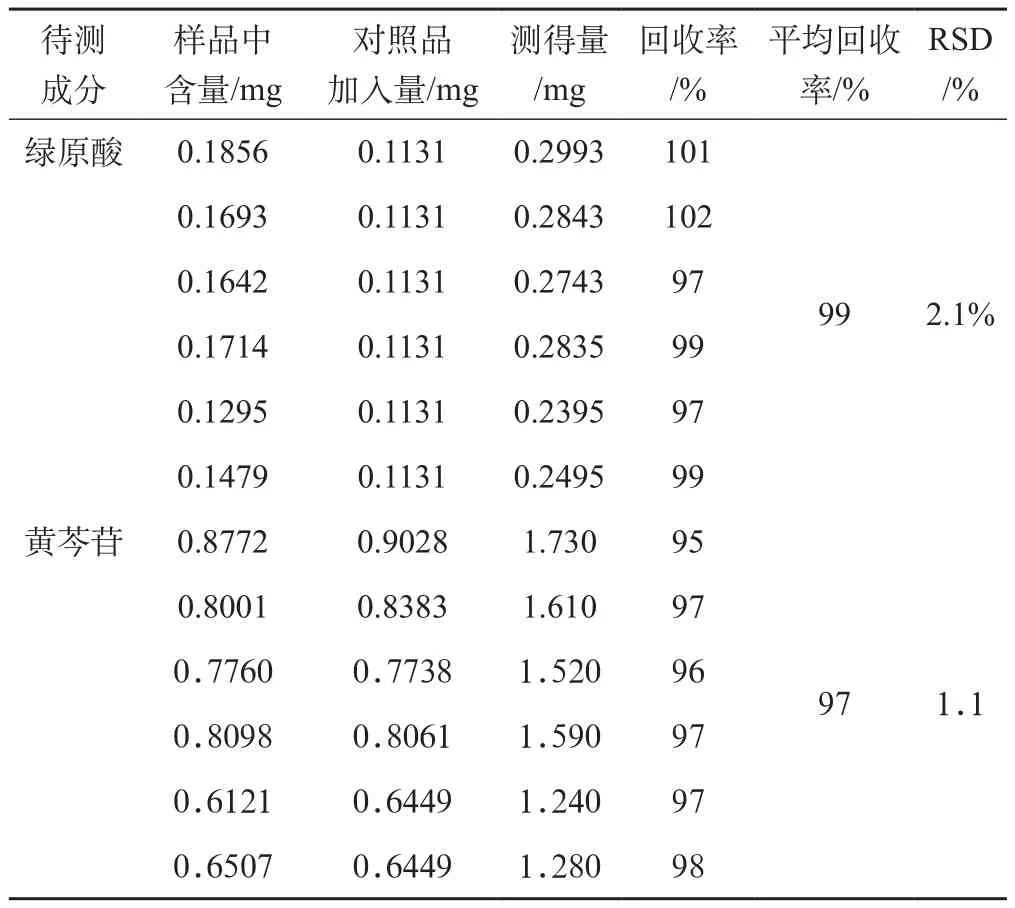
表1 绿原酸和黄芩苷回收率试验结果(n=6)
2.10 样品测定
按正文拟定的含量测定方法对5批银黄软胶囊中黄芩苷和绿原酸含量进行测定,每批平行测定2次,结果见表2。
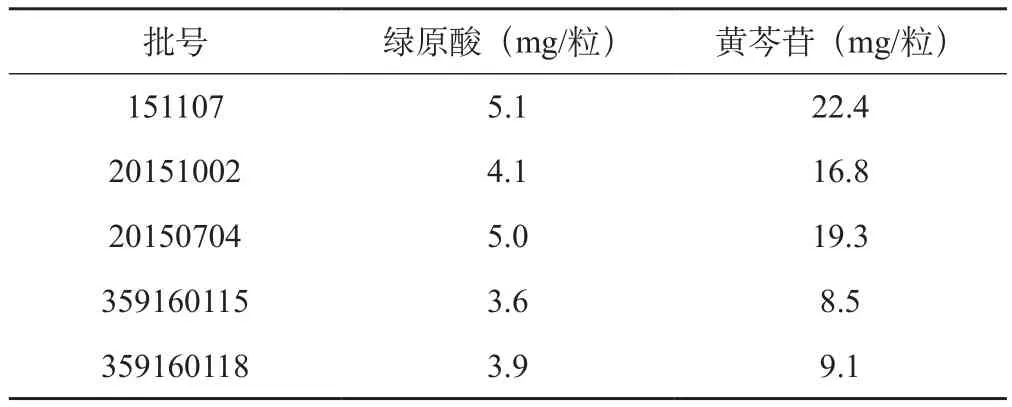
表2 样品含量测定结果(n=2)
3 讨论
3.1 检测波长的选择
绿原酸的最强吸收波长是319 nm ,而黄芩苷在280 nm处有最强吸收, 319 nm有强吸收。银黄制剂中绿原酸含量比黄芩苷低,在同一波长下同时测定黄芩苷和绿原酸,应选择含量相对低的绿原酸的最大吸收波长319 nm 作为检测波长,从而减小误差,不仅能够提高绿原酸检测的灵敏度,而且对黄芩苷的检测也没有明显的影响。
3.2 提取条件的考察
提取方法有回流法、冷浸法、超声法等,试验证明,回流法提取率比超声法低,而冷浸法时间长,不利于试验的进行,超声是最佳的提取方法。超声时间对绿原酸无明显影响,对黄芩苷的影响较大, 30 min绿原酸和黄芩苷都能达到最大提取量。绿原酸成分易溶于甲醇、乙醇等有机溶剂,而黄芩苷成分较难溶于甲醇、乙醇,因此笔者选择了水和醇的混合水溶液作为提取溶剂, 70%甲醇水溶液对绿原酸和黄芩苷的提取率最大。同时比较了用70%甲醇水溶液25 mL、50 mL、100 mL为提取溶剂进行测定,不同溶剂量对含量测定结果影响较小,故选择25 mL进行提取。
3.3 流动相的考察
流动相应有较好的分离度,且绿原酸、黄芩苷的保留时间不宜过长。等度洗脱保留时间短,但绿原酸的色谱峰分离效果不好;而梯度洗脱保留时间适宜,且绿原酸的色谱峰分离效果好。同时考察了甲醇-磷酸水溶液、甲醇-水、乙腈-磷酸水溶液、乙腈-水等体系,结果乙腈-磷酸水溶液的峰形好,分离效果较好,基线平稳,干扰少。据相关文献表明,磷酸加入量对拖尾情况影响较小,根据银黄系列制剂的标准[1,15,16,17],选择0.4%的磷酸水溶液,可得到较好的色谱峰形。
3.4 结果分析
银黄软胶囊为中药复方制剂, 所含成分较为复杂,本文运用HPLC法同时测定银黄软胶囊中绿原酸和黄芩苷的含量, 实验结果表明,该方法简单、准确、重现性好、灵敏度高, 可用于该制剂的质量控制。本实验测定了3个不同厂家、不同批次的银黄软胶囊制剂,实验结果表明, 不同厂家生产的制剂中绿原酸和黄芩苷的含有量相差较大, 同一厂家不同批次内所含绿原酸和黄芩苷也存在差异, 但各厂家药品的服用量是相同的, 这可能会影响该制剂的临床疗效, 故产生的副作用缓急有无也不同。因此, 有必要对银黄软胶囊制剂中绿原酸和黄芩苷含量进行限定。
[1] 国家食品药品监督管理局.新药转正药品标准[S].YBZ17962005.
[2] 张婷,美尔哈巴•热西提,林潇,等.HPLC-MS /MS 法测定银黄颗粒中绿原酸和黄芩苷[J].中草药,2012,43(4):711-713.
[3] 宋粉云,龚红全,林琳,等.毛细管电泳法测定银黄胶囊及银黄颗粒中黄芩苷和绿原酸的含量[J].广东药学院学报2007,23(3):231-233.
[4] 谢东,高彩虹.高效液相色谱法测定银黄软胶囊中绿原酸和黄芩苷的含量[J].中国医院药学杂志,2006,26(5):631-632.
[5] 刘艳,张玉萍.HPLC 法测定银黄滴丸中黄芩苷的含量[J].云南中医中药杂志,2009,30(1):56-57.
[6] 王瑞,李玉娟,毕开顺.RP-HPLC 法测定解毒宣透汤中连翘苷、绿原酸及黄芩苷的含量[J].中药材,2001,24(4):287-288.
[7] 李坚.褶合曲线分析法测定银黄含片中绿原酸和黄芩苷的含量[J].郧阳医学院学报,2006,25( 2):87-89.
[8] 锐利,艾力玛.银黄注射液中黄芩苷利绿原酸的含量测定[J].内蒙古中医药.2001.(4):41-42.
[9] 杨克迪,王丽君,龙云飞.高效液相色谱程序可变波长法测定银黄颗粒中绿原酸和黄芩苷的含量[J].中国医院药学杂志,2007,27(7):992-993.
[10] 白雁,王星,龚海燕,等.NIRS 结合PLS 快速分析银黄颗粒中有效成分含量[J]. 计算机与应用化学,2010,27(12):1703-1706.
[11] 杨菲,冯伟红,王智民,等.一测多评法测定银黄制剂中4种黄酮类成分含量[J].中国药学杂志,2012,47(12):984-989.
[12] 吕凌,路小东,戴萍萍,等.RP-HPLC 测定银黄咀嚼片中绿原酸和黄芩苷的含量[J].中成药,2007,29 (6):921-922.
[13] 韦汉燕,桂劲松,戴平.高效液相色谱法测定银黄颗粒中咖啡酸的含量[J].儿科药学杂志.2012.18 (8):39-41.
[14] 翟淑平,黄斌,王秀敏,等.HPLC法同时测定银黄可溶性粉中绿原酸和黄芩苷的含量[J].中国兽医杂志,2008,44(6):87-88.
[15] 国家药典委员会.中国药典.一部[S].2015:1495-1498.
[16] 卫生部药品标准中药成方制剂.第十九册[S].1996: 199.
[17] 国家药品监督管理局.新药转正药品标准.第十六册[S].1998: 42.
( 责任编辑:胡慧玲)
Simultaneous determination of chlorogenic acid and baicalin in Yinhuang soft capsule by HPLC with gradient elution/
AI Guang-li1, WANG Wei1, ZENG Zhen2, PU Xu-feng2//1.(Chengdu University of Traditional Chinese Medicine, Chengdu 611137.Sichuan; 2.Chengdu Center for Food and drug Control, Chengdu 610000,Sichuan)
Objective: To establish a method for the simultaneous determination of chlorogenic acid and baicalin in Yinhuang soft capsule.Method:The chromatographic separations were obtained on a Symmetry-C18column (250 mm × 4.6 mm, 5 μm). The mobile phase was consisted of acetonitrile and 0. 4% phosphoric acid solution in a gradient elution manner with a fl ow rate of 1. 0 mL.min-1at 35℃.The detection wavelength was set at 319 nm.Sample volume was 10 μL.Result:Linear range of chlorogenic acid was 1.67~16.7 μg.mL-1and that of baicalin was 3.32 ~33.2 μg.mL-1. The recovery of chlorogenic acid and baicalin was 99.0% (RSD=2.1%) and 97% (RSD=1.1%), respectively.Conclusion:The chromatographic method established can be used simply and accurately to detect the content of chlorogenic acid and baicalin in Yinhuang soft capsule. The contents of chlorogenic acid and baicalin are different in different manufacturer productions, and it is necessary to establish the quantitative control of chlorogenic acid and baicalin.
Yinhuang soft capsule; HPLC; chlorogenic acid; baicalin; gradient elution
R 283.6
A
] 1674-926X(2017)02-011-03
2015年成都市食品安全风险研究项目;金银花提取物的风险监测研究(2015cdfx01)
1.成都中医药大学药学院,四川 成都 611137;2.成都市食品药品检验研究院, 四川 成都 610000
艾光丽(1989-),女,在读硕士研究生,主要从事的研究方向:中药新制剂、新剂型、新技术Tel:15828578362 Email:1063681279@qq.com
蒲旭峰,博士研究生,研究员,研究方向: 中药新制剂、新剂型、新技术 Email: pxf68@263.net
2016-06-01

