阿魏属药用植物的物质基础△
杨秀伟
(1.北京大学天然药物及仿生药物国家重点实验室,北京 100191;2.北京大学药学院天然药物学系,北京 100191)
阿魏属(Ferula L.)归类为伞形科(Umbelliferae)、芹亚科(Apioideae)、前胡族(Peucedaneae)、阿魏亚族(Ferulinae),全球约150余种,主要分布在欧洲南部、非洲北部、伊朗、阿富汗、俄罗斯的中亚和西伯利亚、印度和巴基斯坦。我国约有26种,其中7种为中国特有,13种可药用,主产新疆、内蒙古等地区。药用物种见表1。
阿魏在我国有着悠久的药用历史, 《唐本草》记载为 “熏渠”,《本草纲目》称为 “哈昔泥”;《中华人民共和国药典》收载新疆阿魏和阜康阿魏的树脂为阿魏的药材,有止痢、消积、解毒等功能,民间常用于治疗消化系统疾病。因其具有难闻的臭味,民间有 “魔鬼的粪便”之称。
本属药用植物尽管化学成分结构具有多样性,但化学类型集中、特殊,在众多的生理活性成分中以倍半萜、香豆素和多硫化合物(polysulfanes)等类为主要特征性化学成分;在这些成分中,倍半萜又是最有特征性的化合物,多以胡萝卜烷(daucane)为基本骨架,是揭示其药效物质基础、研制现代组分中药的良好资源。本文按物种进行评述,重点突出其中的主要化学成分,并给出了它们的化学结构,便于理解其类同性,为研制现代组分中药提供科学依据。

表1 阿魏属(Ferula L.)药用植物信息
1 圆锥茎阿魏F.conocaula
1.1 产地和功效
圆锥茎阿魏产于新疆乌恰;亦分布于吉尔吉斯坦。药用其树脂。有消积、杀虫之功效;用于癥瘕痞块、虫积、心腹冷痛、疟疾、痢疾。
1.2 化学成分
圆锥茎阿魏的根含倍半萜-香豆素杂合化合物:伞形戊烯内酯(umbelliprenin,1),臭阿魏醇(fezelol,feselol,2),臭阿魏素(feterin,3),伞形酮(umbelliferone),宽叶阿魏素-4′-O-β-D-吡喃葡萄糖基-(1→6)-O-β-D-吡喃葡萄糖苷 [cauferin-4′-O-β-D-glucopyranosyl-(1→6)-O-β-D-glucopyranoside,4][1],宽叶阿魏素(cauferin,kauferin,5),宽叶阿魏定(cauferidin,kauferidin,6)[2],圆 锥 茎 阿 魏 酮 苷(conferoside,7),圆 锥 茎 阿 魏 苷 (cauferoside,8)[3],圆锥茎阿魏素(conferin,9)[4],圆锥茎阿魏醇 (conferol, mogoltacin, 10)[5], 宽 叶 阿 魏 宁(cauferinin,11)[6],二氢圆锥茎阿魏素(dihydroconferin,12)[7],圆锥茎阿魏二酮(conferdione,13)[8]。
圆锥茎阿魏的根和果实中含倍半萜-香豆素杂合化合物:圆锥茎阿魏灵(ferocolin,14),圆锥茎阿魏宁(ferocolinin,15),圆锥茎阿魏定(ferocolidin,16),圆锥茎阿魏辛(ferocolicin,17)[9]。
圆锥茎阿魏的果实含倍半萜-香豆素杂合化合物:圆锥茎阿魏酮(conferone,18)[10]。化学结构见图1。
圆锥茎阿魏的叶含黄酮类化合物:木犀草素(luteolin),槲皮素-3-O-β-D-吡喃葡萄糖苷(quercetin-3-O-β-D-glucopyranoside)[11]。
1.3 生物学活性
阿魏(包括圆锥茎阿魏或阜康阿魏、新疆阿魏、Ferula asafoedida L.、F.narthex Boissier、F.foetida Regel、F.borealis K.、F.rigida W.)根和根茎的低浓度乙醇提取物 [含有古蓬阿魏酸(galbanic acid),卡拉阿魏醇(karatavicinol),伞形戊烯内酯,金合欢阿魏醇(farnesiferol)B、C],及其辅料制成的药物组合物,对人肺癌、卵巢癌、黑色素瘤和结肠癌具有预防和治疗作用[12]。
由牛黄、没药、圆锥茎阿魏、藏菖蒲、雪上一支蒿、黑流矿、仁青佐塔、辰砂、藏青果为原料制成的药剂,通过临床试验证明治疗流行性传染病,尤其是流行性感冒,效果显著[13]。
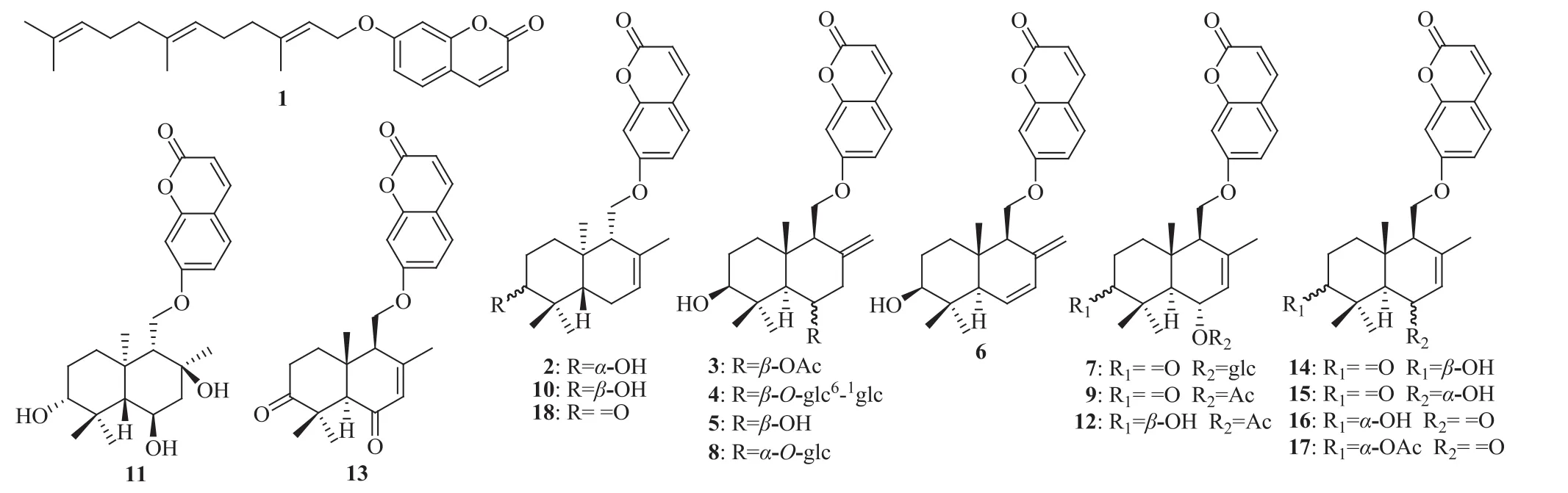
图1 圆锥茎阿魏中部分倍半萜-香豆素杂合化合物的化学结构
2 中亚阿魏F.jaeschkeana
2.1 产地和功效
中亚阿魏产于西藏阿里、扎达;亦分布于阿富汗、俄罗斯、印度、巴基斯坦等地。药用其地上部分树脂。有消积、杀虫之功效;用于肿瘤、创伤、溃疡。
2.2 化学成分
中亚阿魏的根或根茎含倍半萜类化合物:中亚阿魏二醇(jaeschkeanadiol,19)[14-15],5α-对羟基苯甲酰中亚阿魏二醇 [5α-(4-hydroxybenzoyl)jaeschkeanadiol,20],5α-(3-甲氧基-4-羟基苯甲酰基)中亚阿魏二醇 [5α-(3-methoxy-4-hydroxybenzoyl)jaeschkeanadiol,21],阿魏精宁(feruginin,22)[15],阿魏尼定(feruginidin,23),阿魏精(ferugin,24)[16],阿魏酮(feruone,25),中亚阿魏三醇-5α-对羟基苯甲 酸 酯 [ferutriol-5α-(p-hydroxybenzyl) ester,26][17],2,3-环氧中亚阿魏二醇-5α-香荚兰酸酯(2,3-epoxyjaeschkeanadiol-5α-vanillate,27),2β-羟基-3,4-环氧中亚阿魏二醇(2β-hydroxy-3,4-epoxy-jaeschkeanadiol,28),兰萨罗特阿魏醇-5α-对羟基苯甲酸酯 [lancerotol-5α-(4-hydroxybenzoate),29][18],中亚阿魏素(jaeskeanin,30),中亚阿魏萜酮(ferutinone,31),中亚阿魏尼定(jaeskeanidin,32),中亚阿魏宁(ferutinianin,33),当归酰中亚阿魏宁(angeloylferutinianin),山地阿魏定宁(akiferidinin,34),阿魏亭宁(ferutinin,35),中亚阿魏二醇苯甲酸酯(jaeschkeanadiol benzoate,teferdin,teferidin,ferutinol benzoate,36),6-当归酰中亚阿魏二醇(6-angeloyljaeschkeanadiol,37),中亚阿魏二醇-2-羟基苯甲酸酯(jaeschkeanadiol-2-hydroxybenzoate,38)[19],中亚阿魏醇 (ferujaesenol,39),山地阿魏烯醇(akichenol,akitschenol,40),9β-O-当归酰山地阿魏烯醇(9β-O-angeloylakichenol,41),5α-O-对羟基苯甲酰山地阿魏烯醇(5α-O-p-hydroxybenzoylakichenol,42)[20],中亚阿魏萜醇(jaeschkenol,43),2α,3α-二羟基-4-酮基-5α-对羟基苯甲酰基-中亚阿魏二醇(2α,3α-dihydroxy-4-keto-5α-p-hydroxybenzoyl-jaeschkeanadiol,44)[21],异阿魏酮(isoferuone,45),2,3-环氧山地阿魏烯醇(2,3-epoxyakichenol,46)[22],5α-4′-羟 基 苯 甲 酰 中 亚 阿 魏 醇 (5α-4′-hydroxybenzoylferujaesenol,47),5α-3′-甲氧基-4′-羟基苯甲酰中亚阿魏醇 (5α-3′-methoxy-4′-hydroxybenzoylferujaesenol,48)[23],中 亚 阿 魏 二 醇 酯 (jaeschferin,49)[24];含倍半萜-香豆素杂合化合物:环氧金合欢黄白蓍草酯(epoxyfarnachrol,50),辣皮树萜醇 B(drimartol B,51)[19];化学结构见图2。含香豆素类化合物:中亚阿魏酚(ferujol)[25];含单萜和挥发油:对薄荷-3-烯-1,2-二醇 (p-menth-3-ene-1,2-diol),对薄荷-4-烯-1,2-二醇 (p-menth-4-ene-1,2-diol),对薄荷-8-烯-1,2-二醇(p-menth-8-ene-1,2-diol)[26],反式-对薄荷-1,4-二醇(trans-p-menthan-1,4-diol),1-羟基异香芹薄荷醇(1-hydroxyisocarvomenthol),外向-1-甲基-4-(1-甲基乙基)-7-氧代双环 [2.2.1]庚烷-2-醇 [exo-1-methyl-4-(1-methylethyl)-7-oxabicyclo[2.2.1]heptan-2-ol],樟脑(camphor),α-松油醇乙酸酯(α-terpinyl acetate),α-蒎烯(α-pinene),α-松油醇(αterpineol),葛缕子酮(carvone),α-水芹烯(α-phellandrene),对孜然芹烃(p-cymene),柠檬烯(limonene),β-芹子烯(β-selinene),α-龙脑香烯(α-gurjunene),葛缕子酚(carvacrol),对孜然芹烃-7-醇(pcymen-7-ol),α-崖柏 酮 (α-thujone),松油 烯-4-醇(terpinen-4-ol),异长叶松烯(isolongifolene),8,9-p-对薄荷烯-1,2-二醇(8,9-p-menthene-1,2-diol),α-崖柏烯(α-thujene),松油烯-4-醇乙酸酯(terpin-4-yl acetate),3-蒈 烯 (3-carene),表 荜 澄 茄 烯 醇(epicubenol),荜澄茄烯醇(cubenol),大根老鹳草烯 D(germacrene D),顺式-罗勒烯(cis-ocimene),对薄荷-1,2-二醇(p-menthane-1,2-diol),顺式-3-对薄荷烯-1,2-二醇(cis-3-p-menthene-1,2-diol)[27]。
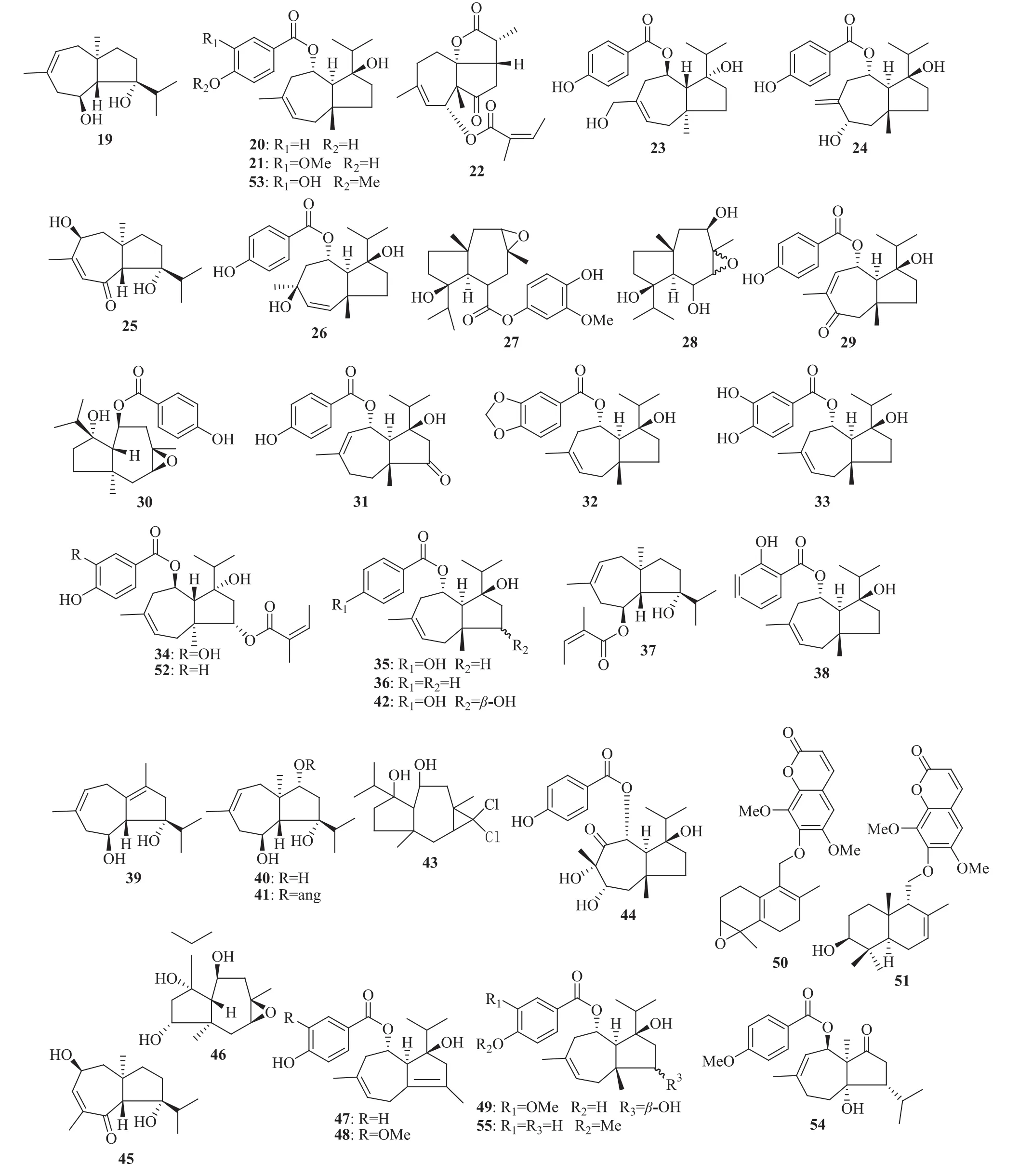
图2 中亚阿魏中部分倍半萜和倍半萜-香豆素杂合化合物的化学结构
中亚阿魏的茎含挥发油:α-蒎烯(α-pinene),β-蒎烯(β-pinene),樟烯(camphene),柠檬烯(limonene),3-蒈烯(3-carene)等[28]。
中亚阿魏的果实含挥发油:d-α-蒎烯(d-α-pinene),孜然芹醛(cumaldehyde),薁(azulene),硫化物(sulfur compound)等[29]。
中亚阿魏的种子含倍半萜类:阿魏亭宁(ferutinin,35),山地阿魏宁素(akitschenin,52),阿魏亭(ferutin,53),大阿魏素(fercomin,54),阿魏替定(ferutidin,55)[30],化学结构见图2;含脂肪油:主要成分为中性脂质(neutral lipids),极性脂质(polar lipids);脂质中包括三甘油酯(triglycerides),游离脂肪酸(free fatty acids),1,3-二甘油酯(1,3-diglycerides),1,2-二甘油酯(1,2-diglycerides),单甘油酯(monoglycerides);脂肪酸中包括酒石酸(margaric acid)[31];含挥发油:α-蒎烯(α-pinene),3-蒈烯(3-carene),樟烯 (camphene),柠檬烯 (limonene),月桂烯(myrcene),松油醇乙酸酯(terpinyl acetate),α-松油醇(α-terpineol),γ-松油烯(γ-terpinene),对孜然芹烃(p-cymene),香叶醇乙酯(geranyl acetate),香叶醇(geraniol)[32]。
2.3生物学活性
抗生育作用:按25 mg·kg-1·d-1剂量给怀孕大鼠灌胃中亚阿魏地上部分的正己烷提取物,可抑制着床[33];灌胃给予其中的单体化合物中亚阿魏酚连续1、2或3 d,亦可发挥避孕作用,但对仓鼠无避孕作用[25]。给雌性大鼠连续灌胃中亚阿魏的正己烷提取物10、20、30 d,能刺激子宫,增加管腔上皮厚度和子宫腺体数目,增重卵巢和子宫,卵巢和子宫的总蛋白、糖原、酸性和碱性磷酸酶活性明显发生改变[34-35]。但对于成年发情期豚鼠可引起骨质疏松[36]。探讨了7个胡萝卜烷型倍半萜的抗生育活性,包括19、22、中亚阿魏二醇-5α-(3-甲氧基-4-羟基苯甲酸酯)(teferin,tefernin)、15、40、52和5α-(3,4-二乙酰氧基苯甲酰氧基)-9β-当归酰氧基中亚阿魏二醇。结果表明灌胃给予大鼠1~7 d,中亚阿魏二醇-5α-(3-甲氧基-4-羟基苯甲酸酯)、阿魏亭宁和山地阿魏宁素显示出避孕作用;对于卵巢切除未成熟雌性大鼠,这3个化合物显示出雌激素活性[37]。
3 新疆阿魏F.sinkiangensis
3.1 产地和功效
新疆阿魏产于新疆伊宁。为 《中华人民共和国药典》 (1977、1985、1990、1995、2000、2005、2010年版)、新疆药品标准(1980年版)、内蒙古蒙药材标准(1986年版)收载 “阿魏”的基原植物之一,药用其树脂。具有消积、化癥、散痞、杀虫之功效;用于肉食积滞、瘀血癥瘕、腹中痞块、虫积腹痛;阿魏油外用于关节痛。藏族、蒙古族、维吾尔族、景颇族、阿昌族、德昂族、傣族亦药用本种。哈萨克族尚用其树脂治神经衰弱、腹懑胀痛、死胎不下;拉祜族用其树脂主治惊风、抽搐;维吾尔族用其树脂治心慌易惊、目赤肿痛等症。
3.2 化学成分
新疆阿魏的根含倍半萜-香豆素杂合化合物:异臭阿魏素(isofeterin,56),大果阿魏酮(lehmannolone,57),大果阿魏醇(lehmannolol,58),新疆阿魏酮(sinkianone,59)[38],金合欢阿魏醇(farnesiferol)B(60)、C(61),托里阿魏诺醇(fekrynol,62),异撒马尔罕阿魏素(isosamarcandin,63),表撒马尔罕阿魏素(episamarcandin,64)[39],化学结构见图 3;含香豆素类化合物:伞形酮(umbelliferone)[39]。
新疆阿魏的油胶树脂含倍半萜-香豆素杂合化合物:伞形戊烯内酯(1)[40-41],金合欢阿魏醇(farnesiferol)A(65)[40]、B(60)、C(61)[40-41],(3′S,8′R,9′S,10′R)-新疆阿魏醇 A [(3′S,8′R,9′S,10′R)-sinkianol A,66],(3′R,5′R,10′R)-新疆阿魏醇 B[(3′R,5′R,10′R)-sinkianol B,67],(5′S,8′R,9′S,10′R)-托里阿魏酮 [(5′S,8′R,9′S,10′R)-ferukrinone,68],托里阿魏素(ferukrin,69),(3′S,5′S,8′R,9′S,10′R)-凯莱阿魏素 [(3′S,5′S,8′R,9′S,10′R)-kellerin,70],(3′S,5′S,8′R,9′S,10′R)-去乙酰凯莱阿魏素 [(3′S,5′S,8′R,9′S,10′R)-deacetylkellerin,71],金合欢阿魏酮A(farnesiferone A,72),多胶阿魏素(gummosin,73),多花素宁(polyanthinin,74)[40],古蓬阿魏酸(galbanic acid,75)[40-41],古蓬阿魏酸甲酯(methyl galbanate,76)[40],卡拉阿魏醇(karatavicinol,10′R-karatavicinol,77)[40-41],卡拉阿魏醇 A(karatavicinol A,78)[41],化学结构见图3;含香豆素类化合物:伞形酮(umbelliferone)[41-42];含苯丙素类化合物:阿魏酸(ferulic acid),3-(3,4-二甲氧基苯基)-2-丙烯醛 [3-(3,4-dimethoxyphenyl)-2-propenal],松柏醛(coniferaldehyde)[42];含 酚类 化 合 物:香 荚兰 素(vanillin)[42];含甾体类化合物:β-谷甾醇[42];含挥发 油:2,3-二 甲 基-3-己 醇 (2,3-dimethyl-3-hexanol),2-乙硫基-丁烷(2-ethylthio-butane),丙基丁基二硫醚(propylbutyldisulfide),十八烷基三烯(octadecatriene),油酸(oleic acid)[43],2,4-二甲基噻吩,丙烯基硫醚,二仲丁基二硫醚,1,3-二噻烷,α-蒎烯,甲基丙烯基二硫醚,α-萜品烯,β-蒎烯,β-月桂烯,2,3,4-三甲基噻吩,β-罗勒烯,α-罗勒烯,别罗勒烯,α-榄香烯,喇叭茶醇,γ-桉叶醇[44],仲-丁基-反式-1-丙烯基二硫烷 (sec-butyltrans-1-propenyl disulfane),仲-丁基-反式-2-丁烯基二硫烷(sec-butyl-trans-2-butenyl disulfane),仲-丁基二硫醚(sec-dibutyl disulfide)[45],仲-丁基-顺式-1-丙烯基二硫烷(sec-butyl-cis-1-propenyl disulfane)等[46],顺式-仲-丁基-1-丙烯基二硫化物(cis-sec-butyl-1-propoenyldisulphide),反式-仲-丁基-1-丙烯基二硫化物(trans-sec-butyl-1-propoenyldisulphide)[47]。
新疆阿魏的种子含倍半萜-香豆素杂合化合物:伞形戊烯内酯(1),大果阿魏醇(58)[48-49],大果阿魏酮(57),新疆阿魏酮(59),金合欢阿魏醇 C(61),托里阿魏诺醇(62),表撒马尔罕阿魏素(64),新疆阿魏烯素(sinkiangenorin)D(79)[49]、E(80)[50]、F(81),8-O-乙酰新疆阿魏烯素 F(8-O-acetylsinkiangenorin F,82)[51], 科 佩 特 阿 魏 酮(fekolone, 83)[49], 克 拉 顿 芹 素 (colladonin,84)[49,52];含半 萜 类 化 合 物:新 疆 阿 魏 烯 素 C(sinkiangenorin C,85)[53];化学结构见图 3。含甾体类化合物:新疆阿魏烯素(sinkiangenorin)A(86)、B(87)[53](化学结构见图 3),豆甾醇(stigmasterol),豆甾醇-3-O-β-D-吡喃葡萄糖苷(stigmasterol-3-O-β-D-glucopyranoside)[52,54], β-谷 甾 醇 (βsitosterol),胡萝卜苷(daucosterol)[54];含木脂素类化合物:(7,8-顺式-8,8′-反式)-2′,4′-二羟基-3,5-二甲氧基落叶松脂醇 [(7,8-cis-8,8′-trans)-2′,4′-dihydroxyl-3,5-dimethoxylariciresinol][48],落叶松脂醇(lariciresinol),牛蒡子苷元(arctigenin)[48,53],马台树脂醇(matairesinol)[53],裂环异落叶松脂醇(secoisolariciresinol)[53-54],松 脂 素 (pinoresinol),(7,8-顺式-8,8′-反式)-2′,4′-二羟基-3,5-二甲氧基-落叶 松 脂 素 [(7,8-cis-8,8′-trans)-2′,4′-dihydroxyl-3,5-dimethoxylariciresinol],牛蒡苷(arctiin),新牛蒡素 A(neoarctin A)[54];含黄酮类化合物:槲皮素(quercetin)[48,54],异槲皮素苷(isoquercitrin)[54],木犀草素-7-O-β-D-葡萄糖醛酸苷(luteolin-7-O-β-D-gluronide)[54],芦丁(rutin)[54];含香豆素类化合物:伞形酮[52,54];含苯丙素类化合物:马克拉丙素酚(macrathoin F)[48,54],阿魏酸[52,54],咖啡酸(caffeic acid),绿原酸(chlorogenic acid),绿原酸甲酯(methyl chlorogenate),1,5-二-O-咖啡酰奎宁酸(1,5-di-O-caffeoylquinic acid),5-O-咖啡酰奎宁酸(5-O-caffeoylquinic acid)[54];含蒽醌类化合物:两型曲霉醌 A(variecolorquinone A)[54];含脂肪醇、酸类化合物:正二十六醇(n-hexacosanol),1-(3-乙基苯 基)-1,2-乙 二 醇 [1-(3-ethylphenyl)-1,2-ethanediol],丁二酸(butanedioic acid)[54];含核苷类化合物:尿嘧啶核苷(uridine),肌苷(inosine)[54];含其他类化合物:(R)-2′-羟基-N-[(2S,3S,4R)-1,3,4-三羟基二十六烷-2-基]壬烷酰胺 {(R)-2′-hydroxy-N-[(2S,3S,4R)-1,3,4-trihydroxyhexacosan-2-yl] nonadanamide},5-羟 甲 基 糠 醛 (5-hydroxymethyl fufural),蔗糖(sucrose),檬果酚 G(parvifoliol G),香草酸(vanillic acid)[54]。
3.3 生物学活性
3.3.1 抗炎作用 在脂多糖刺激的脑小胶质细胞BV-2系,新疆阿魏油胶树脂的三氯甲烷提取物抑制一氧化氮(NO)产生的最大半数抑制浓度(IC50)值为(1.66±1.10)μg·mL-1。其中鉴定的化合物 70、73、75和76呈现出明显的抑制神经炎症的活性,IC50值分别为 4.96、6.93、10.50、5.95μmol·L-1;化合物60、61、69、71、72、74和77能降低NO的产生,IC50值为19.88~47.43μmol·L-1;化合物1、65、66和 68亦能抑制 NO的产生,IC50值为50μmol·L-1[40]。去除挥发油的树脂对皮下注射吲哚美辛(3 mg·kg-1)所致胃溃疡小鼠有抗胃溃疡作用[41]。
3.3.2 镇痛和镇静作用 顺式-仲-丁基-1-丙烯基二硫化物和反式-仲-丁基-1-丙烯基二硫化物的1∶3混合物对吗啡依赖性动物具有脱毒作用,抑制脱瘾综合征和生理依赖性,显示出明显的镇痛和镇静作用;小鼠静脉注射的半数致死量(LD50)为 1.42 g·kg-1[47]。
3.3.3 肿瘤细胞毒活性 新疆阿魏树脂三氯甲烷提取物在 100 mg·mL-1质量浓度下对肺癌 A549、H292、H1792、H460细胞株的增殖抑制率分别为75.45%、65.39%、46.54%、73.68。低极性部位在100 mg·mL-1质量浓度下对A549、H292、H1792、H460细胞株的增殖抑制率分别为88.74%、80.62%、60.11%、92.35%。从低极性部位中分离得到主要倍半萜杂合香豆素化合物60、72、61、74,其中61、74的IC50值分别为35.49、15.44、44.25、21.63μmol·L-1和23.60、17.90、38.33、12.35μmol·L-1,且呈剂量相关性。提示新疆阿魏树脂的低极性部位是体外抑制人肺癌细胞增殖作用的活性部位,化合物61为其主要活性成分[55]。化合物1和落叶松脂醇对人胃癌AGS细胞株增殖具有抑制作用,IC50值分别为(13.67±1.73)、(20.82±2.86)μmol·L-1;使细胞分裂停滞在 G0/G1期,诱导其凋亡[48];化合物58、61、64、79、83、84对人胃癌AGS细胞株增殖亦具有抑制作用,IC50值为12.7~104.8μmol·L-1;化合物57、58、59、61、62和79对宫颈癌HeLa细胞增殖具有抑制作用,IC50值为20.4~226.2μmol·L-1[49];化合物 80[50]、81、82[51]、85、牛蒡子苷元和马台树脂醇[53]对人胃癌AGS细胞株增殖亦具有抑制作用,IC50值分别为12.7、27.1、62.7、36.9、78.2、99.4μmol·L-1;化合物81和82对人癌 K562和HeLa细胞株增殖均无抑制作用[51]。
3.3.4 抗病毒活性 化合物80对流感病毒A H1N1具有抑制作用,IC50值为 4.0μmol·L-1[50]。
3.3.5 抗氧化活性 新疆阿魏树脂的乙酸乙酯提取物呈现非常强的抗氧化作用[56]。
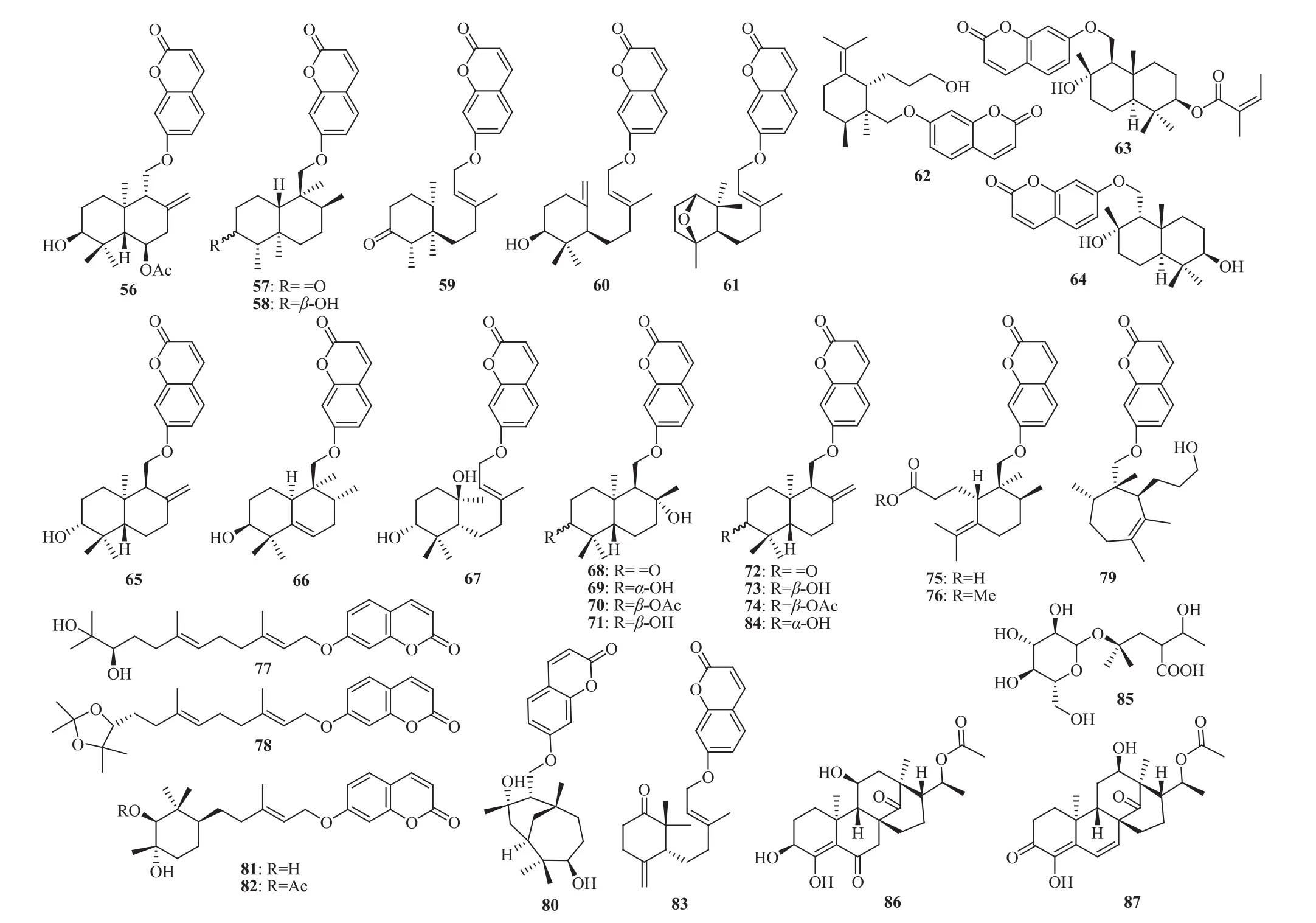
图3 新疆阿魏中的部分化学成分的结构
4 阜康阿魏F.fukanensis
4.1 产地和功效
阜康阿魏产于新疆阜康。药用其根及树脂。有消积、化癥、散痞、杀虫之功效;用于肉食积滞、瘀血癥瘕、腹中痞块、虫积腹痛、肿瘤、创伤、溃疡。阜康阿魏为 《中华人民共和国药典》(1977、1985、1990、1995、2000、2005、2010年版)、新疆药品标准(1980年版)、内蒙古蒙药材标准(1986年版)收载 “阿魏”的基原植物之一,药用其油胶树脂。藏族亦药用;傣族药用其根治小儿高热抽搐、胃痛。
4.2 化学成分
阜康阿魏的根含倍半萜-香豆素杂合化合物:阜康阿魏呋喃香豆素(fukanefuromarin)A(88)、B(89)、C(90)、D(91)[57]、E(92)、F(93)、G(94)[58]、H(95)、I(96)、J(97)、K(98)、L(99)、M (100)[59],2,3-二氢-7-羟基-2R*,3R*-二甲基-2-[4,8-二甲基-3(E),7-壬二烯基-6-酮基]呋喃并 [3,2-c]香豆素 {2,3-dihydro-7-hydroxy-2 R*,3R*-dimethyl-2-[4,8-dimethyl-3(E),7-nonadien-6-onyl]furo[3,2-c]coumarin,101},白根素 C(baigene C,102),阜康阿魏香豆素(fukanemarin)A(103)[57]、B(104)[58],2,3-二氢-7-甲氧基-2 S*,3R*-二甲基-2-[4,8-二甲基-3(E),7-壬二烯基]呋喃并 [3,2-c]香豆素 {2,3-dihydro-7-methoxy-2S*,3R*-dimethyl-2-[4,8-dimethyl-3(E),7-nonadienyl]furo[3,2-c]coumarin,105},2,3-二氢-7-甲氧基-2R*,3R*-二甲基-2-[4,8-二甲基-3(E),7-壬二烯基]呋喃并 [3,2-c]香豆素 {2,3-dihydro-7-methoxy-2R*,3R*-dimethyl-2-[4,8-dimethyl-3(E),7-nonadienyl]furo[3,2-c]coumarin,106}[60],伞形戊烯内酯(1),大果阿魏酮(57),科佩特阿魏酮(83),阿魏素(assafoetidin,107),巴德拉阿魏酮(badrakemone,108)[61],化学结构见图4;含倍半萜类化合物:橙花叔醇(nerolidol),1-(2,4-二羟苯基)-3,7,11-三甲基-3-乙烯基-6(反式),10-十二烷二烯-1-酮 [1-(2,4-dihydroxyphenyl)-3,7,11-trimethyl-3-vinyl-6(E),10-dodecadien-1-one],1-(2,4-二羟苯基)-3,7-二甲基-3-乙烯基-8-(4-甲基-2-呋喃基)-6(反式)-癸烯-1-酮 [1-(2,4-dihydroxyphenyl)-3,7-dimethyl-3-vinyl-8-(4-methyl-2-furyl)-6(E)-octen-1-one],沙生阿魏酮(dshamirone;secoammoresinol)[60],阜康阿魏萜酮(fukanedone)A(109)、B(110)、C(111)、D(112)、E(113)[62],阜康阿魏色酮(fukanefurochromone)A(114)、B(115)、C(116)、D(117)、E(118),(2R,3S)-相对-2-[(3E)-4,8-二甲基-3,7-壬二烯-1-基]-2,3-二氢-7-羟基-2,3-二甲基-4H-呋喃并[2,3-b][1]苯并吡喃-4-酮 {(2R,3S)-rel-2-[(3E)-4,8-dimethyl-3,7-nonadien-1-yl]-2,3-dihydro-7-hydroxy-2,3-dimethyl-4H-furo[2,3-b][1]benzopyran-4-one,119}[63],化学结构见图 4;含酚性基团化合物:阜康阿魏酮酯A(fukaneketoester A)[62],阿魏酸(ferulic acid)[64]。
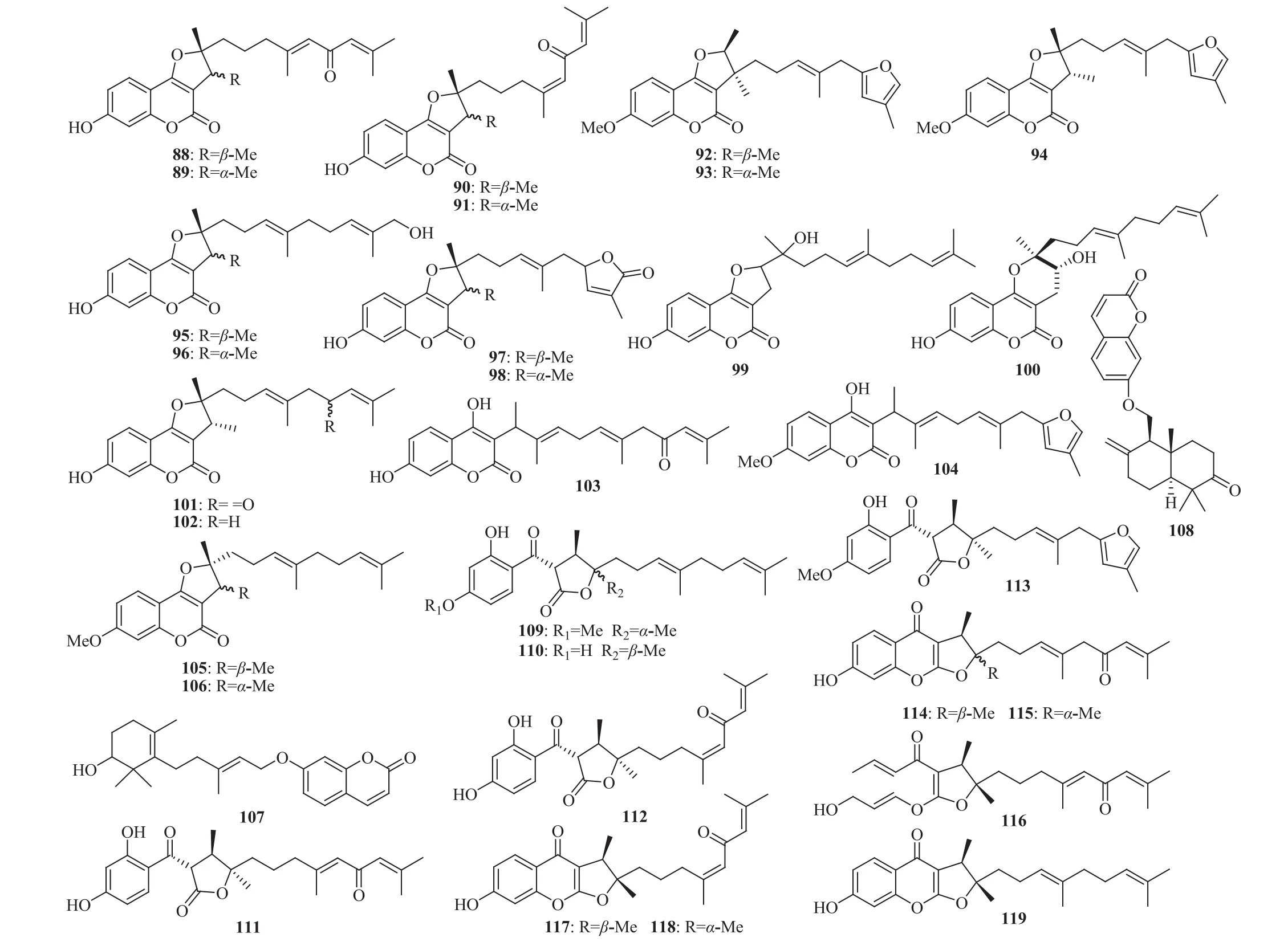
图4 阜康阿魏中部分化学成分的结构
阜康阿魏的油胶树脂含挥发油:仲-丁基-反式-2-丁烯基二硫烷 (sec-butyl-trans-2-butenyldisulfane)[45],仲-丁基-反式-1-丙烯基二硫烷(sec-butyltrans-1-propenyldisulfane)等[45,65], 仲-丁 基-甲 基-二硫烷(sec-butyl-methyl-disulfane),仲-丁基-乙基-二硫烷(sec-butyl-ethyl-disulfane),正丁基-乙基-二硫烷(n-butyl-ethyl-disulfane),二甲基-三硫烷(dimethyltrisulfane),仲-丁 基-顺 式-1-丁烯 基-二 硫 烷 (secbutyl-cis-1-butenyl-disulfane),仲-丁基-反式-1-丁烯基-二硫烷(sec-butyl-trans-1-butenyl-disulfane)[65]。
阜康阿魏的叶含苯丙素类化合物:阿魏酸[64]。
4.3 生物学活性
在脂多糖(LPS)刺激的巨噬细胞RAW 264.7细胞 模 型,化 合 物 88、89、90、91[57]、92、93、94[58]、95、96、97、98[59]、103[57]、104[58]、105和106[60]能抑制 NO的生成,IC50值分别为 13.0、16.2、11.1、8.9、29.0、30.7、27.3、24.3、55.6、11.1、35.7、19.5、30.2、33.5、36.9μmol·L-1;作用机制分析表明,化合物 90、91[57]、92[58]、95、98[59]、103[57]和 105[60]剂量依赖性抑制 iNOSmRNA的表达。
在LPS刺激的巨噬细胞RAW 264.7细胞模型,倍半萜类化合物111、112、113能抑制NO的生成,IC50值分别为 6.7、27.8、76.2μmol·L-1[62];化合物114、115、116、117和119能抑制NO的生成,IC50值分别为 24.7、22.5、29.0、24.0、10.7μmol·L-1;作用机制分析表明,化合物117剂量依赖性抑制iNOS mRNA的表达[63]。
5 大果阿魏F.lehmannii
5.1 产地和功效
大果阿魏产于新疆玛纳斯;亦分布于巴基斯坦、阿富汗、伊朗以及苏联中亚地区。药用其根及树脂。有消积之功效;用于虫积、肉积、心腹冷痛。
5.2 化学成分
大果阿魏的根含倍半萜-香豆素杂合化合物:大果阿魏酮(57)[66],大果阿魏醇(58)[67],新疆阿魏酮(59)[66-67],金合欢阿魏醇 C(61),托里阿魏诺醇(62),阿魏素(107),大果阿魏酮 A(lehmannolone A,120)[66],大果阿魏灵(lehmferin,121),巴德拉阿魏素(badrakemin,122),大果阿魏定(lehmferidin,123)[68],化学结构见图5;含氨基酸类化合物:赖氨酸(Lys)、组氨酸(His)、精氨酸(Arg)、天冬氨酸(Asp)、苏氨酸(Thr)、丝氨酸(Ser)、谷氨酸(Glu)、甘氨酸(Gly)、丙氨酸(Ala)、缬氨酸(Val)、蛋氨酸(Met)、异亮氨酸(IIe)、亮氨酸(Leu)、酪氨酸(Tyr)、苯丙氨酸(Phe)、脯氨酸、胱氨酸[69];含微量元素及重金属元素:Fe、Mn、Zn、K、Na、Ca、Cu、Pb、As、Cd、Hg、Cr[69]。
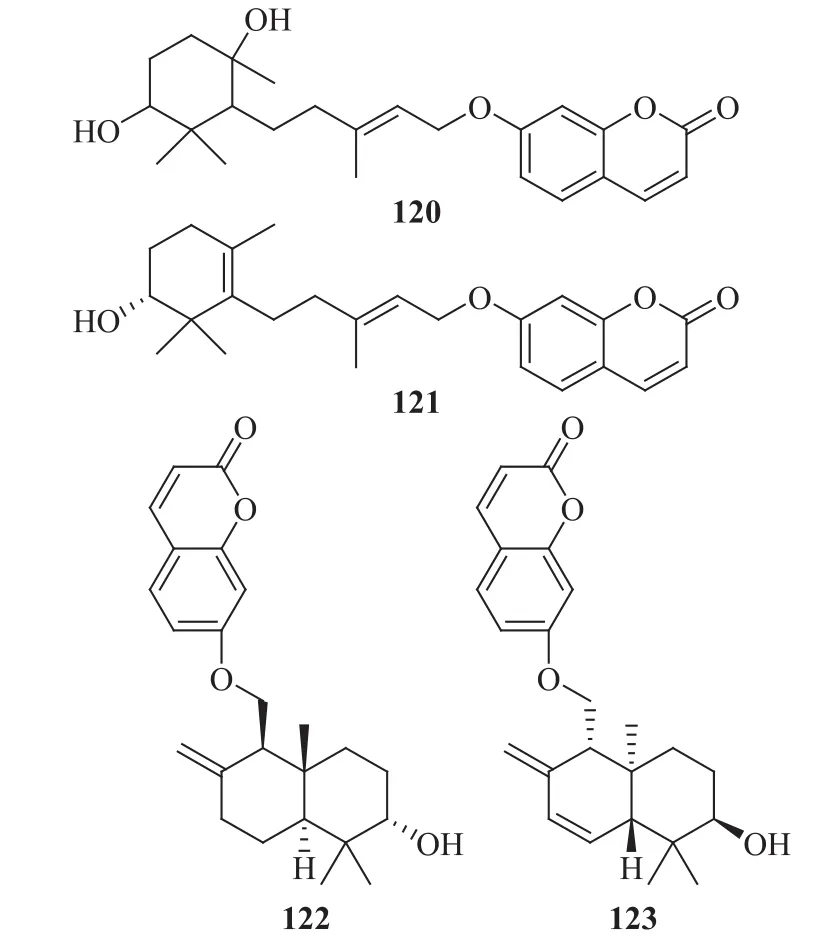
图5 大果阿魏中部分倍半萜-香豆素杂合化合物的化学结构
树脂和基生叶含挥发油:愈创木醇(guaiol),α-蒎烯(α-pinene),β-蒎烯(β-pinene),3-蒈烯(3-carene),反式-罗勒烯(trans-ocimene),茴香醇乙酸酯(fenchyl acetate),龙脑(borneol),(-)-异杜香烯[(-)-isoledene],(-)-姜烯[(-)-zingiberene]等[70]。
大果阿魏的叶含氨基酸类化合物:与根相同[69];含微量元素及重金属元素:Fe、Mn、Zn、K、Na、Ca、Cu、As、Hg[69]。
6 臭阿魏F.teterrima
6.1 产地和功效
臭阿魏产于新疆北部伊犁;亦分布于俄罗斯的西伯利亚西部和克萨克斯坦。臭阿魏为藏药标准(1979年版)收载 “阿魏”的基原植物。药用其树脂。有杀虫、散痞、消积之功效;用于虫积腹痛、腹中痞块、肉食积滞、瘀血癥瘕;阿魏油外用于关节痛。
6.2 化学成分
臭阿魏的根含倍半萜-香豆素杂合化合物:臭阿魏素(feterin,3)[71-72],异臭阿魏素(56)[73],克拉顿芹素(colladonin,84)[72],巴德拉阿魏酮(badrakemone,108),巴德拉阿魏素(badrakemin,122),巴德拉阿魏素乙酸酯(badrakemin acetate,124)[72,74],史特阿魏素(feshurin,125),史特阿魏素乙酸酯(feshurin acetate,126)[72],撒马尔罕阿魏素乙酸酯(samarkandin acetate,127)[74],化学结构见图6;含甾体类化合物:孕甾-4-烯-3,20-二酮(pregn-4-ene-3,20-dione),胡萝卜苷[72]。
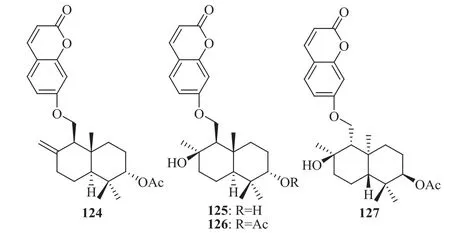
图6 臭阿魏中部分倍半萜-香豆素杂合化合物的化学结构
6.3 毒性
臭阿魏挥发油小鼠灌胃的LD50为491.61mg·kg-1;急性毒性出现呼吸系统、神经系统中毒症状,中毒症状比多伞阿魏挥发油重[75]。
7 托里阿魏F.krylovii
7.1 产地和功效
托里阿魏产于新疆托里;亦分布于中亚和俄罗斯西伯利亚地区。托里阿魏的树脂在新疆地区亦作“阿魏”药用。药用其树脂。有杀虫、散痞、消积之功效;用于虫积、肉积、食积、脘腹冷痛、痞积肿块、胸胁胀满、胆经湿热。
7.2 化学成分
托里阿魏的根含倍半萜-香豆素杂合化合物:托里阿魏诺醇(62)[76],托里阿魏素(69)[77-78],托里阿魏诺醇乙酸酯(fekrynol acetate,128)[76],羽脉阿魏醇(camolol;kamolol,129),羽脉阿魏酮(camolone; kamolone, 130)[77], 托 里 阿 魏 醇 (fekrol,131)[79],化学结构见图 7。
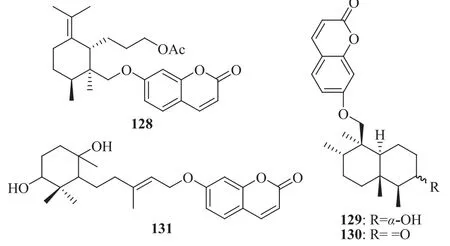
图7 托里阿魏中部分倍半萜-香豆素杂合化合物的化学结构
8 硬阿魏F.bungeana
8.1 产地和功效
硬阿魏产于东北、华北以及甘肃、河南、宁夏、陕西。药用全草和根。带根全草称 “砂茴香”,种子称 “砂茴香子”,内蒙古地区药用。带根全草有清热解毒、祛痰、消肿止痛、祛风除湿之功效;用于感冒、发热、头痛、气管炎、咳嗽、喘息、胸闷、骨痨、瘰疬、乳蛾、胸胁痛、脓疮。种子有理气健胃之功效;用于脘腹胀痛、消化不良、急慢性肠炎。
8.2 化学成分
迄今无化学成分研究报道。
9 准噶尔阿魏F.songarica
9.1 产地和功效
准噶尔阿魏产于新疆北部阿勒泰、塔城,亦分布于俄罗斯西伯利亚西部和克萨克斯坦。药用树脂和全草。其树脂在新疆地区也作 “阿魏”药用。树脂有消积、散痞、杀虫之功效;全株有消积杀虫之功效;用于虫积、肉积、腹部肿块、肝脾肿大、脘腹冷痛;配膏药外治关节疼痛。
9.2 化学成分
准噶尔阿魏根含酚类化合物:2,4-二羟基苯乙酮(2,4-dihydroxylacetophenone),2,4-二羟基-α-氧代-苯乙酸(2,4-dihydroxy-α-oxo-phenylacetic acid)[80];含有机酸类化合物:3,3′,4,4′-二苯基四羧酸(3,3′,4,4′-biphenyltetracarboxylic acid)[80];含 挥 发 油:Δ3-蒈烯(Δ3-carene)等[81],1,2,3,4,5,6-六氢白杨烯(1,2,3,4,5,6-hexahydrochrysene),1,4-二甲基-2,5-二异丙基苯(1,4-dimethyl-2,5-diisopropylbenzene),1,5,7-三甲基四氢化萘(1,5,7-trimethyltetralin),2,4-二甲基-2-癸烯(2,4-dimethyl-2-decene),樟烯(camphene),2-甲氧基苯酚(2-methoxy-phenol),马兜铃烯 (aristolene),香树烯(aromadendrene),香柠檬烯(bergapten),龙脑乙酸酯(bornyl acetate),巴尔兰定(berlandin),菖蒲烯(calamenene),水菖蒲烯(calarene),葛缕子酚(carvacrol),丁香三 环 烯 (clovene),姜 黄烯 (curcumene),邻苯二甲酸二丁酯(dibutylphthalate),依杜兰 I(edulan I),二十一烷(heneicosane),二十七烷(heptacosane),二十六烷(hexacosane),十六酸(hexadecanoic acid),香堇烯(ionene),异松蒎醇(isopinocampheol),柠 檬 烯 (limonene),月 桂 烯(myrcene),正辛基环己烷(n-octylcyclohexane),降蒎酮(nopinone),二十八烷(octacosane),对孜然芹烃(p-cymene),对薄荷-1,5,8-三烯(p-mentha-1,5,8-triene),对正丙基苯酚(p-n-propylphenol),过氢金合欢烯丙酮(perhydrofarnesyl aceton),植醇(phytol),二十四烷(tetracosane),麝香草酚(thymol),香荚兰酸(vanillic acid),α-蒎烯(α-pinene),α-芹子烯(α-selinene),β-杜松烯(β-cadinene),β-雪松烯(β-cedrene),β-环柠檬醛(β-cyclocitral),β-金合欢烯(β-farnesene),β-愈创木烯(β-guaiene),β-蒎烯(β-pinene),δ-芹子烯(δ-selinene),β-松油醇(βterpineol),δ-杜松烯(δ-cadinene)[82]。
10 麝香阿魏F.moschata
10.1 产地和功效
麝香阿魏产于新疆昭苏;亦分布于吉尔吉斯坦、塔吉克斯坦。药用其根,有镇静、解痉之功效;用于治疗癔病等。
10.2 化学成分
麝香阿魏的根含倍半萜-香豆素杂合化合物:臭阿魏醇(2)[83],圆锥茎阿魏醇(10)[84],圆锥茎阿魏酮(18)[83,85],麝香阿根醇(sumferin,132)[85],麝香阿魏醇(moschatol,133)[85-86];含香豆素类化合物:麝香阿魏素(fesumtuorin)A(134)、B(135)、C(136)、D(137)、E(138)、F(139)、G(140)、H(141),白亮独活素 E(candibirin E,142),心叶棱子芹素 D(rivulobin D,143),甲氧基欧芹酚(osthol,144),橙皮油内酯烯醇(auraptenol,145),水合橙皮内酯(meranzin hydrate,146),水合羟基前胡素(oxypeucedanin hydrate,147),羟基前胡素(oxypeucedanin,148),羟基前胡素甲醚(oxypeucedanin methnolate,149),阿魏栓翅芹内酯醇(pranferol,150),栓翅芹烯醇(pabulenol,151),白芷属脑(heraclenol,152),独活素(heraclenin,153),白芷属脑-3′-甲醚(heraclenol-3′-methyl ester,154),欧前胡素(imperatorin,155),花椒毒酚(xanthoxol,156),花椒毒素(xanthotoxin,157)[83]。化学结构见图8。
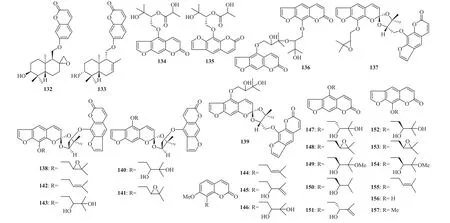
图8 麝香阿魏中部分化合物的化学结构
10.3 生物学活性
化合物144、147、148、149、152、153和155对人类免疫缺陷病毒在H9淋巴细胞的复制具有抑制作用,IC50值(mg·mL-1)分别为 11.7、21.1、23.4、>100、 >100、20.1、 >100;EC50值(mg·mL-1)分别为 0.155、10、1.05、33.3、0.115、2.37、 <0.10;治疗指数(TI)分别为 75.5、2.11、22.2、3.00、870、8.48、 >1000[83]。
10.3.2 细胞因子(cytokine)释放抑制作用 化合物137、144、147、148、149、152、153、154和155对LPS刺激的人外周单核细胞释放肿瘤坏死因子α(TNF-α)的抑制率分别为61.3%、85.4%、80.1%、81.3%、83.9%、80.8%、83.9%、79.4%和63.1%;对释放白细胞介素(IL)-4的抑制率分别为42.8%、50.7%、34.4%、41.8%、38.6%、42.1%、47.3%、42.1%和 42.8%[83]。
11 橄绿阿魏F.olivacea,Peucedanum olivaceum
11.1 产地和功效
橄绿阿魏产于云南丽江。药用其根,有祛痰止咳、散寒发表、降气之功效。
11.2 化学成分
迄今无化学成分研究报道。
12 多伞阿魏F.feruloides,Peucedanum feruloides
12.1 产地和功效
多伞阿魏产于新疆北部,沿准噶尔盆地边缘普遍分布;亦分布于哈萨克斯坦、吉尔吉斯坦、乌兹别克斯坦、俄罗斯西伯利亚地区和蒙古。药用其根及树脂,树脂有健胃消积、散寒止痛之功效;用于食积、消化不良、心腹冷痛、肠胃炎、风湿关节炎。
12.2 化学成分
多伞阿魏的根含倍半萜-香豆素杂合化合物:巴德拉阿魏素(122),巴德拉阿魏素乙酸酯(124),圆锥茎阿魏醇乙酸酯(conferol acetate,158)[87],多伞阿魏 素 (ferulin) A (159)、B (160)[88-89]、C(161)[88],2,3-二氢-7-羟基-2S*,3R*-二甲基-2-[4,8-二甲基-3(E),7-壬二烯基]-呋喃并 [3,2-c]香豆素 {2,3-dihydro-7-hydroxy-2S*,3R*-dimethyl-2-[4,8-dimethyl-3(E),7-nonadienyl]-furo[3,2-c]coumarin,162}[88-90],2,3-二氢-7-羟基-2R*,3R*-二甲基-2-[4,8-二甲基-3(E),7-壬二烯基]-呋喃并 [3,2-c]香豆素 {2,3-dihydro-7-hydroxy-2R*,3R*-dimethyl-2-[4,8-dimethyl-3(E),7-nonadienyl]-furo[3,2-c]coumarin,163},2,3-二氢-7-羟基-2S*,3R*-二甲基-2-[4-甲基-5-(4-甲基-2-呋喃基)-3(E)-戊烯基]-呋喃并 [3,2-c]香豆素 {2,3-dihydro-7-hydroxy-2S*,3R*-dimethyl-2-[4-methyl-5-(4-methyl-2-furyl)-3(E)-pentenyl]-furo[3,2-c]coumarin,164},2,3-二氢-7-羟基-2R*,3R*-二甲基-2-[4-甲基-5-(4-甲基-2-呋喃基)-3(E)-戊烯基]-呋喃并 [3,2-c]香豆素 {2,3-dihydro-7-hydroxy-2R*,3R*-dimethyl-2-[4-methyl-5-(4-methyl-2-furyl)-3(E)-pentenyl]-furo[3,2-c]coumarin,165}[88,90],2,3-二氢-7-甲氧基-2S*,3R*-二甲基-2-[4,8-二甲基-3(E),7-壬二烯基]-呋喃并 [3,2-c]香豆素 {2,3-dihydro-7-methoxy-2S*,3R*-dimethyl-2-[4,8-dimethyl-3(E),7-nonadienyl]-furo[3,2-c] coumarin,166},2,3-二 氢-7-甲 氧 基-2R*,3R*-二甲基-2-[4,8-二甲基-3(E),7-壬二烯基]-呋喃并 [3,2-c]香豆素 {2,3-dihydro-7-methoxy-2R*,3R*-dimethyl-2-[4,8-dimethyl-3(E),7-nonadienyl]-furo[3,2-c]coumarin,167}[88-90],2,3-二氢-7-羟基-2S*,3R*-二甲基-3-[4,8-二甲基-3(E),7-壬二烯基]-呋喃并 [3,2-c]香豆素{2,3-dihydro-7-hydroxy-2S*,3R*-dimethyl-3-[4,8-dimethyl-3(E),7-nonadienyl]-furo[3,2-c]coumarin,168},2,3-二氢-7-羟基-2R*,3R*-二甲基-3-[4,8-二甲基-3(E),7-壬二烯基]-呋喃并 [3,2-c]香豆素 {2,3-dihydro-7-hydroxy-2R*, 3R*-dimethyl-3-[4,8-dimethyl-3(E),7-nonadienyl]-furo[3,2-c] coumarin,169}[88,91],4,7-二羟基-3-[3,7,11-三甲基-2(E),6(E),10-十二碳三烯基]香豆素 {4,7-dihydroxy-3-[3,7,11-trimethyl-2(E),6(E),10-dodecatrienyl] coumarin,170}[88],2,3-二 氢-7-羟 基-2S*,3R*-二 甲 基-2-[4,8-二甲基-3(E),7-壬二烯-6-酮基]-呋喃并[3,2-c]香 豆 素 {2,3-dihydro-7-hydroxy-2S*,3R*-dimethyl-2-[4,8-dimethyl-3(E),7-nonadien-6-onyl]-furo[3,2-c]coumarin,171},2,3-二氢-7-甲氧基)-2S*,3R*-二 甲 基-2-[4,8-二甲 基-3(E),7-壬二烯基-6-酮基]-呋喃并 [3,2-c]香豆素 {2,3-dihydro-7-methoxy-2S*,3R*-dimethyl-2-[4,8-dimethyl-3(E),7-nonadien-6-onyl]-furo[3,2-c]coumarin,172},2,3-二氢-7-甲 氧基)-2S*,3R*-二甲基-2-[4-甲基-5-(4-甲基-2-呋喃基)-3(E)-戊烯基]-呋喃并 [3,2-c]香豆素 {2,3-dihydro-7-methoxy-2S*, 3R*-dimethyl-2-[4-methyl-5-(4-methyl-2-furyl)-3(E)-pentenyl]-furo[3,2-c]coumarin,173}[90],2,3-二氢-7-羟基-2S*,3R*-二甲基-3-[4-甲 基-5-(4-甲 基-2-呋 喃 基)-3(E)-戊 烯基]-呋喃并 [3,2-c]香豆素 {2,3-dihydro-7-hydroxy-2S*,3R*-dimethyl-3-[4-methyl-5-(4-methyl-2-furyl)-3(E)-pentenyl]-furo[3,2-c]coumarin,174}[91],2,3-二氢-7-甲氧基-2S*,3R*-二甲基-3-[4,8-二甲基-3(E),7-壬二烯基]-呋喃并 [3,2-c]香豆素 {2,3-dihydro-7-methoxy-2S*,3R*-dimethyl-3-[4,8-dimethyl-3(E),7-nonadienyl]-furo[3,2-c] coumarin,175}[89,91],2,3-二氢-7-甲氧基-2R*,3R*-二甲基-3-[4,8-二甲基-3(E),7-壬二烯基]-呋喃并 [3,2-c]香豆素 {2,3-dihydro-7-methoxy-2R*,3R*-dimethyl-3-[4,8-dimethyl-3(E),7-nonadienyl]-furo[3,2-c] coumarin,176},2,3-二氢-7-羟基-2R*,3S*-二甲基-2-[8-羟基-4,8-二甲基-3(E)-壬烯-1-基]-呋喃并 [3,2-c]香豆素{2,3-dihydro-7-hydroxy-2R*,3S*-dimethyl-2-[8-hydroxy-4,8-dimethyl-3(E)-nonen-1-yl]-furo[3,2-c] coumarin,177},2,3-二 氢-7-甲 氧 基-2R*,3S*-二甲基-2-[8-羟基-4,8-二甲基-3(E)-壬烯-1-基]-呋喃并 [3,2-c]香豆素 {2,3-dihydro-7-methoxy-2R*,3S*-dimethyl-2-[8-hydroxy-4,8-dimethyl-3(E)-nonen-1-yl]-furo[3,2-c] coumarin,178}[89],化学结构见图 9。
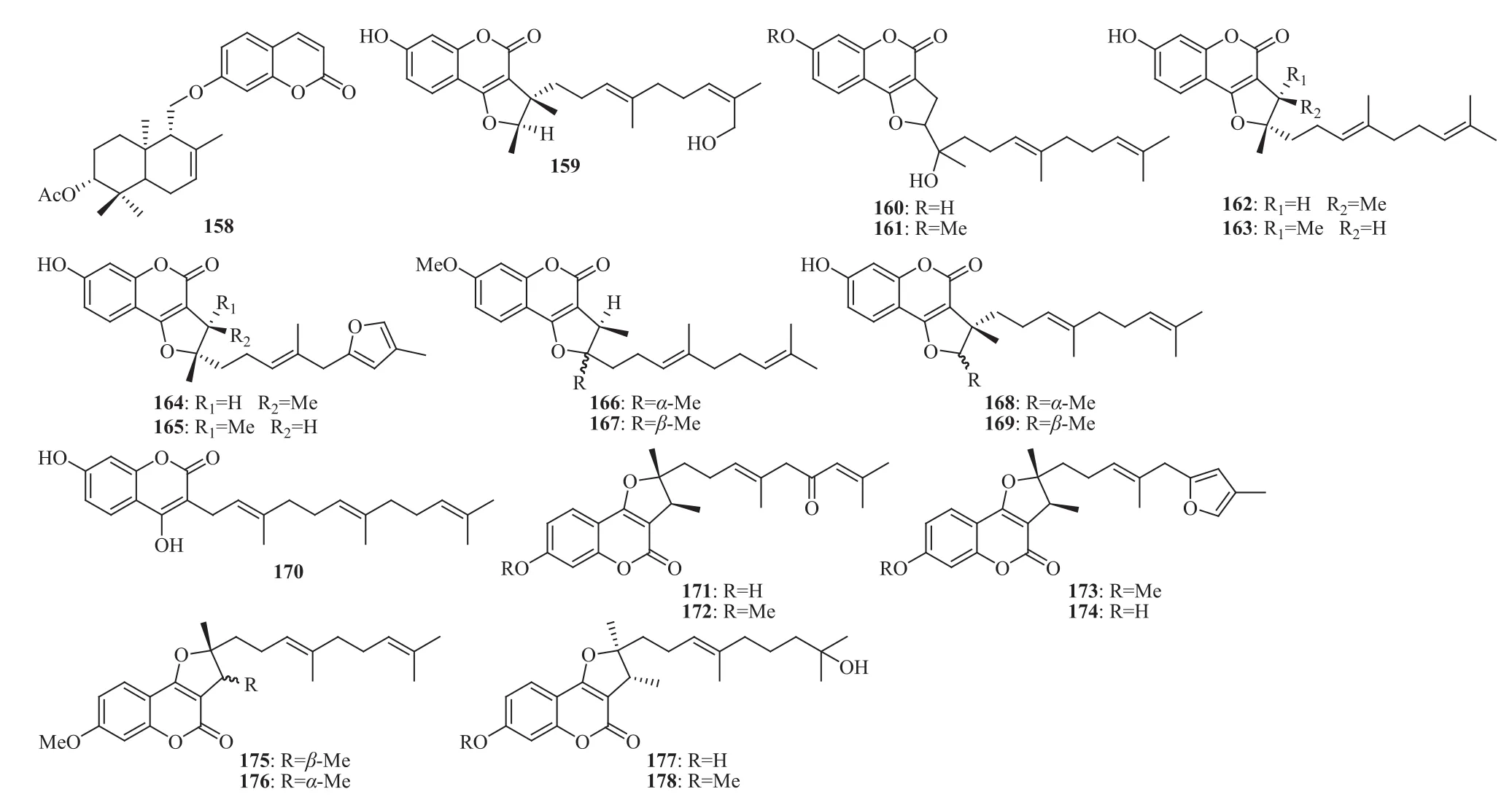
图9 多伞阿魏中部分倍半萜-香豆素杂合化合物的化学结构
多伞阿魏的根含倍半萜-色酮杂合化合物:多伞阿魏素(ferulin)D(179)、E(180),2,3-二氢-7-羟基-2S*,3R*-二甲基-2-[4,8-二甲基-3(E),7-壬二烯基]-呋喃并 [3,2-b]色酮 {2,3-dihydro-7-hydroxy-2S*, 3R*-dimethyl-2-[4, 8-dimethyl-3(E),7-nonadienyl]-furo [3,2-b] chromone,181},2,3-二氢-7-羟基-2R*,3R*-二甲基-2-[4,8-二甲基-3(E),7-壬二烯基]-呋喃并 [3,2-b]色酮 {2,3-dihydro-7-hydroxy-2R*,3R*-dimethyl-2-[4,8-dimethyl-3(E),7-nonadienyl]-furo[3,2-b]chromone,182}[88],2,3-二氢-7-羟基-2S*,3R*-二甲基-2-[4,8-二甲基-3(E),7-壬二烯基]-呋喃并 [2,3-b]色酮 {2,3-dihydro-7-hydroxy-2S*,3R*-dimethyl-2-[4,8-dimethyl-3(E),7-nonadienyl]-furo[2,3-b]chromone,183},2,3-二氢-7-羟基-2S*,3R*-二甲基-2-[4-甲基-5-(4-甲基-2-呋喃基)-3(E),7-戊烯基]-呋喃并 [2,3-b]色酮{2,3-dihydro-7-hydroxy-2S*,3R*-dimethyl-2-[4-methyl-5-(4-methyl-2-furyl)-3(E),7-pentenyl]-furo[2,3-b]chromone,184},2,3-二氢-7-羟基-2R*,3R*-二甲基-2-[4-甲基-5-(4-甲基-2-呋喃基)-3(E),7-戊烯基]-呋喃并 [2,3-b]色酮 {2,3-dihydro-7-hydroxyl-2R*, 3R*-dimethyl-2-[4-methyl-5-(4-methyl-2-furyl)-3(E),7-pentenyl]-furo[2,3-b]chromone,185}[92];含倍半萜-酚性基团杂合化合物:沙 生 阿 魏 酮 (dshamirone,secoammoresinol,186),(4E,8E)-1-(2-羟基-4-甲氧基苯基)-5,9,13-三甲基十四碳-4,8,12-三烯-1-酮 [(4E,8E)-1-(2-hydroxy-4-methoxyphenyl)-5,9,13-trimethyltetradeca-4,8,12-trien-1-one,187],(4E,8E)-1-(2,4-二羟基苯基)-2-羟基-5,9,13-三甲基十四碳-4,8,12-三烯-1-酮 [(4E,8E)-1-(2,4-dihydroxyphenyl)-2-hydroxy-5,9,13-trimethyltetradeca-4,8,12-trien-1-one,188][89],1-(2,4-二羟基苯基)-3,7,11-三甲基-3-乙烯基十二碳-6(E),10-二烯-1-酮[1-(2, 4-dihydroxyphenyl)-3, 7, 11-trimethyl-3-vinyldodeca-6(E),10-dien-1-one,189][89,93],8,9-氧代异丙基沙生阿魏酮(8,9-oxoisopropanyldshamirone,190),多伞阿魏呋内酯A(ferulaeolactone A,191),8,9-二羟基沙生阿魏酮(8,9-dihydroxydshamirone,192)[89,94],8-乙酰氧基-9-羟基沙生阿魏酮(8-acetoxy-9-hydroxydshmirone,193),8-乙酰氧基-9-羟基-4′-甲氧基沙生阿魏酮(8-acetoxy-9-hydroxy-4′-methoxydshmirone,194)[89],3S*-(2,4-二羟基苯甲 酰 基)-4R*,5R*-二 甲 基-5-(4,8-二 甲 基-3(E),7(E)-壬二烯-1-基)-四氢-2-呋喃酮 [3S*-(2,4-dihydroxybenzoyl)-4R*, 5R*-dimethyl-5-(4, 8-dimethyl-3(E),7(E)-nonadien-1-yl)-tetrahydro-2-furanone,195][89,95],(3S,4R,5S)-相对-3-(2,4-二羟基苯甲酰基)-二氢-5-[(3E)-8-羟基-4,8-二甲基-3-壬烯-1-基]-4,5-二 甲 基-2(3H)-呋 喃 酮[(3S, 4R, 5S)-rel-3-(2, 4-dihydroxybenzoyl)-dihydro-5-[(3E)-8-hydroxy-4,8-dimethyl-3-nonen-1-yl]-4,5-dimethyl-2(3H)-furanone,196],(4E,8R)-相对-(-)-8-乙酰氧基-1-(2,4-二羟基苯基)-5-甲基-8-[(2R,5S)-四氢-5-(1-羟基-1-甲基乙基)-2-甲基-2-呋喃基]-4-辛烯-1-酮 [(4E,8R)-rel-(-)-8-acetyloxy-1-(2,4-dihydroxyphenyl)-5-methyl-8-[(2R,5S)-tetrahydro-5-(1-hydroxy-1-methylethyl)-2-methyl-2-furanyl]-4-octen-1-one,197],(4E,8R)-相 对-(-)-8-乙酰氧基-1-(2,4-二羟基苯基)-5-甲基-8-[(2R,5R)-四氢-5-(1-羟基-1-甲基乙基)-2-甲基-2-呋喃 基]-4-辛 烯-1-酮 [(4E,8R)-rel-(-)-8-acetyloxy-1-(2,4-dihydroxyphenyl)-5-methyl-8-[(2R,5R)-tetrahydro-5-(1-hydroxy-1-methylethyl)-2-methyl-2-furanyl]-4-octen-1-one,198][89],1-(2,4-二羟基苯基)-2-羟基-5,9,13-三甲基-4(E),8(E),12-十四碳三烯-1-酮 [1-(2,4-dihydroxyphenyl)-2-hydroxy-5,9,13-trimethyl-4(E),8(E),12-tetradecatrien-1-one,199],1-(2,4-二羟基苯基)-3,7,11-三甲基-3-乙烯基-6(E),10-十二碳二烯-1,9-二酮 [1-(2,4-dihydroxyphenyl)-3,7,11-trimethyl-3-vinyl-6(E),10-dodecadiene-1,9-dione,200],1-(2,4-二羟基苯基)-3,7-二甲基-3-乙烯基-8-(4-甲基-2-呋喃基)-6(E)-辛烯-1-酮 [1-(2,4-dihydroxyphenyl)-3,7-dimethyl-3-vinyl-8-(4-methyl-2-furyl)-6(E)-octen-1-one,201][93],3S*-(2,4-二羟基苯甲酰基)-4R*,5R*-二甲基-5-[4-甲基-5-(4-甲基-2-呋喃基)-3(E)-戊烯-1-基]-四氢-2-呋喃酮 [3S*-(2,4-dihydroxybenzoyl)-4R*,5R*-dimethyl-5-[4-methyl-5-(4-methyl-2-furyl)-3(E)-penten-1-yl] tetrahydro-2-furanone,202],3S*-(2,4-二羟基苯甲酰基)-4R*,5S*-二甲基-5-[4-甲基-5-(4-甲基-2-呋喃基)-3(E)-戊 烯-1-基]-四氢-2-呋喃酮 [3S*-(2,4-dihydroxybenzoyl)-4R*,5S*-dimethyl-5-[4-methyl-5-(4-methyl-2-furyl)-3(E)-penten-1-yl]-tetrahydro-2-furanone,203][95],2,6-二羟基-2-[3,7,11-三甲基-2(E),6(E),10-十二碳三烯-1-基]-3(2H)-苯并呋喃酮 {2,6-dihydroxy-2-[3,7,11-trimethyl-2(E),6(E),10-dodecatrien-1-y l]-3(2H)-benzofuranone,204}[96],多伞阿魏酚酮(ferulaeone)A(205)、B(206)、C(207)、D(208)、E(209)、F(210)、G(211)、H(212),3-(2,4-二羟基苯甲酰基)-4S*,5R*-二甲基-5-[4,8-二甲基-3(E),7(E)-壬二烯-1-基]-四氢-2-呋喃酮 {3-(2,4-dihydroxybenzoyl)-4S*,5R*-dimethyl-5-[4,8-dimethyl-3(E),7(E)-nonadien-1-yl]-tetrahydro-2-furanone,213},3-(2-羟基-4-甲氧基苯甲酰基)-4S*,5R*-二甲基-5-[4,8-二甲基-3(E),7(E)-壬二烯-1-基]-四氢-2-呋喃酮 {3-(2-hydroxyl-4-methoxybenzoyl)-4S*,5R*-dimethyl-5-[4,8-dimethyl-3(E),7(E)-nonadien-1-yl]-tetrahydro-2-furanone,214}[97],多伞阿魏内酯(ferulactone)A(215)、B(216)[98],化学结构见图10;含倍半萜类化合物:橙花叔醇(nerolidol)[93,99],愈创木醇(guaiol)[93,99-100];含苯丙素类化合物:肉豆蔻醚(myristicin)[93];含酚、酚酸类化合物:2,4-二羟基苯乙酮(2,4-dihydroxyacetophenone),2-羟基-4-甲氧基苯乙酮(2-hydroxy-4-methoxyacetophenone),2,4-二羟基苯甲酸(2,4-dihydroxybenzoic acid),2,4-二羟基-α-氧代苯乙酸(2,4-dihydroxy-α-oxobenzeneacetic acid)[89],β-树脂苔黑酸(β-resorcylic acid),甲氧基树脂苔黑酸(methoxyresorcylic acid)[100];含甾体类化合物:β-谷甾醇[100];含挥发油:从对胃癌细胞SGC-7901株增殖有抑制活性的多伞阿魏三氯甲烷提取部位中鉴定出3-甲氧基-1,2丙二醇(3-methoxy-1,2-propanediol),右旋柠檬烯(D-limonene),左旋乙酸龙脑酯(L-borneol acetate),乙酸松油酯(terpinyl acetate),2,6,10-三甲基-1,5,9-十一烷三烯(2,6,10-trimethyl-1,5,9-undecatriene),α-雪松烯(α-cedrene),α-香柑油烯(α-bergsmotene),β-雪松烯(β-cedrene),8-表-γ-桉叶油醇(8-epi-γ-eudesmol),γ-桉叶油醇(γeudesmol),茅苍术醇(hinesol)[101];另含有 1-甲基-4-(1-甲基乙稀基)环己烯 [1-methyl-4-(1-methylethenyl)cyclohexene][102],甲基乙叉(甲基)丙基二硫化物 [methylethylidene(methyl)propyl disulfide][102-103],甲基乙基-1-甲基丙基二硫化物 [methylethyl-1-(methyl)propyl disulfide],二(1-甲基丙基)二硫化物[bis(1-methylpropyl)disulfide],(E)-1-丁烯基-1-(甲基)丙基二硫化物 [(E)-1-butenyl-1-(methyl)propyl disulfide],(Z)-1-丁烯基-1-(甲基)丙基二硫化物[(E)-1-butenyl-1-(methyl)propyl disulfide],(E)-2-丁烯基-1-(甲基)丙基二硫化物 [(E)-1-butenyl-1-(methyl)propyl disulfide],1-(甲硫基)丙基丙烯基二硫化物 [1-(methylthio)propylpropenyl disulfide][103],(-)-α-蒎烯 [(-)-α-pinene],月桂烯(myrcene),香桧烯(sabnene),β-月桂烯(β-myrcene),L-水芹烯(L-phellandrene),δ-3-蒈烯(δ-3-carene),3,7-二甲基-1, 3, 7-辛 三 烯 (3, 7-dimethyl-1, 3, 7-octatriene),γ-萜品烯(γ-terpinene),α-异松油烯(αterpinolene),对伞花烃-8-醇(p-cymen-8-ol),外-乙酸龙脑酯(exo-bornyl acetate),顺式-3-蒎烯-2-醇(Z-3-pinen-2-ol),二氢葛缕乙酸酯 (dihydrocarvyl acetate),橙花叔醇 (nerolidol),(-)-别香树烯[(-)-alloaromadendrene],金合欢烯(farnesene),α-愈创木烯(α-guaiene),反式-石竹烯(trans-caryophyllene),γ-蛇床烯(γ-selinene),喇叭烯(ledene),α-桉叶油醇(α-eudesmol)等[104]。
树脂含有挥发油:β-金合欢烯(β-farnesene),龙脑乙酸酯(bornyl acetate),愈创木醇[105]。
果实含香豆素[106]。
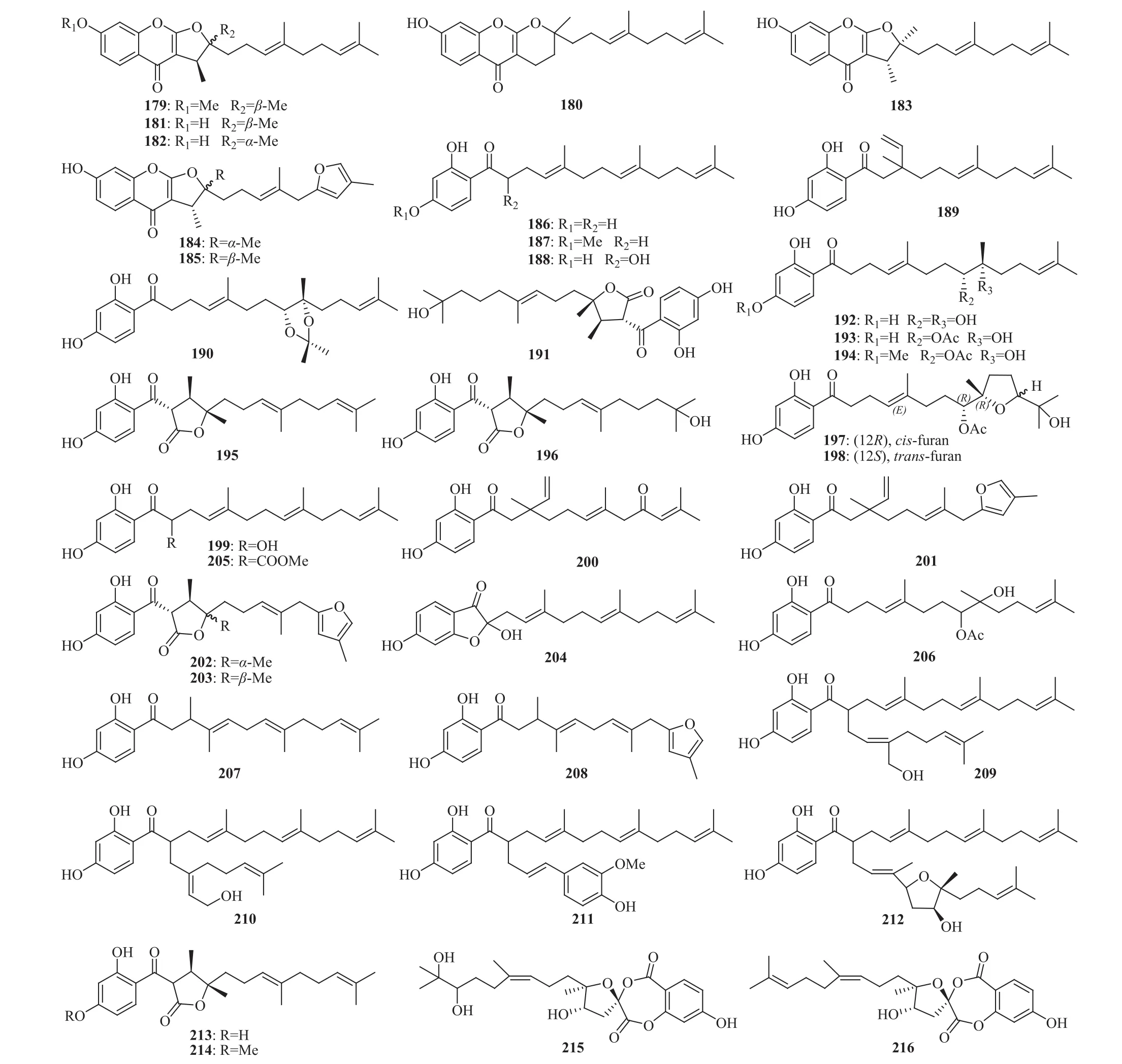
图10 多伞阿魏中部分倍半萜类衍生物的化学结构
12.3 生物学活性
12.3.1 肿瘤细胞毒作用 多伞阿魏不同提取部位在1 mg·mL-1浓度对胃癌SGC-7901细胞株的增殖抑制率,挥发油为78.10%,水提取部位为30.11%,95%乙醇提取部位为75.17%,石油醚提取部位为70.22%,三氯甲烷提取部位为89.17%,乙酸乙酯提取部位为72.12%,其中三氯甲烷提取部位活性最强[101]。采用水蒸气蒸馏法、溶剂回流提取法、超声提取法、微波萃取法、微波-超声协助萃取法、渗漉提取法和超临界CO2萃取法制备多伞阿魏挥发油,其中只有水蒸气蒸馏法和微波萃取法制备的挥发油对胃癌SGC-7901细胞株增殖具有很强的抑制作用[104]。
倍半萜-香豆素杂合化合物 160、161对胃癌HepG2细胞株增殖具有抑制作用,IC50值分别为89.0、76.1μmol·L-1;对脑胶质瘤C6细胞株增殖亦具有抑制作用,IC50值分别为21.2、36.1μmol·L-1;162对MCF-7和C6增殖具有抑制作用,IC50值分别为60.0、20.1μmol·L-1;163对 HepG2、乳腺癌MCF-7细胞株和C6增殖抑制作用的IC50值分别为39.9、37.7、16.0μmol·L-1;168对 HepG2、MCF-7和C6增殖抑制作用的IC50值分别为49.3、66.0、35.3μmol·L-1;169对HepG2、MCF-7和C6增殖抑制作用的 IC50值分别为 53.5、80.4、32.5μmol·L-1[88];163能通过线粒体介导途径和死亡接受器途径诱导C6神经胶质瘤细胞凋亡;引起 PERK、ATF6α和IRE1α活化[107];提示163对脑胶质瘤具有潜在的应用前景。
倍半萜-色酮杂合化合物181对HepG2和C6细胞株增殖抑制作用的 IC50值分别为 74.5、60.0μmol·L-1[88];酚倍半萜衍生物对HepG2、MCF-7和C6细胞株增殖抑制作用,化合物210的IC50值分别为86.0、87.0、64.5μmol·L-1,211的 IC50值分别为 86.9、92.1、59.3μmol·L-1,212的 IC50值分别为 82.1、81.5、66.0μmol·L-1,186、189、199和213对C6细胞株增殖抑制作用的 IC50值分别为34.1、31.0、36.2、55.4μmol·L-1[97]。
12.3.2 抗菌作用 倍半萜-香豆素杂合化合物159、160、162、163、168和 169对四环素耐药菌株XU212生长具有抑制作用,最小抑菌浓度(MIC)分别为 32、16、2、2、2、2 mg·L-1[89];酚倍半萜衍生物 186、187、188、189、190、192、193、195和196对四环素耐药菌株XU212生长具有抑制作用,MIC分别为1、1、1、4、0.5、64、32、2、2 mg·L-1;化合物186、188、189、192、193、195和196对金黄色酿脓葡萄球菌SA1199B生长抑制作用的MIC分别为 16、2、16、64、16、8、8 mg·L-1;化合物186、188、189、192、195和196对金黄色酿脓葡萄球菌ATCC25923生长抑制作用的MIC分别为6、2、16、64、8、8 mg·L-1;化合物 186、188、189、190、192、193、195和 196对红霉素耐药菌株RN4220生长抑制作用的MIC分别为32、2、4、16、64、64、4、16 mg·L-1;化合物 186、188、189、192、193、195、196对金黄色酿脓葡萄球菌EMRSA-15生长抑制作用的MIC分别为16、4、16、64、64、2、2 mg·L-1;化合物 186、188、189、190、192、193、195、196对金黄色酿脓葡萄球菌EMRSA-16生长抑制作用的MIC分别为1、2、32、0.5、64、32、128、16 mg·L-1[89];化合物 191对金黄色酿脓葡萄球菌SA1199B生长抑制作用的MIC为19.1μmol·L-1;化合物 190、191和192对四环素耐药菌株XU212生长抑制作用的MIC分别为1.2、4.8、164.1μmol·L-1;化合物190和191对红霉素耐药菌株RN4220生长抑制作用的MIC分别为37.2、38.3μmol·L-1;化合物191对医院传染性金黄色酿脓葡萄球菌EMRSA-15菌株生长抑制作用的MIC为4.8μmol·L-1;化合物190对医院传染性金黄色酿脓葡萄球菌EMRSA-16菌株生长抑制作用的MIC为1.2μmol·L-1[94]。
12.3.3 抗炎作用 多伞阿魏对大鼠应激性胃溃疡和乙酰水杨酸致药物性胃溃疡有防治作用;在离体肠肌实脸中,能抑制兔肠肌的自发蠕动[108]。体外对接实验结果表明倍半萜-香豆素杂合化合物173对诱导性一氧化氮合成酶活性具有抑制作用[109]。
12.3.4 杀虫作用 倍半萜类的愈创木醇占多伞阿魏根总挥发油的37.0%,在70 mg·L-1对蚜虫有明显的抑制作用,对水稻粘虫Mythimna separata第四龄幼虫和小菜蛾Plutella xylostella第三龄幼虫抑制作用的LD50分别为每只0.07、8.9 mg;水稻粘虫第四龄幼虫和成虫家蝇Musca domestica熏蒸活性的半数致死浓度(LC50)分别为 3.5、16.9μL·L-1[99]。
12.3.5 毒性 多伞阿魏挥发油小鼠灌胃的LD50为10 240 mg·kg-1;急性毒性较小,出现呼吸系统、神经系统中毒症状,但中毒症状比臭阿魏挥发油轻[75]。
13 里海阿魏F.caspica
13.1 产地和功效
里海阿魏产于新疆北部,分布于亚洲中部和西南部、吉尔吉斯坦、乌兹别克斯坦、俄罗斯西伯利亚、蒙古西部。药用其根及树脂。树脂有杀虫、散痞、消积之功效;用于虫积腹痛、腹中痞块、肉食积滞、瘀血癥瘕。
13.2 化学成分
里海阿魏的根含倍半萜-香豆素杂合化合物:伞形戊烯内酯(1)[110],金合欢阿魏醇 A(65)[111]、C(61)[112];含倍半萜类化合物:金合欢醇(farnesyl alcohol)[112];含香豆素类化合物:伞形酮(umbelliferone)[110];含其他类化合物:氨基酸、有机酸[110]、无机元素[113]。
13.3 毒性
里海阿魏的水煎剂和醇溶性提取物对青蛙、小白鼠、家兔、豚鼠或家犬等不是特别有毒;给家犬静脉注射可引起短暂性低血压;对离体青蛙心脏可降低振幅和增加收缩率;基本无驱虫作用。1∶1000水煎剂能引起离体豚鼠子宫强烈收缩,但醇溶性提取物无效[114]。
14 评述
14.1 化学结构多样性
阿魏化学成分种类和结构具有多样性,主要有挥发油、树胶树脂等,在诸多的化学成分中以倍半萜、香豆素和多硫化合物(polysulfanes)等类为主要特征性化学成分。在这些成分中,倍半萜又是最有特征性的化合物,其中以胡萝卜烷(daucane)为基本骨架,一般C-4位有羟基取代,在C-2、C-6、C-10等发生取代或官能团变化衍生出许多不同结构的化合物。最常见的化合物骨架为I,是多数倍半萜类的存在形式。骨架I的双键发生氧化生成环氧化物II,亦是存在较多的化合物类型。取代基变换,双键位置异构或双键氧化,或有醛、酮羰基位置变化形成III~XVI等一系列骨架及其化合物。此外,亦发现少数几个葎草烯(humulene)和桉烷(eudesmane)型萜以及特殊结构的倍半萜酯XVII、XVIII和XIX等。见图11。
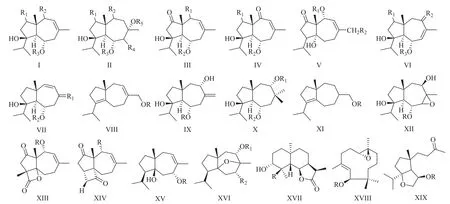
图11 阿魏属植物中倍半萜的结构类型
阿魏属植物中的另一类特征性化学成分为具有香豆素母核结构的化合物,在一些阿魏种中较常见。其中绝大多数香豆素是伞形酮衍生物,少部分是呋喃香豆素衍生物。根据取代基不同,可分为单萜-香豆素杂合物、倍半萜(直链、单环、双环)-香豆素杂合物、以及在含氧环2位上有异戊二烯基取代的香豆素等,其中又以倍半萜-香豆素杂合物数量最多。
在多硫化合物中,从波斯阿魏Ferula persica的根中分离鉴定出波斯阿魏硫化物(persicasulfide)A(3-sec-butyldisulfanylally-acetoxy-3-methylbutyric acid ester,217)、B[3-(1-methylsulfanylpropylsulfanyl)allyl-acetoxy-3-methylbutyric acid ester,218]、C(3-secbutyldisulfanylallyl-hydroxy-3-methylbutyric acid ester,219)[115],化学结构见图12。由此启迪人们这类化合物可能是阿魏有臭味的载体,有待于将来在我国药用阿魏中得到证实。
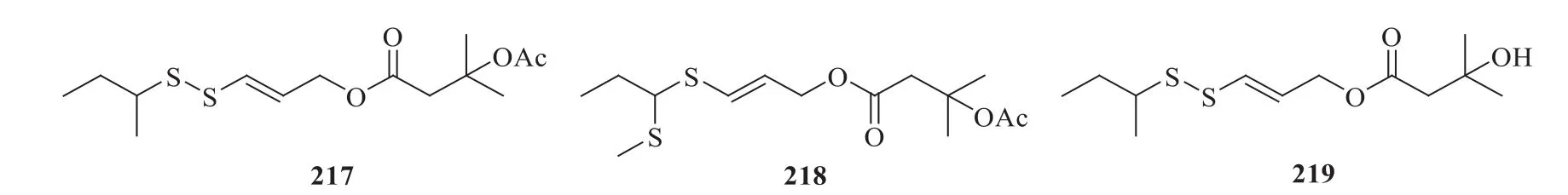
图12 波斯阿魏中多硫化物的化学结构
14.2 化学分类学和药用亲缘学
尽管伞形科植物中广布香豆素类化合物和倍半萜类化合物,但阿魏属植物中广布倍半萜-香豆素杂合物、单萜-香豆素杂合物[116],是该属植物中最具特色的化合物类群,除在上述药用阿魏属植物中发现外,在纳香阿魏 Ferula narthex Bioss的全草[117]、阔裂阿魏 F.latisecta的根[118]、F.hermonis Boiss的根[119]、马兜臭阿魏 F.asa-foetida的树脂[120]、蒙塔阿魏 F.mogoltavica的根[121]、波斯阿魏 F.persica的根[122]和扇裂阿魏 F.flabelliloba的根[123]中亦分离鉴定出倍半萜-香豆素杂合物,不受地域限制,只与物种有关。单萜、倍半萜-香豆素杂合物在自然界中的分布十分狭窄,在阿魏属植物化学分类学上具有特殊的意义。这一化合物类群,应是阿魏属药用植物的药用亲缘学的核心议题。倍半萜-酚性基团杂合物目前仅在中亚阿魏、阜康阿魏、多伞阿魏等中发现,是否具有属内分类特征有待进一步研究。
14.3 生物学活性研究
近年来由于发现阿魏属植物中具有抗炎、抗癌、抗病毒、P-糖蛋白抑制剂和植物雌激素等活性成分,使其受到关注[122]。从阜康阿魏F.fukanensis根中分离得到的倍半萜-色酮(sesquiterpene chromone)杂合物阜康阿魏色酮(fukanefurochromone)A、B、C、D、E,倍半萜-香豆素杂合物(sesquiterpene coumarin)阜康阿魏香豆素(fukanemarin)A、B,阜康阿魏呋喃香豆素(fukanefuromarin)A、B、C、D、E、F、G,倍半萜-酚性基团杂合物如阜康阿魏萜酮(fukanedone)A、B、C、D、E以及阜康阿魏酮酯 A(fukaneketoester A)等在鼠性巨噬细胞样细胞RAW 264.7对脂多糖和重组鼠源γ-干扰素诱导的NO产生和诱导性NO合酶基因表达具有抑制作用,它们可能是阜康阿魏抗炎作用的物质基础,对于与NO过表达相关的疾病的治疗可能具有潜在的应用前景。伞形戊烯内酯(umbelliprenin,1)似乎是阿魏属植物普遍存在的一个倍半萜-香豆素杂合物,是较强的基质金属蛋白酶抑制剂(IC50=14μg·mL-1),而金合欢阿魏醇A(farnesiferol A,65)、多胶阿魏素(gummosin,73)和巴德拉阿魏酮(badrakemone,108)对基质金属蛋白酶抑制活性较弱。金合欢阿魏醇C(farnesiferol C,61)是一个有潜在应用价值的癌症化疗药物先导化合物,具有抗血管生成活性、抑制肿瘤细胞增殖、抑制血管内皮生长因子和基质金属蛋白酶-2活性;在离体和在体模型中,对血管内皮生长因子处理的大鼠主动脉的芽生式血管生成具有抑制作用;按1 mg·kg-1·d-1剂量给药,对移植性小鼠肺癌抑制的有效率可达60%。十分有意义的是,某些倍半萜-香豆素杂合物对 12-O-十四碳酰佛波醇-13-乙酸酯(TPA)所致 Raji细胞 Epstein-Barr病毒早期抗原(EBV-EA)活化具有抑制作用,其 IC50值(nmol·L-1):伞形戊烯内酯为9.1,金合欢阿魏醇A为13.1,巴德拉阿魏酮为13.3,臭阿魏醇(feselol,2)为13,圆锥茎阿魏酮(conferone,18)为14.3,托里阿魏酮(ferukrinone,68)为 13.7,古蓬阿魏酸(galbanic acid,75)为11.8,古蓬阿魏酸甲酯(methyl galbanate,76)为 11.7,蒙塔阿魏素(圆锥茎阿魏醇,mogoltacin,conferol,10)为 12.6,活性较强[122,124]。在抗病毒活性方面,某些倍半萜-香豆素杂合物对甲型流感(influenza A)病毒具有抑制作用,甚至强于金刚烷胺(amantadine,IC50为 0.92μg·mL-1);其 IC50值(μg·mL-1):10′-R-乙酰氧基-11′-羟基伞形戊烯内酯(10′-R-acetoxy-11′-hydroxyumbelliprenin)为 0.94,5′-羟基伞形戊烯内酯(5′-S-hydroxyumbelliprenin)为0.36,8′-乙酰氧基-5′-S-羟基伞形戊烯内酯(8′-acetoxy-5′-S-hydroxyumbelliprenin)为 0.81,蒙塔阿魏素(圆锥茎阿魏醇,10)为0.47,金合欢阿魏醇B(60)为0.51,金合欢阿魏醇C(61)为0.29,古蓬阿魏酸(75)为0.45,古蓬阿魏酸甲酯(76)为 0.26,10′R-卡拉阿魏醇(10′R-karatavicinol,77)为 0.99,表圆锥茎阿魏二酮(epi-conferdione)为 0.32。白根素 C(baigene C,102)和 O-甲基白根素 C(O-methyl baigene C)对 α-糖苷酶活性具有抑制作用[122]。但总的来看,阿魏属药用植物的生物活性研究还不够活跃,缺乏物质基础与药效作用的相关性研究,似乎缺乏供筛选单体化合物研究样品,今后应倡导学科交叉研究,以确定其特异的药效物质基础。
14.4 研制现代中药
单萜-或倍半萜-香豆素杂合物是阿魏属药用植物的独特化学资源,是研制组分现代中药的良好天然素材。
14.5 质量标准
任何一味中药都有其独特的疗效,取决于其特色的物质基础[125-126]。今后要在化学成分和生物活性内容研究成果的基础上,确定质量标准标识物,建立合理、切实可行、科学的质量标准。
[1] Kuliev Z A,Khasanov T Kh,Malikov V M.Ferula conocaula coumarins[J].Khim Prir Soedin,1982,18(1):120-121.
[2] Kuliev Z A,Khasanov T Kh.Structure of kauferin and kauferidin[J].Khim Prir Soedin,1978,14(3):327-331.
[3] Kuliev Z A,Khasanov T Kh,Malikov V M.Terpenoid glycocoumarins of Ferula conocaula[J].Khim Prir Soedin,1979,15(4):477-480.
[4] Vandy shev V V,Perel’son M E,Sklyar Yu E,et al.Conferin,a new coumarin from Ferula conocaula roots[J].Khim Prir Soedin,1974,10(5):660-661
[5] Vandyshev V V,Sklyar Yu E,Perel’son M E,etal.Conferol,a new coumarin from Ferula conocaula and F.moschata roots[J].Khim Prir Soedin,1972,8(5):670-671.
[6] Kuliev Z A,Khasanov T Kh,Malikov V M.Structure and configuration of cauferinin[J].Khim Prir Soedin,1979,15(2):151-154.
[7] Perel’son M E,Vandyshev V V,Sklyar Yu E.Structure and stereochemistry of conferin[J].Khim Prir Soedin,1975,11(2):248-249.
[8] Vandyshev V V,Sklyar Yu E,Perel’son M E,etal.Conferdion,a new coumarin from Ferula conocaula[J].Khim Prir Soedin,1974,10(5):658-659.
[9] Kuliev Z A,Khasanov TKh.Structure of ferocolin,ferocolinin,ferocolidin,and ferocolicin[J].Khim Prir Soedin,1978,14(3):322-327.
[10]Vandyshev V V,Sklyar Yu E,Perel’son M E,etal.Conferone,a new terpenoid coumarin from Ferule conocaula fruits[J].Khim Prir Soedin,1972,8(5):669-670.
[11]Chen X Y,Liu Q X.Luteolin glycosides as taxonomicmarkers in Ferula and related genera[J].Biochem System Ecol,1989,17(4):309-310.
[12]Ryu SY,Lee C O,Choi SU,et al.Anticancer composition comprising sesquiterpenes isolated from Resina Ferulae:US 20040043083[P].2004-03-04.
[13]泽仁班鸠.一种治疗流行性传染病的药物组合物及其制备方法:200410021998X[P].2005-09-14.
[14]Sriraman M C,Nagasampagi BA,Pandey R C,etal.Sesquiterpenes.XLIX.Sesquiterpenes from Ferula jaeschkeana.1.Jaeschkeanadiol,structure and stereochemistry[J].Tetrahedron,1973,29(7):985-991.
[15]Garg SN,Misra L N,Agarwal SK,et al.Carotane derivatives from Ferula jaeschkeana[J].Phytochemistry,1987,26(2):449-450.
[16]Garg S N,Agarwal S K,Mahajan V P,et al.Feruginidin and ferugin,two new sesquiterpenoids based on the carotane skeleton from Ferula jaeschkeana[J].JNat Prod,1987,50(2):253-255.
[17]Garg S N,Agarwal S K.New sesquiterpenes from Ferula jaeschkeana[J].Planta Med,1987,53(4):341-342.
[18]Garg S N,Agarwal S K.Further new sesquiterpenes from Ferula jaeschkeana[J].JNat Prod,1988,51(4):771-774.
[19]Razdan T K,Qadri B,QurishiM A,et al.Sesquiterpene esters and sesquiterpene-coumarin ethers from Ferula jaeskeana[J].Phytochemistry,1989,28(12):3389-3393.
[20]Garg SN,Vishwapaul,Rastogi S N.Isocarotane and carotane derivatives from Ferula jaeschkeana[J].Phytochemistry,1990,29(2):531-533.
[21]Garg SN,Agarwal SK,Fidelis K,et al.New jaeschkeanadiol derivatives from Ferula jaeschkeana[J].JNat Prod,1993,56(4):539-544.
[22]Garg S N,Agarwal S.New carotane sesquiterpenes from Ferula jaeschkeana[J].JMed Arom Plant Sci,1996,18(1):7-9.
[23]Garg S N,Gupta M M,Kumar S.Isocarotane esters from Ferula jaeschkeana[J].J Indian Chem Soc,1998,75(9):536-537.
[24]Bizhanova K B,Saidkhodzhaev A I,Malikov V M.Structure of jaeschferin[J].Khim Prir Soedin,1980,16(1):127-128.
[25]Singh M M,Gupta D N,Wadhwa V,et al.Contraceptive efficacy and hormonal profile of ferujol:a new coumarin from Ferula jaeschkeana[J].Planta Med,1985,(3):268-270.
[26]Garg SN,Agarwal SK.Newmonoterpene diols from essential oil of Ferula jaeschkeana[J].Phytochemistry,1988,27(3):936-937.
[27]Garg SN,Misra LN,Agarwal SK.Essential oil from rhizomes of Ferula jaeschkeana[J].Phytochemistry,1989,28(2):634-636.
[28]Goryaev M I,Tikhonova L K,Dembitskii A D,et al.Essential oil composition.XXIII.Essential oil hydrocarbons from Ferula jaeschkeana stems[J].Izvest Akad Nauk Kazakh SSR,Ser Khim,1967,17(3):80-84.
[29]Bersutskii V P.Chemical investigation of the fruits of Ferula jaeschkeana Vatke[J].Bull Univ Asie centrale,1938,22:119-124.
[30]Khalilova E K,Saidkhodzhaev A I.Sesquiterpenoid esters of Ferula jaeschkeana[J].Chem Nat Compd,1998,34(4):516.
[31]Tiwana S J,Saleem M,Ahmad M,et al.Lipid composition of Ferula jaeschkeana-presence of an odd fatty acid[J].Pakistan JSci Ind Res,1988,31(9):626-628.
[32]Ahmad M,Maqbool JR,Sabir A W,et al.Studies on the essential oils of the Pakistani species of the family Umbelliferae.Part LIV.Ferula jaeschkeana seeds and stalk oil[J].Pakistan JSci Ind Res,1987,30(9):667-668.
[33]Prakash A O,Pathak S,Mathur R.Postcoital contraceptive action in rats ofa hexane extractof the aerial parts of Ferula jaeschkeana[J].J Ethnopharmacol,1991,34(2/3):221-234.
[34]Prakash A O,Jonathan S.Effectof hexane extractof Ferula jaeschkeana on the reproductive organs in cyclic female rats[J].Philippine JSci,1996,125(2):129-146.
[35]Pathak S,Prakash A O.Effect of hexane extract of ferula jaeschkeana on the uterus of adult ovariectomised rats[J].Ancient Sci life,1992,12(1-2):231-241.
[36]Pathak S,Jonathan S,Prakash A O.Timely administration of extractof Ferula jaeschkeana causes luteolysis in the ovary of cyclic guineapig[J].Indian J Physiol Pharmacol,1995,39(4):395-399.
[37]Singh M M,Agnihotri A,Garg SN,et al.Antifertility and hormonal properties of certain carotane sesquiterpenes of Ferula jaeschkeana[J].Planta Med,1988,54(6):492-494.
[38]Yang JR,An Z,Li ZH,et al.Sesquiterpene coumarins from the roots of Ferula sinkiangensis and Ferula teterrima[J].Chem Pharm Bull,2006,54(11):1595-1598.
[39]杨俊荣,敬松,李志宏,等.新疆阿魏化学成分研究[J],中国中药杂志,2007,32(22):2382-2384.
[40]Xing Y C,Li N,Zhou D,et al.Sesquiterpene coumarins from Ferula sinkiangensis act as neuroinflammation inhibitors[J].Planta Med,2017,83(1/2):135-142.
[41]Teng L,Ma G Z,Li L,et al.Karatavicinol a,a new anti-ulcer sesquiterpene coumarin from Ferula sinkiangensis[J].Chem Nat Compd,2013,49(4):606-609.
[42]邢亚超,汤迎湛,潘英,等.新疆阿魏树脂的化学成分研究[J].现代药物与临床,2013,28(1):11-13.
[43]邓卫萍,解成喜,符继红,等.新疆阿魏挥发油成分气相色谱-质谱分析[J].质谱学报,2007,28(2):114-116.
[44]郭亭亭,姜林,卢军,等.新疆阿魏及其不同炮制品挥发油成分 GC-MS分析 [J].中成药,2014,36(7):1551-1553.
[45]戴斌,丘翠嫦.中国传统药物阿魏挥发油成分的气相色谱-质谱分析比较[J].药物分析杂志,1992,12(5):285-288.
[46]Min ZD,MaiQ F,Mizuno M,etal.Polysulfanes in the volatile oils of Ferula species[J].Planta Med,1987,53(3):300-302.
[47]Ye B G,Wang S,Zhang L.Studies on the detoxification effects and acute toxicity of amixture of cis-sec-butyl-1-propoenyl disulphide and trans-sec-butyl-1-propoenyl disulphide isolated from crude essential oil of Ferula sinkiangensis K.M.Shen,a Chinese traditional herbalmedicine[J].Nat Prod Res,2011,25(12):1161-1170.
[48]Zhang L J,Si JY,LiG Z,et al.Umbelliprenin and lariciresinol isolated from a long-term-used herb medicine Ferula sinkiangensis induce apoptosis and G0/G1arresting in gastric cancer cells[J].RSCAdvances,2015,5(110):91006-91017.
[49]Li G Z,Li X J,Cao L,et al.Sesquiterpene coumarins from seeds of Ferula sinkiangensis[J].Fitoterapia,2015,103:222-226.
[50]Li G Z,Wang JC,Cao L,et al.An unusual sesquiterpene coumarin from the seeds of Ferula sinkiangensis[J].JAsian Nat Prod Res,2016,18(9):891-896.
[51]LiG Z,Wang JC,Li X J,etal.Two new sesquiterpene coumarins from the seeds of Ferula sinkiangensis[J].Phytochem Lett,2015,13:123-126.
[52]王月娥,斯建勇,李晓瑾,等.新疆阿魏种子化学成分的研究(I)[J].中国现代中药,2011,13(1):26-28.
[53]Li G Z,Li X J,Cao L,et al.Steroidal esters from Ferula sinkiangensis[J].Fitoterapia,2014,97:247-252.
[54]李广志,李晓瑾,曹丽,等.新疆阿魏种子化学成分的研究[J].中草药,2015,46(12):1730-1736.
[55]高源,邢亚超,郭俐含,等.新疆阿魏树脂不同极性部位对人肺癌细胞的体外抑制作用研究[J].现代药物与临床,2015,30(4):366-369.
[56]Zhang H Y,Lu J,Jiang L,et al.Antioxidant and antitumor effects of ferula sinkiangensis K.M.Shen[J].Int JClin Exp Med,2015,8(11):20845-20852.
[57]Motai T,Daikonya A,Kitanaka S.Sesquiterpene coumarins from Ferula fukanensis and nitric oxide production inhibitory effects[J].JNat Prod,2004,67(3):432-436.
[58]Motai T,Kitanaka S.Sesquiterpene coumarins from Ferula fukanensis and nitric oxide production inhibitory effects[J].Chem Pharm Bull,2004,52(10):1215-1218.
[59]Motai T,Daikonya A,Kitanaka S.Sesquiterpene coumarins from Ferula fukanensis and their proinflammatory cytokine gene expression inhibitory effects[J].Chem Pharm Bull,2013,61(6):618-623.
[60]Motai T,Kitanaka S.Sesquiterpenoids from Ferula fukanensis and their inhibitory effects on nitric oxide production[J].J Nat Med,2006,60(1):54-57.
[61]许琼明,李国强,刘艳丽,等.阜康阿魏中倍半萜香豆素类化学成分研究[J].中国药学杂志,2009,44(4):255-257.
[62]Motai T,Kitanaka S.Sesquiterpene phenylpropanoids from Ferula fukanensis and their nitric oxide production inhibitory effects[J].JNat Prod,2005,68(3):365-368.
[63]Motai T,Kitanaka S.Sesquiterpene chromones from Ferula fukanensis and their nitric oxide production inhibitory effects[J].JNat Prod,2005,68(12):1732-1735.
[64]王东东,刘宏炳,宋海龙.HPLC法测定阜康阿魏根和叶中阿魏酸的含量[J].新疆医科大学学报,2012,35(9):1139-1142.
[65]Min ZD,MaiQ F,Mizuno M,etal.Polysulfanes in the volatile oils of Ferula species[J].Planta Med,1987,53(3):300-302.
[66]李肖宇,李国玉,王航宇.大果阿魏化学成分的研究[J].中国现代中药,2010,12(8):17-20.
[67]顾新宇,张涵庆,薛怡琛,等.大果阿魏酮化学结构的研究[J].植物资源与环境,1995,4(2):13-16.
[68]Sagitdinova GV,Saidkhodzhaev A I,Malikov V M.Structure and stereochemistry of Ferula lehmanni coumarins[J].Khim Prir Soedin,1983,19(6):709-712.
[69]赵文彬,谭勇,相颖,等.新疆大果阿魏中氨基酸和矿物元素含量测定[J].现代中药研究与实践,2009,23(3):67-68.
[70]赵文彬,朱芸,相颖,等.气相色谱-质谱法分析新疆阿魏挥发油化学成分[J].时珍国医国药,2007,18(5):1063-1064.
[71]Perel’son M E,Sokolova A I,Sklyar Yu E.Structure of feterin-a new terpenoid coumarin from Ferula teterrima[J].Khim Prir Soedin,1978,14(3):318-22.
[72]杨俊荣,李国强,李志宏,等.臭阿魏化学成分研究[J].天然产物研究与开发,2006,18(2):246-248.
[73]Yang JR,An Z,Li Z H,et al.Sesquiterpene coumarins from the roots of Ferula sinkiangensis and Ferula teterrima[J].Chem Pharm Bull,2006,54(11):1595-1598.
[74]Sokolova A I,Sklyar Yu E,Pimenov M G.Terpenoid coumarins from Ferula teterrima[J].Khim Prir Soedin,1978,14(1):134-135.
[75]罗茜,马桂芝,单萌,等.两种阿魏挥发油急性毒性及其化学成分的比较研究[J].中成药,2015,37(5):1130-1135.
[76]Veselovskaya N V,Sklyar Yu E,Savina A A.Fekrynol and its acetate from Ferula krylovii[J].Khim Prir Soedin,1981,17(6):798-799.
[77]Veselovskaya N V,Sklyar Yu E,Perel’son M E,etal.Terpenoid coumarins from Ferula krylovii[J].Khim Prir Soedin,1979,15(2):227-228.
[78]Perel’son M E,Sklyar Yu E,Veselovskaya N V,et al.Ferukrin-a new terpenoid coumarin from Ferula krylovii[J].Khim-Farm Zh,1977,11(3):78-80.
[79]Veselovskaya N V,Sklyar Yu E,Fesenko D A,et al.Fekrol-a terpenoid coumarin from Ferula krylovii[J].Khim Prir Soedin,1979,15(6):851.
[80]胡跃,李晓东,李国玉,等.阿魏的化学成分研究[J].中国现代中药,2009,11(7):18-19.
[81]堵年生,曲淑惠,支玲.新疆托里阿魏根中精油成分的研究[J].中国药科大学学报,1989,20(3):164-166.
[82]Suleimenov Ye M,Machmudah S,Ishmuratova M Yu,et al.Investigation of kazakhstani flora.II.GC/MS analysis of Ferula soongarica pall.ex schult.essential oil obtained by supercritical CO2extraction[J].Khim Rastit Syr’ya,2010(4):183-184.
[83]Zhou P,Takaishi Y,Duan H Q,etal.Coumarins and bicoumarin from Ferula sumbul:anti-HIV activity and inhibition of cytokine release[J].Phytochemistry,2000,53(6):689-697.
[84]Vandyshev V V,Sklyar Yu E,Perel’son M E,etal.Conferol,a new coumarin from Ferula conocaula and F.moschata roots[J].Khim Prir Soedin,1972,8(5):670-671.
[85]Khalilova EKh,Saidkhodzhaev A I.Terpenoid coumarins of Ferula sumbul[J].Chem Nat Compd,1999,34(4):506-507.
[86]Sklyar Yu S,Perel’son M E,Pimenov M G.Moschatol,a new coumarin from Ferula moschata roots[J].Khim Prir Soedin,1973,9(3):428.
[87]Eshbakova K A,Saidkhodzhaev A I,Vdovin A D,etal.Terpenoid coumarins from Ferula feruloides[J].Chem Nat Compd,2009,45(5):708-709.
[88]Meng H,Li G Y,Huang J,et al.Sesquiterpene coumarin and sesquiterpene chromone derivatives from Ferula ferulaeoides(Steud.)Korov.[J].Fitoterapia,2013,86:70-77.
[89]Liu T,Wang SY,Xu L L,etal.Sesquiterpenoidswith anti-MDR Staphylococcus aureus activities from Ferula ferulioides[J].Chem Biodivers,2015,12(4):599-614.
[90]Isaka K,Nagatsu A,Purev O.Sesquiterpenoid derivatives from Ferula ferulioides V[J].Chem Pharm Bull,2001,49(9):1072-1076.
[91]Kojima K,Isaka K,Purev O.Sesquiterpenoid derivatives from Ferula ferulioides IV[J].Chem Pharm Bull,2000,48(3):353-356.
[92]Nagatsu A,Isaka K,Kojima K,et al.New sesquiterpenes from Ferula ferulaeoides(STEUD.)KOROVIN.VI.Isolation and identification of three new dihydrofuro[2,3-b]chromones[J].Chem Pharm Bull,2002,50(5):675-677.
[93]Kojima K,Isaka K,Purev O,et al.Sesquiterpenoid derivatives from Ferula ferulioides[J].Chem Pharm Bull,1998,46(11):1781-1784.
[94]Liu T,Osman K,Kaatz GW,et al.Antibacterial sesquiterpenoid derivatives from Ferula ferulaeoides[J].Planta Med,2013,79(8):701-706.
[95]Kojima K,Isaka K,Ondognii P,et al.Sesquiterpenoid derivatives from Ferula ferulioides.III[J].Chem Pharm Bull,1999,47(8):1145-1147.
[96]Kojima K,Isaka K,Purev O,et al.Sesquiterpenoid derivatives from Ferula ferulioides.II.[J].Chem Pharm Bull,1999,47(5):690-691.
[97]Meng H,LiG Y,Huang J,et al.Sesquiterpenoid derivatives from Ferula ferulaeoides(Steud.)Korov.[J].Phytochemistry,2013,86:151-158.
[98]Hu Y,Li X D,Li G Y,et al.Two novel sesquiterpenoids from the roots of Ferula ferulaeoides(Steud.)Korov.[J].Helv Chim Acta,2010,93(5):1019-1024.
[99]Liu T,Wang C J,Xie H Q,etal.Guaiol-a naturally occurring insecticidal sesquiterpene[J].Nat Prod Commun,2013,8(10):1353-1354.
[100]Borisov V N,Ban’kovskii A I,Sheichenko V I,et al.Guaiol and hydroxy-aromatic acids from Ferula ferulaeoides[J].Khim Prir Soedin,1976,12(5):666-667.
[101]王飒,盛萍,姚蓝,等.维药多伞阿魏体外抗胃癌活性部位GC-MS指纹图谱的研究[J].中草药,2015,46(19):2874-2879.
[102]宋东伟,赵文军,吴雪萍,等.新疆多伞阿魏化学成分研究[J].中草药,2006,37(11):1627-1629.
[103]倪慧,姜传义,陈茂齐.新疆多伞阿魏根中挥发油成分研究[J].中成药,2001,23(1):54-57.
[104]盛萍,王飒,苗莉娟,等.不同方法提取的多伞阿魏挥发油化学成分及其体外抗胃癌活性比较[J].中成药,2013,35(11):2442-2448.
[105]倪慧,姜传义,刘淑兰,等.新疆多伞阿魏中挥发油成分报道[J].中药材,1997,20(1):34-35.
[106]Eshbakova K A,Saidkhodzhaev A I,Vdovin A D,et al.Terpenoid coumarins from Ferula feruloides[J].Chem Nat Compd,2009,45(5):708-709.
[107]Zhang L,Tong X P,Zhang J,etal.DAW22,a natural sesquiterpene coumarin isolated from Ferula ferulaeoides(Steud.)Korov.that induces C6 glioma cell apoptosis and endoplasmic reticulum(ER)stress[J].Fitoterapia,2015,103:46-54.
[108]熊元君,刘发,叶尔波,等.新疆三种阿魏对胃肠道作用的比较[J].新疆医学院报.1993,16(4):300-302.
[109]Wang X,Ren Z Z,He Y,et al.A combination of pharmacophoremodeling,molecular docking and virtual screening for iNOS inhibitors from Chinese herbs[J].Bio-Med Mater Eng,2014,24(1):1315-1322.
[110]Zhukov G O.Extraction and investigation of coumarins from Ferula caspica[J].Farm Zh(Kiev),1963,18(6):20-22.
[111]Zhukov G A,Prokopenko A P,Kolesnikov D G.Coumarins of roots of Ferula caspica[J].Med Promy-st′SSSR,1965,19(5):32-34.
[112]Zhukov G A,Prokopenko A P.Coumarins of Ferula caspica[J].Khim Prir Soedin,1967,3(3):214-215.
[113]Yelkenci S,Altundag H,Sagiroglu M,et al.Quantitative ICP-OES determination of trace and essential elements in the plant species of genus ferula[J].At Spectrosc,2016,37(3):102-107.
[114]Dzhumazhanov O D.Pharmacodynamics of preparations of Ferula caspica[J].Izvest Akad Nauk Kazakh SSR,Ser Med i Fiziol,1957,(1):111-121.
[115]IranshahiM,Noroozi S,Behravan J,etal.Persicasulphide C,a new sulphur-containing derivative from Ferula persica[J].Nat Prod Res,2009,23(17):1584-1588.
[116]Abd El-Razek M H,Ohta S,Hirata T.Terpenoid coumarins of the genus Ferula[J].Heterocycles,2003,60(3):689-716.
[117]Alam M,Khan A,Wadood A,et al.Bioassay-guided isolation of sesquiterpene coumarins from Ferula narthex bioss:a new anticancer agent[J].Front Pharmacol,2016,7:26/1-26/6.
[118]Iranshahi M,Amanolahi F,Schneider B.New sesquiterpene coumarin from the roots of Ferula latisecta[J].Avicenna JPhytomed,2012,2(3):133-138.
[119]Abourashed E A,Galal A M,El-Feraly F S,et al.Separation and quantification of themajor daucane esters of Ferula hermonis by HPLC[J].Planta Med,2001,67(7):681-682.
[120]Cha M R,Choi Y H,Choi CW,etal.Galbanic acid,a cytotoxic sesquiterpene from the gum resin of Ferula asafoetida,blocks protein farnesyltransferase[J].Planta Med,2011,77(1):52-54.
[121]Khasanov T Kh,Saidkhodzhaev A I,Nikonov G K.Structure ofmogoltacin[J].Khim Prir Soedin,1976,12(1):95-96.
[122]Nazari Z E,Iranshahi M.Biologically active sesquiterpene coumarins from Ferula species[J].Phytother Res,2011,25(3):315-323.
[123]IranshahiM,Kalategi F,Sahebkar A,etal.New sesquiterpene coumarins from the roots of Ferula flabelliloba[J].Pharm Biol,2010,48(2):217-220.
[124]IranshahiM,Kalategi F,Rezaee R,et al.Cancer chemopreventive activity of terpenoid coumarins from Ferula species[J].Planta Med,2008,74(2):147-150.
[125]杨秀伟.中药新药有效成分研究及其标准制定的科学依据[J].中草药,2009,40(增刊):8-13,18.
[126]杨秀伟.中药物质基础研究是中药继承、发展、创新的关键科学问题[J].中国中药杂志,2015,40(17):3429-3434.
——结构和生物活性

