AT1、Mas在反流性食管炎中的表达及意义
陈 吉, 田 燕, 杨 磊
1.内蒙古包钢医院消化内科,内蒙古 包头 014010; 2.长治医学院附属和平医院消化内科; 3.内蒙古包钢医院病理科
反流性食管炎(reflux esophagitis, RE)是常见的消化道动力障碍性疾病,属胃食管反流病(gastroesophageal reflux disease, GERD)的一种,是由于胃或十二指肠内容物长期、反复反流至食管所致的食管黏膜慢性炎症,其主要临床表现为消化道症状,部分患者表现为食管外症状[1]。RE在西方国家的发病率为10%~20%[2]。标准剂量的质子泵抑制剂(PPI)可使RE的症状缓解率和治愈率达到85%[3],但是仍有10%~40%的患者对PPI治疗无效或症状不能彻底缓解。
Barrett’s食管(Barrett’s esophagus, BE)是指食管末端柱状上皮取代鳞状上皮,可增加食管腺癌(esophageal adenocarcinoma, EA)的发生风险[3]。BE胃镜检出率6.8%,引起越来越多的关注[4]。EA患病率逐年增长,且预后差。因此,对BE及EA的早期诊疗非常重要。人们普遍认同,EA要经历RE-BE-异型增生-EA这一演化过程,RE作为起始病变,其发病机制复杂,普遍认为RE是由于抗反流屏障、酸清除机制及黏膜屏障等防御机制与来自胃及十二指肠的侵袭因素之间的不平衡所致[5-6],但具体的分子生物学机制尚不明确。
血管紧张素Ⅱ受体1亚型(Ang Ⅱ type 1 receptor, AT1)、Mas受体(Mas receptor)分别是血管紧张素Ang Ⅱ、Ang-(1-7)的特异性受体,均为肾素-血管紧张素系统(renin-angiotensin system, RAS)的重要成分。RAS分布广泛,存在于大多数器官包括胃肠道[7]。Ang Ⅱ是RAS中主要的生物活性肽。Ang Ⅱ的病理生理学效应绝大多数是通过其作用于AT1来实现的。Ang-(1-7)可通过Mas发挥扩张血管、降低血压、抑制平滑肌细胞増殖、利尿、利钠及抑制血管新生内膜增生等多种生物学功能,是血管紧张素转化酶2(ACE2)的主要催化产物,同时也被认为是Ang Ⅱ的内源性拮抗因子。AT1、Mas表达量的多少在一定程度上决定了Ang Ⅱ、 Ang-(1-7)的生物学效应。
RAS激素调节机制在宏观控制消化道功能和消化道微循环中发挥重要作用[8],本研究主要以AT1、Mas在RE、BE中的表达作为切入点,讨论RE的发生、发展是否与食管黏膜局部RAS异常表达有相关性。
1 资料与方法
1.1一般资料选取2014年12月至2016年9月就诊于内蒙古医科大学第三附属医院(内蒙古包钢医院)消化内科符合入选标准且临床资料完整的患者。正常食管黏膜30例,男22例,女8例,年龄(54.89±11.58)岁(24~78岁),均以腹胀、中上腹不适为主要症状就诊,行胃镜检查未见异常;RE 45例,男24例,女21例,年龄(58.69±14.13)岁(25~80岁),联合胃镜及病理结果证实的RE组织标本;BE 30例,男16例,女14例,年龄(57.30±11.81)岁(35~80岁),联合胃镜及病理结果证实的BE组织标本。组织标本还应排除合并下列情况者:食管其他器质性疾病、胃十二指肠疾病及消化道手术史;恶性肿瘤患者;患有内分泌系统疾病或合并其他系统慢性器官功能衰竭;入组前3周内服用非甾体抗炎药(NSAIDs)、PPI、血管紧张素受体阻断剂(ARB)、血管紧张素转化酶(ACEI)等药物及饮酒史。 各组患者年龄组间比较差异无统计学意义(P>0.05),具有可比性。
1.2实验方法
1.2.1 SP免疫组化:将30例正常食管黏膜、45例RE、30例BE组织均经质量浓度为100 g/L的中性甲醛固定48 h以上, 经脱水、浸蜡、包埋处理,分别连续切片3张,每张切片的厚度约5 μm,其中1张作HE 染色确定组织类型,另2张分别作以兔抗人AT1多克隆抗体、兔抗人Mas单克隆抗体作为一抗进行SP免疫组织化学染色法。 具体步骤如下:60 ℃烤片40 min;二甲苯Ⅰ、Ⅱ、Ⅲ,100%、95%、85%、75%梯度酒精浸泡脱蜡;自来水充分冲洗后置于蒸馏水中;高压锅900 ℃抗原修复2 min,PBS冲洗5 min×3次;内源性过氧化物酶阻断剂室温孵育20 min,PBS冲洗3次,每次5 min;非免疫兔血清室温孵育20 min;一抗(AT1/Mas)4 ℃过夜,PBS冲洗10 min×3次;生物素标记的羊抗鼠/兔室温孵育10 min,PBS冲洗10 min×3次;链霉素抗生物素蛋白-过氧化物酶室温孵育10 min,甩去试剂D,PBS冲洗5 min×3次;滴加DAB显色3~6 min,自来水充分冲洗; 苏木素复染7~15 s;乙醇脱水、二甲苯透明;中性树胶封片、镜检。
1.2.2 结果判定标准[9-10]:AT1、Mas阳性染色呈黄色或棕黄色颗粒,定位于细胞的胞浆内,PBS代替一抗作为阴性对照。采用半定量积分法判定结果,各切片均随机选取5个高倍视野,然后观察并计数100个细胞,阳性细胞数≤5%为0分,6%~25%为1分,26%~50%为2分,51%~75%为3分,>75%为4分;根据免疫细胞染色结果评分,未着色计为0分,浅黄色计为1分,棕黄色计为2分,棕褐色计为3分。综合评分由两类评分的乘积计算,0~1分计为阴性(-),2~4分计为弱阳性(+),5~8分计为阳性(++),9~12分计为强阳性(+++)。将+、++、+++归为阳性组计算阳性率。
1.3统计学处理采用SPSS 22.0软件系统对数据进行分析。对实验数据进行Krusral-wallisH非参数检验;对正常对照组、RE组、BE组用bonferroni法进行多重比较(组间采用Mann-WhitneyU检验);采用Kendall’s taur-b等级相关分析法分析AT1与Mas表达的相关性。P<0.05为差异有统计学意义。
2 结果
2.1食管不同黏膜组织的HE染色RE组织可见基底层厚超过15%,固有膜乳头伸入上皮超过65%,且上皮内出现淋巴细胞、嗜酸性粒细胞和中性粒细胞。BE组织可见柱状上皮成片被覆于食管下段或呈岛屿状散分布于鳞状上皮黏膜组织内(见图1)。
2.2AT1在食管不同黏膜组织中的表达免疫组化结果如图2所示,AT1表达于正常食管黏膜、RE、BE组织上皮细胞的胞浆中,其免疫阳性产物为棕黄色,采用Krusral-wallisH方法检验AT1在正常食管黏膜、RE、BE组织中的表达,秩均值分别为38.70、55.46、63.62,差异有统计学意义(χ2=11.262,P<0.01),表达呈逐渐升高趋势。组间比较采用Mann-WhitneyU检验,正常对照组与RE组AT1的表达差异有统计学意义(U=463,P<0.05);BE显著高于正常对照组(U=243,P<0.01);BE组高于RE组,但差异无统计学意义(U=563.5,P>0.05)。

图1 食管不同黏膜组织HE染色(HE 400×) A:正常组;B:RE组;C:BE组
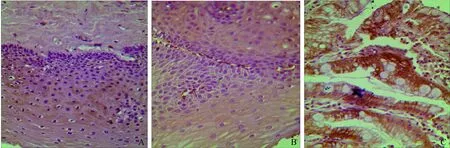
图2 AT1在食管不同黏膜组织中的表达(HE 400×) A:正常组;B:RE组;C:BE组
2.3Mas在食管不同黏膜组织中的表达免疫组化结果如图3所示,Mas表达于正常食管黏膜、RE、BE组织的上皮细胞细胞浆中,其免疫阳性产物为棕黄色,采用Krusral-wallisH法检验Mas在正常食管黏膜、RE、BE组织中的表达,秩均值分别为68.47、52.43、38.38,差异有统计学意义(χ2=17.985,P<0.01),表达呈逐渐下降趋势。组间采用Mann-WhitneyU检验,正常对照组与RE组Mas表达差异有统计学意义(U=461,P<0.05);正常对照组与BE组的Mas表达差异有统计学意义(U=200,P<0.05);RE组与BE组Mas表达差异有统计学意义(U=486.5,P<0.05)。
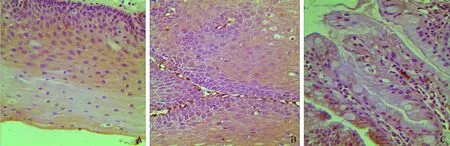
图3 Mas在食管不同黏膜组织中的表达(HE 400×) A:正常组;B:RE组;C:BE组
2.4在食管不同黏膜组织中AT1与Mas表达的相关性采用Kendall’s taur-b等级相关分析检验RE组、BE组中Mas与AT1之间的相关性。在RE组中,Mas与AT1的表达呈负相关(r=-0.303,P<0.05)(见表1);在BE组中,Mas与AT1的表达呈负相关,差异有统计学意义(r=-0.342,P<0.05)(见表2)。
3 讨论
RE是在全球范围发病率呈快速增长的消化道常见疾病,因此,本研究通过AT1及Mas蛋白的表达,探讨RE的分子生物学机制,以期对提高人群生活质量、RE的早期诊治及降低BE和EA发生率有一定意义。
AT1受体为跨膜G蛋白偶联受体超家族成员之一,是由359个氨基酸组成蛋白质多肽链,分子量约为41 kD,为AngⅡ的特异性受体,主要分布于心、脑、肺、肝、胃肠道。AngⅡ作为RAS中主要的生物活性肽,具有收缩血管、调节机体电解质平衡的作用。在局部组织中,AngⅡ通过与受体AT1、AT2结合发挥作用,其中主要是AT1受体。AT1与AngⅡ结合可发挥氧化应激、血管收缩、交感神经激活、血管加压素的释放和促进细胞增生等作用。当AT1表达升高时,AngⅡ所发挥的生物学效应增强,可引起黏膜血管收缩,血供减少,局部黏膜缺血会增加胃肠和食管黏膜的脆弱性,进而出现黏膜炎症、糜烂、溃疡及并发症。食管黏膜微循环对食管黏膜的完整性发挥着重要作用,黏膜血流量可为细胞间隙提供更多碳酸氢盐,并去除氢离子、二氧化碳和其他代谢物,以维持正常的黏膜酸碱平衡[11],从而保障黏膜的防御作用。一旦AT1表达升高,可使食管黏膜屏障功能受损,水、电解质及小分子物质在食管黏膜的通透性就会增加,细胞间隙增宽,酸和蛋白酶反流至食管并作用于食管黏膜的神经末梢,引起反酸、烧心、胸痛等症状。AT1可通过多种途径发挥生物学效应:(1)AngⅡ通过激活AT1可调节细胞的生长及分化,激活磷脂酶A2,诱导炎性介质的表达及释放, 例如生成花生四烯酸、白三烯和血栓烷、内皮生长因子、纤维细胞生长因子等[12]。局部促炎细胞因子的生成和释放可使食管黏膜受损进而导致食管炎的发生、发展[13]。(2)通过激活磷脂酶D,促进磷脂酰胆碱的水解,进而刺激细胞增殖[14]。组织增生及纤维化可降低食管的蠕动功能,从而增加胃反流及酸清除机制受损的可能性,加重食管的损伤。(3)调控细胞膜离子通道活性,可通过激活蛋白激酶C降低黏膜电位差,进而抑制离子的运输,抑制HCO3-的分泌,胃内容物频繁反流可引起酸负荷超载进而导致食管黏膜损伤。若AT1蛋白表达升高可促使AngⅡ与AT1结合增多,可能引起局部血管收缩,通过增加局部血管张力和强有力的血管收缩效应可减少胃肠道的血液供应,考虑RE组织学最具特征表现,黏膜糜烂、溃疡形成可能与此相关。
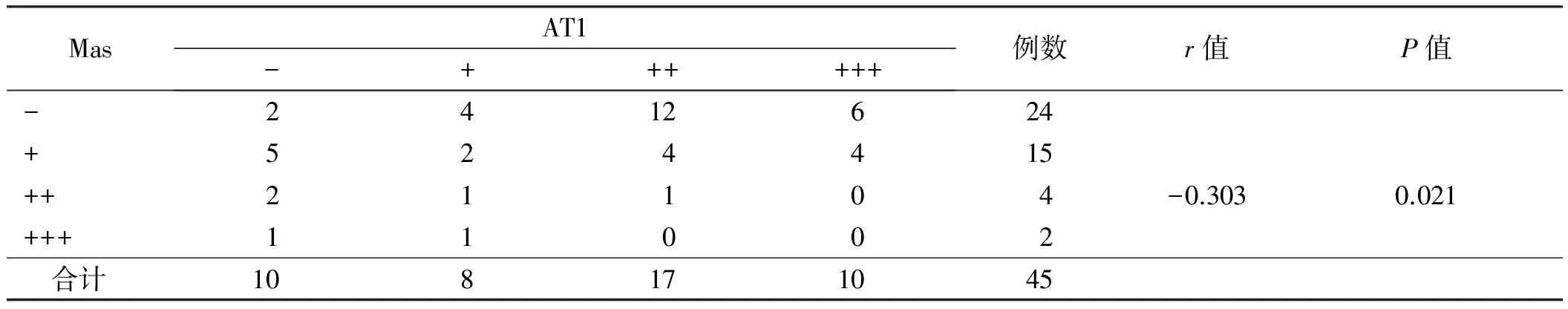
表1 AT1与Mas在RE中表达的相关性Tab 1 The correlation of the expressions of AT1 and Mas in RE
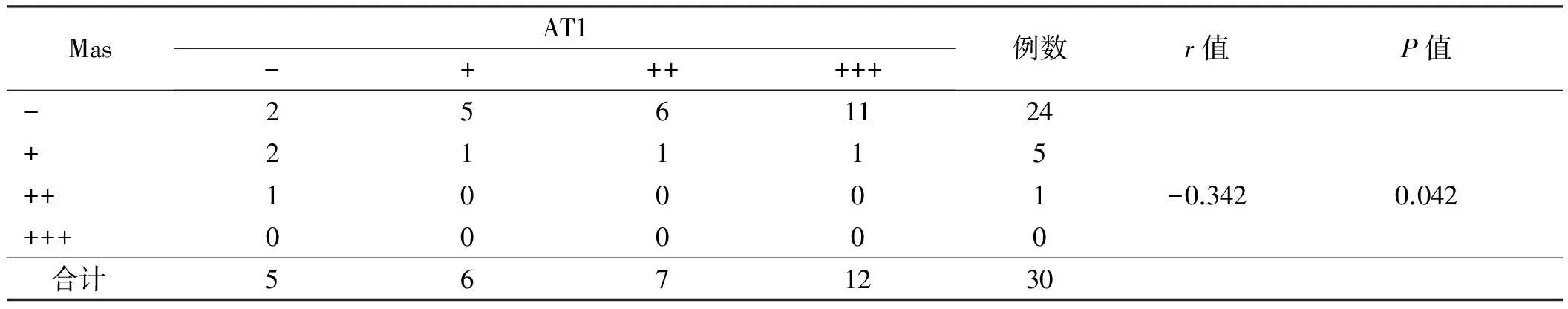
表2 AT1与Mas在BE中表达的相关性Tab 2 The correlation of the expressions of AT1 and Mas in BE
本实验中,无论RE组织还是BE组织中AT1表达均较正常食管黏膜明显升高,提示食管黏膜由正常转化为异常病变(RE、BE,甚至癌变)时,AT1蛋白可能作为血管收缩因子及促炎因子牵涉其中。如果能通过利用抑制AT1的表达或生物活性作用,或有可能阻止RE发生或发展。MIWA等[15]对在使用PPI的RE患者进行了分析,发现加用AT1阻滞剂患者的治愈率得到了提高,也证实了这一推论。多重比较RE组织与BE组织中AT1的表达差异无统计学意义,考虑有以下可能:(1)AT1经AngⅡ激活发挥生物学作用,当AT1表达明显升高时,AngⅡ-AT1结合可刺激更多的AT1蛋白生成,使AT1持续处于高表达水平,放大血管收缩作用及炎症反应。因此,当RE、BE发生时,AT1持续高表达,引发一系列放大效应。(2)本研究样本量较小,存在一定的局限性,临床研究人口规模较小且无序,考虑可能存在选择性偏差的风险和关联分析的不足。基于实验数据我们推测AT1通过AngⅡ参与BE从正常黏膜到肠化生这一癌前病变的发生过程。有学者研究表明,AngⅡ作为RAS中的重要成分,与胰腺癌等多种恶性肿瘤的发生存在相关性[16],那么,其与EA是否存在相关性?流行病学研究显示,使用血管紧张素转化酶抑制剂或AT1拮抗剂的食管癌患者发病率有所降低[17],由此推测可能是食管黏膜局部的AngⅡ生物活性作用受到抑制的结果。综上所述,AT1表达升高与RE的形成和发展有重要关系,推测利用抑制AT1的表达或生物活性作用,或有可能阻止RE形成及进一步发展。
Mas蛋白由325个氨基酸组成,属于G蛋白超偶联受体亚家族,是Ang-(1-7)的特异性受体,Ang- (1-7)也是RAS重要组成成分之一,是ACE2的主要催化产物,同时也被认为是AngⅡ的内源性拮抗因子。Mas受体与Ang-(1-7)结合可发挥扩张血管、抑制细胞増殖、抗炎和抗氧化等多种生物学功能。研究[17-18]发现,Mas由Ang-(1-7)激活,可通过内皮细胞一氧化氮(NO)、血管内皮舒张因子、前列腺素的释放从而参与血管舒张的调节。Ang-(1-7)可能通过舒张血管为局部微脉管系统提供保护作用,从而改善组织供氧,增加代谢底物的排出,并能更快速地清除代谢废物。有研究[7]显示,当人为阻断Mas受体,消除Ang-(1-7)的保护作用,可引起血管收缩,组织缺血、缺氧,从而加重局部氢离子浓度,可能诱发食管黏膜损伤。有文献[19]报道,Mas受体与Ang-(1-7)结合通过活化酪氨酸磷脂酶(SHP)-1,进而抑制AngⅡ引起的P38 MAPK磷酸化作用,对细胞增殖过程可能起到一定的抑制作用。
本实验中,Mas蛋白在RE、BE组织中的表达均低于正常对照组,当Mas表达减少时,局部微循环血流量减少,导致局部中性粒细胞的黏附,增加胃肠道微循环系统内皮细胞的黏附分子等炎症介质的表达[11,18]。局部促炎细胞因子的生成和释放可使食管黏膜受损,促使食管炎发生[20]。研究[21]表明,RE形成时,Mas受体与Ang-(1-7)结合参与食管黏膜保护机制,避免胃内容物反流对食管黏膜的损伤。BE中的表达较RE降低,几乎为阴性,提示Mas表达明显减少时,其对食管黏膜的保护作用缺失,可能促使RE的形成,并发展成为BE,由此推测Mas受体激活Ang-(1-7)后,可能通过舒张食管黏膜血管、抑制上皮细胞增殖和拮抗局部炎症反应等途径,对食管黏膜有一定的保护作用。综上分析,Mas对胃肠道包括对RE损伤的黏膜可产生有益影响,因此合理假设Mas受体激动剂可能作为治疗RE的可行方法。
Mas受体与AT1受体分别是AngⅡ、Ang-(1-7)特异性受体,通过两条代谢轴:ACE-AngⅡ-AT1受体轴与ACE2-Ang-(1-7)-Mas受体轴发挥作用,且AngⅡ经ACE2水解转化为Ang-(1-7),ACE2在两个代谢轴中起到桥梁作用。其中AngⅡ-AT1发挥致病作用,Ang-(1-7)-Mas对AngⅡ所发挥的生物学效应有拮抗作用,对组织起保护作用。Mas受体与AT1受体两者相互拮抗,前者与Ang-(1-7)相结合起到舒张血管,改善局部组织血供,抑制细胞增生及纤维化改变的作用。文献[17]报道,Mas受体与Ang-(1-7)结合抑制AngⅡ引起的P38 MAPK磷酸化作用,通过活化酪氨酸磷脂酶(SHP)-1,进而对细胞增殖起抑制作用。正常情况下,由于Ang-(1-7)作用与AngⅡ相反,通过发挥相互拮抗的作用,使机体达到平衡状态。RE发生时,Mas受体减少,则Mas与Ang-(1-7)结合减少,生物学效应减弱,可能导致失平衡状态发生,容易出现黏膜炎症、缺血糜烂,甚至溃疡等一系列病理变化。
本研究结果表明,AT1与Mas在RE组和BE组中表达呈负相关。已有报道Ang-(1-7)可能通过Mas受体介导,抑制AngⅡ激活NF-κB通路及对MMP-9的诱导作用,抑制其引起的慢性炎症及增生反应[22]。本实验中食管黏膜发生RE这一病理改变时,Mas表达明显减少,则其拮抗AngⅡ- AT1结合引发的炎症反应的作用减弱,印证了上面的推测。当RE发生时,Mas蛋白表达减少或缺失,推测Mas表达的减少甚至缺失会导致无法平衡AT1所致的慢性炎性信号通路,造成平衡失调,内分泌紊乱,可能促使食管黏膜发生炎症、增生、缺血、糜烂、肠化生等异常病变。国外部分学者在大鼠模型中的研究表明,肾素-血管紧张素系统(RAS)在控制食管功能、食管宏观和微循环的激素调节机制中发挥重要作用[8],本实验结果与之相符。
综上所述,AT1蛋白的高表达和Mas蛋白的低表达在RE的发生、发展过程中具有密切的负相关性,二者的表达对RE的形成及发展起到一定的作用。目前考虑肾素-血管紧张素系统代谢产物可能在食管防御机制中扮演重要的角色,或可在分子生物学层面为RE发病机制的探索开辟新的方向。基于上述结果推测,使用血管紧张素AT1受体抑制剂、激活或放大Ang-(1-7)-Mas轴生物效应,可能为日后对RE的治疗发挥重要作用。
[1] 刘建军, 汪忠镐, 田书瑞, 等. 内镜下Stretta射频治疗难治性及食管外症状性胃食管反流病临床观察[J]. 中华临床医师杂志(电子版), 2010, 4(10): 171-173. DOI: 10.3877/cma.j.issn. 1674-0785.2010.10.051.
[2] EL-SERAG H B, SWEET S, WINCHESTER C C, et al. Update on the of gastro-oesophageal reflux disease: a systematic review [J]. Gut, 2014, 63(6): 871-880. DOI: 10.1136/gutjnl-2012-304269.
[3] 陈龙平, 王雯. 难治性胃食管反流病的内镜治疗进展[J].中华消化内镜杂志, 2014, 31(10): 609-613. DOI: 10.3760/cma.j.issn.2007-5232.2014.10.018.
[4] 李安全, 王雯. 内镜诊断技术在 Barrett 食管中的应用及进展[J]. 医学综述, 2011, 17(8): 1239-1242.
LI A Q, WANG W. Development and application of diagnostic techniques of endoscope in Barrett esophageal [J]. Medical Recapitulate, 2011, 17(8): 1239-1242.
[5] FARRE R. Pathophysiology of gastro-esophageal reflux disease: a role for mucosa integrity? [J]. Neurogastroenterol Motil, 2013, 25(10): 783-799. DOI: 10.1111/nmo.12201.
[6] ORLANDO R C. The integrity of the esophageal mucosa. Balance between offensive and defensive mechanisms [J]. Best Pract Res Clin Gastroenterol, 2010, 24(6): 873-882. DOI: 10.1016/j.bpg.2010.08.008.
[7] FANDRIKS L. The renin-angiotensin system and the gastrointestinal mucosa [J]. Acta Physiol (Oxf), 2011, 201(1): 157-167. DOI: 10.1111/j.1748-1716.2010.02165.x.
[8] PAWLIK M W, KWIECIEN S, PAJDO R, et al. Esophagoprotective activity of angiotensin-(1-7) in rat model of acute reflux esophagitis. Role of sensory neuropeptides and proinflammatory cytokines [J]. J Physiol Pharmacol, 2014, 65(6): 809-822.
[9] VAZ-SILVA J, CARNEIRO M M, FERREIRA M C, et al. The vasoactive peptide angiotensin-(1-7), its receptor Mas and the angiotensin-converting enzyme type 2 are expressed in the human endometrium [J]. Reprod Sci, 2009, 16(3): 247-256. DOI: 10.1177/1933719108327593.
[10] 许良中, 杨文涛. 免疫组织化学反应结果的判断标准[J]. 中国癌症杂志,1996, 6(4): 229-231.
[11] SANTOS R A, FERREIRA A J, VERANO-BRAGA T, et al. Angiotensin-converting enzyme 2, angiotensin-(1-7) and Mas: new players of the renin angiotensin system [J]. J Endocrinol, 2013, 216(2): R1-R17. DOI: 10.1530/JOE-12-0341.
[12] SUAUKI Y, RUIZ-ORTEGA M, LORENZO O, et al. Inflammation and angiotensin Ⅱ [J]. Int J Biochem Cell Biol, 2003, 35(6): 881-900.
[13] BRZOZOWSKI T, KWIECIEN S, SZLACHCIC A, et al. Involvement of renin-angiotensin system and angiotensin-(1-7) metabolite of angiotensin Ⅱ in gastric mucosal injury and gastroprotection [M]. In: Cell/Tissue Injury and CytoProtection/OrganoProtection in the Gastrointestinal Tract: Mechanisms, Prevention and Treatment. Filaretowa LP, Takeuchi K. (eds). Basel, Karger, 2012: 181-190.
[14] PFEILSCHIFTER J, HUWILER A, MERRIWEATHER C, et al. AngiotensinⅡstimulation of phospholipase D in rat renal mesangial cells is mediated by the AT1 receptor subtype [J]. Eur J Pharmacol, 1992, 225(1): 57-62.
[15] MIWA H, HONGO M, KUSANO M, et al. Combination of angiotensin Ⅱ receptor blockers promotes proton pumpinhibitor-based healing of reflux esophagitis [J]. J Gastroenterol, 2012, 47(3): 249-255. DOI: 10.1007/s00535-011-0479-6.
[16] LAU S T, LEUNG P S. Role of the RAS in pancreatic cancer [J] . Curr Cancer Drug Targets, 2011, 11(4): 412-420.
[17] GARG M, ANGUS P W, BURRELI L M, et al. Review article: the pathophysiological roles of the renin-angiotensin system in the gastrointestinal tract [J]. Aliment Pharmacol Ther, 2012, 35(4): 414-428. DOI: 10.1111/j.1365-2036.2011.04971.x.
[18] SANTOS R A. Angiotensin-(1-7) [J]. Hypertension, 2014, 63(6): 1138-1147. DOI: 10.1161/HYPERTENSIONAHA.113.01274.
[20] PAWLIK M, PAJDO R, KWIECIEN S, et al. Nitric oxide (NO)-releasing aspirin exhibits a potent esophagoprotection in experimental model of acute reflux esophagitis. Role of nitric oxide and proinflammatory cytokines [J]. J Physiol Pharmacol, 2011, 62: 75-86.
[21] MAGIEROWSKI M, JASNOS K, PAWLIK M, et al. Role of angiotensin-(1-7) in gastroprotection against stress-induced ulcerogenesis. The involvement of mas receptor, nitric oxide, prostaglandins, and sensory neuropeptides [J]. J Pharmacol Exp Ther, 2013, 374(3): 717-726. DOI: 10.1124/jpet.113.207233.
[22] MULLER D N, DECHEND R, MERVAALA E M, et al. NF-κB inhibition ameliorates angiotensin Ⅱ-induce inflammatory damage in rats [J]. Hypertension, 2000, 35 (1 Pt 2): 193-201.

