运动联合抗抑郁药物对大鼠海马细胞和BDNF/pERK信号通路的影响
(华中科技大学同济医学院附属武汉精神卫生中心 精神科,湖北 武汉 430022)
抑郁症是一种常见的心境和认知功能障碍性疾病,发病率高。维持海马神经细胞增殖和凋亡的动态平衡有助于缓解抑郁症的恶化。研究表明,长期缺乏运动是导致抑郁症的主要因素之一[1]。采用运动疗法治疗精神疾病和脑疾病疗效较好[2]。因此,本实验研究运动联合帕罗西汀对抑郁症大鼠行为学、海马细胞凋亡、氧化应激损伤的影响及其作用机制,为抑郁症的治疗提供理论依据。
1 材料与方法
1.1 主要试剂
帕罗西汀(台州海辰药业有限公司),膜联蛋白V-FITC(Annexin V-FITC)/碘化丙啶(propidium iodide,PI)凋亡检测试剂盒(美国罗氏公司),活性氧(reactive oxygen species,ROS)检测试剂盒(上海碧云天生物技术研究所),DMEM培养基、胎牛血清(fatal bovine serum,FBS)购自美国Gibco公司,脑源性神经营养因子(brain-derived neurotrophic factor,BDNF)一抗、磷酸化细胞外信号调节激酶(phosphorylation extracellular regulated protein kinases,pERK)一抗、神经肽(Neuropeptide,VGF)一抗购自美国Santa Cruz公司,辣根过氧化物酶标记的山羊抗兔抗体(北京中杉金桥生物技术有限公司)。
1.2 方法
1.2.1大鼠抑郁模型的复制68只健康成年雄性SD大鼠由湖北省实验动物中心提供,安静饲养3 d后进行7 d的跑台适应性训练,将不爱运动的8只大鼠去掉。参照赵立波[3]和王珑等[4]的模型复制方法,采用慢性不可预知性温和应激(chronic unpredictable mild stress,CUMS)结合孤养法复制慢性应激抑郁模型:第1天禁食24 h,第2天夹尾3 min,第3天0℃游泳5 min,第4天水平振荡2 min,第5天昼夜颠倒,第6天禁食24 h,第7天45℃温箱热烘5 min,第8天禁水24 h,第9天45℃温箱热烘5 min,第10天禁食24 h,第11天昼夜颠倒,第12天0℃游泳5 min,第13天水平振荡2 min,第14天夹尾3 min,第15天禁水24 h,第16天0℃游泳5 min,第17天夹尾3 min,第18天45℃温箱热烘5 min,第19天昼夜颠倒,第20天禁食24 h,第21天水平振荡2 min,将抑郁大鼠单独饲养。模型复制结束后观察行为学试验作为缺乏快感的客观指标,判定模型是否复制成功。
1.2.2实验分组根据体重均衡的原则将实验分为5组:对照组、模型组、运动组、给药组、联合组,每组12只。对照组为正常饲养的大鼠,其余均接受21 d的CUMS。模型复制同时,给药组、联合组大鼠每次应激前灌胃10 mg/kg帕罗西汀,对照组、运动组大鼠给予等量的生理盐水;运动组、联合组每天上午以转轮跑的方式进行训练,运动量为跑速10 m/min,30 min/次,1 次 /d[5]。
1.2.3行为学试验①糖水实验:应激0、7、14和21 d测量剥夺饮水24 h后大鼠1 h内的糖水消耗量,糖水的饮用量反映大鼠快感反应。②Morris水迷宫实验:将大鼠置于Morris水迷宫中,水温控制在24~26℃,记录大鼠的逃避潜伏期,即在1 min内找到透明平台的时间,循环5次/d,连续测试3 d,取平均数为大鼠空间学习记忆成绩。
1.2.4流式细胞术将大鼠麻醉后断头取出脑组织,在冰盘上分离出右侧海马,采用酶消化法收集细胞,加入磷酸盐缓冲液(phosphate buffered saline,PBS)制成单细胞悬液,调整细胞浓度为1×106个/ml。取1 ml细胞悬液,1 500 r/min离心5 min,弃上清,加入1 ml预冷PBS重悬细胞,重复3次,加入10μl Annexin V-FITC和5μl PI轻轻振荡混匀,4℃避光染色20 min,采用流式细胞仪检测4组大鼠海马细胞凋亡率。
1.2.5DCFH-DA法采用DCFH-DA法检测细胞中ROS的含量。细胞悬浮液的制作方法同1.2.4。培养24 h后,PBS洗涤2次,重悬使细胞浓度调整为1.5×105个/ml,取2 ml接种至6孔板上,每孔加入浓度为10μmol/L的DCFH-DA探针,37℃避光培养30 min,弃去DCFH-DA,使用无血清的培养液洗涤细胞3次,离心收集细胞,加入100μl PBS重悬细胞,检测485/535 nm波长处的荧光值。
1.2.6Western blot检测将应激结束后的大鼠断头取脑组织,冰上分理出海马,置于液氮中迅速冷冻,放入-80℃冰箱中保存。实验时取出海马组织,加入组织裂解液,振荡混匀,置于冰上裂解30 min,离心取上清,按BCA试剂盒说明书进行操作,检测蛋白的表达水平。在蛋白样品中加入上样缓冲液稀释,沸水浴5 min,根据目的蛋白配置相应浓度的分离胶和5%浓缩胶进行十二烷基磺酸钠-聚丙烯酰胺凝胶电泳,待溴酚蓝迁移至凝胶底部,停止电泳,经浸渍转至硝酸纤维素膜上,用3% FBS封闭液4℃过夜,加入稀释好的一抗,置于摇床上4℃孵育过夜,PBS缓冲液清洗3次,10 min/次,加入二抗,室温孵育1 h,PBS缓冲液清洗3次,10 min/次,加入增强化学发光法显色液,暗室中曝光,定影液中浸泡5 min,凝胶成像系统中测定蛋白的灰度值。以目的条带灰度值与内参β-actin灰度值的比值为pERK、BDNF、VGF蛋白的相对表达量。
1.3 统计学方法
数据分析采用SPSS 20.0统计软件,计量资料以均数±标准差(±s)表示,多组比较用单因素方差分析或重复测量设计的方差分析,两两比较用LSD-t检验,P<0.05为差异有统计学意义。
2 结果
2.1 运动联合帕罗西汀对大鼠行为学的影响
2.1.1运动联合帕罗西汀对各组大鼠不同时间糖水饮用量的影响对照组、模型组、运动组、给药组、联合组大鼠应激0、7、14和21d的糖水饮用量比较,采用重复测量设计的方差分析,结果:①不同时间点的糖水饮用量有差别(F=9.238,P=0.000);②4组大鼠糖水饮用量有差别(F=6.932,P=0.003);③4组糖水饮用量变化趋势有差别(F=8.742,P=0.000)。进一步两两比较经LSD-t检验,模型组大鼠7、14和21 d的糖水消耗量较对照组降低(t=4.405、7.214和11.135,均P=0.000),提示大鼠抑郁模型复制成功。运动组、给药组、联合组大鼠14和21 d的糖水消耗量较模型组增加(P<0.05);联合组大鼠21 d的糖水消耗量较运动组、给药组增加(t=2.846和2.927,P=0.009和0.008),提示运动和给药可一定程度上增加大鼠的糖水饮用量,缓解抑郁大鼠的快感缺乏,且联合作用效果高于单独使用。见表1。
表1 运动联合帕罗西汀对各组大鼠不同时间糖水饮用量的影响(n=12,g,±s)
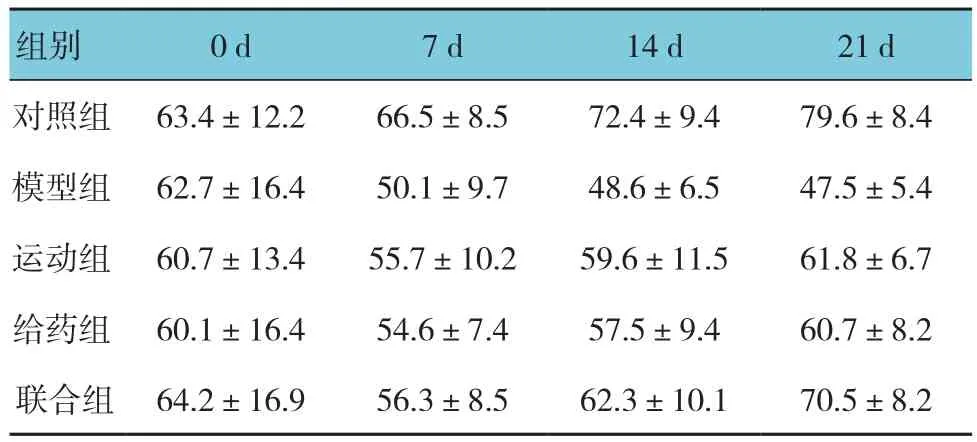
表1 运动联合帕罗西汀对各组大鼠不同时间糖水饮用量的影响(n=12,g,±s)
组别 0 d 7 d 14 d 21 d对照组 63.4±12.2 66.5±8.5 72.4±9.4 79.6±8.4模型组 62.7±16.4 50.1±9.7 48.6±6.5 47.5±5.4运动组 60.7±13.4 55.7±10.2 59.6±11.5 61.8±6.7给药组 60.1±16.4 54.6±7.4 57.5±9.4 60.7±8.2联合组 64.2±16.9 56.3±8.5 62.3±10.1 70.5±8.2
2.1.2运动联合帕罗西汀对各组大鼠空间记忆学习的影响对照组、模型组、运动组、给药组、联合组大鼠应激0、7、14和21 d的大鼠空间记忆学习能力比较,采用重复测量设计的方差分析,结果:①不同时间点的逃避潜伏期有差别(F=11.291,P=0.000);②4组大鼠逃避潜伏期有差别(F=14.357,P=0.000);③4组大鼠逃避潜伏期变化趋势有差别(F=9.637,P=0.000)。进一步两两比较经LSD-t检验,模型组大鼠7、14和21 d的逃避潜伏期较对照组延长(t=6.931、9.923和14.763,均P=0.000),表明大鼠空间记忆学习增强,糖水消耗结果一致,也提示本实验抑郁模型复制成功。运动组、给药组大鼠21 d逃避潜伏期较模型组缩短(t=5.612和7.720,均P=0.000);联合组14和21 d逃避潜伏期较模型组缩短(t=14.460,P=0.000)。联合组大鼠14和21 d逃避潜伏期较给药组、运动组缩短(P<0.05),提示运动和给药在14 d后可缩短大鼠逃避潜伏期,联合使用效果优于单独使用。见表2。
表2 运动联合帕罗西汀对各组大鼠不同时间逃避潜伏期的影响(n=12,s,±s)

表2 运动联合帕罗西汀对各组大鼠不同时间逃避潜伏期的影响(n=12,s,±s)
组别 0 d 7 d 14 d 21 d对照组 33.4±6.3 28.1±5.4 23.4±4.5 20.1±5.3模型组 34.5±6.4 43.1±5.2 48.7±7.6 53.9±5.6运动组 35.4±6.2 42.3±5.2 45.2±5.3 40.0±6.5给药组 35.4±7.1 40.4±8.3 42.1±6.2 38.3±4.2联合组 34.2±4.5 38.4±6.5 33.4±6.3 28.3±2.5
2.2 运动联合帕罗西汀对大鼠海马细胞凋亡的影响
对照组、模型组、运动组、给药组、联合组大鼠海马细胞凋亡率分别为(10.5±1.7)%、(48.5±6.7)%、(35.1±5.9)%、(23.6±5.7)% 和(22.6±6.1)%,经单因素方差分析,差异有统计学意义(F=81.300,P=0.000)。进一步两两比较经LSD-t检验,模型组、运动组、给药组、联合组大鼠海马细胞凋亡率高于对照组(t=19.044、13.879、7.629和6.619,均P=0.000);运动组、给药组、联合组细胞凋亡率低于模型组(t=19.044、13.879和7.629,均P=0.000);运动组细胞凋亡率高于给药组(t=4.856,P=0.000);联合组细胞凋亡率低于运动组(t=5.102,P=0.000)。提示抑郁症提高大鼠海马细胞的凋亡率,运动和给药可降低抑郁大鼠海马细胞的凋亡率,联合使用缓解细胞凋亡,可改善抑郁症。见图1。

图1 运动联合帕罗西汀对各组大鼠海马细胞凋亡的影响
2.3 运动联合帕罗西汀对大鼠海马细胞ROS的影响
对照组、模型组、运动组、给药组、联合组大鼠海马细胞ROS的相对表达量分别为(1.0±0.1)、(4.8±0.9)、(3.2±0.8)、(2.5±0.7) 和(2.3±0.4),经单因素方差分析,差异有统计学意义(F=54.967,P=0.000)。进一步两两比较经LSD-t检验,模型组、运动组、给药组、联合组大鼠海马细胞ROS高于对照组(P<0.05);运动组、给药组、联合组大鼠海马细胞ROS低于模型组(t=4.603、6.988和8.793,均P=0.000);运动组大鼠海马细胞ROS高于给药组(t=2.218,P=0.033);联合组大鼠海马细胞ROS低于运动组(t=3.486,P=0.002)。提示抑郁大鼠氧化损伤增加,运动和给药可抑制氧化应激损伤,联合治疗优于单独作用。
2.4 运动联合帕罗西汀对大鼠海马pERK、BDNF、VGF蛋白表达的影响
4组大鼠海马海马pERK、BDNF、VGF蛋白表达水平比较,经单因素方差分析,差异有统计学意义(P<0.05)。进一步两两比较经LSD-t检验,模型组大鼠海马pERK、BDNF、VGF蛋白表达水平低于对照组(t=9.798、9.798和7.349,均P=0.000);运动组、给药组、联合组大鼠海马pERK、BDNF、VGF蛋白表达水平高于模型组(P<0.05);运动组pERK蛋白表达水平高于给药组(t=17.146,P=0.000),运动组BDNF、VGF蛋白表达水平低于给药组(t=4.899和2.450,P=0.000和0.023);联合组pERK、BDNF、VGF蛋白表达水平高于给药组(t=6.794、4.201和4.382,均P=0.000);联合组pERK、BDNF、VGF蛋白表达水平高于运动组(t=2.228、5.881和5.477,P=0.046、0.000和0.000)。提示抑郁大鼠抑制BDNF、pERK、VGF的表达,运动联合给药逆转BDNF/pERK细胞信号转导通路及其靶基因的含量优于单一运动疗法或药物治疗。见图2和表3。
表3 运动联合帕罗西汀对各组大鼠海马pERK、BDNF、VGF 蛋白表达的影响(n=12,±s)

表3 运动联合帕罗西汀对各组大鼠海马pERK、BDNF、VGF 蛋白表达的影响(n=12,±s)
组别 pERK BDNF VGF对照组 0.7±0.1 0.8±0.1 0.8±0.1模型组 0.3±0.1 0.4±0.1 0.5±0.1运动组 1.2±0.1 0.6±0.1 0.7±0.1给药组 0.5±0.1 0.8±0.1 0.8±0.1联合组 1.5±0.5 1.3±0.4 1.2±0.3F值 51.310 33.600 30.000P值 0.000 0.000 0.000

图2 各组大鼠海马pERK、BDNF、VGF蛋白的表达
3 讨论
近年来,随着生活水平的提高、节奏的加快,全球>9亿人患有抑郁症,且发病率逐年升高,仅次于心脏病。目前针对抑郁症的治疗药物一般起效较慢,有效性也不高,对于部分难治性抑郁症更是束手无策。长期缺乏锻炼可导致抑郁症的发生,是抑郁症产生的重要影响因素。有研究表明,很少从事体力劳动的人患精神疾病的概率明显高于经常从事体力锻炼的人[6]。临床研究也显示,运动对精神患者的治疗和康复疗效较好[7],而且体育锻炼结合药物的疗效远远高于单一药物治疗[8],但是其作用机制尚不完全清楚。应激性事件是诱发抑郁症的主要因素之一,应激可引起机体诸多功能障碍,如认知功能、消化功能、情绪障碍等。CUMS是近年来研究抑郁症作用机制、药物研发与使用等功能时最常用的抑郁动物模型之一,可模拟抑郁症患者的快感缺失和行为绝望等核心症状。帕罗西汀是一种新型的抗抑郁药物,起效快,耐受性好,能够有效改善抑郁症状[9]。
本研究通过复制CUMS抑郁模型大鼠,观察运动联合抗抑郁药物对大鼠行为学的影响。通过糖水Morris水迷宫实验发现,模型组大鼠糖水消耗量降低,逃避潜伏期延长,表明抑郁大鼠模型复制成功,快感缺乏。慢性应激同时给予运动或药物中的一种或者联合使用可改善该核心症状,其中药物联合运动的缓解效果较好。
抑郁症的发病机制和抗抑郁药物的研发与细胞内信号转导相关蛋白或者靶基因关系密切,其中BDNF是最重要的影响因子之一。BDNF通过激活酪氨酸激酶受体B和有丝分裂原激活蛋白激酶(mitogenactivated protein kinase,MAPK)信号转导级联,影响抑郁症的病理生理结构和细胞功能。BDNF表达量可影响海马神经细胞的凋亡率。细胞外信号调节激酶(extracellular regulated protein kinases,ERK)是MAPKs的一个亚族,分为ERK1、ERK2、ERK3等多种亚型,其中脑组织中以ERK1、ERK2为主,统称为ERK1/2,是MAPK信号级联的重要蛋白之一。ERK1/2水平降低可促进抑郁症的发生、发展。ERK磷酸化后可激活胞浆内底物和转录因子cAMP反应元件结合蛋白CREB,调控细胞的增殖、凋亡,以及促进下游因子BDNF的表达[10]。VGF最早是作为神经生长因子在PC12细胞中诱导的基因产物而被发现的。近年来研究证明,VGF主要通过作为BDNF的靶基而发挥抗抑郁作用[11-12]。本实验通过流式细胞术检测海马细胞凋亡率和DCFH-DA法检测ROS水平,发现CUMS抑郁模型大鼠海马细胞ROS和凋亡率增加,运动、给药单独或者联合使用均可降低细胞ROS和凋亡率,缓解氧化应激损伤;Western blot检测发现,慢性刺激降低海马细胞中BDNF、pERK、VGF的表达量,运动和抗抑郁药物具有缓解BDNF、pERK、VGF表达量降低的作用,但运动联合药物逆转BDNF、pERK、VGF表达量优于单一运动疗法或抗抑郁药物治疗,其可能是通过运动和抗抑郁药物增强pERK的表达,进而上调BDNF,从而调控下游靶基因VGF的水平,发挥抗抑郁效果。
总之,运动联合抗抑郁药物帕罗西汀能够有效缓解慢性应激引起的抑郁症状,逆转大鼠快感缺乏,降低海马细胞凋亡率和氧化应激损伤,其作用机制可能是通过BDNF/pERK信号通路,调控下游靶基因的表达而发挥作用。

