白云鄂博矿气基还原试验研究
杨立锋 彭望君 王 顺 张捷宇
(省部共建高品质特殊钢冶金与制备国家重点实验室、上海市钢铁冶金新技术开发应用重点实验室和上海大学材料科学与工程学院,上海 200072)
内蒙古的白云鄂博矿是世界上极其罕见的多金属共生的大型综合矿床,铁、铌、稀土等资源储量非常丰富,其中稀土元素主要存在于氟碳铈矿和独居石等十多种矿物中[1- 2]。但是白云鄂博矿中矿物结构复杂、单种元素的品位低、互相嵌入,而且分布不均匀[3],这就导致了矿物金属之间的分离难度较大,流程长,成本高,资源有效回收率低等问题。目前冶金工作者对白云鄂博矿中的铁矿物和稀土矿物在还原、提取工艺以及高炉冶炼等方面已做了大量工作[4- 5]。采用传统高炉冶炼白云鄂博矿,工艺能耗高,而且二氧化碳的排放量大,有价元素不能被有效地利用。配碳还原需要的温度又较高,还原效率低[6]。而氢气等气体还原则可以在较低温度下进行,并且能实现清洁生产。
本文以氢气和一氧化碳两种气体为还原剂,对白云鄂博矿进行还原,考察温度、流速和时间等参数对还原过程的影响,并计算了各个条件下的金属化率,从而为高效低成本开发白云鄂博矿资源提供了试验依据。
1 试验材料与方案
1.1 试验材料
试验所使用的白云鄂博矿产自包头,矿石取自包钢选矿厂。原料先经过颖式破碎机粗碎,再用对辊破碎机细碎至0.5~3.0 mm,将破碎后的白云鄂博原矿在研钵中进行手工研磨,研磨通过100目的筛子进行筛分,每次将不符合要求的矿粉返回研钵中继续研磨,直至所有矿粉都通过100目(0.15 mm)的筛。所有试验均采用此粒度的白云鄂博原矿进行。
将研磨干燥后的矿粉进行XRF成分分析,主要元素含量如表1所示。
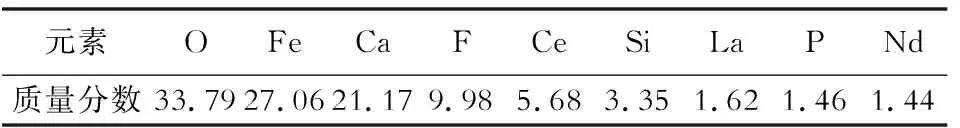
表1 白云鄂博原矿的化学成分(质量分数)Table 1 Chemical composition of Bayan obo ore (mass fraction) %
从表1中可以看出,该矿中铁的质量分数较低,仅为27%,Ca的质量分数为21%。主要金属元素包括铁、铈、镧、钕等,而其他稀土元素含量则比较低,未列在表中。
进一步对试验矿粉进行XRD物相分析,结果如图1所示。可以看出:该矿的物相组成比较复杂,主要矿相包括赤铁矿(Fe2O3)、磁铁矿(Fe3O4)、萤石(CaF2)、氟碳铈矿(CeCO3F)。

图1 原矿的X射线衍射分析Fig.1 X- ray diffraction patterns of raw ore
1.2 试验过程
为了确定还原过程中物相变化的温度点与适宜的还原条件,先通过热重分析来确定还原试验所需温度范围,然后在此温度范围进行不同条件下的还原试验,再对还原产物进行XRD和扫描电镜观察分析。
热重分析过程:称取约1 g的白云鄂博矿样品,将样品置于样品台上,在不同气氛中,以10 ℃/min的速率升温至1 200 ℃。反应过程中样品的质量变化由一台接入Ther Max- 700热重分析仪的计算机记录。试验结束后,关闭反应气体阀门,并将惰性气体氩气阀门打开。之后再按照事先设定的降温程序进行降温,直至室温。
恒温还原:在卧式炉中对白云鄂博矿粉进行不同条件下的还原反应。首先将炉子以10 ℃/min的速度升到试验设定温度,进行保温,然后通入300 mL/min高纯氩气约10 min,将气体管包括炉管内的空气排除干净。再将5 g白云鄂博矿粉置入炉管的恒温带上,立即封闭炉子,通入还原气体,然后计时,在恒定温度下进行还原反应。反应结束后关闭还原气体,并再次打开高纯氩气,排出残余还原气体的同时保护样品不被氧化,待样品温度冷却至室温后,取出进行分析。
使用化学滴定法测定还原样品的金属化率,误差较小。采用扫描电镜观察还原后样品的微观形貌。
2 试验结果与讨论
2.1 非等温热重试验
试验条件:分别在纯Ar、纯H2、纯CO的气氛中进行非等温热重试验,气体流速均为100 ml/min。升温速率均为10 ℃/min,温度范围为室温至1 200 ℃。
不同气氛中测得的非等温热重曲线分别如图2~图4所示,dm/dt表示质量分数对时间的求导。
从图2纯Ar气保护气氛中的非等温热重曲线可以看出,在约400 ℃时,失重曲线开始明显下降,根据相关文献,可以判断此时应该是结晶水的失去过程而引起的峰值,峰值温度约520 ℃。在600 ℃左右时,失重曲线达到一个平台,说明样品内结晶水已经完全失去,质量暂时没有变化,失重约占样品总质量的3%。随着温度的继续升高,在900 ℃时,失重曲线又开始变化,而且失重速率在接下来一定范围内逐渐增大,在约1 000 ℃时出现峰值,这里可能是发生了氟碳铈矿分解反应,氟碳铈矿转化为含稀土相(CaO·2Ce2O3·3SiO2)[3]。具体反应为:4CeCO3F+3CaO+3SiO2=CaO·2Ce2O3·3SiO2+2CaF2+4CO2(g)。

图2 Ar气氛中的非等温热重曲线Fig.2 Non- isothermal thermo- gravimetric curve in Ar atmosphere
图3显示了在H2气氛中白云鄂博原矿还原的失重曲线。可以看出,从320 ℃开始,失重曲线就开始有微小变化,结合Ar保护气氛中的曲线相比较,可以分析得出是铁氧化物开始被氢气还原而引起的质量变化,同时这个过程中有结晶水的失去,是两者的叠加曲线。在470~750 ℃之间样品质量明显减小,则是Fe2O3、Fe3O4与H2的还原反应,生成的水蒸气随气体排出,使质量减小。在1 000 ℃左右的位置,样品质量又进一步减小,这是CeCO3F分解而产生的峰。
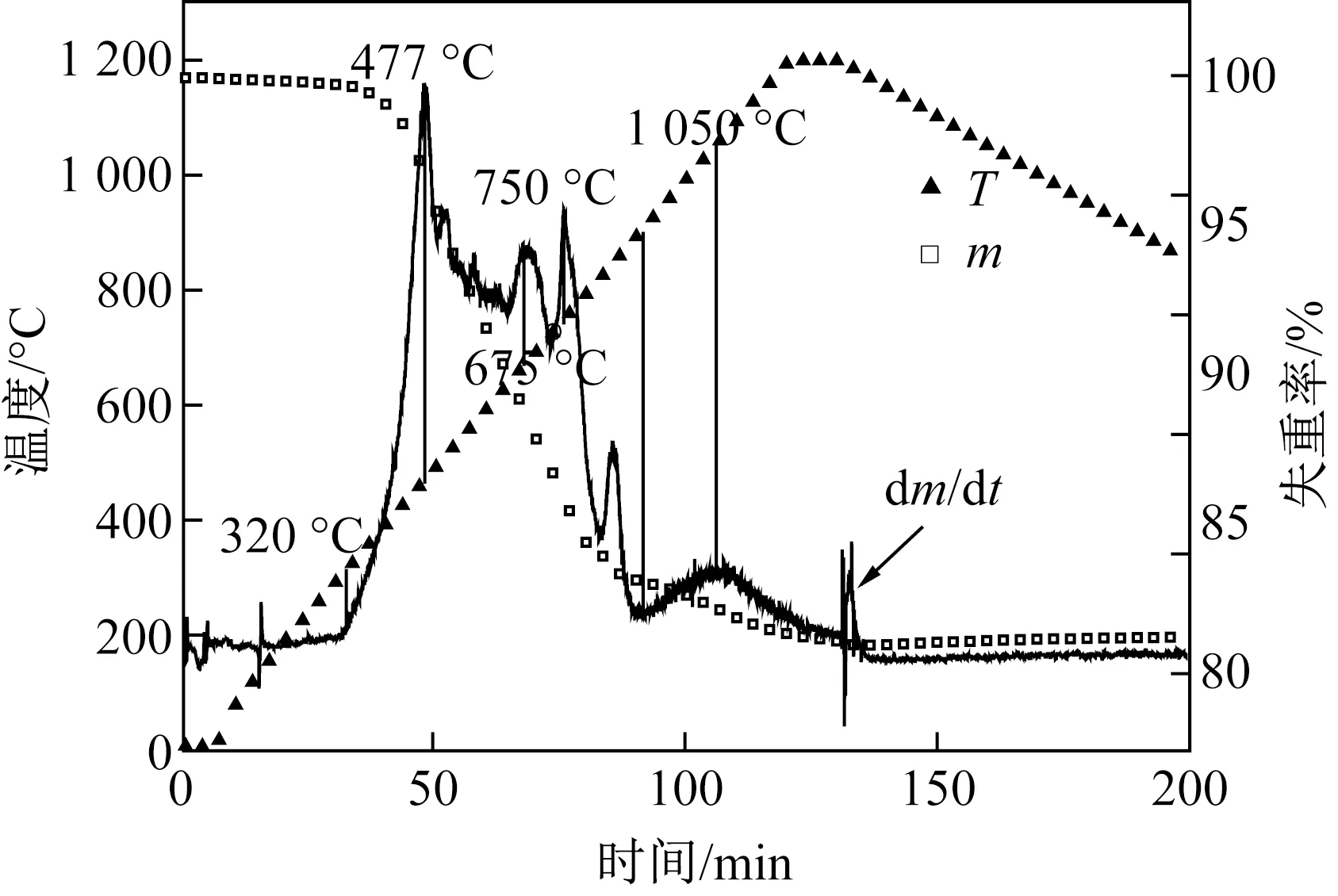
图3 H2气氛中的非等温热重曲线Fig.3 Non- isothermal thermo- gravimetric curve in H2 atmosphere
图4显示了CO气氛中白云鄂博矿还原的失重曲线,对比上述试验,一直到500 ℃之前,样品质量都没有明显减小,但在400 ℃左右时,样品质量反而增加,并且在490 ℃左右时出现峰值,结合在400 ℃左右时有结晶水的失去,此段可能发生了较为明显的析碳反应。而在500 ℃左右时,样品质量才开始有减小的趋势,并且在之后产生了一个小的平台,此时应该是析碳反应达到了短暂的平衡,导致质量没有发生变化。而当温度继续升高,约600 ℃之后,样品质量继续减小,此时应是CO与样品中的铁氧化物逐渐开始还原反应。

图4 CO气氛中的非等温热重曲线Fig.4 Non- isothermal thermo- gravimetric curve in CO atmosphere
通过以上热重试验的分析,可以看出对于H2和CO气氛保护的还原反应,主要集中在500~1 100 ℃之间的温度段,同时考虑到动力学因素,将后续恒温还原反应的温度设置在650~1 050 ℃之间,每100 ℃一个梯度进行研究。
2.2 恒温还原试验
2.2.1 气体流速的影响
试验条件:固定还原温度为850 ℃,还原时间为10 min,考察H2流速在100、200、300 mL/min时样品的金属化率;CO还原的时间固定为30 min,考察CO流速在50、100、200、300 mL/min时样品的金属化率,结果如图5所示。
从图5可以看出,无论是氢气还是一氧化碳的还原,在时间恒定的条件下,对同种气体,随着流速的增大,金属化率逐渐增大。氢气流速为100 mL/min时,还原10 min的金属化率仅为27.62%,氢气流速达到200 mL/min时,金属化率已经达到41.85%,而随着流速的继续增加,300 mL/min时的还原效果与200 mL/min的接近,说明继续增加氢气流速已经没有必要。同样地,一氧化碳还原时流速为300 mL/min与流速为200 mL/min的还原效果也很接近。

图5 以不同H2(a)和CO(b)流速还原后样品的金属化率Fig.5 Metallization rate of samples after reduction at different flow rate in H2 (a) and CO (b) atmosphere
因此在研究其他因素的影响时,气体流速均固定为200 mL/min,此流速已经能保证还原时还原气体有合适的分压,继续增加流速则会有过多还原气体的流失,增加还原成本。
2.2.2 还原温度的影响
试验条件:H2还原时间为10 min,CO还原时间为30 min,气体流速200 mL/min,还原温度650~1 050 ℃,每100 ℃为一个温度梯度。不同条件还原后测得样品的金属化率如图6所示。
通过图6可以看出,随着还原温度的升高,铁的金属化率显著提高,超过一定温度后,又开始下降。H2还原过程中,从650 ℃到950 ℃,金属化率从7.27%提高到81.67%,其中从850 ℃到950 ℃变化最为明显,而温度继续升高到1 050 ℃,金属化率则明显下降;CO还原过程中,变化趋势与H2还原基本类似,不同的是从温度提高到950 ℃开始,金属化率就出现下降的趋势。
究其原因在于:氢气还原氧化铁是逐级反应的,而氢气与Fe3O4和FeO的反应均是吸热反应,温度升高有利于反应进行[4];但当温度提高到950 ℃以上,矿粉会发生明显的粘结现象,虽然在热力学上更有利于反应进行,但由于矿粉的致密影响了氢气的向内扩散,导致动力学上反应受阻,会发生金属化率下降的趋势。而一氧化碳还原FeO的反应是放热反应,温度升高,从热力学上看不利于反应进行,同时850 ℃时粉矿也会产生轻微的粘结,因此在850 ℃以上,金属化率也会下降。这一点在文献中也有指出,还原温度过高将会使样品中产生一定量的液相,从而导致还原动力学条件恶化。
由此也可以看出,反应温度对白云鄂博矿的还原有着非常重要的影响,因为整个还原过程中,金属铁晶粒形核、晶核长大以及晶粒间的兼并长大均受还原温度的影响[5]。而且渣金分离的效果也取决于铁颗粒的大小、形状以及存在状态。金属颗粒越大,越有利于渣的分离。弱还原度过低、金属颗粒过小,则会形成渣金相互包裹的现象,渣金就不能有效分离。
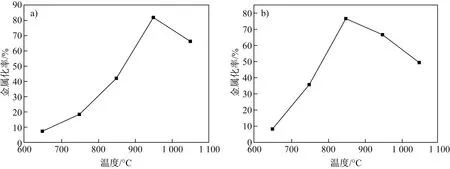
图6 不同温度下H2(a)和CO(b)气氛还原后样品的金属化率Fig.6 Metallization rate of samples after reduction at different temperatures in H2(a) and CO (b) atmosphere
2.2.3 还原时间的影响
试验条件:固定还原温度为850 ℃,考察氢气还原5、10、20、60 min后,一氧化碳还原5、10、20、30、40、60 min后样品的金属化率,结果如图7所示。
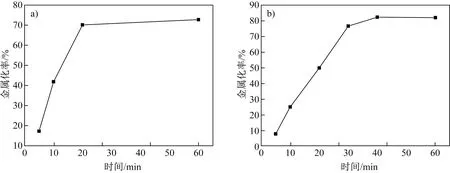
图7 H2(a)和CO(b)还原不同时间后样品的金属率Fig.7 Metallization rate of samples after reduction for different times in H2 (a) and CO (b) atmosphere
从图7中可以看出,氢气还原时,随着还原时间增加至20 min,金属化率大幅增加,20 min之后基本没有变化,金属化率最高达到70.15%。
一氧化碳还原时,随着还原时间逐渐增加至30 min,金属化率大幅增加,还原30 min时,金属化率已经达到76.64%;随着时间继续增加,还原速率逐渐放缓,40 min时金属化率为82.36%,金属化率仅增长了7%;时间继续延长至1 h,金属化率变化不大。
对比850 ℃时H2和CO还原不同时间的数据可以看出,H2还原集中在前20 min,CO还原集中在前40 min,这符合H2还原能力强于CO的结论,因为H2的分子小,扩散能力更强。
2.3 还原产物的形貌分析
在CO气氛中经850 ℃还原5、120 min后,样品中金属铁相和稀土矿相的扫描电镜形貌如图8所示。

图8 CO气氛中850 ℃还原5 min (a)和120 min(b)后铁相、还原120 min后稀土相(c)的微观形貌Fig.8 Microstructures of iron phase(a,b) and raw earth phase(c) in sample after reduction at 850 ℃ for 5 min and 120 min
从图8中可以看出,当还原时间为5 min时,已经有微量的金属铁零星地在铁氧化物周围析出,或在颗粒气孔附近析出,其他区域则暂未发现。当还原时间达120 min后,已有大片的金属铁聚集,说明已经经历了结晶形核、晶核的长大以及晶粒的互相兼并过程。
对图8(c)中灰色物相进行EDS分析,确定是稀土矿相聚集的区域,主要成分为CaO·2Ce2O3·3SiO2、CaO·2La2O3·3SiO2、CaO·2Nd2O3·3SiO2以及反应产生的CaF2,与原矿成分进行对比可知,CaF2是在高温还原过程中含稀土的氟碳铈矿与脉石反应所生成的。
3 结论
(1)通过对白云鄂博矿的非等温热重试验分析,可知结晶水在400 ℃左右时开始失去,氢气还原在约320 ℃即有微小的质量变化,而一氧化碳则在近500 ℃才开始发生反应。
(2)通过研究还原反应温度和时间、气体流速等因素的影响,初步得到当气体流速为200 mL/min,还原温度为850 ℃,氢气和一氧化碳的还原时间分别为20、40 min时,金属化率可分别达到70%和80%以上。
(3)氢气恒温还原10 min,随着还原温度的升高,金属化率逐渐增大,950 ℃时达最大值为81.67%,但继续升高温度到1 050 ℃,金属化率反而下降;一氧化碳恒温还原30 min条件下,则在温度850 ℃时金属化率就开始下降,此时金属化率为76.64%。
(4)随着还原时间的增加,还原金属铁逐渐从铁氧化物周围析出并聚集长大。850 ℃还原120 min后,原矿中的稀土矿相逐渐从ReCO3F转变为CaO·2Re2O3·3SiO2。

