非小细胞肺癌脑转移放疗时机和方案选择的分析
洪 福 钱立庭 詹必红 张洪波
安徽省肿瘤医院放疗科,安徽合肥 230031
约有20%~40%的非小细胞肺癌(NSCLC)患者在疾病进程中会发生脑转移,若未得到积极治疗,患者自然状态下中位生存期往往不足3个月[1]。放疗及综合治疗技术使NSCLC脑转移患者的预后得到了明显改善,但目前临床关于放疗时机和方案的选择尚存在争议[2]。有学者认为,全脑放疗可造成神经认知功能损害,且与全身治疗同时进行时往往使得毒性反应加重[3];但也有报道指出,推迟放疗可能会影响患者生存[4]。此外,关于调强放疗(IMRT)与立体定向放射治疗(SBRT)在NSCLC脑转移治疗中的应用价值,目前尚无定论。此次研究就不同放疗时机和方案选择预后进行回顾性分析,现将研究方法与结果予以总结报道。
1 资料与方法
1.1 一般资料
研究对象为2014年12月至2018年7月于我院接受放疗及全身治疗的61例NSCLC脑转移患者。患者均经病理组织学或细胞学检查明确NSCLC诊断,头颅MRI或CT检查证实脑转移,且病例资料及随访资料均保存完整。61例患者中,男42例,女19例,年龄42~87岁,中位年龄62岁,病理分型:腺癌48例,鳞癌13例;脑转移数量:单发30例,多发31例。基因突变(EGFR/ALK突变):15例。
1.2 放疗方案
患者于我院接受综合治疗,化疗54例,靶向治疗20例。IMRT放疗方案:患者仰卧位定位,予头部面罩固定。大体肿瘤体积(GTV)定义为影像学可见脑转移瘤,不包括周围水肿区;临床靶体积(CTV)即全脑(包括硬脑膜);计划肿瘤靶区(PGTV):GTV均匀外放摆位误差;计划靶体积(PTV):CTV均匀外放摆误差位,外放后根据解剖屏障及病灶位置适当调整。采用95%等剂量曲线覆盖靶区,每日1次,每周5次,PGTV共45.0~59.4 Gy/15~33 F,PTV共30~40 Gy/10~20 F。限定危及器官受量:晶体≤8 Gy,脑干≤54 Gy,眼球、视神经和视交叉≤50 Gy。SBRT(伽马刀)放疗方案:患者仰卧位定位,予头部面罩固定。螺旋CT 3~5 mm层厚连续扫描病变区域获得定位图像,核准Z线值及患者体表标记点的X、Y、Z坐标参数及重复摆位读数,以不易移动的骨性标志作为体表标记点,将定位扫描所获得的定位图像通过网络或光盘传输系统输入到伽玛刀治疗计划系统。靶区勾画,GTV:为影像学(头颅CT结合MRI)所示脑转移肿瘤病灶范围;PTV:GTV均匀外扩摆位误差,外放后根据解剖屏障及病灶位置适当调整。由副主任以上医师审核勾画肿瘤靶区及计划,由医师及物理师共同对治疗计划进行评价及优化,根据病灶大小和部位选用不同大小的准直器,以单靶点或多靶点照射,采用50%等剂量曲线覆盖PTV,每日1次,每周5次,共28~51 Gy/7~17 F。
1.3 分组方案
1)根据放疗时机早期放疗组:于全身治疗开始后2周期内实施放疗;晚期放疗组:于全身治疗开始后2周期后实施放疗。2)根据放疗方案,将其分别纳入IMRT组、SBRT(伽马刀)组。
1.4 观察指标分析
比较各组患者近期疗效、不良反应发生情况以及生存情况。疗效评价参照实体瘤疗效评价新标准(RECIST)[5]进行评价。总有效率=(CR+PR)/总例数×100%。不良反应发生情况参照常用药物毒性标准3.0(CTCAE)及肿瘤放射治疗协作组(RTOG)急性放射性损伤分级标准予以评估[6-7]。生存情况相关指标包括颅内疾病无进展生存期(PFS)、总生存期(OS),PFS定义为确诊脑转移后首治疗至疾病进展或死亡,OS定义为确认脑转移至死亡或末次随访[8]。
数据采用SPSS 18.0进行分析,计数资料以(n/%)表示,采用χ2检验,生存率分析采用Kalpan-Meier法,并采用Log-rank检验,以P<0.05为差异有统计学意义。
2 结果
2.1 早期放疗组与晚期放疗组对比
2.1.1 近期疗效和不良反应 早期放疗组共37例CR5例、PR17例、SD5例、PD10例,CR与PR合计22例,总有效率59.45%,晚期放疗组共24例CR3例、PR11例、SD4例、PD6例,CR与PR合计14例,总有效率58.33%,组间比较差异无统计学意义(P>0.05)。
早期放疗组与晚期放疗组各类型不良反应发生率比较,差异无统计学意义(P>0.05)。见表1。
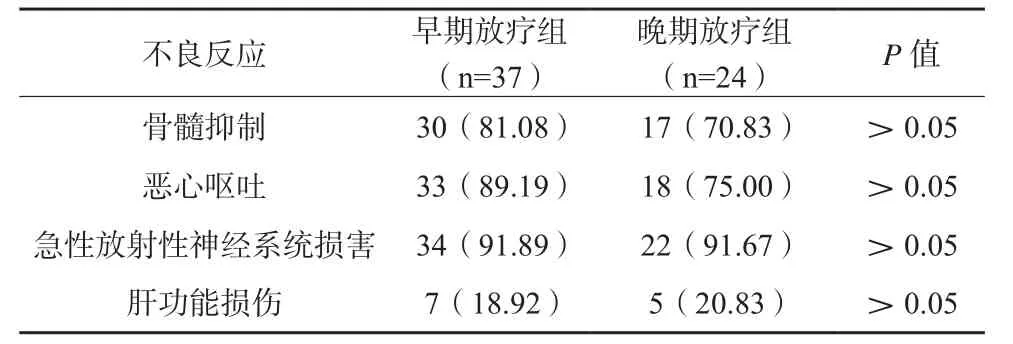
表1 早期放疗组与晚期放疗组不良反应对比(n/%)
2.1.2 生存情况 早期放疗组中位OS与PFS分别为17.8个月、4.0个月,均高于晚期放疗组的12.5个月、3.0个月,差异有统计学意义(P<0.05)。见图1。
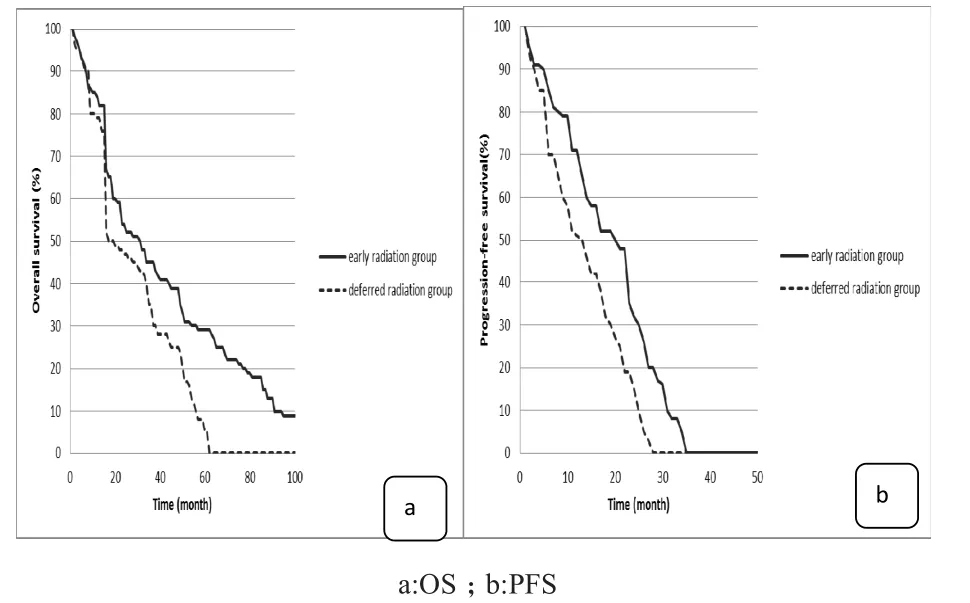
图1 早期放疗组与晚期放疗组OS 和PFS分析(Kalpan-Meier法)
2.2 IMRT组与SBRT(伽马刀)组对比
2.2.1 近期疗效与不良反应 IMRT组共32例,CR3例、PR9例、SD8例、PD12例,CR与PR合计12例,近期总有效率37.50%,SBRT(伽马刀)组共29例,CR5例、PR17例、SD5例、PD2例,CR与PR合计22例,近期总有效率75.86%,SBRT(伽马刀)组高于IMRT组,差异有统计学意义(P<0.05)。IMRT组与SBRT(伽马刀)组各类型不良反应发生率比较,差异无统计学意义(P>0.05)。见表2。
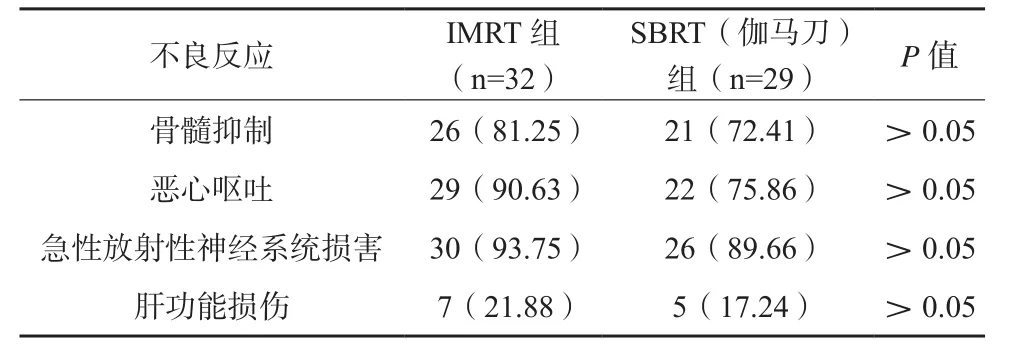
表2 IMRT组与SBRT(伽马刀)组不良反应对比(n/%)
2.2.2 生存情况 IMRT组中位OS与PFS分别为9.5个月、3.0个月,均低于SBRT(伽马刀)组的18.0个月、5.0个月,差异有统计学意义(P<0.05)。见图2。
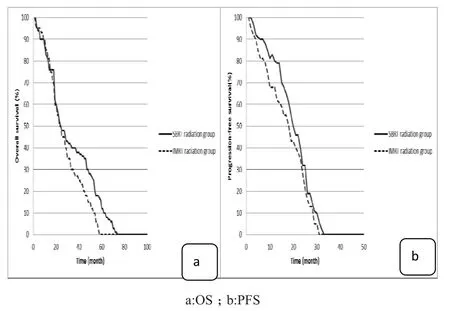
图2 IMRT组与SBRT(伽马刀)组OS、PFS分析(Kalpan-Meier法)
3 讨论
脑转移是NSCLC晚期重要表现,也是疾病进展和死亡的主要原因。综合治疗结合脑转移放疗,能够改善患者预后[9]。但脑放疗所致神经认知功能损害仍是不可忽视的一大问题,且有研究认为,脑放疗与全身治疗同时进行可导致毒性反应进一步加剧[10],故目前临床关于NSCLC脑转移放疗时机的选择尚存在较大争议。
此次研究观察早期放疗与晚期放疗,两组患者近期疗效及不良反应发生率比较均未见明显差异,而早期放疗组OS、PFS优于晚期放疗组,考虑与早期放疗能够更好地控制脑转移进展有关,同时,两组患者不良反应均以1~2级为主。有研究显示,于全身治疗开始后2周内实施放疗,患者脑转移进展倾向于颅外转移,而全身治疗开始后2周后实施放疗,患者脑转移进展则倾向于颅内转移[11-12],其原因可能为:早期放疗的实施可造成血脑屏障功能破坏,使得化疗药物、靶向治疗药物更易透过血脑屏障达到病灶,从而有效控制颅内转移。较颅内转移而言,颅外转移的诊治难度均更低,故患者往往可获得更为理想的生存质量[13]。
NSCLC属中度放射敏感肿瘤,肿瘤细胞分为富氧细胞和乏氧细胞,前者对常规剂量敏感,后者需高剂量方可产生杀伤效应[14]。IMRT具有精确定位、精准计划、精确照射等特点,能够实现靶区高剂量、靶区外低剂量照射,在满足肿瘤局部控制的同时,有效减少正常组织损伤;伽玛刀立体定向放疗系统是我国自主研发的立体定向设备,具有高度剂量聚集特性和三维适形功能,可实现超大剂量小靶区单次照射[15-16]。在NSCLC脑转移放疗时机研究的基础上,此次研究就两种放疗方案的临床应用价值进行了对比,结果显示,采用伽玛刀立体定向放疗系统实施的SBRT的近期疗效优于IMRT,患者OS、PFS更为理想且不良反应发生率并未增加。其优势在于放射治疗剂量分布高度集中,呈同心圆状紧密排列,而峰值以外的剂量梯度锐减,故能够在有效提高肿瘤组织治疗剂量的基础上,降低周围正常组织照射剂量、缩短治疗时间[17]。此外,对NSCLC而言,若需达到50%以上的肿瘤控制率,常规分割剂量需超过84 Gy,SBRT采用大分割放疗技术,能够满足抑制肿瘤细胞再增殖、保护正常组织的要求,而IMRT常规分割剂量往往难以达到84 Gy,也是导致近期疗效与生存情况不及SBRT的重要原因[18]。
综上所述,对于NSCLC脑转移患者,在全身治疗开展早期给予SBRT,能够改善患者生存质量,同时并不会导致不良反应的增加。

