高脲酶活性褐土的宏基因组测序与微生物来源脲酶基因的筛选
轩贝贝,郭建华,王爱国,牟文君,戴华鑫,闫 鼎,蔡宪杰,奚家勤,薛超群,周汉平,张艳玲,胡利伟*,宋纪真
1. 中国烟草总公司郑州烟草研究院,郑州高新技术产业开发区枫杨街2 号450001
2. 上海烟草集团有限责任公司采购中心, 上海市杨浦区长阳路717 号 200082
脲酶(Urease),是土壤中水解尿素的主要酶类,可将施入土壤的尿素水解成氨离子,然后氨离子被氨氧化细菌硝化成NO3-。有研究表明,目前我国尿素肥效一般为20%~35%,通常情况下常低于30%,其重要原因之一是土壤脲酶过多或者活性过高导致尿素分解过快,致使其利用率降低[1-2]。一般认为,土壤脲酶与其他从生物体中分离的纯脲酶在性质上存在很大差异,土壤脲酶只对尿素而不能对尿素衍生物起催化作用。有研究表明,土壤脲酶活性与有机物、全氮、速效磷含量和土壤微生物数量呈正相关,是评价土壤氮素状况、土壤生产力等的重要指标[3]。土壤脲酶通常是由简单蛋白构成的生物催化剂,一般由土壤微生物产生,而不同微生物所产生的脲酶单体结构、数目与类型不完全相同。脲酶基因簇由结构基因、辅助基因和调节基因三部分组成。一般情况下,脲酶结构基因位于调节基因的上游,结构基因编码α、β、γ亚基,构成没有活性的脲酶酶原;辅助基因通常编码UreD、UreE、UreF、UreG 和UreH 等亚基,其作用是协助镍离子转运到无活性的脲酶酶原上,以激活脲酶[4-6]。目前对产脲酶细菌的研究相对较多,克氏杆菌(Klebsiella)和巴氏杆菌(Pasteurella)所产生的脲酶结构只有结构基因编码的三聚体[7-8]。另外腐生性葡萄球菌(Staphylococcus saprophyticus)和雷葡萄球菌(Staphylococcus leei)产生的脲酶结构为四聚体和五聚体[9-11]。尽管亚基单位数存在差异,但是从蛋白序列比对结果来看,真菌和细菌来源的脲酶具有较高的同源性[12]。土壤中好氧性微生物、微好氧性微生物、厌氧性微生物均能水解尿素,土壤细菌、真菌甚至古细菌都能分泌脲酶[13]。Alizadeh等[14]对新西兰牧场土壤的研究发现,肠杆菌(Enterobacter ludwigii)、绿针假单胞菌(Pseudomonas chlororaphis)、变形斑沙雷菌(Serratia proteamaculans)、克氏耶尔森菌(Yersinia kristensenii)等9 种细菌以及瓜枝孢菌(Cladosporium cladosporioides)、黄色镰孢菌(Fusarium culmorum)、肉色拟青霉(Paecilomyces carneus)和小刺青霉(Penicillium spinulosum)等24 种真菌参与了牧场土壤中尿素的代谢,并且具有较强的脲酶活性;李萌等[15-16]从苗圃中分离得到芽孢杆菌(Bacillus)和芽孢八叠球菌(Sporosarcina)等,其分泌脲酶的酶活性均较高,表明产脲酶微生物在土壤中是广泛存在的。
目前以Roche/454 FLX、Illumina/Solexa 和SOLID system 等为代表的第二代测序技术已比较成熟,二代测序技术通量高、成本较低[17-19],也越来越多地被应用于宏基因组学的研究。宏基因组学一般是通过采集环境样品,以整个环境微生物为研究对象,以测序分析为研究手段,研究环境中微生物的多样性、种群结构、进化关系、基因功能及分类等[20]。绝大多数的环境微生物处于可检测但不可分离状态,导致通过分离培养来研究相关功能微生物的效果并不理想,而宏基因学技术则是直接提取环境样本DNA 进行测序,克服了传统培养方法的缺陷,且通量高,信息获取也较为全面。因此,在环境微生物和医学微生物等领域得到较为广泛应用[21-22]。褐土是河南烟叶产区的代表性土壤,分布于郑州、三门峡、洛阳、许昌、平顶山、安阳等地[23]。有研究表明,与潮土和棕壤相比较,褐土施用尿素后,氨释放较快[24],这与褐土中产脲酶微生物的种类与数量是否有关目前尚不清楚。为此,在郑州、洛阳、许昌、平顶山和安阳等产区采集褐土样品,测定其脲酶活性,并将脲酶活性较高的土壤样品用富集培养基培养,提取土壤DNA。利用Hiseq XTen 平台进行宏基因组测序,深度挖掘并筛选脲酶基因,然后对其进行物种注释,旨在从分子水平上揭示褐土中产脲酶微生物的群落构成与物种来源。
1 材料与方法
1.1 土壤样品的采集
2018 年6~10月在河南省平顶山市郏县、洛阳市洛宁县、许昌市襄城县、郑州市上街区和荥阳市、安阳林州市等产区进行土壤样品采集,取0~10 cm表层土壤样品,采用5 点混合采样法,将混合土壤样品剔除砂石和植物残体后装入塑料袋,密封后带回实验室置于低温通风处(10~15 ℃)保存。每个地级市取样10 份,共取土样50 份。
1.2 土壤脲酶活性的测定
将土壤样品在干燥箱(北京普立泰科仪器有限公司)中风干,过2 mm筛后放在通风、干燥处待测,采用靛酚蓝比色法进行土壤脲酶活性的检测,按照土壤脲酶测试盒(苏州科铭生物技术有限公司)的说明书进行检测,每个土壤样品分别测定3 次生物学重复。
1.3 产脲酶菌的富集培养
根据文献[25]进行产脲酶菌富集培养基的配制,即在0.95 L去离子水中加入蛋白胨1.0 g,氯化钠1.2 g,磷酸二氢钾0.8 g,葡萄糖1.5 g,硫酸镍0.1 g,酚红0.016 g,然后调节pH 至7.0,121 ℃高压灭菌20 min后,待温度降至30 ℃以下时,加入50 mL 过滤除菌的尿素溶液(内含20 g 尿素)。
分别从洛阳、许昌、郑州、安阳和平顶山等产区采集的土样中选取脲酶活性较高的土样,即XC-10、ZZ-07、AY-06、LY-07 和PDS-01 等5 个样品,每个土壤样品分别称取3 次,每次称取10 g,共计15 份,分别加入含有50 mL 高浓度尿素液体培养基的250 mL三角瓶中,在30 ℃、180 r/min 条件下摇菌培养24 h,然后将其混合后直接提取DNA。采用土壤DNA 提取试剂盒(美国OMEGA 生物科技公司)提取DNA,具体操作按照试剂盒说明书进行。
1.4 宏基因组测序
采用Covaris ME220(美国Covaris 公司)将DNA片段打断,用Agencourt AMPure XP 核酸纯化试剂盒(德国Beckman Coulter 公司)将破碎后的DNA 片段浓缩回收。利用Next®UltraTMIIDNA 文库制备试剂盒(英国NEB 公司)构建高质量文库,接着采用Next Q5 Hot Start HiFi PCR 预混液(英国NEB 公司)进行文库的扩增并纯化扩增产物,使用生物分析仪(Agilent 2100,美国Agilent 公司)确定扩增产物片段大小、纯度和浓度,最后采用Hiseq XTen 平台(美国Illumina公司)进行测序。
1.5 基因预测与生物信息学分析
由于测序结果中存在一定比例的测序错误,所以获得测序原始数据后,采用FastQC 软件对原始数据进行质量评估与过滤,过滤后得到有效数据,然后对各样本的有效序列进行拼接组装[26-27],获得拼接后的重叠群即Contigs,明确各个Contigs 的先后顺序,并综合评定多个Kmer 的组装结果。采用Prodigal 对最佳拼接结果进行ORF 预测[28],并将长度≥100 bp的基因序列翻译成氨基酸序列。采用CD-HIT 软件对基因预测结果进行去冗,获得非冗余的基因集[29]。采用Bowtie2 将各样本序列比对到非冗余基因集序列上[30-31]。将获得的基因翻译成蛋白序列与包括NR等在内的相关数据库进行比对,获得基因功能及物种注释信息[32-34]。
2 结果与分析
2.1 褐土脲酶酶活性的检测
从河南平顶山、洛阳、许昌、郑州、安阳等产区采集褐土土壤样品进行脲酶活性检测,每天每克土样中产生1 μg NH3-N 定义为一个酶活性单位。结果表明,脲酶活性最高的为来自洛阳市洛宁县的土壤样品LY07,脲酶活性为67.18 μg·d-1·g-1,最低的是来自平顶山郏县的土壤样品PDS-10,为8.34 μg·d-1·g-1。脲酶活性在0~20、20~40、40~60 和60~80 μg·d-1·g-1之间的土壤样品分别有3、16、28 和3 个,所占比例分别为6%、32%、56%和6%,见图1。其中,郑州、洛阳、许昌、安阳和平顶山等地土壤样品中脲酶活性最高值分别为46.98、67.18、57.68、45.97 和64.15 μg·d-1·g-1,见表1。
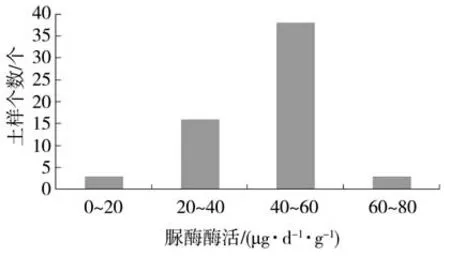
图1 褐土脲酶活性的分布区间Fig.1 Distribution interval of urease activity in cinnamon soil
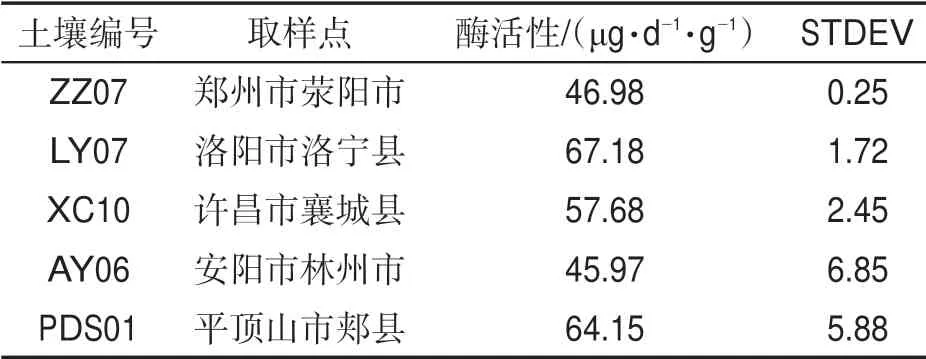
表1 褐土取样点及脲酶活性Tab.1 Sampling sites and urease activity of cinnamon soil
2.2 褐土中产脲酶微生物的富集培养与宏基因组测序
选取各产区的脲酶活性最高的土壤样品XC10、ZZ07、AY06、LY07 和PDS01,采用高浓度尿素液体培养基进行富集培养,混合后提取土壤DNA 并进行宏基因组测序。初步获得总数据量约31.43 Gb,拼接后获得855.32 Mb 基因组数据,组装后的N50为1 251 bp,N90为558 bp,平均长度1 138 bp,GC 含量为54.96%,见表2。

表2 宏基因组的测序结果Tab.2 Results of metagenome sequencing
2.3 基因预测与脲酶蛋白筛选
使用Prodigal 对拼接的Contigs 进行序列翻译和ORF 预测,拼接获得约855 Mb 基因组数据,共预测基因1 375 921 个,并筛选到406 个脲酶结构蛋白与437 个脲酶辅助蛋白。
筛选到的406个脲酶结构蛋白中有234个α亚基、85 个β亚基、87 个γ亚基;437 个脲酶辅助蛋白中有110 个UreD 亚基、81 个UreE 亚基、102 个UreF 亚基、114 个UreG 亚基、19 个UreH 亚基以及11 个UreJ 亚基,见图2。利用NCBI 中的NR 数据库中已经收录的蛋白序列与筛选的脲酶蛋白序列进行BLASTP 分析,结果表明,406 个脲酶结构蛋白和NCBI 的NR 数据库中收录蛋白的同源性为40.7%~100%,437 个脲酶辅助蛋白和NR 数据库中已收录蛋白的同源性为29.4%~100%。
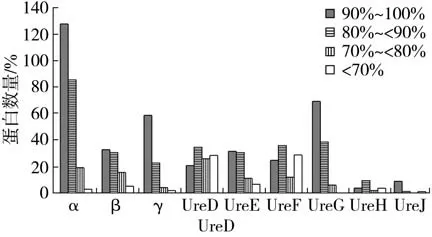
图2 不同脲酶蛋白亚基数量与NR 数据库中的序列同源性Fig.2 Number and sequence homology in NR database of different urease protein subunits
2.4 脲酶和脲酶辅助蛋白的来源
利用NCBI 中的NR 数据库将406 个脲酶结构蛋白和437 个脲酶辅助蛋白进行BLASTP 比对,结果表明,褐土中与细菌来源的脲酶蛋白同源性较高的有797 个,包括384 个脲酶结构蛋白和413 个辅助蛋白;19 个脲酶结构蛋白和23 个脲酶辅助蛋白与古细菌来源的脲酶蛋白同源性较高;与真菌来源的脲酶蛋白同源性较高的有4 个,包括3 个脲酶结构蛋白和1个脲酶辅助蛋白。
将同源性大于95%的细菌来源的脲酶蛋白进行归类,共筛选出190 个脲酶蛋白,包括脲酶结构蛋白106 个,脲酶辅助蛋白84 个。注释到的细菌主要有链霉菌属(Streptomyces)、节杆菌属(Arthrobacter)、不动杆菌属(Acinetobacter)、假单胞菌属(Pseudomonas)、丛毛单胞菌属(Comamonas)和贪铜菌属(Cupriavidus),表明这些属的细菌在褐土尿素水解过程中发挥着关键作用。其中来源于链霉菌属(Streptomyces)、节杆菌属(Arthrobacter)、不动杆菌属(Acinetobacter)、假单胞菌属(Pseudomonas)、丛毛单胞菌属(Comamonas)和贪铜菌属(Cupriavidus)等的脲酶蛋白数量均大于10 个,分别为48、32、19、16、12 和10 个,由不同数量的脲酶结构蛋白和脲酶辅助蛋白组成。不同细菌来源的脲酶结构蛋白和脲酶辅助蛋白数量见表3。
将同源性小于95%的细菌来源的脲酶蛋白进行归类,结果见表3。表3表明,与芽孢杆菌属(Bacillus)、节杆菌属(Arthrobacter)、链霉菌属(Streptomyces)、芽孢八叠球菌属(Sporosarcina)、类芽孢杆菌属(Paenibacillus)、假单胞菌属(Pseudomonas)、鞘氨醇杆菌属(Sphingobacterium)和硝化螺旋菌属(Nitrospira)等来源的脲酶蛋白的序列同源性相对较高。说明褐土中产脲酶细菌可能与上述属的亲缘关系较近。此外,还筛选到42 个来源于古细菌的脲酶蛋白,脲酶结构蛋白亚基α、β、γ和脲酶辅助蛋白亚基UreD、UreE、UreF 和UreG 等均被筛选到,其中29 个脲酶蛋白来源于亚硝化球菌属(Nitrososphaera);另外有4 个脲酶蛋白来源于氨氧化古菌属(Nitrosopumilus),3 个脲酶蛋白来源于奇古菌(Thaumarchaeota archaeon MY3),见表4。
褐土中真菌来源的脲酶蛋白共筛选到3 个脲酶结构蛋白和1 个脲酶辅助蛋白,与NR 数据库中收录蛋白的同源性为81.2%~94.4%。1个α亚基(CSU_orf_949809)和UreG 亚基(CSU_orf_743410)与足马杜拉分枝菌(Madurella mycetomatis)来源的脲酶蛋白同源性较高,而另外1 个α(CSU_orf_949808)和β亚基(CSU_orf_968211)分别来源于蓝莓枝枯病菌(Neofusicoccum parvum)和嗜热毛壳菌(Chaetomium thermophilum)。
2.5 富集培养后褐土中产脲酶微生物的丰度
从图3中可以看出,用尿素培养基富集培养的褐土中优势菌群为芽孢杆菌属(Bacillus),占17.48%;其次为短芽孢杆菌属(Brevibacillus),占13.64%,以及节 杆 菌 属(Arthrobacter,8.07%)、 链 霉 菌 属(Streptomyces,7.88%)、丛毛单胞菌属(Comamonas,6.62%)、类芽孢杆菌属(Paenibacillus,4.15%)和不动杆菌属(Acinetobacter,3.46%)等6 个属所占比例大于60%;其他所占比例超过1%的属有黄杆菌属(Flavobacterium)、贪铜菌属(Cupriavidus)、芽孢八叠球 菌 属 (Sporosarcina)、鞘 氨 醇 杆 菌 属(Sphingobacterium)、假单胞菌属(Pseudomonas)和霉菌属(Agromyces)等。
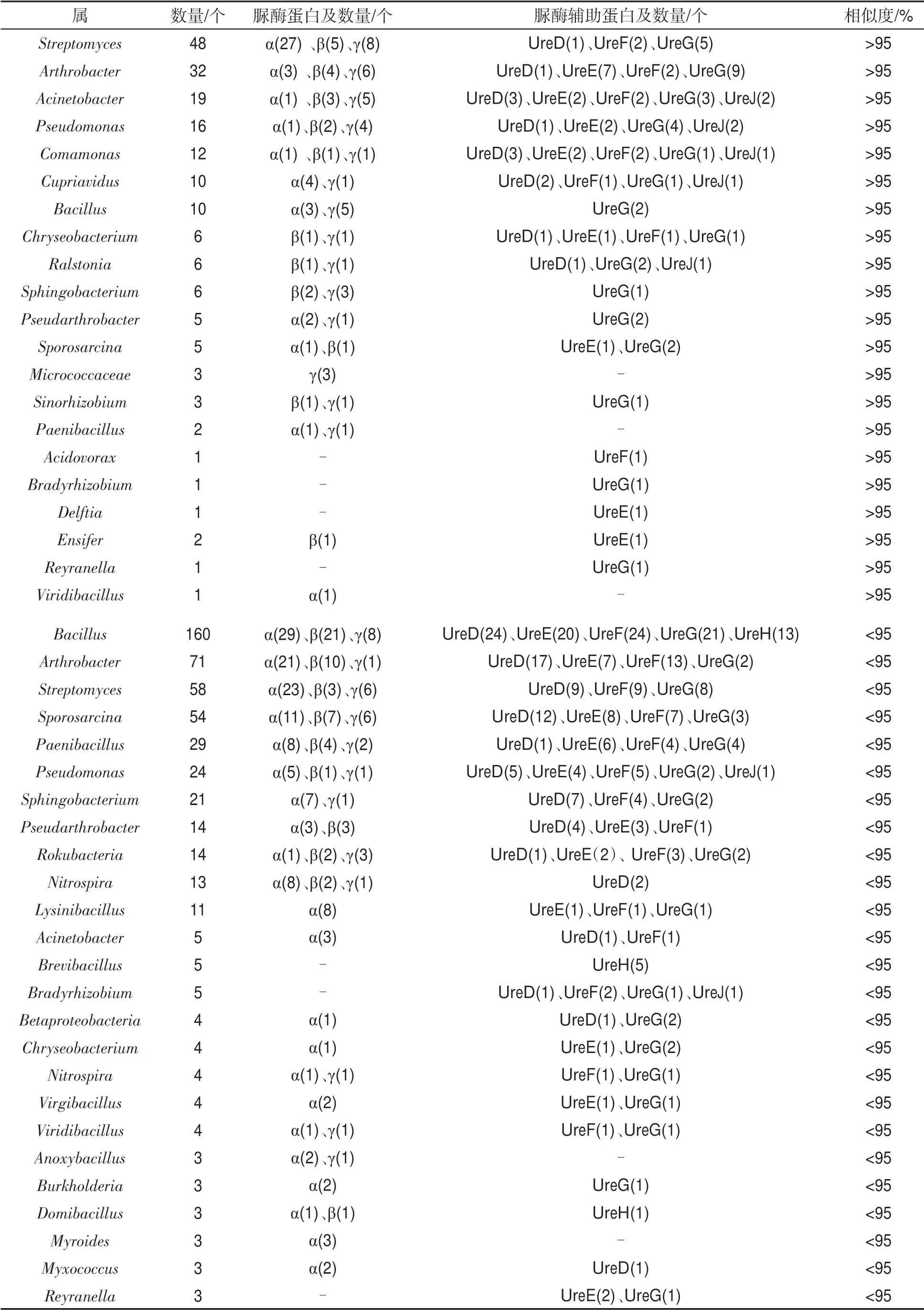
表3 来源于细菌的脲酶蛋白亚基及数量①Tab.3 Number and subunits of urease protein from bacteria
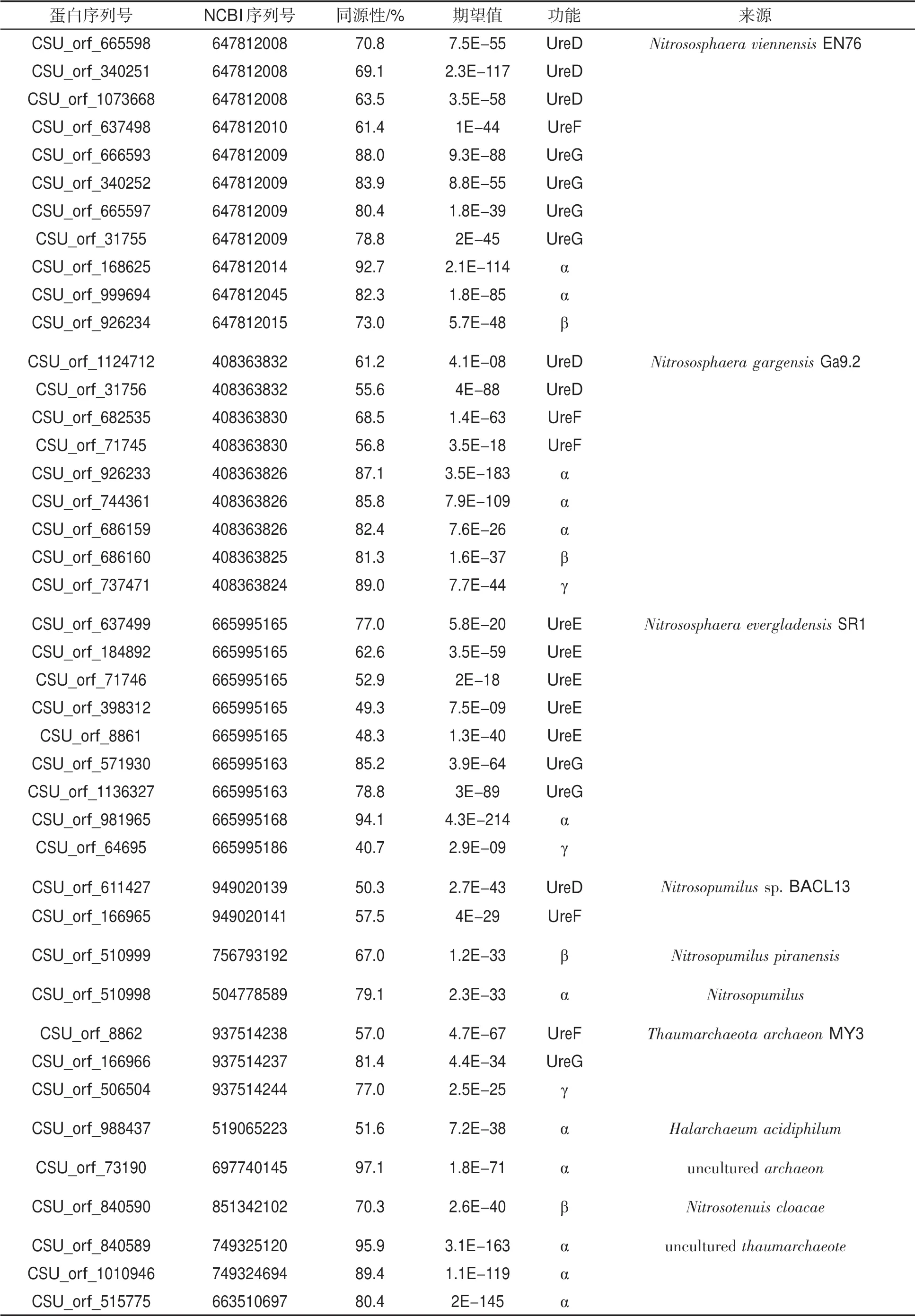
表4 古细菌来源的脲酶蛋白及同源性Tab.4 Urease protein subunits from archaea and sequence homology

图3 富集培养后褐土中产脲酶微生物的丰度Fig.3 Abundance of urease-producing microbes in richly cultured cinnamon soil
3 讨论
土壤中存在大量的产生脲酶微生物,土壤脲酶作为土壤中最重要的酶类之一,其活性已成为表征土壤氮素状况等的重要指标[35]。土壤有机质、全氮、全磷含量会直接或间接影响脲酶活性,而不同土壤类型其脲酶活性存在较大差异[36],土壤中的脲酶活性随着尿素及磷肥施用量的增加而有所降低[37]。本研究结果显示,河南省多地土壤脲酶活性在8.34~67.18 μg·d-1·g-1之间,在脲酶活性较高的土壤样品中筛选到406 个脲酶结构蛋白与437 个脲酶辅助蛋白,这些脲酶蛋白大多来源于产脲酶细菌,这与前人研究结果基本一致[38]。
褐土中细菌来源的脲酶蛋白与NCBI 收录的脲酶同源性在95%以上的有190 个,仅占23.84%,表明褐土土壤中存在着大量产脲酶细菌还未被发掘和利用。物种注释结果显示,褐土中产脲酶细菌主要为链霉菌属(Streptomyces)、节杆菌属(Arthrobacter)、不动杆菌属(Acinetobacter)、假单胞菌属(Pseudomonas)、丛毛单胞菌属(Comamonas)、贪铜菌属(Cupriavidus)、芽孢杆菌属(Bacillus)、金黄杆菌属(Chryseobacterium)、劳尔氏菌属(Ralstonia)、鞘氨醇杆菌属(Sphingobacterium)和芽孢八叠球菌属(Sporosarcina)等,这些产脲酶菌广泛存在于不同类型的土壤中。其中假单胞菌属(Pseudomonas)和贪铜菌属(Cupriavidus)在新西兰牧场土壤中曾被分离到[4];芽孢杆菌属(Bacillus)在马来西亚热带沼泽地泥炭中被分离到[25];芽孢八叠球菌属(Sporosarcina)和芽孢杆菌属(Bacillus)在我国苗圃土壤中被分离到[15-16]。除以上筛选注释的产脲酶微生物之外,对相似度在95%以下的脲酶蛋白进行归类结果显示,褐土中还可能存在与鞘氨醇杆菌属(Sphingobacterium)、类芽孢杆菌属(Paenibacillus)等或者与其亲缘关系较近的产脲酶微生物。还发现了古细菌中亚硝化球菌属(Nitrososphaera)和氨氧化古菌属(Nitrosopumilus)可能也参与了尿素的降解过程。宏基因组测序结果中筛选的真菌来源的脲酶结构蛋白和脲酶辅助蛋白均较少,可能是因为富集培养基不适合真菌的生长繁殖,且真菌基因组较大,拼接获得单个脲酶蛋白的几率可能会随之降低[39],也有研究显示真菌在不同环境中的数量变化较大[40]。因此,在针对真菌的富集培养基优化、挖掘真菌来源的脲酶方面尚有待进一步研究。
4 结论
河南褐土中产脲酶微生物的来源丰富,通过分析宏基因组测序数据,筛选到406 个脲酶结构蛋白和437 个脲酶辅助蛋白基因。物种注释表明,褐土中产脲酶细菌最多,主要有链霉菌属(Streptomyces)、节杆菌属(Arthrobacter)、不动杆菌属(Acinetobacter)等。褐土中还存在部分产脲酶古细菌,与亚硝化球菌属(Nitrososphaera)和氨氧化古菌属(Nitrosopumilus)等亲缘关系较近,这说明古细菌可能也参与了褐土中尿素的降解;还鉴定出极少量的产脲酶真菌,与其亲缘关系较近的有足马杜拉分枝菌(Madurella mycetomatis)、蓝莓枝枯病菌(Neofusicoccum parvum)和嗜热毛壳菌(Chaetomium thermophilum)等。筛选到的脲酶结构蛋白和脲酶辅助蛋白显示,褐土中产脲酶微生物具有高度多样性,也表明参与褐土尿素降解的脲酶是一个极其复杂的多物种来源的酶系复合体,同时也证明富集培养后进行宏基因组测序对脲酶基因的挖掘和物种注释是较为可行和有效的方法。

