基于核心素养理念的教学设计
——以“二氧化硫”教学为例
高兆芬1,鞠亚青1,徐敏
(1.上饶师范学院 化学与环境学院,江西 上饶 334001;2.上饶中学,江西 上饶 334000)
随着社会的变迁,教育的任务不仅仅是传承知识,把知识转化成生产力,更应该注重提升公民的科学素养。2018年1月发布的《普通高中课程标准(2017版)》明确提出了培养高中化学学科核心素养目标,以“素养为本”是化学课堂所秉持的教学基本理念。值得注意的是,基础教育阶段是青少年形成、发展素养的关键时期,因此要在基础教育中重视培养学生的学科核心素养。中学化学是中学学科领域的一门重要课程,也是提升化学学科核心素养的载体,教师在进行教学设计时,要以培养学生学科核心素养为主线设计教学。
下面以人教版化学必修1第四章第三节中的“二氧化硫”的教学设计为例来谈谈如何在课堂教学中渗透对化学学科的核心素养的培养。
1 教学背景分析
1.1 教学内容分析
二氧化硫的性质被安排在钠、镁、铝、氯等元素及其化合物性质之后,属于元素化合物的知识体系,其内容既承接了硫单质的性质,又进一步揭示非金属化合物的重要性质及其在生产生活中的运用,是高中化学的一个重要知识点。二氧化硫是集氧化性、还原性、漂白性于一身的酸性氧化物,通过对二氧化硫性质的认知,巩固和提高对氧化还原反应知识认识,同时也将为本专题后续章节“硫酸的制备”及“氮及其化合物”等相关知识的学习提供必要的基础。
1.2 学生情况分析
高一年级的学生思维比较活跃,具备一定的抽象思维能力,但对形象具体、有实验的教学模式比较感兴趣。在前面的教学过程中,学生已经完成了一些元素化合物的学习,形成了一定的学习元素化合物知识的方式,知道“宏观-微观-符号”三重表征对于学习元素化合物知识的意义所在,宏观辨识与微观探析能力得到一定的提升,具备了基础科学探究所必备的素养。但是学生的思维不够严谨,缺乏正确的学习思维方式,科学探究能力也需要加强,因此需要进一步加强实验探究,较全面地掌握学习的思维方式,增强对化学学科本身认识。
2 基于核心素养理念的教学思路及教学目标设计
2.1 教学思路
(1)通过实验的改进与探究,培养学生科学探究和创新意识。(2)运用“微观-宏观-符号”三重表征的思维方法学习物质的性质。(3)建立物质之间的联系,认识物质的变化规律。(4)学会运用所学知识进行推理,形成物质结构决定性质,性质决定用途的观念并构建起对物质性质的模型认知。
2.2 教学目标
化学学科核心素养其着重点在于培养学生学科思维方式和创新意识,据此设计的教学目标如图1所示:
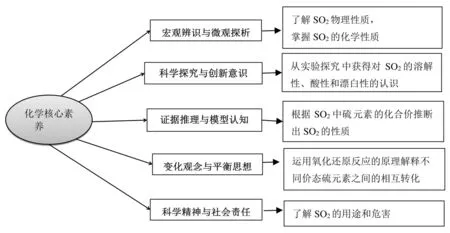
图1 二氧化硫性质的教学目标[1]
3 教学重难点
本节课的重点是二氧化硫的性质,难点是可逆反应。
4 基于核心素养的课堂教学设计
4.1 以培养“科学探究与创新意识”的素养为理念,设计创新性实验。
教学情景一:二氧化硫的水溶性
[实验一]在一个装满SO2的矿泉水瓶中迅速地加一点水振荡,观察实验现象。并思考为什么会有这个现象发生?
[学生]产生疑问,鼓励学生讨论,激发学习兴趣。
[实验二]将两变瘪的矿泉水瓶(装同样多的水,变瘪的程度大致相同。一个水中溶解了SO2,一个只有水)同时放在50℃的热水中,观察现象。
设计意图:采用实验导入式教学,激发学生对新课内容的兴趣,从实验一中我们可以很容易观察到瓶子变瘪,并且发出“咔咔咔”的声音,这是我们从视觉和听觉都可以观察到的现象,比书本上的实验更加形象生动,再由实验二引出SO2与H2O反应生成H2SO3是不稳定的(特别申明H2SO3就是在常温情况下也会分解),为讲解可逆反应做铺垫。这些实验设计增加了学生对知识的好奇心和探究欲望,同时培养了学生的创新意识。
教学情境二:二氧化硫的酸性
[设问]初中我们学习了CO2的性质,SO2与CO2都是酸性氧化物,同学们可以推测SO2水溶液呈什么性呢?
[学生]酸性。
[追问]用什么方法可以验证SO2水溶液呈酸性?
[学生]用酸碱指示剂或pH试纸来检测。
[设问]怎样设计实验说明SO2的水溶液的酸性强弱呢?
[过渡]教师引导学生回顾在初中学习过用较强的酸制取较弱的酸的原理。
[追问]同学们能否用SO2与BaCl2反应来证明SO2水溶液酸性的强弱?
[学生]思考讨论。
设计意图:通过这样的教学设计让学生认识SO2水溶液的酸性,比直接描述SO2水溶液呈酸性更能引起学生注意,再设计SO2与BaCl2能否反应引发学生思维的冲突,从另一视角说明SO2水溶液的酸性没有盐酸强,加深学生对SO2水溶液酸性的理解。其过程含有创新意识,能给学生以启示。
教学情境三:二氧化硫的漂白性
[引导]在学习氯的性质的时候,我们知道新制的氯水具有漂白性,现在同学们将新制的SO2水溶液和新制氯水分别加到品红溶液中,观察现象。
[学生]两种溶液都褪色。
[设问]上述二者的漂白结果会一样吗?我们再分别给两支褪色的试管进行加热,观察现象。
[学生]加入SO2水溶液的试管加热后品红恢复成原来的颜色。而加入新制氯水的试管不恢复成原来的颜色。
[归纳]将上述两个实验进行进行对比,并完成表1的填写。

表1 氯水和二氧化硫漂白性的比较
设计意图:利用SO2与氯水漂白性实验的对比,加深学生对SO2漂白性的认识,让学生学会对比、区分异同。同时增加了氯水与品红的实验,让学生在创新的实验中认识物质的性质并体会探究的乐趣,增强探究与创新的意识。
4.2 以培养“证据推理与模型认知”的素养为理念,学会推测性质
教学情境四:借助CO2的性质推理SO2的性质
[引入]通过前面的实验同学们已经知道SO2的水溶液呈酸性,更加证实了SO2与CO2一样都是酸性氧化物,根据对CO2性质的认知,请同学们列出SO2作为酸性氧化物所具备的性质并完成表2的填写。
[学生]完成表2的填写。

表2 CO2与SO2性质对比表
设计意图:利用学生对CO2性质的认知,即运用“先行组织者”教学模式,建立起酸性氧化物性质的模型,进而推导出SO2作为酸性氧化物应具有的性质,让学生从思维层面上把握学习的方法。
教学情境五:根据氧化还原反应中价态变化规律推测SO2的性质
[设问]根据前面所学习的内容,回忆一下,硫有几种常见的化合价?
[学生]-2、0、+4、+6。
[追问]从二氧化硫中硫的化合价推测它有什么化学性质?
[学生]既有氧化性又有还原性。
[实验]根据氧化还原反应的原理,从下面所列的试剂中选择试剂来探究SO2的还原性和氧化性。
试剂:SO2的水溶液、KMnO4溶液、溴水、碘水、Ba(NO3)2溶液、H2S溶液。
[学生]思考讨论实验方案并实施实验。
实验①在SO2的水溶液中加入少量KMnO4溶液。
实验②在SO2的水溶液中加入少量溴水或碘水。
实验③在SO2的水溶液中加入少量向 Ba(NO3)2溶液。
实验④在SO2的水溶液中加入H2S的水溶液。
学生边实验边完成表3的填写。

表3 二氧化硫的还原性和氧化性
设计意图:结构决定性质,引导同学们从SO2的化合价去推理出它的化学性质,把握学习元素化合物知识的一般规律。SO2的硫的化合价为+4价,+4价在硫的化合价中属于中间价态,根据前面所学氧化还原的知识,同学们可以很容易推理出SO2既有氧化性又有还原性。根据推理进行实验方案的设计,通过实验验证其推理的准确性,学生在这个过程中一定会经历“发现问题-分析问题-提出假设-制定计划-进行实验-观察现象-分析现象-得出结论”等过程,通过不断地探索,同学们的推理能力得到进一步提升,同时,帮助学生用“宏观-微观-符号”三重表征思维方式认识元素化合物的性质。在实验中有意识地加入Ba(NO3)2试剂,就是要拓展学生的发散性思维,建立“模型认知”的思维方式。根据对硝酸在水溶液中的存在形式认知,而导出硝酸根离子和SO2水溶液营造的酸性氛围与其有等同效应,能够将亚硫酸根离子氧化成硫酸根离子,从而生成硫酸钡沉淀。
4.3 以培养“变化观念与平衡思想”的素养为理念,建立物质的转化关系
教学情境六:
[引入]通过硫及其化合物的学习,同学们知道硫元素是多价态元素,依据氧化还原反应理论,选择合适的氧化剂和还原剂就可以实现含硫物质的转化。
[设问]请同学们整理一下含有不同价态硫元素的物质之间是怎样相互转化的?并完成表4的填写。
[学生]思考、讨论。
[归纳]由学生讨论之后,教师引导学生填写表4中的(B)(C)(D)项。
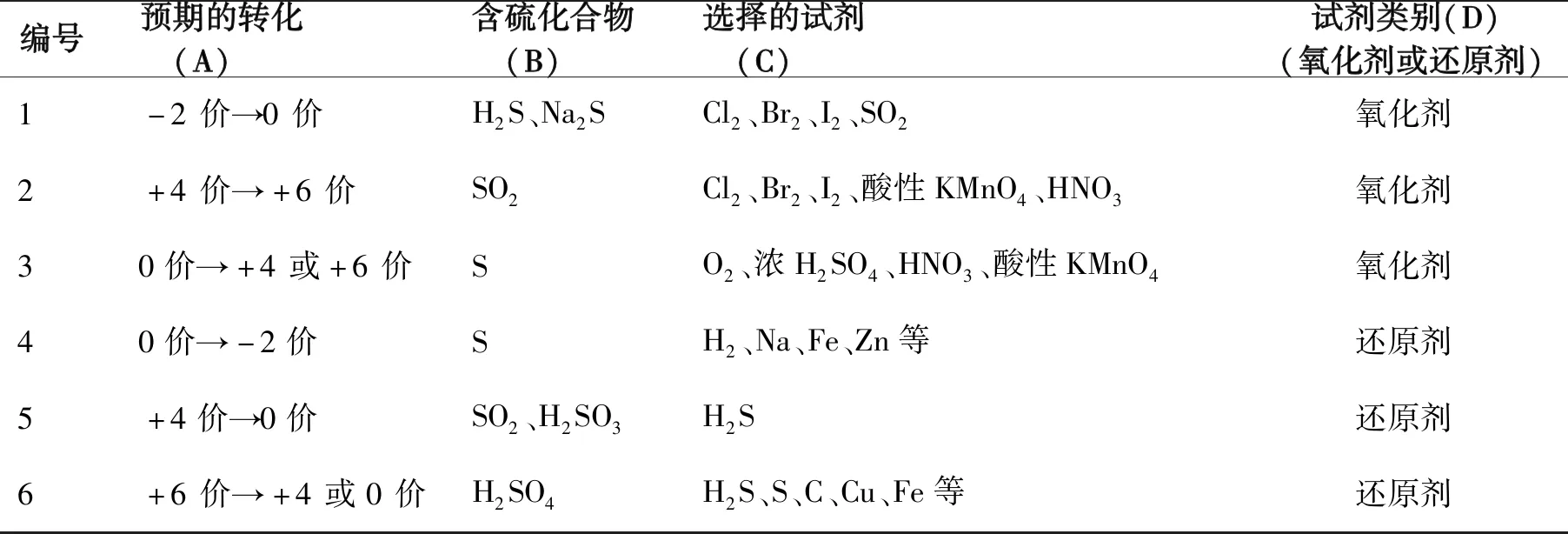
表4 含硫化合物之间的转化[2]
[引导]在完成表4的填写之后,引导学生建立起不同价态硫元素之间的相互转化关系图(图2)。
图2不同价态硫元素之间的相互转化关系
设计意图:SO2是硫元素的重要化合物,通过SO2能建构起不同价态硫元素之间的相互转化关系,让学生学会将知识按照一定的线索进行归类、整理,使零散、孤立的知识变为彼此相互联系的整体,形成一个系统化、结构化的知识网络结构;同时让学生认识物质是会变化的,化学变化是有条件的、可控制的,从变化与平衡相统一的视角考察分析化学反应和解决化学问题。
4.4 以培养“科学态度与社会责任”的素养为理念,学会认识事物的两面性
教学情境七:
[设问]我们知道“结构决定性质,性质决定用途”,请同学根据二氧化硫性质分析二氧化硫有哪些用途?
[学生]积极思考、讨论。
[归纳]结合学生讨论归纳二氧化硫用途:
二氧化硫是一个很好的还原剂,利用二氧化硫的还原性,在红酒中充一点二氧化硫可以防止红酒被氧化;在城市的污水处理中,二氧化硫用来处理排放前的氯化污水,进行脱氯。
在水的存在下,二氧化硫可以使物质褪色,它是纸张和衣物用的漂白剂;二氧化硫可以用作一些干果和食物的防腐剂,能够抑制霉菌和细菌的滋生,防止腐烂;由于二氧化硫容易液化,且汽化热很大,因此适合作为制冷剂。另外在农药,人造纤维,染料等方面也有广泛的使用。
[设问]任何事物都有两面性,接下来讨论一下二氧化硫有什么危害?
[学生]交流讨论,说出自己的看法。
[引导]刚才很多同学都谈到了二氧化硫的危害主要是会形成酸雨,那同学们知道酸雨会给人类带来怎样的危害吗?(引导学生从①危害土壤和植物;②危害人类健康;③腐蚀建筑物、机械和市政设施三个方面思考)
[学生]学生讨论。
[归纳]二氧化硫有毒是大气的主要污染物之一,能形成酸雨。酸雨的危害有三个方面:(1)导致土壤酸化。酸雨能加速土壤矿物质营养元素的流失,改变土壤结构,导致土壤贫瘠化,影响植物正常发育;(2)危害人类的身体健康。酸雨对人类最严重的影响就是呼吸方面的问题,二氧化硫和二氧化氮会引起例如哮喘、干咳、头痛、和眼睛、鼻子、喉咙的过敏。酸雨间接的影响就是它会溶解水中的有毒金属,被水果、蔬菜和动物的组织吸收后,吃下这些东西会对人类的健康产生严重影响;(3)酸雨会腐蚀建筑物、机械和市政设施。酸雨能使非金属建筑材料(混凝土、砂浆和灰砂砖)表面硬化水泥溶解,出现空洞和裂缝,导致强度降低,从而损坏建筑物,造成建筑物的使用寿命下降,影响城市市容和景观,同时可能引发安全危险。
酸雨给地球生态环境和人类社会经济都带来严重的影响和破坏,所以要合理利用好二氧化硫,特别是要减少二氧化硫的排放,以免造成环境污染。
设计意图:学习了二氧化硫的性质,就要让学生明白二氧化硫的性质与用途的关系。这样的设计,既让学生形成性质决定用途的思维方式,又对课堂内容进行了强化,同时使学生认识任何事物都有两面性,告诫学生要将资源进行合理的利用,保护好人类赖以生存的环境,培养学生科学的态度和社会责任感。
5 教学反思
化学核心素养是科学素养的重要组成部分,基于化学核心素养理念下的教学,要求教师要将知识传授与培养能力结合起来,充分发挥学生的主体作用,让学生在学习中体验实验探究的过程,培养学生的创新意识,形成化学学科观念和学科思维,认同化学学科价值和社会责任感。

