肝移植术后多重耐药菌感染分布特征及危险因素
申存毅,王婧,林婷,王丽,田敏,吕毅,王博
(西安交通大学第一附属医院 肝胆外科,陕西 西安 710061)
由于手术创伤大、使用免疫抑制剂等,感染成为肝移植术后早期最重要的并发症[1],尤其是多重耐药菌(multi-drug resistance bacteria,MDRO)感染,可增加受体病死率[2-4]。我国多个移植中心研究显示,感染在肝移植患者细菌性感染中的发生率高达50%以上[5-6]。所以,分析了解肝移植术后MDRO感染的危险因素,并以此制定更具针对性的防控措施,对于减少MDRO感染发生及传播、降低感染相关并发症,提高移植质量具有重要意义。本研究回顾性分析西安交通大学第一附属医院5年间肝移植术后发生MDRO感染的临床资料,探讨其危险因素,为早期提供感染控制策略和指导治疗提供依据,现报道如下。
1 资料和方法
1.1 一般资料
2014年1月至2018年12月在西安交通大学第一附属医院肝胆外科接受同种异体肝移植术的431例患者,所有患者均通过我院伦理委员会审批,供体器官获取由中国人体器官分配与共享系统完成。接受心脏死亡器官捐献(donation after cardiac death,DCD)411例(95.36%),其中男337例(78.19%),女94例(21.81%),平均年龄21~67(46.30±9.97)岁。纳入标准:年龄18岁及以上;术前无感染及细菌定植;病例资料完善。排除标准:术后24 h内死亡;病例资料缺如;对于多次发生多重耐药菌感染的肝移植术后患者,只分析其首次感染。
1.2 术后免疫抑制治疗
肝移植术后应用他克莫司或环孢素A+吗替麦考酚酯(MMF)+皮质激素预防排斥反应,根据监测的血药浓度调整他克莫司或环孢素A剂量。
1.3 术后抗生素预防方案
根据《抗菌药物临床应用指导原则》,首选广谱三代头孢抗菌药物如头孢哌酮舒巴坦或青霉素类哌拉西林钠他唑巴坦钠进行预防性用药,预防感染用药时机均为术前0.5~2 h,手术时间超过3 h术中均追加用药,术后继续预防感染用药;其次依据病原微生物的培养结果及药敏试验结果进一步调整抗感染用药方案。
1.4 研究方法
根据《医院感染诊断标准》,连续2次以上或2处以上检测为相同菌株阳性,对通常敏感的常用的3类或3类以上抗菌药物同时呈现耐药时,确定诊断为肝移植术后多重耐药菌感染[7]。采用回顾性调查研究,根据是否发生多重耐药菌感染,并以此分为MDRO感染组及非MDRO感染组。收集两组患者术前临床资料(性别、年龄、诊断、合并症、实验室指标、肝脏储备功能)、术中临床资料(供体灌洗液感染、手术时间、无肝期、冷缺血时间、输血量、失血量、胆道重建方式、胆道支架)、术后临床资料(机械通气时间、留置尿管时间、留置中心静脉导管(CVC)时间、禁饮食时间、是否再插管、术后ICU留置时间、术后并发症、住院时间)。应用统计学方法分析,确定MDRO感染的高危因素。
1.5 纳入监测的多重耐药菌
耐甲氧西林金黄色葡萄球菌(MRSA)、耐万古霉素肠球菌(VRE)、耐碳青霉烯类鲍曼不动杆菌(CR-AB)、产超广谱β-内酰胺酶(ESBLs)肠杆菌科细菌(如大肠埃希菌和肺炎克雷伯菌)、耐碳青霉烯类肠杆菌科细菌(CRE)和多重耐药铜绿假单胞菌(MDR-PA)。
1.6 质量控制
双人以统一标准采集病历信息,并准确记录于自制调查表中。另一人对收集的资料进行检查,保证资料完整、真实、可靠。
1.7 统计学分析
应用SPSS 21.0软件进行统计分析。计数资料采用频数(n)和百分比(%)表示,单因素分析采用χ2检验或Fisher确切概率法,多因素分析采用Logistic回归模型,P<0.05为差异有统计学意义。
2 结果
2.1 MDRO感染情况
5年间,我中心共发生肝移植术后MDRO感染53例(53/431,12.29%),非MDRO感染组378例(378/431,87.71%)。两组在性别、年龄、原发病情况、是否术前合并高血压、糖尿病等方面无统计学差异。具体见表1。MDRO组院内死亡4例(4/53,7.55%),其中3例与感染直接相关。非MDRO组院内死亡6例(6/378,1.59%)。两组病死率比较有统计学差异(P<0.05)。
2.2 感染发生部位与菌株种类
53例MDRO感染患者中,46例感染发生于术后4周内。肺部感染最多见,占54.72%,其次是胆道感染21.13%,腹腔感染15.49%。送检病原学标本中,共检出多重耐药菌菌株78株,以耐碳青霉烯类鲍曼不动杆菌、耐碳青霉烯肠杆菌、产ESBLs肠杆菌为主。具体菌株分布及构成比见表2。
2.3 MDRO感染的单因素分析
单因素分析显示,术前血清总胆红素水平、MELD评分、Child-Pugh评分、术中输注红细胞>8 U、术中失血量≥3 L、机械通气时间≥10 h、术后ICU留置时间≥7 d、腹腔内出血、急性肾功能衰竭、多脏器功能衰竭、血液净化、留置尿管>3 d、禁食≥2 d、住院时间≥21 d共14个因素为肝移植术后MDRO感染的潜在危险因素,有统计学差异(P<0.05)。见表3。
2.4 MDRO感染的多元Logistic回归分析
以是否发生多重耐药菌感染作为因变量,将单因素分析中具有统计学意义的14个因素作为自变量,进行多因素Logistic模型回归分析。结果显示术后ICU留置时间≥7 d、急性肾衰是肝移植术后多重耐药菌感染的独立危险因素。见表4。
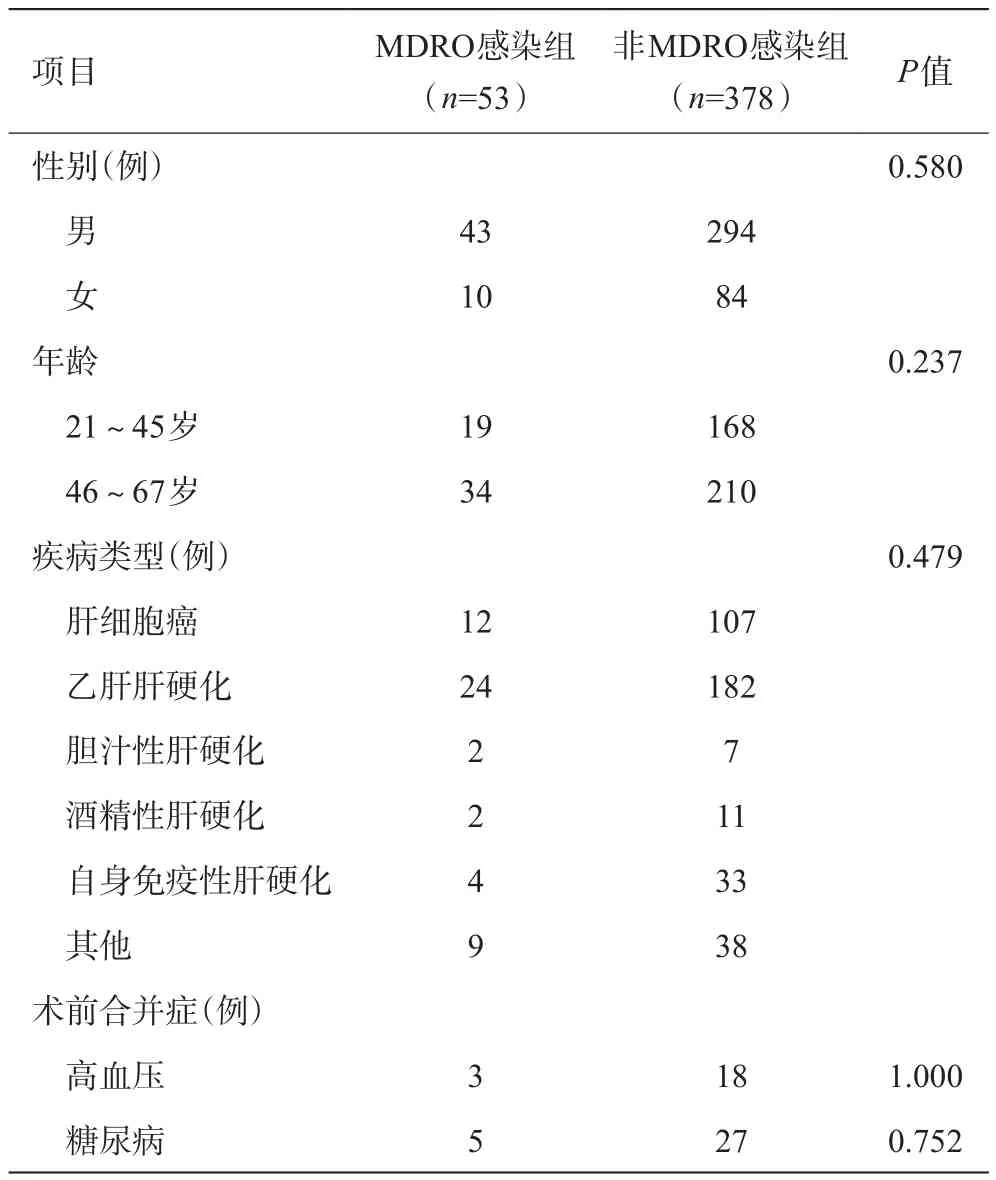
表1 两组一般情况和原发病比较(例)
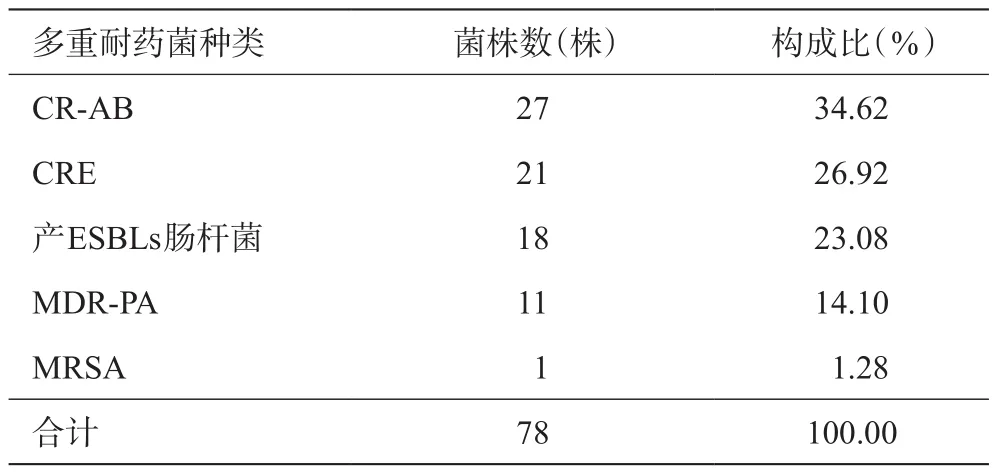
表2 MDRO菌株分布
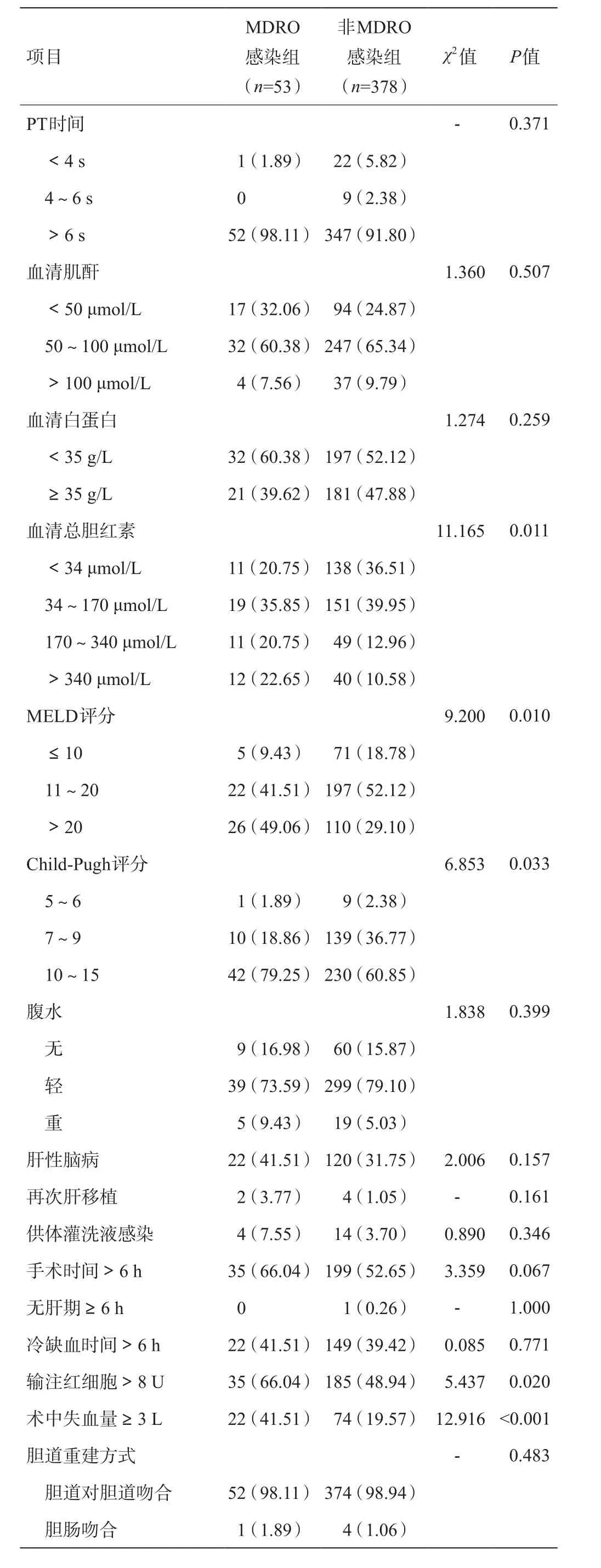
表3 MDRO感染的单因素分析[例(%)]

续表3
3 讨论
近年来,广谱抗菌药物的不合理应用以及侵入性医疗设备的频繁使用等因素使得MDRO感染率大大增加,成为影响肝移植术患者预后的重要原因之一[8-9]。本组53例MDRO感染者中4例死亡,其中3例死亡与感染相关,远高于非MDRO组,具体原因分别为脓毒症、脓毒性休克和多器官功能衰竭。因此,早期预防和控制多重耐药菌感染对于提高肝移植术治疗效果至关重要。
多重耐药菌主要分为革兰阳性菌感染和革兰阴性菌感染,以革兰阴性菌居多。MRSA和VRE是主要两种革兰阳性菌。据报道,实体器官移植受体MRSA感染的流行率为1.3%~22.7%[10]。本组病例中,发生MRSA感染1例,占1.28%。菌株标本来源于痰液,发生于术后2周内,与文献报道基本类似[11]。
文献显示,CR-AB、CRE、产ESBLs肠杆菌为肝移植患者主要的多重耐药革兰阴性菌[12]。近年来,CR-AB的发病率在实体器官移植受体中呈增长趋势,常见于菌血症(0.8%~15.9%)和腹腔内感染(3.7%),CR-AB感染者的病死率为50%~90%[13]。本组病例中,CR-AB检出率最高,78株MDRO菌株中,27株为CR-AB,占34.62%。而且,3例与感染相关的死亡病例中,2例与CR-AB相关,菌株标本来源于痰和胆汁。结果提示,对CR-AB感染的防控是降低肝移植术后多重耐药菌感染病死率的关键,尤其是加强呼吸道管理[14]。本组另外两个高发的革兰阴性菌是产ESBLs肠杆菌和CRE,分别占到26.93%和23.08%。1例死亡与CRE相关,与文献报道的CRE感染导致移植术后高病死率基本相符[15]。
肝移植术后MDRO感染的危险因素涉及受体、供体及移植手术3个方面[16-17]。关于受体因素,本研究的单因素分析结果显示,术前血清总胆红素水平、MELD评分、Child-Pugh评分为受体MDRO感染的危险因素(P<0.05)。但经过多元Logistic回归分析,以上均不是MDRO感染的独立危险因素。供体器官灌洗液培养留取方法是抽取修肝容器内的器官灌洗液进行细菌培养。比较MDRO组和非MDRO组的供体灌洗液感染情况,其中MDRO组供体器官灌洗液感染4例(7.55%),2例受体细菌培养结果与供体灌洗液培养结果一致,1例为产ESBLs肠杆菌,1例为CRE;非MDRO组供体器官灌洗液感染14例(3.70%),主要包括大肠埃希菌、屎肠球菌、白色念珠菌。两组无统计学差异(P=0.346)。
关于移植手术因素,本研究的单因素分析结果显示,输注红细胞>8 U、术中失血≥3 L、机械通气时间≥10 h、术后ICU留置时间≥7 d、腹腔内出血、急性肾功能衰竭、多脏器功能衰竭、血液净化、留置尿管>3 d、禁食≥2 d、住院时间≥21 d为MDRO感染的手术方面危险因素(P<0.05)。经过多元Logistic回归分析,术后MDRO感染的发生的独立危险因素主要与术后ICU留置时间和术后急性肾功能障碍有关(P<0.05)。患者若术后ICU留置时间≥7 d,多重耐药菌感染的风险会增加1.836倍。与文献报道的术后ICU留置时间≥10 d,危险性明显增加结果类似[18]。急性肾功能障碍是独立危险因素,可能原因是体内毒素聚积、水电解质酸碱平衡紊乱,免疫力进一步降低。另外,此类患者常需行连续肾脏替代治疗(CRRT),双腔静脉管路等也可能是原因之一。
关于肝移植术后MDRO感染的防控,借鉴《多重耐药菌医院感染预防与控制中国专家共识》[19],主动筛查与去定植、抗菌药物的规范化管理与应用以及强化感染控制管理是预防MDRO感染的主要措施。主动筛查能够早期发现病原体的定植,监测病原体感染的流行病学变化趋势及防控措施实施的有效性[20]。应该依据患者的病原学检测与药敏实验结果等制定个体化的抗感染治疗方案,减少抗菌药物的滥用或过度应用[21]。强化感染控制管理,如加强手卫生及依从性的管理、强化医务人员及工勤人员的教育与培训等[22]。
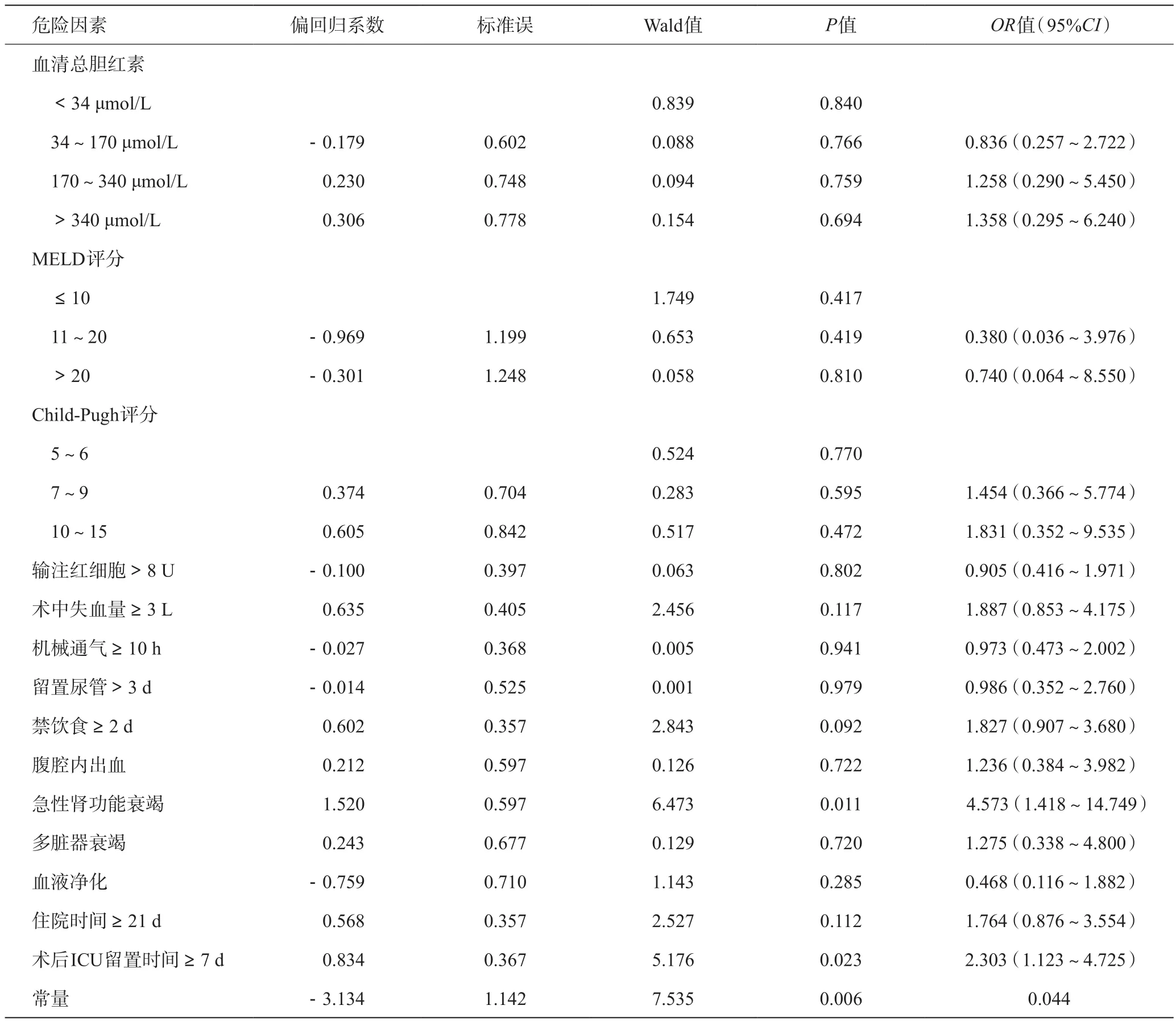
表4 MDRO感染危险因素的多元Logistic回归分析
4 小结
多重耐药菌感染已成为肝移植术后受体预后的极大威胁,为临床治疗和护理带来了严峻的挑战。因此,移植单位都应该根据自己的特点探索MDRO感染的危险因素,早期识别高危患者,调整可干预的防控措施,从而提高患者治愈率,改善预后。结合本次回顾性研究,尽量缩短术后ICU留置时间,保护术后肾功能可作为控制肝移植术后MDRO感染的重要参考。