对叶百部标准汤剂UPLC特征图谱研究
林碧珊,高永坚,陈锦霞,陈科成,张文芳
(国药集团广东环球制药有限公司,广东顺德528303)
对叶百部(Stemona tuberosaLour.)是《中国药典》2020 年版百部Stemonae Radix 项下收载的3 种基原之一,具有润肺下气止咳、杀虫灭虱之功,主要用于止咳祛痰平喘、抗寄生虫、抗病原菌及杀虫等[1]。对叶百部化学成分种类多,主要有蛋白质、氨基酸、香豆素、内酯、多肽、糖、苷类、多糖、生物碱、有机酸、酚类等化学成分[2-3]。目前,文献报道主要通过原植物形态、药材性状、显微性状、生物碱种类及含量的不同进而鉴别百部3种基原[4-5]。
饮片标准汤剂是以中医理论为指导、临床应用为基础,参考现代提取方法,经标准化工艺制备而成的单味中药饮片水煎剂[6]。中药配方颗粒的各项指标及生产过程必须与标准汤剂确定的质量标准相吻合[7-8]。关于百部的基原研究,樊兰兰[9]研究了百部地下不同部位的HPLC指纹图谱,且比较了3种不同基原百部的指纹图谱;钟莹[10]建立了对叶百部的HPLC 指纹图谱,并对比了3 种不同基原百部的HPLC 指纹图谱。本研究采用UPLC 法建立对叶百部标准汤剂的特征图谱,不仅可以为百部配方颗粒的质量标准提供一定的参考依据,同时可以用于不同基原及劣质品的对叶百部药材鉴别,还可用于对叶百部的质量控制,为其质量评价提供科学依据。
1 仪器与试药
1.1 仪器
H-class UPLC 高效液相色谱仪(PDA 二极管阵列检测器,美国Waters公司);AL104电子天平(梅特勒-托利多公司);KQ-500DE 数控超声清洗仪(昆山超声仪器有限公司);M MILLIPORE Synergy UV 超纯水仪(美国默克公司)。
1.2 试药
绿原酸对照品(批号:140709-201404)、对叶百部对照药材(批号:121221-201604)、直立百部对照药材(批号:121588-201502)由中国食品药品检定研究院提供;隐绿原酸对照品(批号:DST170210-035)、新绿源酸对照品(批号:DST180130-015)由成都德思特生物技术有限公司提供;甲醇、乙腈、磷酸均为色谱纯,其他试剂均为分析纯。
1.3 样品
21 批对叶百部药材分别从湖北、湖南、四川、云南等不同产地购得,经国药集团广东环球制药有限公司质管部黄国满助理工程师按照《中国药典》2020 年版对叶百部药材检验15 批符合规定,6 批不符合规定。药材及相关样品具体信息见表1和表2。
2 方法与结果
2.1 标准汤剂的制备
取S1-S15 批对叶百部饮片100 g,置5 L 电控温煎药壶中,加水煎煮两次。第一次煎煮加9倍量水,浸泡30 min 后,先武火煮沸后再文火保持微沸煎煮30 min,用350 目筛网趁热过滤,滤液迅速用水冷却。第二次煎煮加7 倍量水,先武火煮沸后再文火保持微沸煎煮25 min,用350 目筛网趁热过滤,滤液迅速用水冷却,合并两次滤液。将合并后的滤液转移至旋转蒸发仪中浓缩(水浴温度:48 ℃,真空度:-0.1 MPa),浓缩至约200 g 左右,测定含固率,加入纯化水至清膏含固率为15%,分装至10 mL 西林瓶中,每瓶分装体积为2.5 mL,分装完毕后转移至真空冷冻干燥机中冻干,取出,轧铝盖,即得冻干粉。
2.2 色谱条件与系统适应性
色谱柱为CORTECS T3 柱(100 mm×2.1 mm,1.6 μm);乙腈为流动相A,0.1%磷酸为流动相B,梯度洗脱(0~10 min,1%→22%A;10~15 min,22%→50%A;15~18 min,50%→90%A;18~20 min,90%A;20~20.1 min,90%→1%A;20.1~23 min,1%A);柱温为25 ℃;流速为0.25 mL/min;检测波长为210 nm;进样量1 μL;理论塔板数按绿原酸峰计算应不低于10 000。

表1 15批符合规定的对叶百部样品信息表Table 1 Sample information of 15 batches of compliant Stemona tuberosa Lour

表2 6批不符合规定的对叶百部样品信息表Table 2 Sample information of 6 batches of non-compliant Stemona tuberosa Lour
2.3 参照物溶液的制备
2.3.1 对照品溶液的制备 取绿原酸、新绿原酸、隐绿原酸对照品适量,精密称定,分别加80%(体积分数,下同)甲醇制成每1 mL含20 μg的对照品溶液;
2.3.2 对照药材溶液的制备 取对叶百部对照药材0.5 g,精密称定,置20 mL 量瓶中,加入80%甲醇适量,超声处理(500 W,40 kHz)30 min,取出,放冷,用80%甲醇稀释至刻度,摇匀,用0.22 μm 滤膜滤过,即得对叶百部对照药材溶液。
2.4 供试品溶液的制备
取百部标准汤剂冻干粉适量,研细,取约0.1 g,精密称定,置10 mL 量瓶中,加入80%甲醇适量,超声(500 W,40 kHz)处理10 min,取出,放冷,用80%甲醇稀释至刻度,摇匀,用0.22 μm滤膜滤过,即得。
2.5 特征图谱方法学考察
2.5.1 精密度试验 取对叶百部标准汤剂1 份,按“2.4”项方法制备供试品溶液,按“2.2”项色谱条件连续进样6 次,以绿原酸为参照峰,计算各峰与参照峰的相对保留时间及相对峰面积。各色谱峰的相对保留时间和相对峰面积的RSD 均小于3.5%,表明仪器精密度良好。
2.5.2 稳定性试验 取对叶百部标准汤剂1 份,按“2.4”项方法制备供试品溶液,按“2.2”项色谱条件分别在0、2、4、8、12、16、20、24 h 进样检测,以绿原酸为参照峰,计算各峰与参照峰的相对保留时间及相对峰面积。各色谱峰的相对保留时间和相对峰面积的RSD 均小于3.0%,表明供试品液在24 h内稳定性良好。
2.5.3 重复性试验 取同一批对叶百部标准汤剂,分别精密称取6 份,按“2.4”项的方法平行制备供试品溶液,按“2.2”项色谱条件进行测定,以绿原酸为参照峰,计算各峰与参照峰的相对保留时间及相对峰面积。各色谱峰的相对保留时间和相对峰面积的RSD均小于1.0%,表明本方法重复性良好。
2.6 特征图谱的建立与分析
2.6.1 特征峰指认 分别吸取“2.3.1”项对照品溶液和“2.4”项供试品溶液,按“2.2”项色谱条件进样,记录色谱图,见图1。将供试品色谱峰与对照品色谱峰保留时间进行比较,确定供试品图谱中的3 号峰为绿原酸,1号峰为新绿原酸,4号峰为隐绿原酸。
2.6.2 特征图谱的建立 取S1-S15符合规定的对叶百部饮片,按“2.1”项制备15 批标准汤剂样品,按“2.4”项制备供试品溶液,按“2.2”项的色谱条件测定,记录15批标准汤剂色谱图。采用国家药典委员会推荐的“中药色谱指纹图谱相似度评价系统”对15 批对叶百部标准汤图谱进行分析,选择8 个分离度较好的共有色谱峰为特征峰。通过与对叶百部对照药材色谱图进行对比,确定峰1为新绿原酸、峰3为绿原酸、峰4为隐绿原酸,结果见图2~图4。
2.6.3 共有峰相对保留时间和相对峰面积的测定根据《中药注射剂指纹图谱研究的技术要求(暂行)》[11],以绿原酸峰3 为参照峰(S 峰),计算各共有峰的相对保留时间和各相对峰面积,结果见表3~表4。

图1 新绿原酸、绿原酸、隐绿原酸对照与对叶百部标准汤剂图谱Figure 1 Chromatograms of Neochlorogenic acid,Chlorogenic acid, Cryptochlorogenic acid and standard decoction of Stemona tuberose Lour

图2 15批对叶百部标准汤剂UPLC叠加图谱Figure 2 UPLC superimposed chromatograms of 15 batches of standard decoction for Stemona tuberosa Lour

图3 对叶百部对照药材UPLC图谱Figure 5 UPLC chromatogram of the control medicinal material of Stemona tuberosa Lour

图4 对叶百部标准汤剂UPLC对照图谱Figure 4 UPLC comparison chromatogram of standard decoction for Stemona tuberosa Lour
2.6.4 不同产地标准汤剂特征图谱相似度分析 将15 批样品的UPLC 特征图谱数据导入“中药色谱指纹图谱相似度评价系统(2012 版)”,以S1 图谱为参照图谱,时间窗设置为0.1,进行峰匹配,计算得到15 批对叶百部标准汤剂与对照图谱之间的相似度,结果见表5。可见,15 批对叶百部标准汤剂的相似度分别为0.974、0.993、0.998、0.975、0.926、0.977、0.905、0.984、0.977、0.969、0.973、0.992、0.968、0.981、0.972,均大于0.9,表明不同产地的对叶百部药材具有较高的相似性。
2.7 特征图谱的应用
2.7.1 不同基原百部的鉴别 本文所建立的特征图谱,其特征峰的相对保留时间具有特征性,结果见图5,能区分不同基原百部,为百部药材的质量控制提供参考方法。
2.7.2 对叶百部劣质品的鉴别 取“1.3”项的S16-S21等6批不符合规定的对叶百部药材,采用本研究方法与对叶百部对照药材进行特征峰的对比,结果见图6。可见,6批药材的特征峰与对叶百部对照药材特征峰比均少了2 个特征峰(峰6 和峰7),经过鉴定确定为S16-S18 及S20 为走油,S19 为部分走油,S21 为霉败,表明通过本研究方法可以进行对叶百部药材劣质品的鉴定。
3 讨论
考察了检测波长(210、230、250、270 nm)、流动相系统(乙腈-0.1%磷酸、乙腈-0.1%甲酸溶液)及柱温(25、30、35 ℃)的分离效果,结果以检测波长为210 nm、流动相系统为乙腈-0.1%磷酸及柱温为35 ℃时的分离效果较好。
比较提取溶剂(水、50%甲醇、80%甲醇、甲醇、乙醇)、提取方式(超声提取、回流提取)及提取时间(10、20、30 min)的提取效果,结果以提取溶剂为80%甲醇、提取方式为超声提取及提取时间为30 min时的提取效果较好。

表3 15批对叶百部标准汤剂的相对保留时间Table 3 Relative retention time of 15 batches of standard decoction for Stemona tuberosa Lour(n=15)

表5 15批对叶百部标准汤剂的相似度测定结果Table 5 The similarity results of 15 batches of standard decoction for Stemona tuberosa Lour
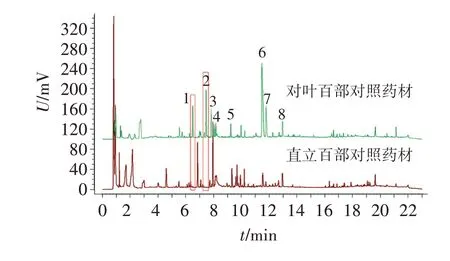
图5 对叶百部与直立百部对照药材UPLC图谱的对比图Figure 5 Comparison of UPLC chromatograms of the control medicinal material of Stemona tuberosa Lour and Stemona sessilifolia

图6 6 批不符合规定的对叶百部与对叶百部对照药材UPLC图谱的对比图Figure 6 Comparison of UPLC chromatograms of 6 batches of Stemona tuberosa Lour samples that do not meet the requirements and Stemona tuberosa Lour contral
本研究对15 批对叶百部标准汤剂样品进行相似度评价计算,结果表明15批对叶百部标准汤剂的相似度均大于0.9,表明不同产地的对叶百部饮片具有较高的相似性,产地差异较少。选择峰3 绿原峰作为S峰,测定共有峰相对保留时间和相对峰面积,结果表明各共有峰保留时间稳定,相对峰面积比值差别较大,表明不同产地对叶百部饮片的质量存在一定差异。
在中药材品种的发展变迁中,不仅存在多基原品种现象,导致药材品种混乱、质量难以控制,同时也存在劣质品掺杂的现象,不同程度地影响着药材质量的安全性、有效性和可控性。本研究初步建立的方法可应用于不同基原及劣质品的对叶百部药材的鉴别,为对叶百部药材提供更全面的质量控制方法。

