碱处理结合盐辅助分散液液微萃取GC-MS/MS检测即食鱼制品中7种N-亚硝胺
侯彤瑶,王宗义,潘晓玉,张丽萍,刘 珊,吴天俁
(北京农学院 食品科学与工程学院/食品质量安全北京实验室/农产品有害微生物及农残安全检测与控制北京市重点实验室, 北京 102206)
N-亚硝胺(N-nitrosamines)是一类重要的致癌性食品污染物[1],主要由亚硝酸盐和胺类物质作用生成[2-3]。调查显示,鱼类加工食品容易受到此类物质的污染[4],其食品安全风险值得关注。我国水产动物食品中N-二甲基亚硝胺(NDMA)的安全限量为4 μg/kg[5],其他N-亚硝胺类物质,尚未规定限量。
目前,检测样品中痕量N-亚硝胺的有效方法,主要是色谱与串联质谱[6-8]或高分辨质谱[9]的联用技术。由于食品基质相对复杂,目标物含量低,通常N-亚硝胺的检测需要对样品进行有效提取、净化和浓缩,且还需要有效控制部分目标物的挥发损失;而经典的水蒸气蒸馏- 液液萃取- 氮吹浓缩方法[10]则较为费时费力, 批量样品筛查检测的压力较大。分散固相萃取[11]、活性炭柱固相萃取[12-13]、QuEChERS技术[4,14-15]和分散液液微萃取(dispersive liquid-liquid microextraction, DLLME)[16-18]是近年来报道的较为有效的改进方法。其中DLLME是将微升级高密度提取剂,在分散剂的作用下分散到样品溶液中,形成乳浊液,从而扩大相界面,实现高效萃取,离心分离萃取剂后,样品直接用于检测的方法。DLLME具有成本低、操作简单、富集倍数大和环境污染小的特点[19];但经典DLLME方法常用的四氯化碳、三氯甲烷等提取剂,毒性仍相对较大,并且四氯化碳对N-亚硝胺等极性相对较大的化合物萃取效果较差。研究报道,在高浓度盐辅助和不使用分散剂的条件下,毒性相对较低、极性稍大的二氯甲烷也可做萃取剂,其与水溶液形成乳浊液,实现对极性相对较大的目标物的有效萃取,即盐辅助分散液液微萃取(salt-assisted dispersive liquid-liquid microextraction, SADLLME)方法[20],从而补充了经典DLLME方法的不足。但关于使用SADLLME检测N-亚硝胺的方法还少有报道。
本研究利用氢氧化钡溶液处理法将N-亚硝胺转移至水溶液,进一步优化SADLLME参数,再结合气相色谱- 串联质谱法(GC-MS/MS)的高选择性、高灵敏性和同位素内标定量的准确性,旨在建立一种针对即食鱼制品的样品前处理简单、成本低廉,对人员、环境更为友好的适合7种N-亚硝胺的SADLLME-GC-MS/MS检测新方法,希望为简化食品中N-亚硝胺检测方法提供新的借鉴。
1 材料与方法
1.1 材料与试剂
即食鱼制品,北京地区超市;50 mL塑料离心管,BD Biosciences公司。
分析纯八水合氢氧化钡、硫酸钠、四氯化碳、三氯甲烷等,国药集团化学试剂有限公司;二氯甲烷、甲醇,色谱纯,美国J.T.Baker公司;质量浓度2 000 mg/L的7种N-亚硝胺的混合标准溶液,美国O2si公司;质量浓度1 000 μg/mL的N-亚硝二甲胺-d6(NDMA-d6)、N-亚硝二丙胺-d14(NDPA-d14)、N-亚硝基吡咯烷-d8(NPYR-d8)的甲醇溶液,美国Accustandard Inc公司。
1.2 仪器与设备
7890B-7000C型气相色谱- 串联质谱联用仪、量程为1.0 mL精密注射器,美国Agilent Technologies公司; Centrifuge 5810R型高速冷冻离心机,德国Eppendorf公司;MS200型自动多管涡旋混匀仪,杭州瑞诚仪器有限公司;800A型样品均质机,天津市泰斯特仪器有限公司。
1.3 实验方法
1.3.1标准溶液的配制
定值混合标准溶液和3种定值内标溶液,分别经甲醇稀释得到200 μg/mL的混合标准储备液和100 μg/mL的混合内标储备液(棕色贮液瓶,-18 ℃储存),再进一步稀释至质量浓度分别为1.0、0.1 μg/mL的混合标准中间工作液和质量浓度均为1 μg/mL的NDMA-d6、NDPA-d14和NPYR-d8内标混合液。最后,用二氯甲烷稀释,得到质量浓度为1、5、10、25、50、100 ng/mL和内标质量浓度为50 ng/mL的系列标准工作液。
1.3.2样品前处理
1.3.2.1 样品的提取
称取经均质的即食鱼干样品5.0 g于50 mL塑料离心管中,加入1 μg /mL的3种稳定同位素内标混合溶液50 μL,静置5 min,加入1 g氢氧化钡,35 mL纯水,拧紧盖子,混匀涡旋30 s,于90 ℃烘箱中处理2 h(处理30 min时取出涡旋混匀1次)。取出稍冷,直接置于离心机中8 000 r/min离心10 min,上清液完全倾入另一预先装有7 g硫酸钠的50 mL的离心管中,拧紧盖子,手动摇匀至反应充分,再于8 000 r/min离心10 min,上清液完全倾入另一50 mL的离心管中备用。
1.3.2.2 SADLLME处理
注射器吸取500 μL二氯甲烷,快速打入1.3.2.1节中溶有硫酸钠的样品提取液中,形成乳浊液,并于自动多管涡旋混合器上涡旋5 min,再以8 000 r/min离心10 min, 弃去部分体积的水相后,移液枪吸取下层二氯甲烷100 μL于带有体积为200 μL内插管的进样瓶中待测。
1.3.2.3 加标回收实验样品处理
按1.3.2.1节的方法称取样品后,分别加入0.1 μg/mL的混合标准溶液50 μL,1 μg/mL的混合标准溶液25、50 μL和1 μg/mL内标混合溶液各50 μL,即加标水平分别为1、5、10 μg/kg,再继续按1.3.2.1节和1.3.2.2节方法进行处理,每个水平重复6次。
1.3.3分析条件
1.3.3.1 色谱条件
色谱柱:DB-WAXUI色谱柱(30 m×250 μm×0.25 μm );升温程序:初始温度35 ℃保持1 min,以10 ℃/min升至90 ℃,30 ℃/min 升至240 ℃保持6 min;载气(He)流速0.9 mL/min,恒流模式;进口样温度190 ℃,进样量1 μL,不分流进样;溶剂延迟5 min。
1.3.3.2 质谱条件
电子轰击(EI)离子源,电子能量70 eV,传输线温度250 ℃,离子源温度230 ℃,四极杆温度150 ℃,采集模式为多重反应监测模式(MRM),参数见表1。

表1 N-亚硝胺的MRM参数Tab.1 MRM parameters of N-nitrosamines
1.3.4定性、定量方法
定性分析通过核对目标物与相应标样的保留时间、前级离子、碎片离子及丰度比进行;定量分析使用内标法,其中NDMA以NDMA-d6为内标,NDEA和NPYR以NPYR-d8为内标, 其他均以NDPA-d14为内标。
1.4 数据处理
数据处理使用MassHunter B.07.01软件和Microsoft Office Excel 2013进行。
2 结果与分析
2.1 提取方法的确定
SADLLME方法需要样品中目标物有效转移至水溶液中,对于即食鱼制品,有效的提取方法有水蒸气蒸馏[11]、高压热水处理[21]、氢氧化钠溶液(或含甲醇)[18]或饱和氢氧化钡溶液皂化处理[13];其中水蒸气蒸馏费时、费力,高压水处理需专门的设备,碱溶液皂化处理相对简单;而使用饱和氢氧化钡溶液则更为简单,样品溶液不黏稠,不需使用蛋白沉淀剂处理,仅需加入一次固体氢氧化钡即可完成。本研究在使用氢氧化钡处理的基础上[14],离心后加入过量硫酸钠,再经离心除去生成的硫酸钡,使样品溶液得到进一步净化,同时过量的硫酸钠可作为下一步SADLLME方法的盐辅助剂,有效简化了样品提取方法。
2.2 辅助用盐的确定及用量的优化
为便于观察乳浊液的形成情况,研究首先使用30 mL盐浓度均为1 mol/L的水溶液(N-亚硝胺加标量100 ng),按1.3.2.2节的方法比较了硫酸钠、氯化钠、碳酸钠和磷酸二氢钠4种常用盐的效果。结果显示:4种盐均能促使二氯甲烷与水溶液形成乳浊液,响应值除氯化钠最低外,其他盐均有足够的强度,但以硫酸钠最高,见图1。这主要是相同物质的量浓度下,氯化钠溶液的离子强度最小,盐析效应较差。考虑使用硫酸钠容易获得较大的离子强度,同时可与样品提取液中的氢氧化钡形成硫酸钡沉淀,有辅助进一步净化样品溶液的作用,故本研究以硫酸钠为辅助用盐。
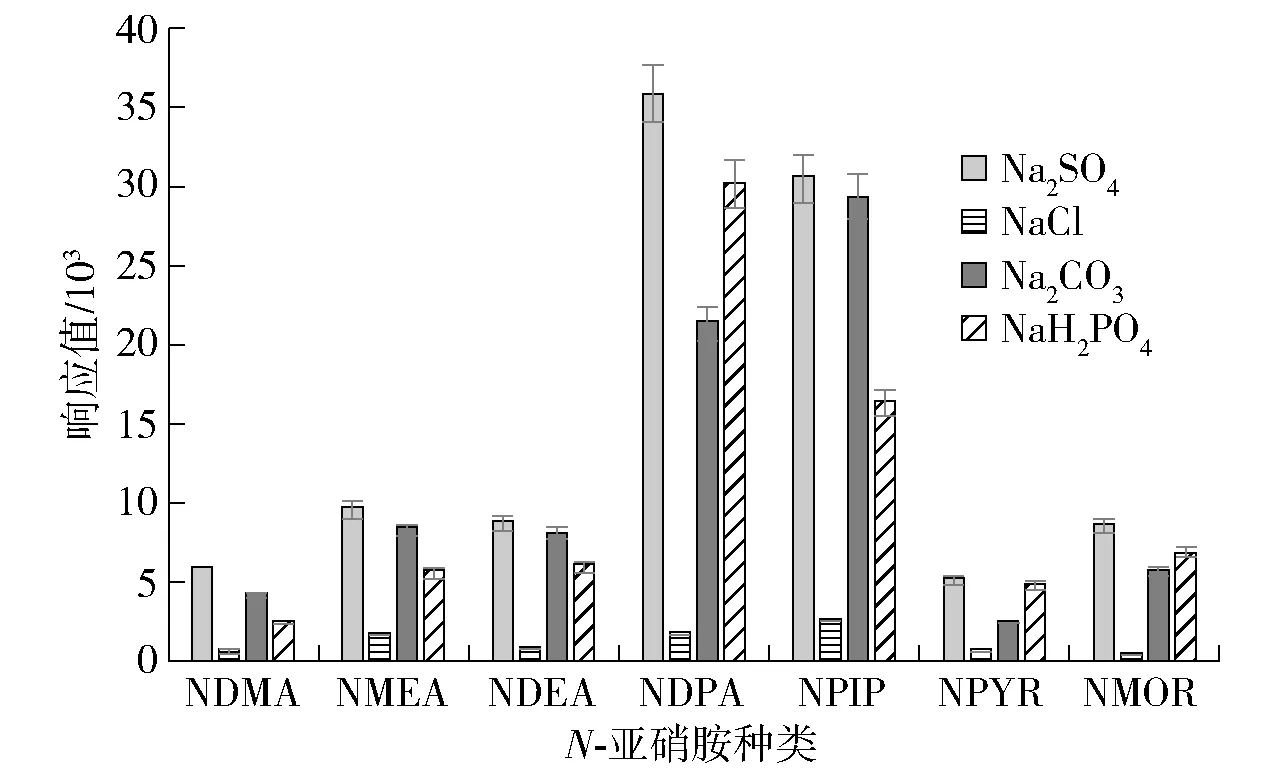
图1 不同辅助用盐的效果比较Fig.1 Comparison of effects of different auxiliary salts
实验进一步按1.3.2.1节方法对硫酸钠用量进行了优化,结果见图2。当硫酸钠用量为5~7 g时,响应值趋于平稳,进一步提高硫酸钠用量时,溶液达到饱和,会有结晶沉淀析出,不利于萃取剂的分离。考虑沉淀钡离子需要消耗一定量硫酸钠,故确定用量为7 g。

图2 硫酸钠用量的优化Fig.2 Optimization of sodium sulfate dosages
2.3 萃取剂体积的优化
同样使用1.3.2.1节得到样品溶液(加标量为100 ng)对二氯甲烷体积进行了考察,结果见图3。当二氯甲烷用量小于200 μL时,离心后体积过小;用量为300~600 μL时,目标物响应值变化不大。为便于离心后取出和自动进样分析(体积需大于50 μL),确定二氯甲烷用量为500 μL。
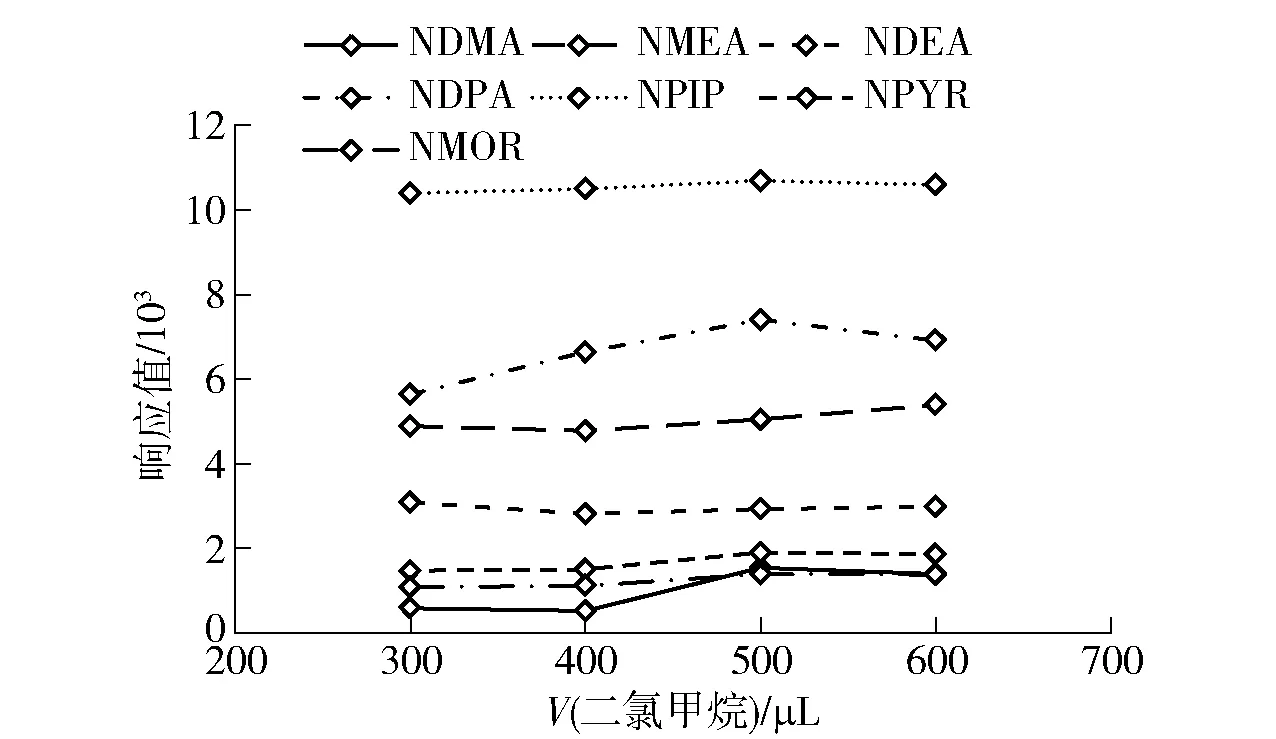
图3 二氯甲烷用量的优化Fig.3 Optimization of dichloromethane dosages
pH值亦对N-亚硝胺的萃取有影响,但影响不十分显著[17]。由于酸性条件有利于可能存在的胺和亚硝酸盐反应形成新的N-亚硝胺[2];但本研究的样品溶液为碱性,故未对pH值的影响进一步讨论。
2.4 SADLLME与DLLME萃取效果的比较
使用1.3.2.1节处理得到的样品溶液(加标量为100 ng,其中用于DLLME的样品溶液不加硫酸钠),分别进行SADLLME和DLLME[19-20],其中DLLME使用三氯甲烷和乙醇、四氯化碳和甲醇分别做萃取剂和分散剂,每组平行测定4次,见图4。结果显示:同等实验条件下,SADLLME方法的萃取效果总体优于经典的DLLME方法。

图4 SADLLME与DLLME方法萃取N-亚硝胺 效果的比较Fig.4 Comparison of SADLLME and DLLME for extraction effects of N-nitrosamines
2.5 SADLLME方法对色谱和质谱检测的影响
考察3种不同品牌的鱼干制品,发现在本研究确定的碱处理结合SADLLME方法和优化的色谱分离与质谱检测条件下,各类N-亚硝胺均不受共同流出物的干扰,典型MRM色谱见图5。

图5 标准品及一种鱼干样品的MRM色谱Fig.5 MRM chromatograms of standards and one dried fish sample
2.6 检出限、定量限、线性关系和回收率分析
检出限(LOD)和定量限(LOQ)分别在定性离子色谱峰可有效识别的前提下,以实际样品和低水平加标样品分析物的信噪比约为3和10进行评估[22],结果见表2。LOD为0.10~0.19 μg/kg,LOQ为0.28~0.56 μg/kg,参照水产品中NDMA安全限量4 μg/kg,本方法的检出能力满足N-亚硝胺监测的需要。根据样品SADLLME萃取液的目标物可能质量浓度,对1~100 ng/mL的系列标准溶液进行考察,线性良好,R2>0.997。根据实际即食鱼制品中N-亚硝胺的含量水平,进行1、5、10 μg/kg的加标回收实验,回收率为79.19%~117.40%,相对标准偏差(RSD)为1.06%~10.30%,见表3。

表2 目标物的线性关系、检出限和定量限Tab.2 Linearity,limits of detection and limits of quantitation of analytes

表3 样品中7种N-亚硝胺的回收率及精密度Tab.3 Recoveries and precisions of seven N-nitrosamines in samples
2.7 实际样品的检测结果
应用本方法对购自本地超市的3种即食鱼制品进行检测,除NPYR未检出外,其他N-亚硝胺均被不同程度检出,其中NDMA质量分数为4.21~8.84 μg/kg,与文献[4]报道类似,其他N-亚硝胺含量介于LOD和LOQ之间。
3 结 论
本研究建立了氢氧化钡处理-SADLLME结合GC-MS/MS检测即食鱼制品中7种N-亚硝胺的新方法。该方法具有样品前处理简单,成本低廉,灵敏、可靠的优点,能够满足相关食品中N-亚硝胺检测的需要,以期为相关食品的安全监测提供方法和借鉴。

