我院异基因造血干细胞移植患者环孢素血药浓度监测情况分析
符祥俊,黄 莉,郭 丽,刘 丹,林良沫(海南省人民医院/海南医学院附属海南医院血液内科,海南 海口 570311)
异基因造血干细胞移植(allogeneic hematopoietic stem cell transplantation,allo-HSCT)是患者经大剂量放化疗或免疫抑制剂预处理后,通过静脉输注供者造血干细胞重建正常造血和免疫系统的治疗手段,用于造血和免疫系统疾病及遗传代谢病如急性白血病、重症再生障碍性贫血和地中海贫血等的治疗。环孢素+短程甲氨蝶呤(CsA+MTX)联合霉酚酸酯和/或抗胸腺细胞免疫球蛋白等药物能够有效降低移植物抗宿主病(graft versus host disease,GVHD)的发生率,目前广泛应用于allo-HSCT后预防GVHD的方案中[1-3]。
环孢素是一种临床常用的钙调神经磷酸酶抑制剂,具有良好的免疫抑制作用。其治疗窗窄,用药过程中需要进行治疗药物监测,共识[1]推荐环孢素目标血药浓度范围为150 ~ 250 ng·mL-1。在allo-HSCT患者中维持有效血药浓度有助于提高GVHD防治效果并降低严重药品不良反应的发生[4-5]。本研究拟分析我院allo-HSCT患者环孢素血药浓度的监测情况,为临床开展环孢素的个体化应用提供参考。
1 材料和方法
1.1 研究对象
以2015年1月– 2020年12月在我院血液内科进行allo-HSCT的患者为研究对象,这些患者采用CsA+MTX为基础的预防GVHD方案,部分患者联合霉酚酸酯和/或抗胸腺细胞免疫球蛋白。收集记录患者的临床资料、环孢素用法用量、血药浓度监测结果和监测次数等信息。所有患者均知情并签署知情同意书,本研究经过伦理委员会批准,批件号:医伦理(2018)68号。
1.2 环孢素给药方法
患者于回输前9 d(– 9 d)或– 3 d开始给予环孢素1.5 ~ 2.5 mg·kg-1·d-1,持续静脉滴注22 h。干细胞回输后待患者胃肠道功能恢复时以口服给药序贯治疗,所有患者定期监测环孢素血药浓度并参考浓度结果进行剂量调整。
1.3 血药浓度监测方法
使用西门子Viva-E全自动药物浓度分析仪,采用均相酶放大免疫分析法测定环孢素全血药物浓度。检测试剂为西门子特异性环孢霉素检测试剂(Emit®2000 Cyclosporine Specific Assay)、样本预处理试剂(Emit®Cyclosporine Sample Pretreatment Reagent)、环孢素定标试剂(Emit®2000 Cyclosporine Calibrators)、质控品(Rap/Tac/CsA Control)等。严格遵守实验操作规范和试剂使用说明进行检测方法的质量控制并绘制标准曲线,定量范围为40 ~ 500 ng·mL-1。
患者给予环孢素2 d后,于静脉滴注结束后2 h或者清晨口服给药前30 min采取外周静脉血2 mL进行血药浓度检测。处理前混匀待测样本,使用正压移液器吸取100 μL血样置于1.5 mL EP管中,加入300 μL样本预处理试剂,立即盖上盖子并快速混匀。样本完全混匀后在室温环境中静置至少2 min,以14 000 r·min-1离心后吸取上清液上机检测。结果> 500 ng·mL-1的样本需要稀释后重新检测。
1.4 数据分析方法
采用SPSS 19.0对数据进行统计分析,描述性结果以均值±标准差、极小值和极大值表示,组间差异采用Kruskal Wallis检验或者χ2检验,以P< 0.05表示差异具有统计学意义。
2 结果
2.1 基本信息
2015年1月– 2020年12月共有69例患者采用CsA+MTX为基础的预防GVHD方案,半相合或无关供者移植加用霉酚酸酯和/或抗胸腺细胞免疫球蛋白。将上述患者按年龄分为两组,> 14岁的患者40例,其中男性19例,女性21例;≤14岁的患者29例,其中男性20例,女性9例。详见表1、表2。
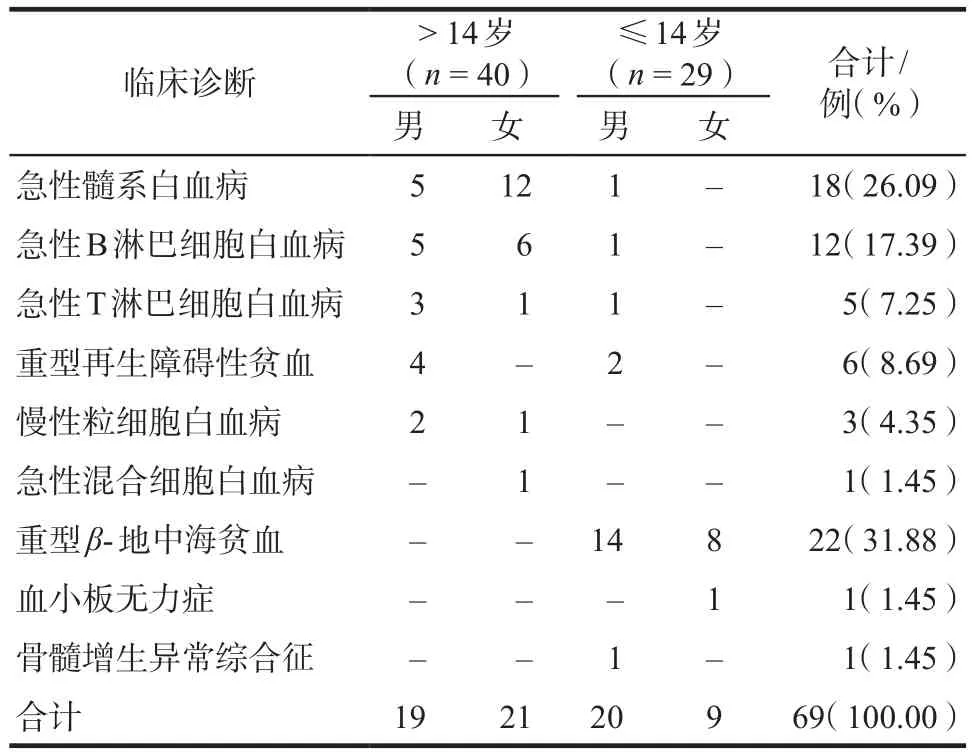
表1 患者临床诊断统计表Tab 1 The clinical diagnosis of patients
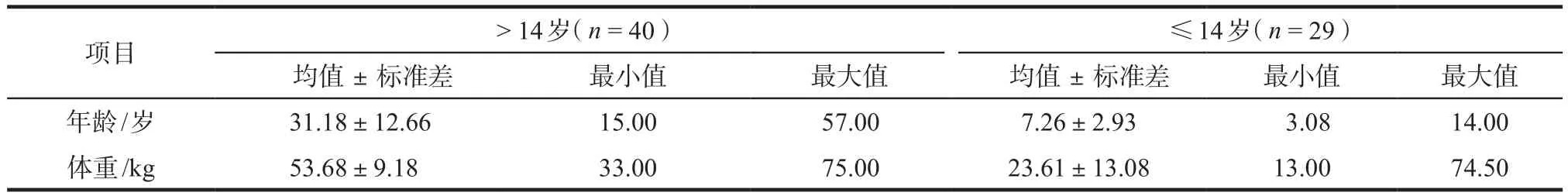
表2 患者年龄和体重情况Tab 2 The age and weight information of patients
2.2 两组患者环孢素血药浓度监测情况
以连续2次环孢素血药浓度监测结果维持在150~ 250 ng·mL-1为达到目标浓度,统计两组患者开始用药6个月内(恶性疾病)或者1年内(良性疾病)进行环孢素血药浓度的监测总次数、达到目标浓度需要监测的次数和用药天数,以及环孢素静脉和口服两种给药途径下的剂量及血药浓度等信息并进行Kruskal Wallis检验(见表3)。所有患者共监测环孢素血药浓度1578例次,其中> 14岁组共监测861例次,≤14岁组共监测717例次。两组患者监测血药浓度的总例次数、达到目标血药浓度所需监测次数均无统计学差异,但是≤14岁组患者达到目标血药浓度所需的天数则显著少于> 14岁组患者(P= 0.005)。两组患者无论是静脉给药还是口服给药血药浓度监测结果均无统计学差异,但≤14岁组患者两种给药途径中环孢素的剂量要显著高于> 14岁组患者,提示儿童可耐受更高的环孢素剂量。

表3 环孢素血药浓度监测情况Tab 3 Monitoring of blood concentration of cyclosporine
2.3 环孢素血药浓度达标率与换药原因分析
将环孢素血药浓度按< 150 ng·mL-1、150 ~ 250 ng·mL-1、> 250 ng·mL-1分组,分别统计不同浓度范围内监测的例数和百分比,采用χ2检验可知上述两组患者环孢素血药浓度的分布情况和达标率无显著性差异。见表4。

表4 环孢素不同血药浓度分布情况和达标率Tab 4 Distribution and standard reaching rate of different plasma concentrations of cyclosporine
69例患者中共有12例(17.39%)在防治GVHD的过程中将环孢素更换为他克莫司,具体换药原因如下:2例患者无法耐受口服环孢素软胶囊;5例患者因环孢素导致的严重不良反应(肝肾毒性和神经系统毒性)换药;3例患者由于治疗GVHD效果欠佳换药;2例患者因停用环孢素后伴发肾脏GVHD换药。
3 讨论
我院行allo-HSCT中> 14岁的患者以急性白血病为主,占比80.00%,儿童患者中则以重型β-地中海贫血为主,占比75.86%,这与海南省地中海贫血发病率高相关[6]。本研究发现,无论是静脉给药还是口服给药,环孢素的血药浓度分布情况及达标率在上述两组年龄段的患者中无显著性差异。本研究结果显示,环孢素血药浓度总达标率为36.88%,低于邱蕾等[7]报道的80.80%(荧光免疫偏振法,治疗窗150 ~ 600 ng·mL-1)和尹玉琴等[4]报道的65.47%(荧光免疫偏振法,治疗窗100 ~ 400 ng·mL-1),这可能与采用的检测方法和设定的治疗窗不同相关[8]。同时某些具有复发高危因素的白血病患者倾向于维持较低的环孢素血药浓度以利于诱发移植物抗白血病效应,上述因素可能是导致我院allo-HSCT患者环孢素血药浓度达标率偏低的原因。环孢素由静脉转化为口服给药时的剂量比例通常为1∶3,联合唑类抗真菌药应适当减少环孢素剂量并积极监测血药浓度[9-10]。环孢素血药浓度过高易导致肝肾毒性等严重药品不良反应[11],浓度> 400 ng·mL-1时肝肾毒性的发生率显著升高[12]。笔者建议在有效预防GVHD的基础上应当尽量维持适宜的血药浓度,以便降低不良反应的发生率。因此建议遵照国内指南并根据检测方法设定相应的浓度参考范围,积极开展治疗药物监测工作。
综上,本研究显示我院allo-HSCT患者平均需要进行4 ~ 5次血药浓度监测才可达目标浓度,> 14岁组患者给药后需要(20.28±8.45)d的时间才达到目标浓度,所需天数多于≤ 14岁组的(12.77±4.46)d,可能与儿童患者初始给药剂量偏大相关。董露露等[13]研究发现移植早期环孢素血药浓度< 200 ng·mL-1时急性GVHD发生率为35.86%,这提示临床应给予适宜的初始剂量使环孢素尽早达到目标血药浓度,从而降低急性GVHD的发生率[14-16]。环孢素的治疗药物监测是allo-HSCT过程中重要的内容,规范开展血药浓度监测有助于制定适宜的免疫抑制剂个体化给药方案,预防GVHD的发生并提高治疗效果。

