团簇Fe4P异构化反应的理论研究
侯欠欠,方志刚,许 友,郑新喜
(辽宁科技大学 化学工程学院,辽宁 鞍山 114051)
过渡态理论有着悠久的历史,是一种非常普遍的反应速率理论,对现代化学动力学产生了深远的影响[1-2]。此外,以统计热力学和量子力学为依据的过渡态理论的提出使化学反应的研究进入微观理论层次,为获得热反应速率常数提供了一种有效的方法。目前,科研人员依据过渡态理论对化学动力学的研究已取得了重大进展,例如Bao等[3]通过对变分过渡态理论(VTST)基本原理的研究进而预测与压力有关的速率常数,回顾了VTST在凝聚相中的使用,包括固-气界面、液体溶液和酶动力学,并且总结了动力学研究的主要步骤。Zheng等[4]发现了一种耦合模理论,称为多结构变分过渡态理论(MS-VTST)和多路径变分过渡态理论(MP-VTST),前者已成功地应用于小分子研究,后者已成功地应用于酶动力学研究。Meana-Paeda等[5]利用多径变分过渡态理论预测了生物燃料2-丁醇燃烧过程中过氧化氢自由基从2-丁醇中提取氢的相关速率常数,此外还发现处于过渡态的氢键可以降低活化焓。对于Fe-P非晶态合金,因其具有长程无序、短程有序的空间结构以及优异的物理化学性质,在析氢[6-7]、析氧[8]、新型电池[9-10]等方面应用广泛。但目前鲜有研究人员依据过渡态理论对Fe-P体系的异构化反应进行研究,因而该方面具有较大的研究前景。此外通过探究Fe-P体系异构化反应的特点,可以为Fe-P非晶态合金新型材料的制备提供有价值的信息。因此,以团簇Fe4P[11]作为研究对象,依据密度泛函理论[12-14]和过渡态理论[15],从化学热力学和动力学两方面对其异构反应进行研究,分析已有的异构化反应的特点,并采用两种不同的方式预测团簇Fe4P未知的异构化反应的反应限度,以满足实际生活中不同的应用条件,同时也为其他科研工作者探究Fe-P体系的优异性能提供理论依据及数据参考。
1 团簇Fe4P优化构型的计算方法
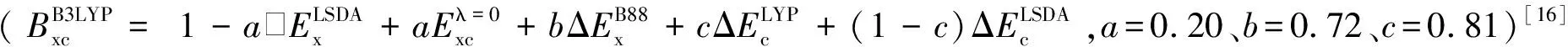
2 结果与讨论2.1 团簇Fe4P的优化结构及异构化反应的空间结构
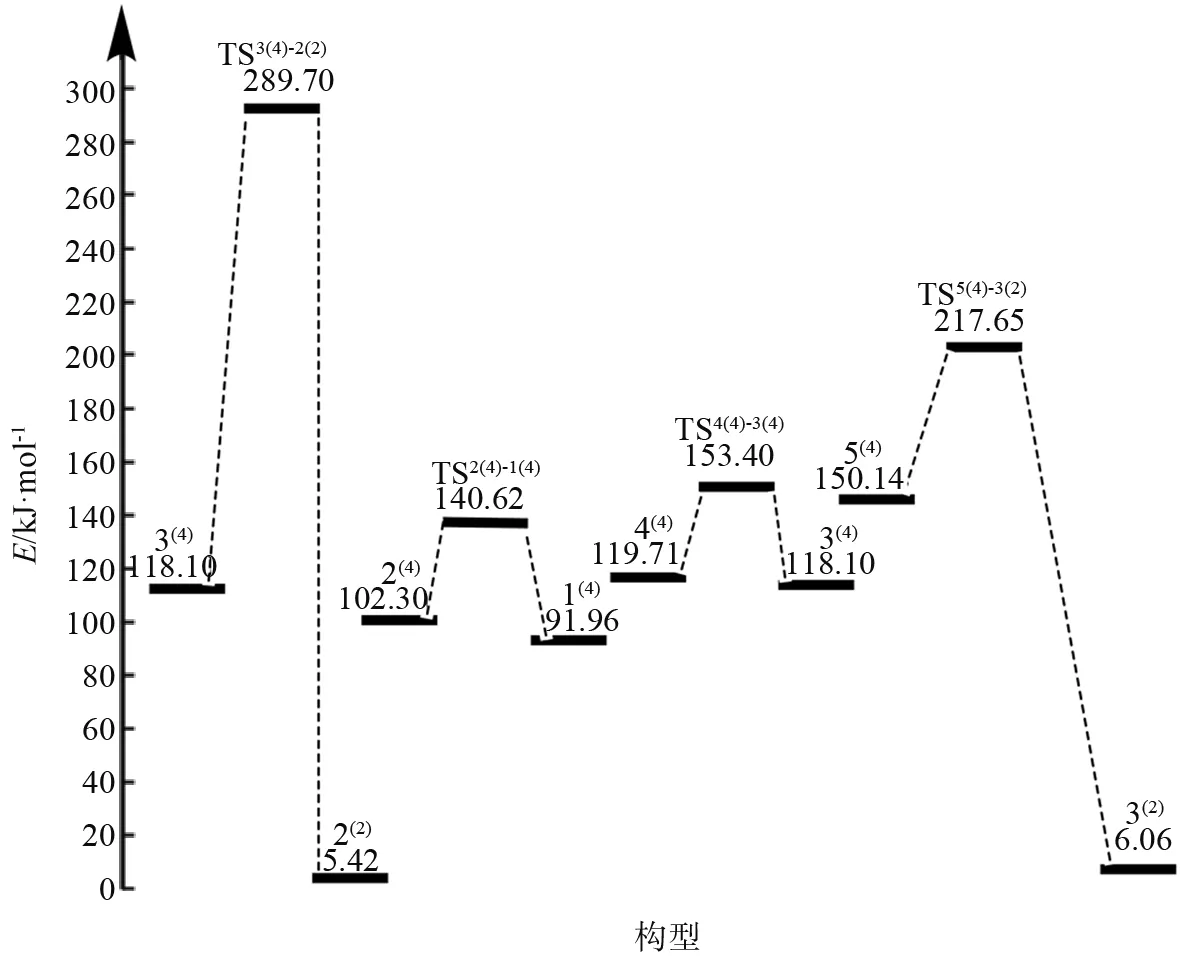
团簇Fe4P有3种二重态构型,分别为构型1(2)、2(2)和3(2);5种四重态构型,分别是构型1(4)、2(4)、3(4)、4(4)、5(4),如图1所示。为便于分析,选取能量最低的构型1(2)为参考点(0 kJ/mol),依次计算出其余7种优化构型的相对能量,并在图1标出。
图2为团簇Fe4P二、四重态优化构型进行异构化反应时所得到的过渡态空间结构。为了便于比较四种过渡态结构的能量大小关系,同样选取构型1(2)为参考点,计算各过渡态构型的相对能量并按照从小到大的顺序进行排列。与图1各优化构型的空间结构进行比较发现,异构化反应过渡态的空间结构与团簇Fe4P的基础结构类型一样,分别为三角双锥型(TS2(4)-1(4))、四棱锥型(TS4(4)-3(4))、带帽三角锥型(TS5(4)-3(2))、平面五边型(TS3(4)-2(2))。此外,为说明各优化构型在异构化转化过程中断键及生成新键的情况,在图2过渡态的结构中用白线表示无变化的键,虚线表示断裂键,绿线表示新生成的键。
观察图2易发现,对于异构化反应2(4)→1(4),过渡态的结构与反应物构型2(4)的空间结构一样,且键的类型并未发生改变,说明在转化过程中该空间结构较为稳定;对于反应4(4)→3(4),过渡态的结构与生成物构型3(4)相似,均为四棱锥型,在转化过程中仅发生了Fe1-P5键的断裂;过渡态TS5(4)-3(2)键的类型变化较为复杂,异构化转化过程有Fe1-Fe2、Fe1-Fe3、Fe3-P5、Fe4-P5键生成;对于反应3(4)→2(2),构型3(4)在向构型2(2)进行转化的过程中,发生了Fe1-Fe4、Fe2-P5、Fe3-P5的断键。

图1 团簇Fe4P的8种优化构型Fig.1 Eight optimized configurations of Fe4P clusters

图2 团簇Fe4P异构化反应过渡态的构型图Fig.2 Configuration diagrams of transition state of cluster Fe4P in isomerization reactions
2.2 团簇Fe4P异构化反应的化学热力学研究
2.2.1 团簇Fe4P的8种优化构型的热力学参数
为探究团簇Fe4P的8种优化构型的热力学性质对其异构化反应的影响,根据公式ΔX=XFe4P-4XFe-XP(X=U、H、G),分别计算出8种优化构型的校正能(E0)、热力学能变(ΔU)、焓变(ΔH)和吉布斯自由能变(ΔG),计算的结果按照校正能由小到大进行排列,如表1所示。观察表1可以发现,二、四重态各优化构型热力学能变、焓变、吉布斯自由能变均为负值,且三种热力学参数的减少量随优化构型能量的升高而降低,说明在团簇Fe4P优化过程中,构型的能量越高,稳定性越差,形成该优化构型所放出的热量越少。综合来看,二重态各优化构型的3种热力学参数变化量的绝对值均大于四重态,说明二重态各优化构型的稳定性大于四重态5种优化构型的稳定性,同时也说明四重态优化构型在异构化反应中易于向比它本身稳定性更高的构型进行转化(如TS3(4)-2(2)、TS5(4)-3(2))。
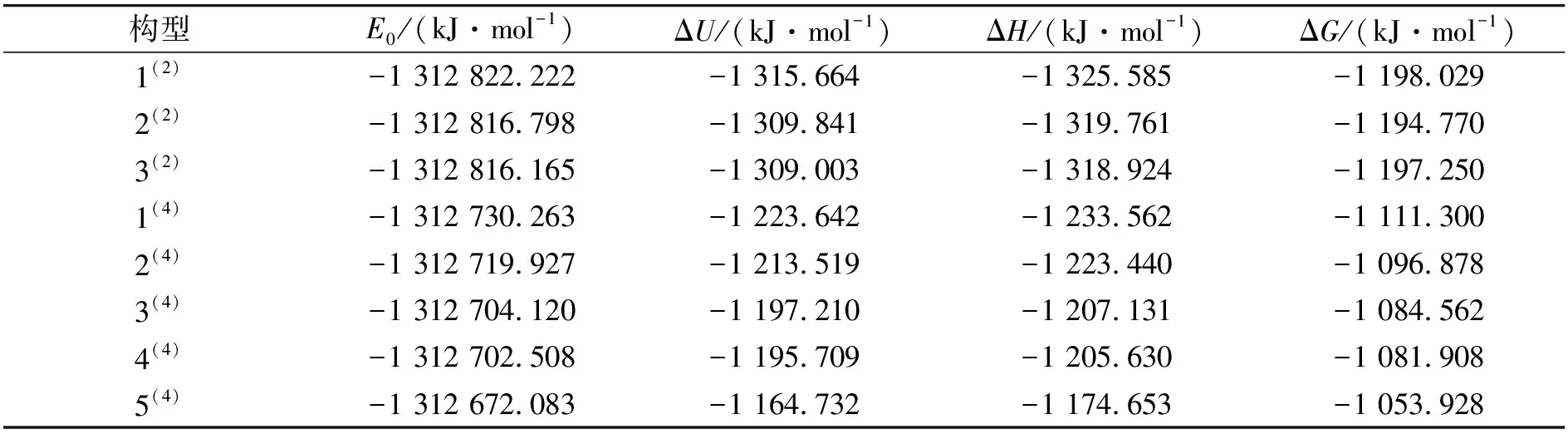
表1 团簇Fe4P的8种优化构型的热力学参数
2.2.2 团簇Fe4P异构化反应的限度和方向
对于一个反应而言,平衡常数K的大小反映了化学反应进行的程度(即反应限度)。K值越大,说明该反应正向进行得越完全,反之就越不完全.因此为研究团簇Fe4P异构化反应理论上进行的限度,将环境压强设置为1.0 atm,温度设置为298.15 K,根据范特霍夫(Van’t Hoff)方程lnK=-ΔH/RT+ΔS/R和表1中的数据,计算出异构化反应的平衡常数K,计算结果如表2所示。

表2 298.15 K下团簇Fe4P的4种异构化转化反应的热力学函数变化量
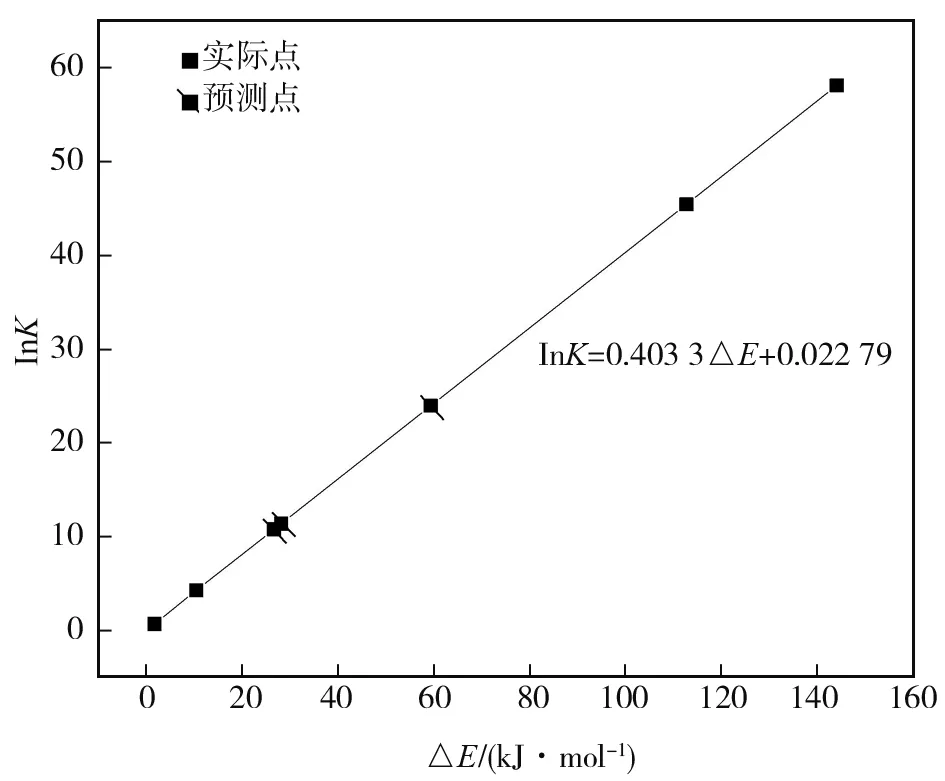
对于一般反应而言,K>105时,该反应正向进行的限度远大于逆向进行的限度;10-5 由物理化学理论可知,反应的吉布斯自由能变(ΔG)、焓变(ΔH)和熵变(ΔS)对于判断一个反应能否自发进行和反应发生的方向有着至关重要的作用,并且反应的吉布斯自由能变小于0在理论上可视为该反应能自发进行,焓变小于0表示反应为放热反应。根据表2数据,可知团簇Fe4P的异构化反应的ΔG、ΔH均小于0,说明已有的异构化反应在理论上均可自发进行,且均为放热反应。对于异构化反应4(4)→3(4)、2(4)→1(4)的ΔS均大于0,而其余两个反应ΔS均小于0。所以为抵消熵变的影响,根据ΔG的定义式:ΔG=ΔH-TΔS可知,反应3(4)→2(2)、5(4)→3(2)在低温条件下更易于自发进行。 2.3.1 团簇Fe4P异构化反应的活化能 为更加深入的对团簇Fe4P的异构化反应进行研究,从动力学的角度对4种异构化反应进行了探究。活化能可用于判断一个化学反应发生的难易程度,其数值越大,异构化反应越不易进行。因此为比较团簇Fe4P的4种异构化反应进行的难易程度,采用自洽场(SCF)近似法,计算出团簇Fe4P的4种过渡态结构的能量以及正逆反应的活化能,如表3所示,其中ETS表示异构化反应中过渡态的能量,EaF、EaB则表示为正逆反应的活化能。此外,为更加直观地观察出4种过渡态的能量与其反应物及生成物之间的能量关系,依据图1和图2各构型的能量绘制如图3所示的4种异构化反应的能垒图。 表3 团簇Fe4P异构化反应的活化能及过渡态的能量 图3 团簇Fe4P异构化反应的能垒图Fig.3 Energy barrier diagram of cluster Fe4P isomerization reaction 结合表2和图3进行分析发现,4种异构化转化反应的反应物与过渡态构型的能量差值均小于生成物与过渡态构型的能量差值,并且在异构化转化过程中正反应活化能均小于逆反应的活化能,说明团簇Fe4P的异构化转化主要向正向进行,即过渡态构型更易于向稳定性高的构型转化。另外,异构化反应2(4)→1(4)、4(4)→3(4)均发生的是四重态构型之间的异构化转化反应,且得到的过渡态的能量相比于其余两个反应中过渡态的能量较低。除此之外,异构化反应2(4)→1(4)、4(4)→3(4)的正逆反应活化能均小于异构化反应5(4)→3(2)、3(4)→2(2)的活化能,说明自旋多重度会影响团簇Fe4P异构化反应的难易程度。综合来看,对于4种已有的异构化转化反应,异构化反应4(4)→3(4)最容易发生,反应2(4)→1(4)次之,而异构化反应3(4)→2(2)发生的难度最大。 2.3.2 团簇Fe4P异构化反应的速率及反应限度 根据过渡态理论中实际速率常数k(T)=к(T)kTST(к(T)为魏格纳校正系数,kTST为理论速率常数)和相关数据可以得出正、逆反应速率常数k+(正反应)和k-(逆反应),进而根据K=k+/k-可得出反应的平衡常数,具体数值如表4所示。 对表4的数据进行对比分析可知,4种异构化反应的平衡常数(K)均大于1,说明团簇Fe4P在进行异构化转化反应时更倾向于向正向进行。此外,在所有异构化反应中,四重态各构型之间进行转化的正逆反应速率远大于四重态构型向二重态构型转化的正逆反应速率,说明四重态构型之间进行异构化转化的可能性更大。对于异构化反应4(4)→3(4),其正反应速率最大,但其反应平衡常数最小,而对于异构化反应3(4)→2(2)则相反,其正反应速率最小,化学平衡常数较大,说明异构化反应4(4)→3(4)比其他3种异构化反应更容易进行但构型转化最不彻底,而异构化反应3(4)→2(2)的反应程度较大但该反应发生的可能性最小。对于异构化反应2(4)→1(4),其正逆反应速率仅次于构型4(4)→3(4)的正逆反应速率,但反应发生的限度较大。此外,构型5(4)→3(2)的反应平衡常数最大,且相比于逆反应的反应速率,正反应的反应速率较大,说明构型5(4)较容易向构型3(2)转化且反应进行的限度最大,但逆向反应发生的可能性较小。综上所述得出的结论与“2.2.2团簇Fe4P异构化反应的的限度和方向”部分相同。 表4 298.15 K下团簇Fe4P异构化反应的正、逆反应速率及平衡常数 综上所述,结合团簇Fe4P异构化反应的热力学和动力学研究可以发现,异构化反应4(4)→3(4)、2(4)→1(4)平衡常数较小、正逆反应活化能相近,即二者可视为可逆反应,且二者在常温条件下正逆反应发生的速率最高。对于反应3(4)→2(2)、5(4)→3(2),虽然反应发生的最为彻底,反应物转化率也最高,但是在常温条件下,二者反应的速率较小,即反应不易发生。为排除化学反应熵变的影响,两者在低温条件下更易于自发进行。 由上述讨论可知,团簇Fe4P已有的异构化反应均遵循能量高的构型更易于向能量低的构型转化,且各反应物与生成物的能量差(ΔE=E0反应物-E0生成物)越大,反应的越彻底。通过对表1和表2的数据进行分析发现,各异构化反应的lnK与ΔE存在线性关系。为探究出lnK与ΔE之间存在何种线性关系,绘制如图4所示团簇Fe4P异构化反应的lnK~ΔE关系图,由此得到两者关系的线性方程:lnK=0.403 3ΔE+0.022 79。 由于四重态构型之间转化的可能性更大,且具有较大的反应速率,另外能量差越大,反应程度越大。因此以四重态中具有最低能量的构型1(4)为生成物,除构型2(4)以外的构型为反应物,即假设构型3(4)、4(4)、5(4)均可与构型1(4)发生异构化转化反应。将3种反应的ΔE代入团簇Fe4P异构化反应的lnK~ΔE线性方程,求出3种反应的lnK值,即图4中的预测点(分别为10.742、11.344、23.939)。由图1可知,四重态构型5(4)与构型1(4)的能量差最大(58.180 kJ·mol-1),且其反应的平衡常数也最大(2.492×107),而构型2(4)与构型1(4)之间的能量差值最小(10.340 kJ·mol-1),与之对应的平衡常数也最小(69.190)。综上可知,团簇Fe4P四重态构型发生异构化转化反应的平衡常数为69.190~2.492×107,且反应的彻底性随能量差的增大而增大。 根据范特霍夫方程:lnK=-ΔH/RT+ΔS/R,可知lnK和1/T呈线性关系。将表5团簇Fe4P的4种异构化转化反应的ΔH、ΔS平均值代入范特霍夫方程中,即可得出lnK与1/T的线性关系方程:lnK=8 074.453/T+0.310,由此线性关系可计算不同温度下团簇Fe4P异构化反应的反应程度,进而满足实际操作所需的条件。除此之外,依据表1团簇Fe4P的8种优化构型的热力学参数,可计算出不同构型进行转化所需的焓变ΔH及吉布斯自由能变ΔG,并结合ΔG的定义式:ΔG=ΔH-TΔS及lnK与1/T关系式,可得出常温下不同构型进行转化的ΔS、lnK,从而可以多角度对团簇Fe4P异构化反应的限度进行预测。采用上述方法对图4中预测点所对应的异构化反应于298.15 K下进行预测,计算结果如表6所示。由表6可知,异构化反应3(4)→1(4)、4(4)→1(4)、5(4)→1(4)的ΔG均为负值,说明常温下此三种异构化反应均可自发发生,且反应的彻底性随反应物与生成物能量差的增大而增大。此外,对于异构化反应5(4)→1(4),其反应的熵变(ΔS)为负值,说明该反应发生的条件较为苛刻,因此可根据条件选择最适宜的反应用于实际操作中。 图4 团簇Fe4P异构化转化反应的lnK与ΔE关系图Fig.4 Relationship between lnK and ΔEin the isomerization of Fe4P clusters 表5 298.15 K下团簇Fe4P的4种异构化转化反应的热力学函数变化量 表6 298.15 K下团簇Fe4P预测异构化转化反应的参数 根据过渡态理论,确定团簇Fe4P的8种优化构型进行异构化反应的4种空间结构,并从化学热力学和动力学方面对团簇Fe4P的异构化反应进行探究,结果如下: 1) 四重态构型之间进行异构化转化的可能性比不同重态构型进行转化的可能性更大,即自旋多重度会影响团簇Fe4P异构化转化反应;对于异构化反应4(4)→3(4),由于其活化能最小,反应速率最大且相近,可视为可逆反应,且较其他3种异构化反应,该反应更容易发生;对于异构化反应3(4)→2(2),因其活化能最大,反应速率最小,可知该反应发生的难度最大。 2) 根据lnK与ΔE的线性关系:lnK=0.403 3ΔE+0.022 79,可知四重态中高能量的构型向低能量构型转化的平衡常数为69.190~2.492×107,且反应的彻底性随能量差的增大而增大。除此之外,由范特霍夫方程:lnK=-ΔH/RT+ΔS/R及吉布斯自由能变的定义式:ΔG=ΔH-TΔS可以计算不同温度下各构型进行转化的平衡常数,进而满足实际操作所需的温度条件。2.3 团簇Fe4P异构化反应的化学动力学研究


3 团簇Fe4P异构化反应的预测


4 结论

