阿维菌素类药物残留检测方法研究进展
*张强英 夏露
(西藏大学理学院 西藏 850000)
引言
随着生产生活水平的不断提高,环境问题逐渐显现,农药残留污染已经成为人类面临的最严重的环境问题之一。农药残留引起了大众的广泛关注,促使科研人员建立采用检测限低,精确度高,特异性好且适宜的药物残留检测方法。环境中阿维菌素类药物浓度的检测一直是值得关注的课题,其对环境保护和人类健康都具有重要的意义。
阿维菌素被誉为当今最有前途的抗虫抗生素,是迄今为止活性最高的生物源杀虫剂[1]。阿维菌素类药物是由阿维链霉菌发酵产物提取出的一类新型抗生素类生物农药,分为A、B两类,每类包含四个组分,其中B1a抗虫活性最强。阿维菌素由B1a(≥80%)和B1b(≤20%)组成。在后续研究中,以阿维菌素主要生物活性物质B1a和B1b结构为基础不断合成新物质,如伊维菌素、多拉霉素、乙酰基阿维菌素等(结构如图1所示)。阿维菌素因药物高效、广谱、独特的作用机制等特点广泛应用于田间作物。我国在80年代后期开始自主研制阿维菌素,将其研发列为国家“七五”“八五”“九五”的重点科技攻关项目,随着攻关目标的不断完成,我国已成为世界上惟一的阿维菌素原药生产国。阿维菌素类药物对人体有毒害作用,中毒轻者出现头疼、呕吐等症状,严重时可危及生命、致人死亡。因阿维菌素原药的半数致死量(LD50)为10ng/g,国际国内都将其列为高毒化合物,我国农业部也明确规定了各类食品中阿维菌素最高残留限量值[2]。
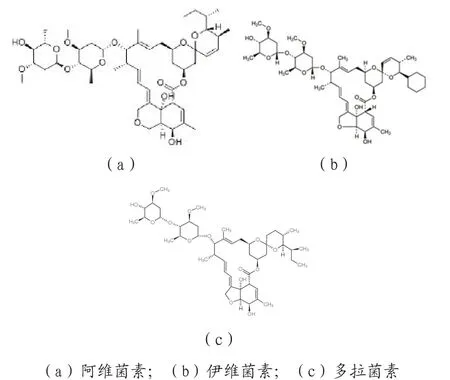
图1 阿维菌素类药物分子结构
本文将详细综述阿维菌素类药物残留检测方法,系统分析被测组分、待测样品、流动相、检出限、变异系数、平均回收率等参数,总结阿维菌素类药物残留检测方法的优缺点及适用范围,为研究人员建立检出限更低、精确度更高、特异性更好的残留检测方法提供参考。
1.阿维菌素类药物残留的检测方法
目前,已有较多的方法用于阿维菌素类药物残留检测,液相色谱法最经典和常用,液相色谱法可以按不同的前处理方法分为高效液相色谱(HPLC)、固相萃取SPE-UHPLC、QuEChERS-HPLC等;也可以按照检测器不同分为高效液相色谱-电二极管阵列检测法(HPLC-PDA)、高效液相色谱紫外检测法(HPLC-UV)、高效液相色谱荧光检测法(HPLEFLD)、高效液相色谱-串联质谱法(HPLC-MS/MS)等。通常紫外检测器灵敏度较差,荧光检测灵敏度较高,但衍生化步骤繁琐,而质谱检测器具有更高灵敏度和低检出限。
下文将重点分析以上三类常用检测方法,从被测组分、样品、流动相、检出限、变异系数、平均回收率等参数总结阿维菌素类药物残留检测方法的优缺点及适用范围。
(1)高效液相色谱紫外检测法
HPLC-UV通过液相色谱法分离被测样品中的待测组分,紫外分光光度计检测各组分的含量。液相色谱法是由于不同组分与流动相之间的分配系数或吸附能力不同的原理实现分离。紫外分光光度计是根据被测物质对紫外-可见光选择性吸收的特性进行检测。通过系统总结报道的HPLC-UV检测阿维菌素类药物的方法,并汇总于表1中。紫外检测法仅被用于检测阿维菌素与甲氨基阿维菌素苯甲酸盐,且以阿维菌素为主,被测组分单一;样品主要为大白菜、菠菜等蔬菜样品,检测样品种类少;最佳检测波长为245nm;甲醇是流动相中主要的有机相且在流动相中比例占85%以上,方法检出限为6~50ng/g,比其他常用方法检出限高1~2个数量级。原因可能是脂类、核酸等物质在阿维菌素吸收波长附近也进行紫外吸收,紫外检测器易受样品基质干扰,所以检测样品种类多为蔬菜。平均回收率在75.0%~112.03%范围内,变异系数在1.65%~9.77%之间。HPLC-UV具有操作流程简单,但紫外检测器灵敏度较差,加之待测样品干扰严重,无法满足农产品分析。
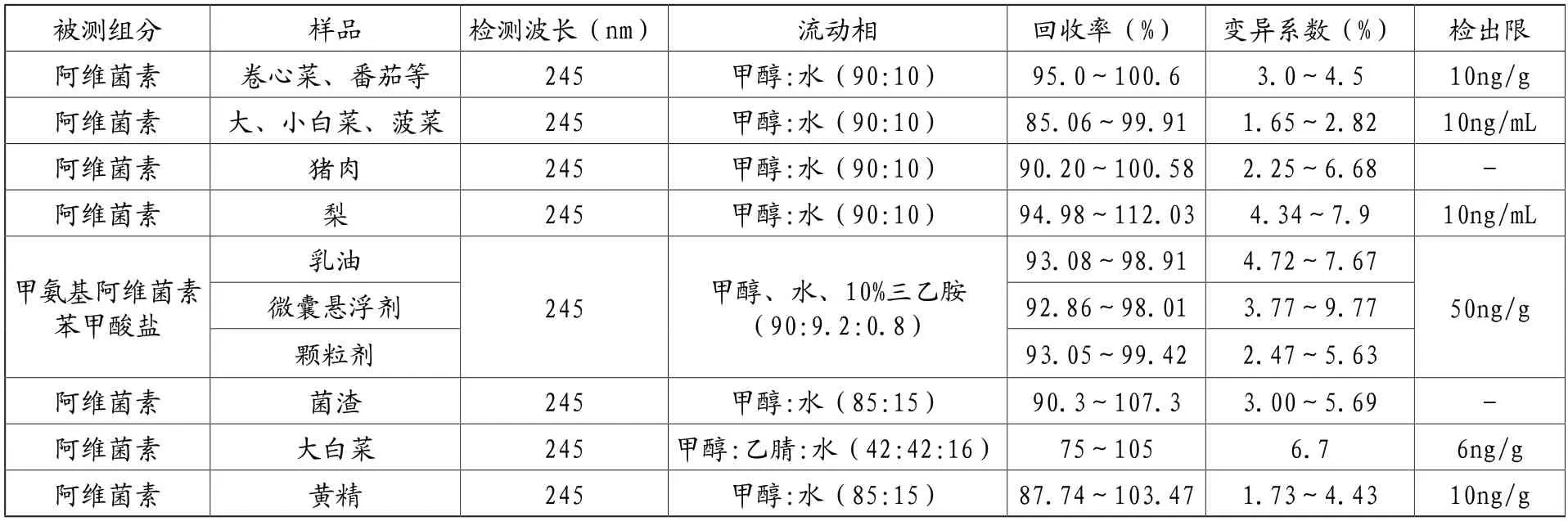
表1 HPLC-UV检测阿维菌素类药物残留
(2)高效液相色谱荧光检测法
HPLC-FLD分离原理与HPLC-UV相同,荧光检测器进行定量分析,荧光检测器是依据待测组分的特定结构能够发射荧光进行检测。阿维菌素类药物需要进行荧光衍生化。通过系统总结报道的HPLC-FLD检测阿维菌素类药物的方法,并汇总于表2中。HPLC-FLD检测组分众多,包括了阿维菌素、伊维菌素、多拉菌素、埃普利诺菌素、甲氨基阿维菌素及其苯甲酸盐、莫西菌素和乙酰氨基阿维菌素,基本涵盖所有的阿维菌素类药物;激发波长为365nm,发射波长有475nm、470nm和463nm,较为常用的是470nm和475nm;所测样品种类丰富,可以检测土壤、水样、蔬果等样品,偏向于检测肉类、动物内脏及其奶制品等样品。该方法需要使用的衍生化剂主要是由N-甲基咪唑和三氟乙酸酐两种物质与乙腈以一定比例配制形成;甲醇和乙腈是流动相中主要的有机相且比例往往在90%以上;检出限在0.1~5.0ng/g之间,低于我国规定的阿维菌素、伊维菌素等的MRL,能够检测样品中的阿维菌素残留量。大部分平均回收率在70.0%~113%范围内,变异系数在1.4%~11.6%之间。HPLC-FLD方法不足之处在于被检测物需要进行荧光衍生化,样品多为脂肪、肉类,需要较为繁琐的前处理技术,操作相对复杂。
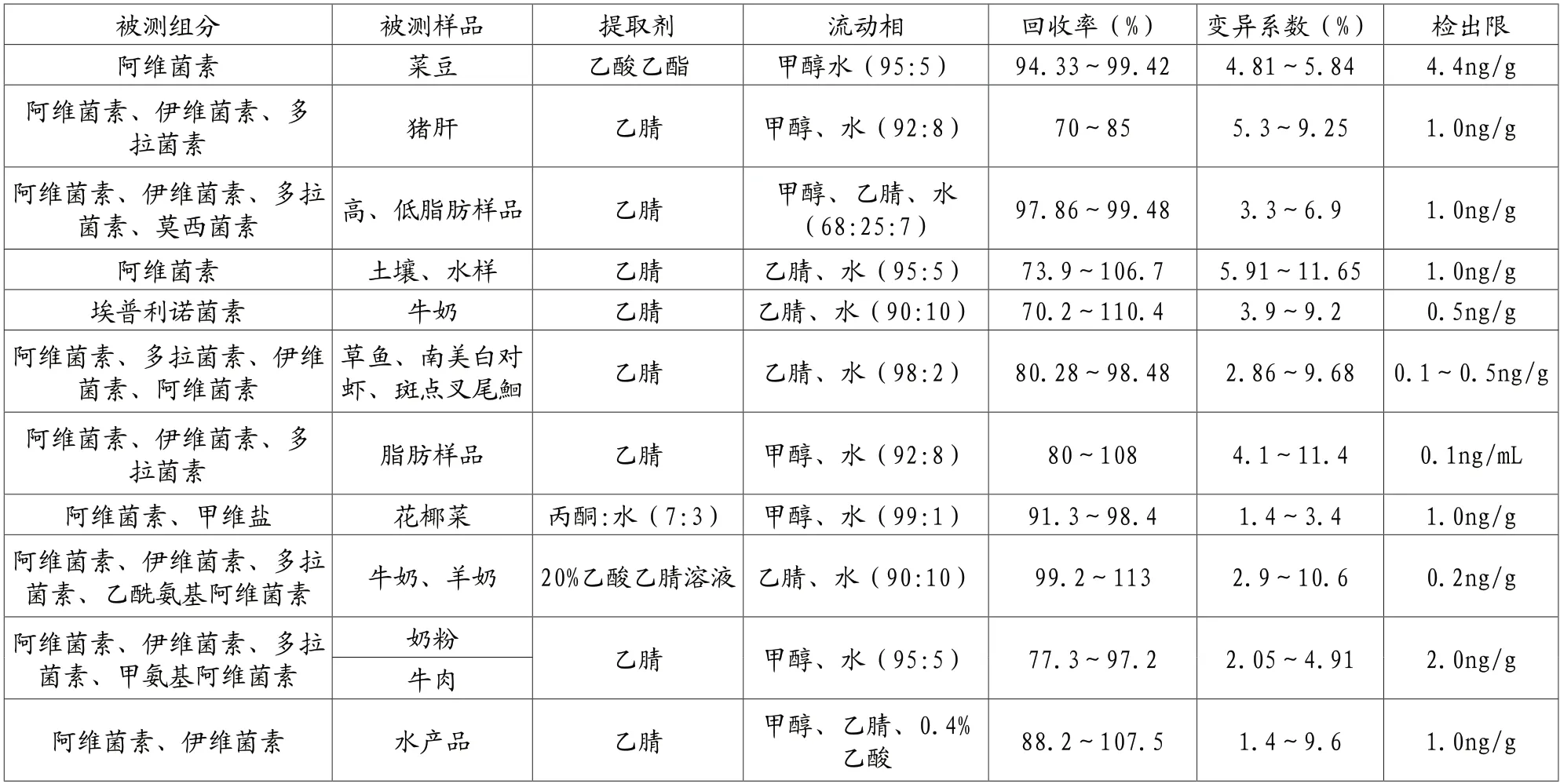
表2 HPLC-FLD检测阿维菌素类药物残留
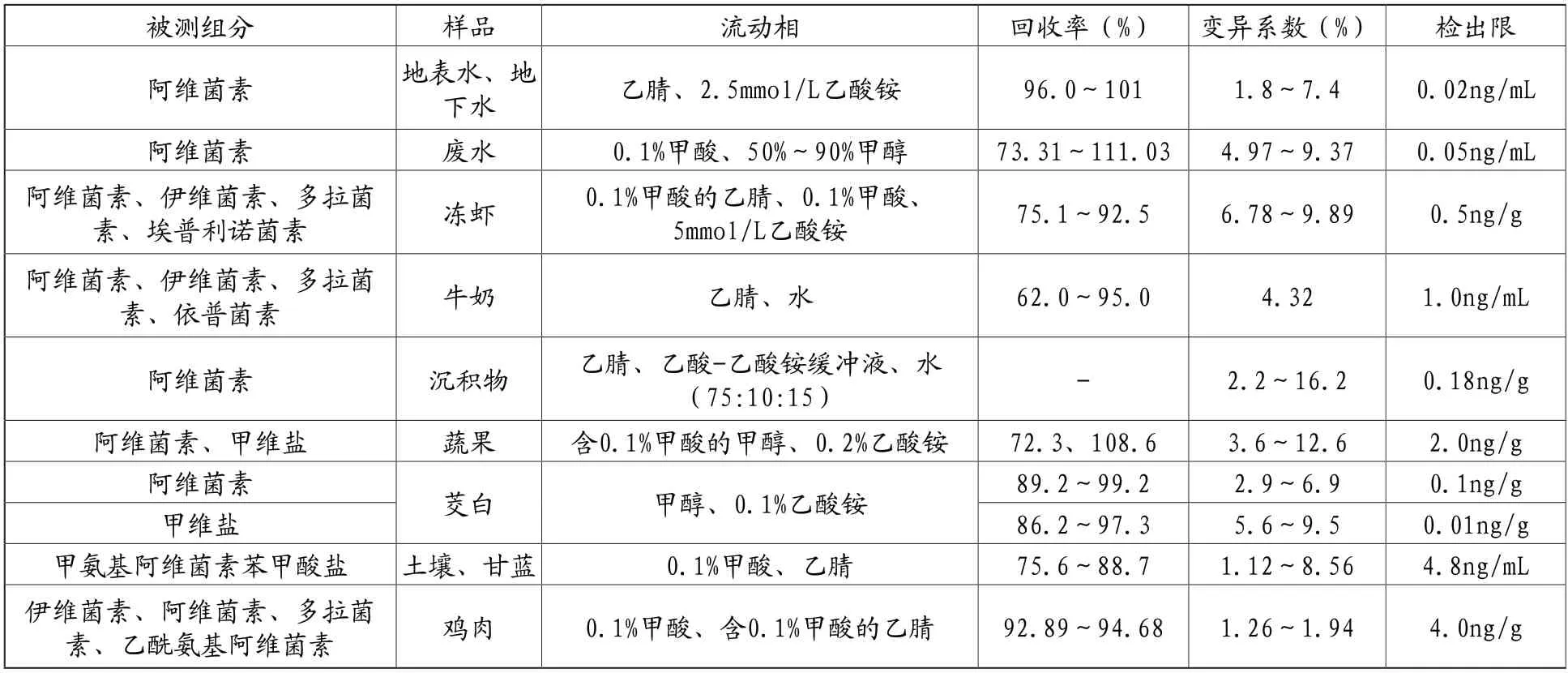
表3 HPLC-MS/MS检测阿维菌素类药物残留
(3)高效液相色谱-串联质谱法
HPLC-MS/MS分离原理与HPLC-UV、HPLC-FLD相同,三重四级杆质谱仪进行定性定量分析。质谱仪是根据质量不同的带电粒子在电磁场中偏转距离不同来分离检测物质。何书海等采用高效液相色谱-串联质谱法检测地表水和地下水中阿维菌素残留量,在2.5mmol/L乙酸铵水溶液-乙腈的流动相下,样品在保留时间2.86min出峰,如图2所示。
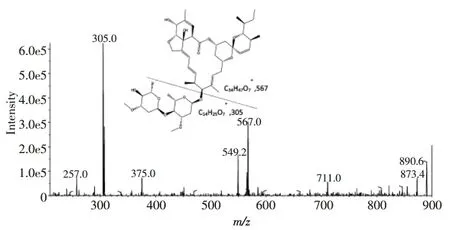
图2 阿维菌素质谱图
2.结论
本文通过检测方法的被测组分、样品、检出限、平均回收率,变异系数等参数总结三种阿维菌素类药物残留量检测方法的优缺点及适用范围,得出以下结论:
HPLC-UV检出限较高,操作流程简单,适用于对检出限要求不高的单一组分,不适合复杂的脂质样品分析,蔬菜是其主要分析对象。
HPLC-FLD检出限比HPLC-UV低1~2个数量级,比HPLCMS/MS的高1~2个数量级。但需要被测组分进行荧光衍生化,需要较为繁琐的前处理技术,操作相对复杂。适用于检测对检出限有一定要求的单一组分或多组分,动物肉类、内脏及其奶制品等样品分析。
HPLC-MS/MS检出限低,准确度和精确度高,适用于检测更低残留的单一组分或多组分,是检测阿维菌素类药物残留的主要发展趋势。

