PCSK9抑制剂在不同危险分层动脉粥样硬化性心血管疾病PCI术后的应用价值
张 亮,刘建正,李 迎,张子鑫,林 琦,王 芳,杨旺伟,杨 华,张亚敏,贺 媛,陈继军
动脉粥样硬化性心血管疾病(ASCVD)的发病率及病死率已经超过恶性肿瘤及其他系统疾病[1-2]。低密度脂蛋白胆固醇(LDL-C)是目前公认的ASCVD发生及发展的主要危险因素[3],降低其水平已被证实与降低心血管事件的发生风险密切相关[4]。他汀类药物可显著降低血清LDL-C水平,进而降低心血管事件的发生风险[5]。根据2018年AHA/ACC胆固醇管理指南[6],对于<75岁的无论超高危或非超高危ASCVD患者,推荐LDL-C下降≥50%。根据2020年“超高危ASCVD患者血脂管理中国专家共识”[7],对于超高危ASCVD患者,建议LDL-C降至1.4 mmol/L以下且较基线LDL-C下降≥50%。然而,部分患者使用他汀类药物后出现LDL-C不达标、肝功能损害、肌痛、乏力等不耐受现象[8],尤其对于需要高强度他汀类药物强化治疗的ASCVD患者,不能达到有效的他汀类药物治疗剂量,最终影响ASCVD的临床转归。前蛋白转化酶枯草溶菌素9(PCSK9)抑制剂是新型降脂药物,为人单克隆免疫球蛋白,通过上调肝细胞表面LDL受体而增加肝脏对LDL-C的清除,从而有效降低血浆LDL-C水平[9]。因此PCSK9抑制剂在各种指南中的推荐级别较高,且越来越多的非超高危ASCVD患者使用PCSK9抑制剂。但PCSK9抑制剂应用范围是否可扩大,目前仍不清楚。故我们设计此回顾性研究,为不同危险分层ASCVD患者行经皮冠状动脉介入(PCI)术后使用PCSK9抑制剂提供参考。
1 资料与方法
1.1 一般资料
回顾性分析2020年1—6月空军军医大学第一附属医院心血管内科收治的行PCI术并使用PCSK9抑制剂的ASCVD 200例的临床资料。根据“超高危ASCVD患者血脂管理中国专家共识”[7],其中100例为非超高危ASCVD患者(非超高危组),100例为超高危ASCVD患者(超高危组)。纳入标准:年龄<75岁;行PCI术后的ASCVD患者。排除标准:年龄≥75岁者;使用PCSK9抑制剂时间<3个月;对PCSK9抑制剂过敏者;孕妇及哺乳期妇女;重度肝功能不全;拒绝使用PCSK9抑制剂者。
1.2 方法
所有患者在入院后行冠状动脉造影联合PCI术治疗,2组调脂治疗方案均为中等强度他汀类药物联合PCSK9抑制剂。其中他汀类药物主要为阿托伐他汀钙20 mg每晚1次或瑞舒伐他汀钙10 mg每晚1次;PCSK9抑制剂140 mg皮下注射,每2周1次,共使用3个月。
1.3 观察指标
收集所有患者的基线资料,包括性别、年龄、肝功能(天冬氨酸转氨酶、丙氨酸转氨酶)、肾功能[肌酐、尿素、肾小球滤过率(GFR)]、血脂[三酰甘油(TG)、总胆固醇(TC)、LDL-C、高密度脂蛋白胆固醇(HDL-C)、脂蛋白-α(Lp-α)]、超敏C反应蛋白(hs-CRP)、高血压病史、糖尿病史、吸烟史、饮酒史、缺血性脑卒中史、周围血管疾病史、左心室射血分数(LVEF)、急性冠状动脉综合征(ACS)病史、既往行PCI术、既往行冠状动脉旁路移植(CABG)及本次造影病变血管数目等。比较基线资料及使用PCSK9抑制剂3个月后的血脂及hs-CRP变化水平。根据2018年AHA/ACC胆固醇管理指南,治疗3个月后,LDL-C≤1.4 mmol/L,且与基线相比下降幅度≥50%,定义为超高危组LDL-C达标;LDL-C下降幅度≥50%,定义为非超高危组LDL-C达标。
1.4 统计学方法
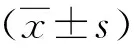
2 结果
2.1 基线资料
超高危组与非超高危组在年龄、性别方面比较差异均无统计学意义(P>0.05)。用药前,超高危组ACS史、脑卒中史、糖尿病史、周围血管疾病史发生率高于非超高危组,病变血管数目多于非超高危组,天冬氨酸转氨酶、肌酐水平高于非超高危组,GFR及LVEF低于非高超危组,差异有统计学意义(P<0.05,P<0.01)。见表1。
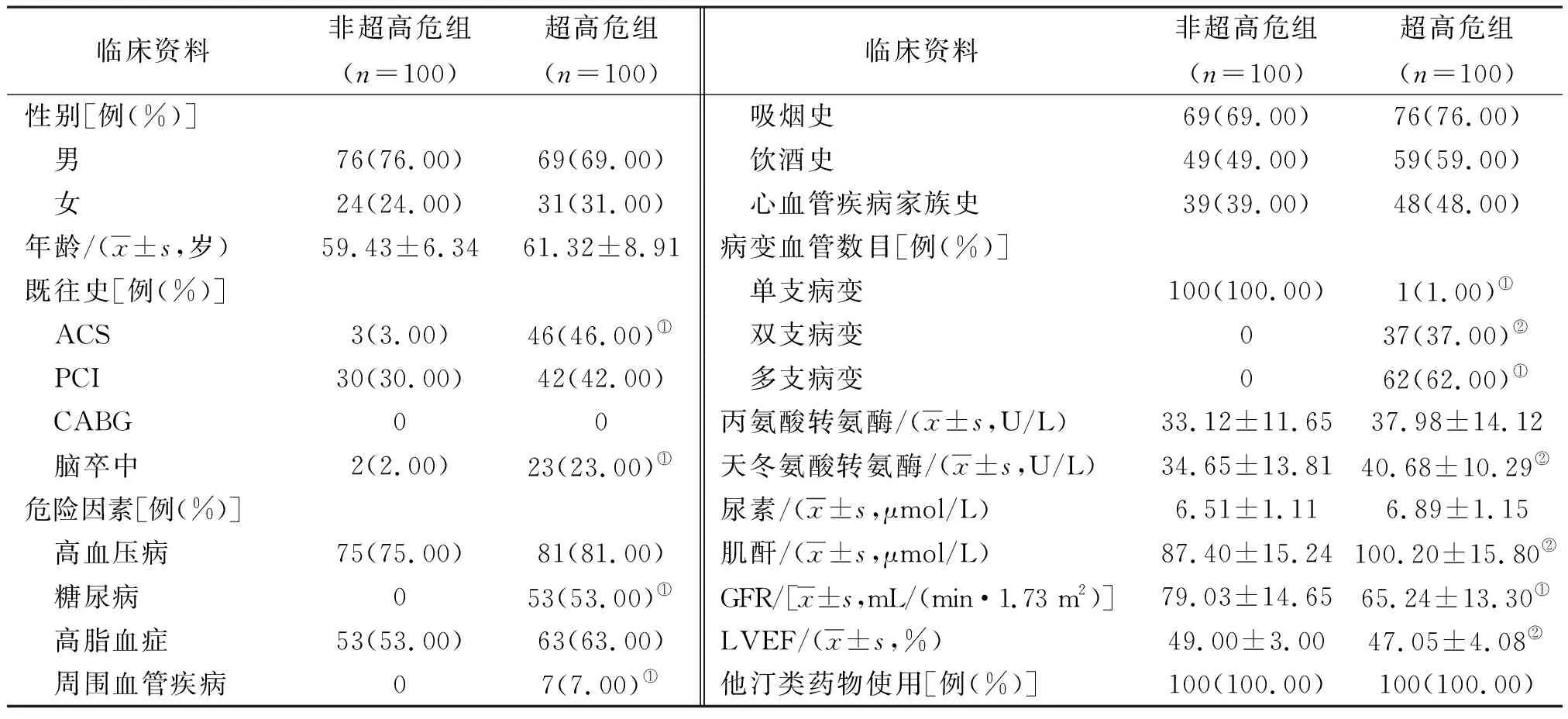
表1 2组行PCI术ASCVD基线资料比较
2.2 血脂指标及hs-CRP
2组治疗前TG、TC、LDL-C、HDL-C、Lp-α比较差异均无统计学意义(P>0.05);但超高危组hs-CRP高于非超高危组,差异有统计学意义(P<0.05)。治疗后,2组TG、TC、LDL-C、Lp-α及hs-CRP均低于治疗前,HDL-C高于治疗前(P<0.05);治疗后,2组间TG、TC、LDL-C、HDL-C、hs-CRP比较差异均无统计学意义(P>0.05),但超高危组Lp-α水平低于非超高危组(P<0.05)。见表2。与治疗前比较,2组治疗后校正了基线LDL-C,超高危组LDL-C下降幅度为(61.35±7.38)%,非超高危组为(60.27±4.46)%,2组比较差异无统计学意义(P>0.05)。根据LDL-C达标的定义,应用PCSK9抑制剂后,LDL-C达标率超高危组为70.0%,非超高危组为82.5%。
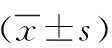
表2 2组行PCI术ASCVD治疗前后血脂及hs-CRP水平比较
2.3 不良事件
应用PCSK9抑制剂治疗3个月后,非超高危组再发心绞痛2例(2.00%),超高危组再发心绞痛4例(4.00%)。2组再发心绞痛发生率比较差异无统计学意义(P>0.05),调整药物后症状均缓解。2组均未发生再次血运重建、靶血管相关的心肌梗死及其他严重心血管不良事件。
2.4 药物不良反应
在200例应用PCSK9抑制剂者中发生局部红肿6例,但均较轻微,不需要特殊治疗,未发生其他严重不良反应。所有患者肝肾功能、血常规无明显变化。
3 讨论
本研究得出的结论有:1)超高危组与非超高危组ASCVD在应用PCSK9抑制剂治疗3个月后,LDL-C均明显下降,下降幅度均>60%,达标率均>70%;2)2组均未发生再次血运重建、靶血管相关的心肌梗死及其他严重心血管不良事件;3)2组均无严重不良反应。
LDL-C是导致冠心病的危险因素之一,降低LDL-C水平是预防与治疗冠心病的重要手段[10]。有研究表明,LDL-C每降低1 mmol/L,可使主要心血管不良事件发生率降低20%,全因病死率降低10%[11]。因此,2019年ESC/EAS血脂管理指南[12]提出了更高的要求:LDL-C越低越好。近年,我国ASCVD发病率仍呈上升趋势,超高危ASCVD患者越来越多,且亚洲人群对高强度的他汀类药物耐受性较差[13],从而导致超高危ASCVD患者LDL-C达标率低。PCSK9抑制剂降低LDL-C水平的安全性及有效性得到了验证。有研究评估了PCSK9抑制剂在心血管事件高危患者二级预防中的作用,结果显示PCSK9抑制剂组可使LDL-C降幅达59%,同时,主要终点事件(心肌梗死、不稳定型心绞痛住院、冠状动脉血运重建、卒中或心血管疾病相关死亡)发生风险降低20%[14]。本研究显示,无论超高危或非超高危ASCVD患者,用药后LDL-C水平明显下降,在校正基线LDL-C后,中等强度他汀类药物联合PCSK9抑制剂治疗后,2组LDL-C水平降幅均>60%,与文献[15]报道一致。
既往有研究发现,Lp-α是独立于LDL-C、HDL-C且与冠心病发生风险呈正相关的危险因素,降低其水平可有效减少冠心病患者不良事件[16]。本研究也发现,应用PCSK9抑制剂可以降低Lp-α水平,尤其是超高危组下降更明显。这可能是用药后心血管不良事件发生率下降的原因之一。但因本研究为回顾性小样本量研究,未来可以根据本研究结果开展多中心、随机对照研究,进一步验证PCSK9抑制剂降低Lp-α水平后与心血管不良事件之间的关系。安全性方面,在推荐剂量下,本研究所观察的200例应用PCSK9抑制剂者中仅6例发生轻微局部红肿,均不需要临床处理,余均未出现严重的不良反应。
综上所述,在中等强度他汀类药物治疗的基础上联合应用PCSK9抑制剂可能会大幅度降低PCI术后不同危险分层ASCVD患者LDL-C及Lp-α水平,且安全性良好。由于本研究属于回顾性研究,混杂因素较多,观察时间较短、样本量较小,PCSK9抑制剂降低心血管事件发生率的统计学效力较低,期待未来开展关于国人的大样本量、随访时间更长的相关性研究,进一步评估PCSK9抑制剂对不同危险分层的ASCVD且行PCI术患者的安全性及有效性。对于非超高危ASCVD患者,使用PCSK9抑制剂的性价比需要更长时间的随访来证实,同时可以证实该药是否可降低靶血管或非靶血管的再次血运重建等心血管不良事件发生率。此外,目前的指南推荐在他汀类药物治疗LDL-C不达标时可以加用依折麦布,以使LDL-C水平降低。那么,根据本研究结果,当LDL-C不达标时是否可以直接应用PCSK9抑制剂,快速有效地降低LDL-C水平,预防心血管不良事件发生?未来可以开展中等强度他汀类药物联合依折麦布与中等强度他汀类药物联合PCSK9抑制剂治疗ASCVD的对比研究,明确对心血管不良事件的影响。

