不同年龄病理性近视脉络膜新生血管患者黄斑形态和微循环指标比较
刘 坤, 徐清怡, 朱 俊, 陈 放
(1. 江苏省建湖县人民医院 眼科, 江苏 盐城, 224700;2. 扬州大学附属苏北人民医院 眼科, 江苏 扬州, 225001)
病理性近视脉络膜新生血管(PM-CNV)是可以导致中心视力突然丧失的严重影响患者视力的病理性近视(PM)并发症之一[1]。研究[2]表明, 50岁以下的脉络膜新生血管(CNV)患者中, PM-CNV是最常见的病因。老年PM-CNV患者可能同时具有老年性黄斑变性和PM的临床病理生理特征[3], 故老年PM-CNV患者的治疗方案与青年患者是否应该有所区别值得进一步探讨。本研究对PM-CNV患者进行常规眼科检查和光学相干断层成像(OCT)、光学相干断层扫描血管成像(OCTA)检查,比较不同年龄层PM-CNV患者的基本特征、患眼黄斑形态和微循环指标水平,现将结果报告如下。
1 资料与方法
1.1 一般资料
采用横断面研究方法分析2019年12月—2022年11月在江苏省苏北人民医院确诊PM-CNV的70例患者(均为单眼发病,共纳入70眼)的临床资料,根据年龄的不同将患者分为≤50岁组18例(18眼)和>50岁组52例(52眼)。纳入标准: ① 有高度近视病史,等效球镜度数(SE)≥-6.0 D或眼轴≥26.5 mm者; ② OCTA检查提示CNV存在者。排除标准: ① 既往接受过光动力疗法,或有玻璃体腔注射抗血管内皮生长因子(VEGF)药物治疗史及玻璃体视网膜手术史者; ② 存在其他可引起CNV的眼部疾病(老年黄斑变性、血管样条纹、中心性渗出性脉络膜视网膜病变、炎症性疾病等)者; ③ 存在其他影响视力的眼部疾病(糖尿病性视网膜病变、青光眼、视网膜静脉阻塞、葡萄膜炎等)者; ④ 屈光介质混浊导致OCT、OCTA图像质量不佳或严重影响视力者。≤50岁组患者平均年龄(38.22±9.59)岁,男9例、女9例; >50岁组患者平均年龄(65.04±9.70)岁,男16例、女36例。2组患者性别构成比较,差异无统计学意义(P=0.142)。本研究遵循《赫尔辛基宣言》要求,且获得苏北人民医院伦理委员会批准(伦理批号2022ky131)。
1.2 方法
记录所有患者的年龄、性别、患病眼别,均给予裂隙灯检查(日本Topcon株式会社)、OCT与OCTA检查(美国Optovue公司RTVue XR)和最佳矫正视力(BCVA)、眼轴(IOL-Master眼科光学生物测量仪,德国Zeiss公司)、SE检查。
检查方法: ① BCVA检查采用国际标准视力表,并转换为LogMAR视力进一步统计分析。② 眼轴测量由同一检查者完成,每只眼进行5次测量后取平均值。③ OCT检查指标由3位经验丰富的眼科技师手动测量取平均值,记录并分析黄斑中心凹下外层视网膜结构,主要包括Bruch膜、嵌合体带完整性,黄斑中心凹1 mm×1 mm范围内连续则视为完整,若不连续则视为不完整。④ OCTA扫描范围为以中心凹为中心的3 mm×3 mm区域,自动去除眼球运动伪影,每次扫描后仔细校对分层是否正确,若遇到机器不能正确分层的情况,由2位经验丰富的眼科技师手动调整错误分区。设备自动测量得到黄斑区浅层及深层毛细血管网血流密度,在Flow工具中,选择脉络膜毛细血管层,以黄斑中心凹为中心对半径1.0 mm的圆形区域自动化测量血流面积,脉络膜毛细血管血流密度(CC-VD)为血流面积与选中圆形区域面积的比值。手动选取CNV后,设备自动测量CNV面积、CNV血流面积,机器自动将黄斑区划分为直径分别为1 mm和3 mm的内环和外环,中心凹为内环以内区域,旁中心凹为内环、外环之间的区域,根据CNV相对中心凹的位置将CNV位置定义为中心凹下及中心凹外。黄斑中心凹视网膜厚度(CMT)为黄斑中心凹1 mm范围内界膜到视网膜色素上皮(RPE)层的平均垂直距离,中心凹下内层视网膜厚度(IRT)为黄斑中心凹1 mm范围内界膜到内丛状层的平均厚度,中心凹下外层视网膜厚度(ORT)为黄斑中心凹1 mm范围内从内核层到RPE层的平均厚度,中心凹下脉络膜厚度(SFCT)为Bruch膜下10 μm至巩膜内表面的垂直距离; 视网膜浅层毛细血管血流密度(SCP-VD)为内界膜至内丛状层上10 μm区域内的血流密度; 视网膜深层毛细血管血流密度(DCP-VD)为内丛状层上10 μm至外丛状层上10 μm区域内的血流密度。
1.3 统计学分析

2 结 果
2.1 眼科常规检查结果
≤50岁组患者平均LogMAR BCVA为(0.56±0.35), >50岁组为(0.69±0.34), 差异无统计学意义(P=0.164); ≤50岁组患者SE为-11.88(-17.00, -9.19)D, >50岁组为-12.00(-15.00, -9.63) D, 差异无统计学意义(P=0.556); ≤50岁组患者平均眼轴为28.70(26.93, 30.16) mm, >50岁组为28.74(27.86, 29.76) mm, 差异无统计学意义(P=0.587)。
2.2 黄斑形态指标水平比较
≤50岁组CMT、ORT均小于>50岁组,但差异无统计学意义(P=0.106、0.134); ≤50岁组IRT大于>50岁组,但差异无统计学意义(P=0.797); ≤50岁组SFCT大于>50岁组患者,差异有统计学意义(P<0.001)。见表1。
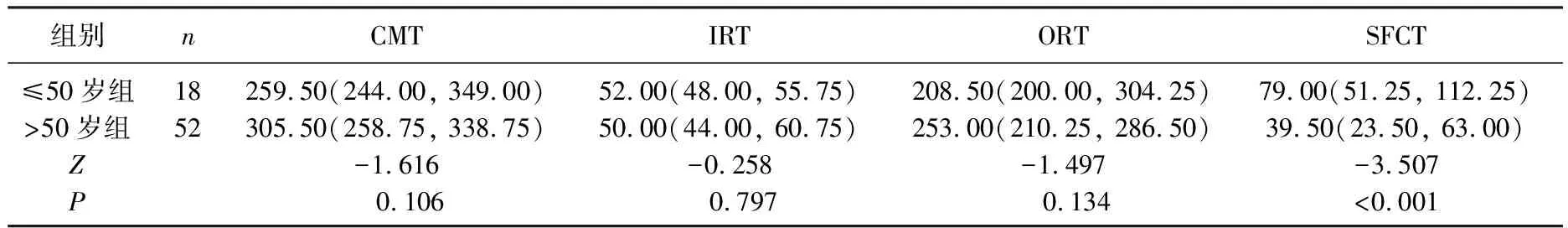
表1 2组黄斑区视网膜厚度比较[M(P25, P75)] μm
黄斑中心凹下外层视网膜结构观察结果显示, ≤50岁组嵌合体完整者7例(占38.89%), >50岁组嵌合体完整者19例(占36.54%), 差异无统计学意义(P=0.859); ≤50岁组Bruch膜完整者14例(占77.78%), >50岁组Bruch膜完整者37例(占71.15%), 差异无统计学意义(P=0.586)。
2.3 黄斑区微循环指标水平比较
≤50岁组的SCP-VD高于>50岁组,差异有统计学意义(P=0.001); 2组DCP-VD、CC-VD比较,差异无统计学意义(P=0.384、0.348)。见表2。

表2 2组黄斑区微循环指标水平比较 %
2.4 CNV相关指标水平比较
≤50岁组CNV面积、CNV血流面积分别为0.43、0.39 mm2, >50岁组则分别为0.38、0.29 mm2, 2组比较差异无统计学意义(P=0.326、0.242)。≤50岁组中, CNV位于中心凹下11例、中心凹外7例; >50岁组中, CNV位于中心凹下35例、中心凹外17例。2组CNV位置比较,差异无统计学意义(P=0.633)。
3 讨 论
PM是全球常见的致盲眼病之一,其并发症CNV会造成严重的视力损害[1]。PM-CNV的发病机制尚未完全明确,既往研究[4]认为PM患者眼轴不断增长造成Bruch膜破裂,促血管生长因子与抗血管生长因子之间的平衡被打破,继而诱导CNV形成。然而有研究[5]发现CNV也可以出现在正常眼轴的高度近视患者中,而这些患者普遍存在黄斑区循环缺血及局部脉络膜组织萎缩,提示包含脉络膜结构的黄斑形态结构及微循环异常可能参与PM-CNV的形成。OCT、OCTA能以无创方式提供视网膜和脉络膜断层结构及分层血流信息,并能定量评估视网膜及脉络膜毛细血管网密度[6], 因此本研究基于OCT、OCTA检查对PM-CNV患者黄斑区视网膜形态、微循环指标水平及CNV相关指标水平进行分析。
西欧地区的一项研究[7]显示,年龄小于50岁的CNV患者中, PM-CNV约占62%, 且PM是西欧地区CNV患者最常见的致病因素。中国一项针对青年CNV患者的研究[8]显示, PM位列青年CNV病因第2位,可见PM-CNV在青年患者中发病率很高。随着时间的推移, PM的高发病率必将导致老年PM-CNV患者数量不断增加,而老年PM-CNV的病因更加复杂,预后结局可能比青年PM-CNV患者更差。比较不同年龄PM-CNV患者黄斑形态与微循环指标水平的差异,或可为PM-CNV的发病机制与治疗策略研究提供更多的临床依据。本研究结果显示, >50岁组PM-CNV患者的SFCT小于≤50岁组,差异有统计学意义。近年来较多研究[5, 9]发现高度近视患者的脉络膜厚度显著小于视力正常人群,脉络膜厚度减小可能提示脉络膜循环不良,可导致患者视功能受损甚至视力丧失,因而脉络膜厚度与BCVA显著相关。脉络膜厚度可间接反映脉络膜供血情况, PM-CNV患者中,老年患者的脉络膜厚度较年轻患者更小,提示老年PM-CNV患者脉络膜循环水平更差,甚至可能存在更严重的脉络膜缺血情况。
相关研究[10]提出,脉络膜循环的血流动力学改变是CNV出现的原因之一,脉络膜变薄会引起脉络膜缺血,促进VEGF分泌,进而促进新生血管产生。本研究中, >50岁组的样本量显著多于≤50岁组, >50岁组患者的SFCT显著小于≤50岁组,提示SFCT与PM、年龄存在相关性,即老年患者脉络膜厚度更小,脉络膜缺血更严重,并发PM-CNV的概率更高。
研究[11]发现, 2年随访期间内发生近视性黄斑病变进展的患者,其基线SFCT较无黄斑病变进展患者更薄,并提出SFCT是近视黄斑病变进展的独立预测因子。因此, SFCT间接反映了脉络膜供血情况,脉络膜变薄是评价脉络膜缺血的生物标志物,是近视黄斑病变发展的一个重要的潜在危险因素,提示老年PM-CNV患者的脉络膜循环不良可能更倾向于发生黄斑病变的进展,进而导致预后较青年患者差。但值得注意的是, >50岁组患者SFCT更低,但>50岁组患者脉络膜毛细血管血流密度与≤50岁组比较差异无统计学意义。由此提示, SFCT可能较微循环指标可以更先一步提示患者脉络膜循环水平下降,更早一步对患者预后进行预测。
黄斑是体内代谢最活跃的组织之一,在许多疾病状态的早期即受到缺氧条件的影响。由于高需氧量,黄斑具有多个周围毛细血管丛,其完整性和功能依赖于这些毛细血管丛的健康。本研究中, ≤50岁组患者SCP-VD显著高于>50岁组,但2组DCP-VD无显著差异,提示>50岁患者的浅层视网膜微循环相较≤50岁患者损害更重,但深层视网膜微循环则无显著差异。PM患者的视敏度会随着DCP-VD的降低而显著降低, SCP-VD则对视敏度无显著影响,提示DCP-VD与PM患者视功能损害有关。深层视网膜毛细血管丛嵌于内核层和外丛状层,有助于为光感受器内节段提供氧气[12]。PM患者的脉络膜变薄,脉络膜毛细血管丧失,因此DCP-VD降低可能导致光感受器缺氧和营养缺乏,进而造成视力下降。本研究中,虽然≤50岁组患者SCP-VD较>50岁组显著更高,但2组的DCP-VD无显著差异,故2组BCVA亦无显著差异。有研究[13]提出,年龄与SCP-VD、DCP-VD、全视网膜平均毛细血管血流密度均呈显著负相关。本研究中>50岁患者的SCP-VD显著更低,可能与其年龄增长带来的影响(如视网膜浅层毛细血管中血液流速减慢及血管阻力增加)有关。
本研究中,部分PM-CNV患者RPE与椭圆体带之间表现为边缘模糊,但2组嵌合体带、Bruch膜完整性差异均无统计学意义。黄斑区外层视网膜结构改变可能由CNV产生的渗出物导致,研究[14]表明黄斑形态结构改变可以早于视觉症状,且多达93%的患者在治疗后可以恢复正常。相关研究[15]发现,术前外层视网膜结构完整的患眼术后视力更好,因此外层结构的完整性对患者病情评估和疗效预测具有重要意义。外层视网膜结构中, Bruch膜被认为参与近视的发生,其病理性改变可能是近视发展的始动因素,也是造成PM进展的要素之一[16]。研究[17]提出, Bruch膜缺损对PM-CNV患者的视力预后和治疗效果有重要影响, Bruch膜形态不完整意味着预后更差,无Bruch膜缺损的患者则视力预后更好。本研究发现, >50岁患者的视网膜外层结构(嵌合体带、Bruch膜完整性)与≤50岁患者无显著差异,表明虽然视网膜外层结构对视力预后较为重要,但外层结构破坏的原因可能与疾病本身更为相关,与患者基线年龄则无关。

