溶胶-凝胶法制备Ce3+掺杂TiO2的研究
徐晓虹,叶 芬,吴建锋,张乾坤,宋 佳,李晓雪,余佳惠
(武汉理工大学材料科学与工程学院,湖北 武汉 430070)
0 前 言
半导体光催化剂因在处理水体污染方面有着优良的特性而得到了广泛的应用,其中TiO2纳米光催化剂是研究最多和最有应用前景的半导体光催化剂。但是由于其禁带宽度为3.2 eV,只能利用紫外光激发,限制了其的利用。因此扩宽TiO2纳米光催化剂吸收范围和提高光催化效率成为了现今的研究热点。目前对TiO2纳米光催化剂改性的方法很多,其中由于稀土易产生多电子组态,且具有丰富的能级、特殊的电子结构以及光谱性质,被广泛的应用到TiO2纳米光催化剂的改性中。
本文拟采用掺入稀土Ce3+来改善TiO2纳米光催化剂的光催化性能。稀土元素Ce3+离子的电子层结构为[Xe]4f1,有失去电子成为[Xe]4f0稳定态,被还原成Ce4+的趋势;该反应的发生引起电荷的不平衡,从而提高样品的光催化效率。Ce3+的半径为0.103 nm大于Ti4+的半径0.075 nm,会引起晶格膨胀,晶胞体积增大,晶格畸变容易引起TiO2晶格表面氧原子逃离;这些会使得TiO2晶格中电荷不平衡,从而减小光生电子-空穴对的复合率,这对提高掺杂TiO2的光催化活性有显著作用。Ce3+能级差为13.555 eV,相对禁带宽度比较大,而且其主要吸收光谱在紫外光区,因此在TiO2纳米光催化剂进行催化反应的时候可起敏化作用,从而提高光催化效率。
1 实 验
1.1 掺杂纳米TiO2的制备
取10 mL钛酸丁酯与20 mL的无水乙醇混合均匀,制成溶液a;将10 mL无水乙醇、5 mL冰醋酸、1.6 mL去离子水和1 mL PEG400混合均匀,并取一定量的硝酸铈晶体加入其中,完全溶解后将其转移至磁力搅拌器上搅拌30 min,制得溶液b。边搅拌边将a溶液逐滴加入到溶液b中,滴加完毕后在35 ℃恒温条件下继续搅拌2 h形成均匀的掺杂TiO2溶胶。室温下在密封的烧杯中置放陈化3d形成湿凝胶;将湿凝胶置于100 ℃恒温干燥箱中24 h,烘干后得到干凝胶,充分研磨成细粉;将干凝胶粉置于程序控温炉以3 ℃/min热处理至550 ℃(2 h),即得掺杂TiO2试验样品。采用同样的方法改变b溶液,不加入掺杂离子。制备纯的TiO2纳米粉体。试验所用化学药品均为分析纯试剂,样品配方见表1。
1.2 结构与性能表征
采用武汉理工大学制造的综合热分析仪(参比为A12O3,升温速率为10 ℃/min)及热重仪进行差热-热重分析(TG-DTA);采用荷兰帕纳科日本理学(Rigaku)公司生产的D-MAX/ⅢA型X射线衍射仪(XRD)研究晶体的结构及结晶性。FE-SEM研究采用的是日本Hitachi公司生产的S-4800型场发射扫描电镜分析;TEM分析采用日本电子公司生产的JEM-2100F 型透射电子显微镜分析;UV-Vis吸收谱测定采用北京瑞利UV-1601型紫外-可见分光光度计来测量样品的紫外-可见光吸收光谱。
1.3 光催化活性评价试验
光催化降解试验是在武汉理工大学制造的反应器中进行,配制的亚甲基蓝溶液初始浓度为10 mg/L,溶液pH值控制在6.5左右,将纯TiO2和掺杂TiO2粉末分别加入到亚甲基蓝溶液,避光环境下超声波分散20 min,达到吸附平衡,采用15 w紫外灯照射,紫外灯离液面的距离固定在15 cm。每隔20 min进行取样,用北京瑞利UV-1601型紫外分光光度计测定溶液在200-800 nm波长范围内的吸收谱,并选取吸收谱中最大吸收峰664 nm(亚甲基蓝的主要吸收峰)处的吸光度计算TiO2光催化剂对亚甲基蓝溶液的降解率。根据朗伯-比耳定律,在低浓度时溶液浓度与吸光度呈良好的线性关系。因此,可用相对吸光度值的变化来表征降解过程中亚甲基蓝浓度的变化,降解率η即:

式中,Ct、At分别为t时刻亚甲基蓝溶液的浓度(mg/L)和吸光度(%);C0、A0分别为亚甲基蓝溶液的初始浓度(mg/L)和吸光度(%)。
由于亚甲基蓝溶液在紫外灯照射下会分解,因此在做实验的同时作了相应的空白试验,以减少对实验结果的影响。
2 结果与讨论
2.1 纳米TiO2热重分析
图1(a)和图1(b)分别为未掺杂TiO2和掺杂样品C2的热重分析曲线图。从图中对比可以看出,b相对a中的吸热峰和放热峰向高温处迁移,这是由于半径较大的Ce3+离子的掺入而引起的。当温度达到515 ℃时,样品的TG曲线接近平缓,表明样品反应完成。
2.2 掺杂纳米TiO2的XRD分析
图2是经550 ℃热处理1h后的Ce3+掺杂纳米TiO2粉体样品的XRD图谱。由图2可见,不同Ce3+掺杂的样品经过热处理得到的样品均为锐钛矿,没有新相和铈的氧化物形成。
表2是不同Ce3+掺杂量的TiO2样品的经过谢乐公式计算的晶体学数据,从表2可看出,Ce3+的掺杂,使得样品的晶粒尺寸增大,晶格畸变减小,晶胞体积增大。样品C1、C2、C3、C4的晶胞体积均大于未掺杂TiO2C0的晶胞体积135.52×10-3nm3。这可能为Ce3+的掺杂引起溶胶-凝胶的性能变化(在实验过程中表现为随着稀土元素量的增加,胶凝时间有延长的趋势),进而影响了掺杂TiO2的烧结性能,使得晶粒更容易长大。掺杂量为n(Ce3+)∶n(TiO2)=0.2%的样品C4,晶粒尺寸较未掺杂TiO2的C0减小至20.3 nm,原因可能为Ce3+的半径为0.103 nm,大于Ti4+的半径0.075 nm,有少量Ce3+进入TiO2晶格引起晶格膨胀和晶格畸变(C4样品晶格畸变为0.4325,大于C1、C2、C3),抑制了晶粒的长大并使晶胞体积增大。

表1 样品配方Tab.1 Batch formulas of the samples

图1 纯TiO2和掺杂样品C2干凝胶粉末的TG-DTA曲线Fig.1 TG-DTA curves of the pure TiO2 and the precursor powder of Ce3+-doped sample C2

表2 不同Ce3+掺杂量的TiO2样品的晶体学数据Tab.2 XRD crystallographic data of TiO2 doped with diferent amounts of Ce3+
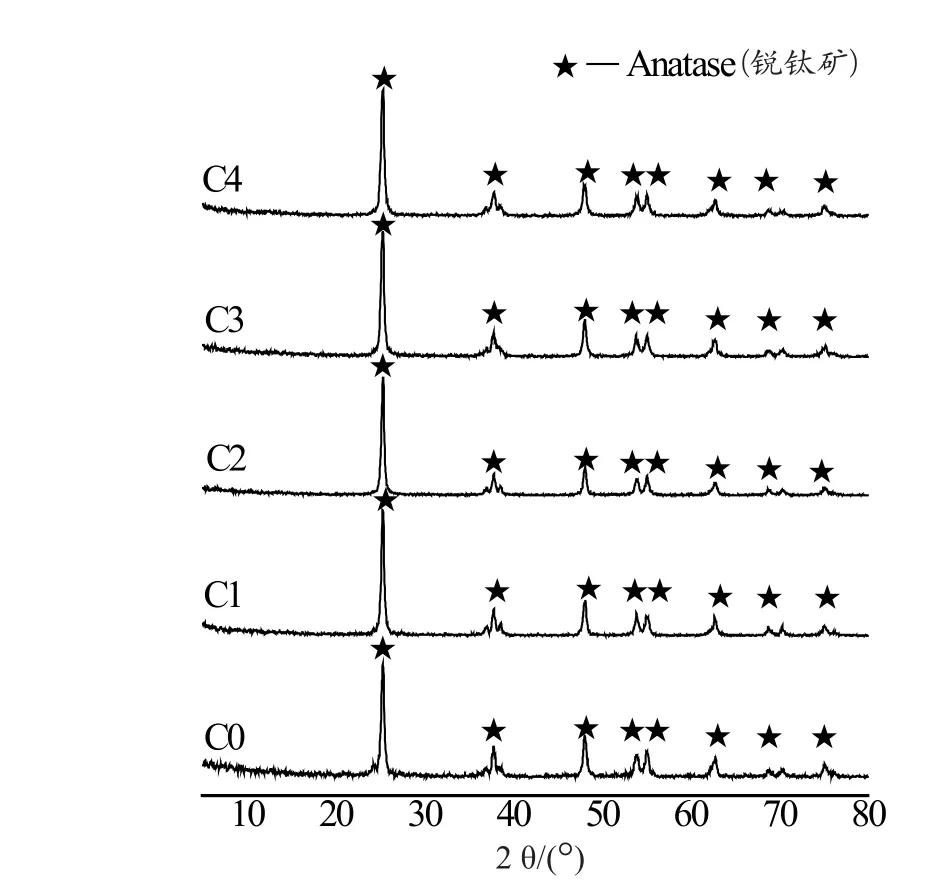
图2 不同量Ce3+掺杂TiO2样品的XRD图Fig.2 XRD patterns of TiO2 doped with diferent amounts of Ce3+
2.3 掺杂纳米TiO2的FE-SEM研究
图3是550 ℃热处理1h样品C2的FE-SEM分析。本实验所制备样品C2颗粒呈球形,样品颗粒尺寸分布比较均一,(c)图可以看出样品的晶粒尺寸在20-30 nm左右,与通过谢乐公式计算得出的结果(表2)24.9 nm基本吻合。另外,在图(a)中可以明显看出颗粒有部分团聚。可能由于样品颗粒粒径较小,比表面积较大,表面活性高,处于不稳定的热力学状态,为了降低体系的自由焓,颗粒之间自发聚集,形成团聚现象。另一方面,本研究采用溶胶-凝胶法合成TiO2,在制备过程中,颗粒表面有可能会吸附少量水分子,颗粒表面存在的羟基与相邻颗粒由于氢键作用结合在一起,在烧结过程中,氢键将转化成强度较高的桥氧键而使颗粒形成团聚。因此,在实验过程中应尽量控制水的加入量。
2.4 掺杂纳米TiO2的TEM分析

图3 经550 ℃热处理1 h的样品C2的场发射扫描图像Fig.3 FE-SEM micrograph of sample C2 fired at 550 ℃ for 1 h

图4 样品C2的TEM图像Fig.4 TEM micrographs of the sample C2
图4 是经550 ℃热处理1h的样品C2进行TEM分析。从图4(a)、(b)可见,C2样品的颗粒团聚较严重,可能是测试制样过程中粉体颗粒分散不均匀所致。由图(c)可见高分辨透射电镜照片中存在多个不同取向的晶格衍射条纹,但经测量其条纹宽度相当,可能与颗粒的团聚与相互重叠有关;但局部的结晶条纹清晰,结晶较为完整。其晶格条纹宽度为0.351 nm(对应于最强衍射峰(101)晶面族的晶面间距),小于标准TiO2(101)晶面间距d(101) = 0.3520 nm,可能为Ce3+的引入,使TiO2晶格发生变化从而影响了样品的衍射图像,使其向高角度方向偏移。电子衍射图像图(d) 得到的衍射斑点较少,且不属于典型的单晶衍射图谱,可能与样品的结晶度以及颗粒的分散程度有关。
2.5 掺杂纳米TiO2的UV-Vis吸收谱分析
图5是表1所示的各样品在200-800 nm范围内进行UV-Vis吸收谱分析,所得结果如图5所示。图6(a)、(b)所示,用切线法估算掺杂样品的λg和Eg,所得结果见表3。
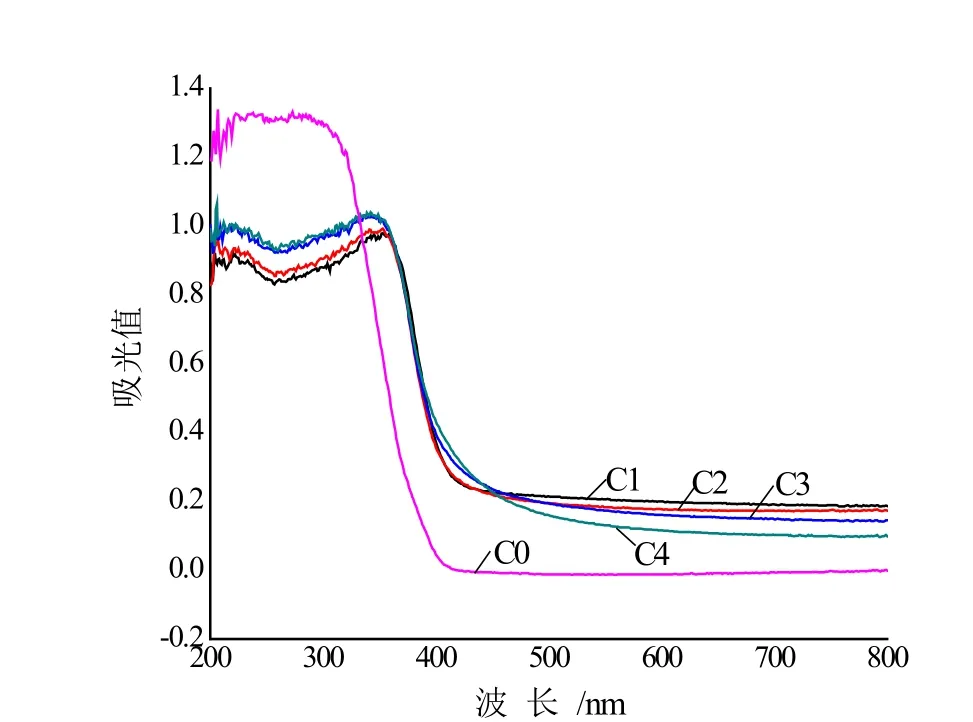
图5 Ce3+掺杂纳米TiO2样品的吸收曲线Fig.5 Ultraviolet-visible light absorption curves of Ce3+ -doped TiO2
从图5可以看出,掺杂样品的吸收峰较为掺杂样品的向可见光区红移,可能与Ce3+和TiO2等作用形成的有机络合物有关。随着掺杂浓度的提高,偏移量增加,C1、C2、C3、C4样品的λg值分别达到427 nm、434 nm、441 nm、446 nm。分析其原因,可能为Ce3+的半径为0.103 nm,大于Ti4+的半径0.075 nm,不容易进入TiO2晶格中,而是沉积在TiO2表面,形成了对TiO2的光敏化结构;而稀土元素Ce3+有丰富的能级和4f电子跃迁特性,有可能使激发电子注入TiO2的导带,扩大了TiO2的光谱响应范围。在掺杂量为(摩尔比)n(Ce3+)∶n(TiO2)=0.2%时,即样品C4的吸收阈值可达446 nm左右(对应的禁带宽度值Eg约为2.91 eV),远远大于未掺杂样品C0的392 nm。
2.6 掺杂纳米TiO2的光催化活性分析
图7为掺杂TiO2对亚甲基蓝溶液的降解率随Ce3+掺杂量的变化曲线图。从图中可以看出,随着掺杂量的增加,出现了一个极值。随着Ce3+掺杂浓度的升高各样品的光催化降解率也提高。掺杂比例(摩尔比)达到n(Ce3+)∶n(TiO2) = 0.05%的C2样品其降解能力最强可达到85.15%。这可能为Ce3+的引入,使得TiO2晶格发生晶格膨胀和晶格畸变,引起TiO2表面氧原子逃离晶格形成氧缺陷,造成电荷不平衡,减缓了电子-空穴对的复合,提高光催化活性。随着掺杂浓度升高至0.1%和0.2%,催化活性分别下降为77.35%和78.72%。这是因为掺杂量过多,稀土元素Ce3+在颗粒表面沉积,增大了电子与空穴复合的几率并影响TiO2表面的空间电荷层厚度,使得有效的光生电子-空穴对减少而使降解率降低。
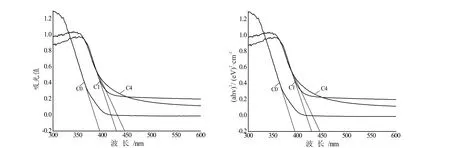
图6 切线法估算样品吸收阈值(λg)和禁带宽度(Eg)Fig.6 Estimation of absorption threshold (λg ) and band gap (Eg) of samples

表3 样品的吸收阈值(λg)和禁带宽度值(Eg)Tab.3 Absorption threshold (λg) and band gap (Eg) of samples
2.7 热处理温度及TiO2晶型对C2光催化活性的影响
本研究中选取光催化活性最佳的配方C2,在不同温度下进行热处理并保温1 h,并进行光催化降解实验。实验方案及结果如表4所示。对各样品进行XRD分析结果如图8所示。根据谢乐公式以及样品的XRD衍射数据计算各样品的晶体学数据,所得结果如表5所示。TiO2粉体中各晶相的质量分数如表3所示。根据锐钛矿相和金红石相的特征衍射峰,由公式(2)计算:

图7 Ce3+掺杂量对降解率的影响Fig.7 Efect of the amount of Ce3+ on the degradation of MB

样品C2在500 ℃-600 ℃范围内,得到的均为锐钛矿型TiO2。温度继续升高至650 ℃,会有金红型TiO2生成其含量为24.13%,且随着温度的升高至700 ℃,金红石相含量增多,可达到48.67%。
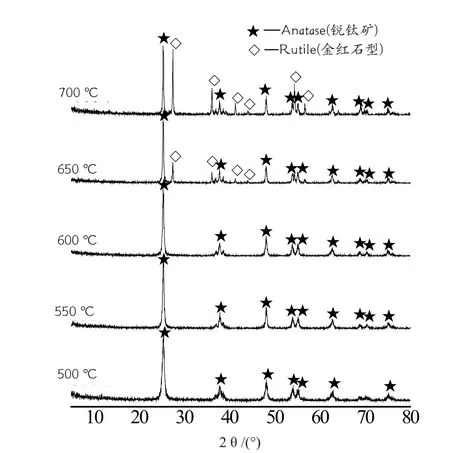
图8 不同温度烧成的C2的XRD图谱Fig.8 XRD patterns of sample C2 fired at diferent temperatures

表4 实验方案及结果Tab.4 The scheme and result of the experiment
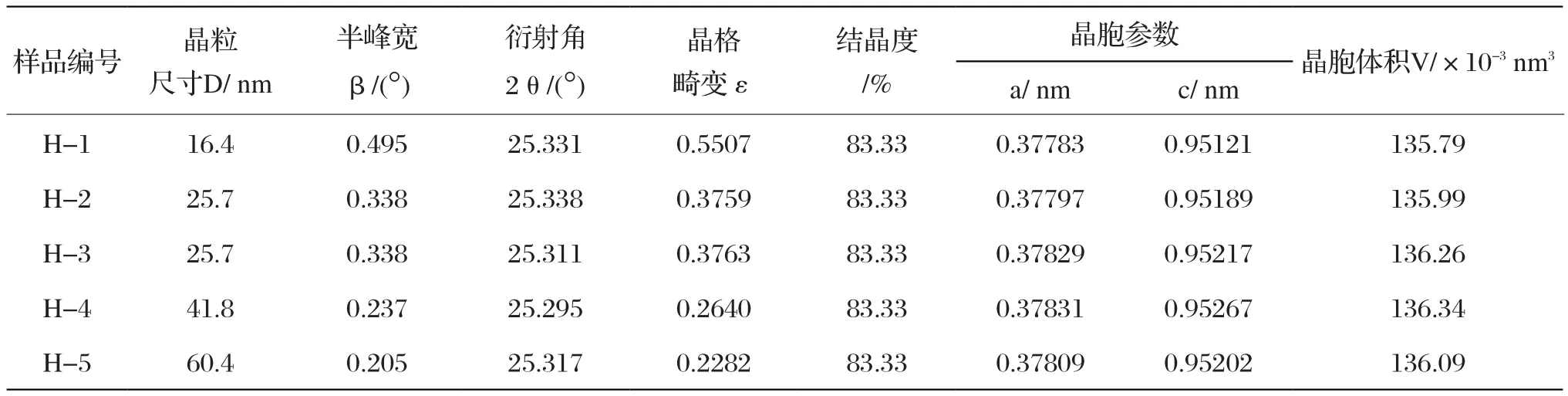
表5 不同温度烧成C2的晶体学数据Tab.5 XRD crystallographic data of C2 fired at diferent temperatures
从表5可以得到经500 ℃热处理的样品H-1晶粒尺寸、晶格畸变和晶胞体积分别为16.4 nm、0.5507和135.79×10-3nm3,其光催化降解率为71.13%。烧成温度升高至550 ℃,光催化效率升高达85.15%,晶粒尺寸为25.7 nm,说明晶粒尺寸不是决定光催化效率的唯一因素,温度升高会使得晶粒发育更好,从而提高了光催化效率。在550 ℃-700 ℃温度范围内,光催化降解率在81%-86%之间波动。虽然H-4、H-5的晶粒尺寸已经达到了41.8 nm和60.4 nm,但其光催化降解率仍然较高分别为85.52%和85.08%,可能为金红石相的生成,对光催化活性的提高起到了促进作用。
由样品的XRD图和表4可以看出,随着烧成温度的升高,XRD衍射峰的强度增强,晶粒尺寸增大,晶胞体积也有增大的趋势,且随着晶粒尺寸的增大晶格畸变减小。H-1样品的晶粒尺寸为16.4 nm、其晶格畸变为0.5507,H-2样品的晶粒尺寸为25.7 nm、而其晶格畸变急剧减小为0.3759,晶粒尺寸减小,晶粒表面的原子数目越多,表面能越大,表面原子通过容纳空位来降低表面能,存在大量的空位引起晶格的畸变。实验发现,随金红石相量的增加,降解率呈增加趋势,H-4样品(热处理温度为650 ℃)的降解率最高达85.52%。表明金红石相的存在有助于提高TiO2的光催化降解率。
3 结 论
(1)溶胶凝胶法制备的Ce3+掺杂TiO2粉体颗粒呈球形,晶粒尺寸为20-30 nm左右,有团聚现象。热处理后Ce3+掺杂TiO2样品的主晶相为锐钛矿型,随着热处理温度的升高,晶粒的尺寸和金红石的含量也随着增大。Ce3+的掺入可引起TiO2晶格的膨胀和畸变,减缓了TiO2晶体生长的速率,抑制了晶粒的大小。
(2)Ce3+掺杂TiO2的吸收边向可见光区移动,吸收阈值可达到446 nm左右,禁带宽度减小至2.91 eV。与纯TiO2相比,红移了54 nm左右。
(3)适量Ce3+的掺入可提高TiO2的光催化活性,而且存在一个最佳掺杂的量,本实验得到在掺杂比例(摩尔比)为n(Ce3+)∶n(TiO2)=0.05%时,样品表现出最佳的光催化活性为85.15%。
参考文献:
[1] FARALDOS M, BAHAMONDE A. Environmental applications of titania-graphene photocatalysts[J]. Catalysis Today, 2017,285: 13-28.
[2] EL-MEKKAWI D M, GALAL H R, WAHAB R M A E, et al.Photocatalytic activity evaluation of TiO2, nanoparticles based on COD analyses for water treatment applications: a standardization attempt[J]. International Journal of Environmental Science &Technology, 2016, 13(4): 1077-1088.
[3] PARK E J, JEONG B, JEONG M G, et al. Synergetic effects of hydrophilic surface modification and N-doping for visible light response on photocatalytic activity of TiO2[J]. Current Applied Physics, 2014, 14(3):300-305.
[4] RESZCZYNSKA J, GRZYB T, SOBCZAK J W, et al.Lanthanide co-doped TiO2: The effect of metal type and amount on surface properties and photocatalytic activity[J]. Applied Surface Science, 2014, 307(307): 333-345.
[5] JIN Q, SHEN Y, ZHU S. Effect of fluorine additive on CeO2(ZrO2)/TiO2, for selective catalytic reduction of NO by NH3[J]. Journal of Colloid & Interface Science, 2017, 487(11): 401-409.
[6] XU Anwu, GAO Yuan, LIU Hanqin. The preparation,characterization, and their photocatalytic activities of rare-earthdoped TiO2nanoparticles [J]. Journal of Catalysis, 2002, 207(2):151-157.
[7] CHO Y M, KYUNG H S, CHOI W Y. Visible light activity of TiO2for the photoreduction of CCl4and Cr(VI) in the presence of nonionic surfactant [J]. Applied Catalysis B: Environmental,2004, 52: 23-32.
[8] 徐晓虹, 田越, 吴建锋, 等. 稀土复合掺杂纳米TiO2薄膜光催化活性的研究[J].武汉理工大学学报, 2009, 31(11): 36-40.
[9] 孙俊英, 孟大维, 汪新星, 等. 稀土元素掺杂对纳米TiO2光催化剂的影响及机理[J]. 材料导报, 2007, 11(21): 70-73.
[10] 陈崧哲, 徐盛明, 徐刚, 等. 稀土元素在光催化剂中的应用及作用机理[J]. 稀有金属材料与工程, 2006, 35(4): 505-509.
[11] RANJIT K T, WILLNER I, BOSSMANN S H, et al.Lanthanide oxide-doped titanium dioxide photocatalysts:Novel photocatalysts for the enhanced degradation of p-chlorophenoxyacetic acid [J]. Environmental Science &Technology, 2001, 35: 1544-1549.
[12] RODRIGUEZ T R, VARGAS S, ARROYO R, et al.Modification of the phase transition temperature in titania doped with various cations [J]. J Mater Res, 1997, 12(2): 439.
[13] 张慧, 陈建华, 陈鸿博, 等. 纳米TiO2混晶的形成及其对光催化性能的影响在可[J]. 分子催化, 2006, 20(3): 250-251.

