甲醛与新制氢氧化铜反应实验的研究
伍强+蔡益
摘要:对过量甲醛与新制氢氧化铜的反应,有人认为生成铜、一氧化碳和水,也有人认为生成氧化亚铜、碳酸钠和水。为了得出正确的反应原理,对反应产物作了检测:反应生成的气体物质是氢气,固体物质主要成分是单质铜,反应后的溶液中不含碳酸根和铜离子。对反应机理作了探究,得出过量甲醛与新制氢氧化铜反应生成铜、甲酸钠和水的结论,氢气是副反应的产物。
关键词:新制氢氧化铜;甲醛;反应机理;实验探究
文章编号:1005–6629(2015)6–0077–04 中图分类号:G633.8 文献标识码:B
甲醛与新制氢氧化铜反应,还原产物是Cu还是Cu2O,氧化产物是CO还是Na2CO3,需通过实验研究作定论。
1 实验试剂
主要试剂:20% NaOH溶液(密度为1.18g/mL)、37%~40%甲醛溶液(密度为1.12g/mL)、0.5 mol·L-1 CuSO4溶液、25%~28%浓氨水、10% AgNO3溶液、HCOONa·2H2O晶体、CuCl晶体、甲醇
2 实验装置
实验装置如图1所示,用温度计测定水浴温度,水浴加热盛有反应物的小试管,排水法收集生成的气体。小试管上口连接竖直长玻璃管,目的是冷凝回流甲醛。
3 生成物成分的检测
各反应物用量:20%的NaOH溶液12mL,含有NaOH约为7.1×10-2 mol;37%~40%的甲醛溶液6mL,含有甲醛约为8.3×10-2 mol;0.5 mol·L-1 CuSO4溶液8mL,含有CuSO4为4.0×10-3 mol。NaOH物质的量为CuSO4的18倍,甲醛物质的量为CuSO4的21倍,确保反应溶液的碱性和Cu(OH)2完全被还原。
取一支容积为38mL的小试管,依次加入20% NaOH溶液12mL、0.5 mol·L-1 CuSO4溶液8mL、37%~40%甲醛溶液6mL,摇匀后,连接装置,放入65℃水浴中加热。
实验过程有三个明显的现象。前期(约3min):反应物由蓝色逐渐变为绿色、黄棕色、红棕色、深棕色,生成深棕色固体小颗粒,产生少量微小气泡。中期(约3min):深棕色固体逐渐变为紫红色蓬松固体,产生大量的微小气泡,反应物上下剧烈翻动,液面上涨,紫红色蓬松固体逐渐沉淀。后期(约7min):溶液变澄清,沉于试管底部的紫红色蓬松固体中放出少量气泡。收集到的气体体积为76mL。
实验1:暴鸣试验。取小试管用排水法收集生成的未知气体,做暴鸣试验,产生暴鸣声。初步断定未知气体为CO或H2。
实验2:银氨溶液检验CO。取10% AgNO3溶液10mL,滴加浓氨水至沉淀恰好溶解(约用1.2mL浓氨水),得到银氨溶液备用。取三支小试管用排水法收集满CO、H2、未知气体,分别加入2mL银氨溶液,用橡皮塞塞紧并振荡试管。盛有CO的试管中溶液立即变黑色并出现较多的黑色小颗粒银[4]。盛有H2和未知气体的试管中均无明显现象。生成的未知气体不是CO,那是不是H2呢?
实验3:CuO检验H2,进一步确认生成的未知气体不是CO。增大反应物用量,在100mL锥形瓶中进行甲醛与新制Cu(OH)2反应,将生成的未知气体用排水法收集做暴鸣试验,验纯后再将气体通入如图2所示实验装置(固定装置略)。点燃酒精灯,加热一段时间。观察到以下实验现象:有少量CuO变红色,无水CuSO4变蓝色,澄清石灰水中无明显现象。结论:生成的气体物质是H2。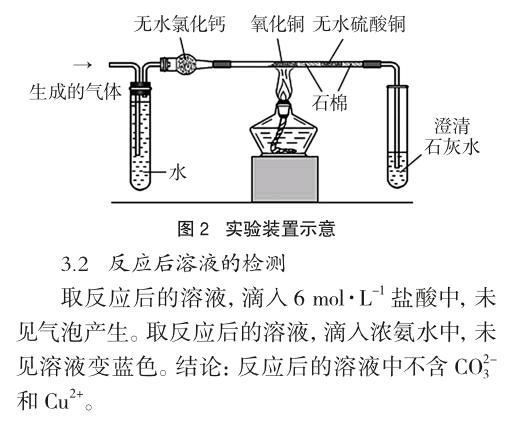
3.3 生成固体物质的检测
Cu2O溶于氨水,反应式为:Cu2O+4NH3·H2O=2[Cu(NH3)2]++2OH-+3H2O,无色的[Cu(NH3)2]+在空气中不稳定,立即被氧化为蓝色的[Cu(NH3)4]2+,反应式为:4[Cu(NH3)2]++8NH3·H2O+ O2=4[Cu(NH3)4]2++4OH-+6H2O[5]。Cu能不能溶于氨水呢?取少量细Cu丝放入小试管中,加满浓氨水,用橡皮塞塞紧(不留气泡),Cu丝没有明显溶解,将无色溶液转移到锥形瓶中,摇动锥形瓶,溶液还呈无色。将细Cu丝转移到锥形瓶中,加适量浓氨水,摇动锥形瓶Cu丝溶解,溶液呈现深蓝色。因此Cu不溶于氨水,但在O2作用下Cu溶于氨水生成[Cu(NH3)4]2+,反应式为:2Cu+O2+ 8NH3·H2O=2[Cu(NH3)4]2++4OH-+6H2O。
第一步实验:Cu2O的溶解和检验。从水浴中取出小试管,吸去小试管中溶液,剩下紫红色固体物质,用煮沸过的水洗涤1~2次。加满浓氨水,用橡皮塞塞紧(不留气泡)。不时上下颠倒摇动试管,2天后将无色溶液转移到锥形瓶中,摇动锥形瓶无色溶液很快变为很浅的蓝色,再转移到50mL的容量瓶(1)中并加浓氨水定容。结论:生成固体物质中含有较少的氧化亚铜。
第二步实验:单质Cu的溶解和检验。将未溶解细小的固体转移到锥形瓶中,加适量的浓氨水,摇动锥形瓶,细小的固体较快溶解,溶液呈很深的蓝色,再转移到50mL的容量瓶(2)中并加浓氨水定容。结论:生成固体物质中含有较多的单质Cu。
第三步实验:单质Cu和Cu2O含量测定。取容量瓶(2)中溶液0.5mL于50mL的容量瓶中,加浓氨水定容,溶液颜色与容量瓶(1)溶液颜色相近,则容量瓶(2)中0.5mL溶液含铜量与Cu2O含铜量相当。生成的固体物质中单质Cu与Cu2O物质的量比为50:0.25,则单质Cu质量百分含量为50mol×64 g·mol-1/(50mol×64 g·mol-1+0.25mol×144 g·mol-1)=98.9%,Cu2O质量百分含量为1.1%。结论:生成的固体物质主要成分是单质Cu。
4 反应机理的探究
Cu2O的制备:由于制备方法和反应条件不同,Cu2O晶粒大小不同而呈现多种颜色,如黄色、红色、深棕色等[6]。取试管,加入0.4g CuCl(含Cu量与8mL 0.5 mol·L-1 CuSO4溶液相当),再加入20mL的水煮沸水解,滴加几滴2%NaOH溶液再煮沸,生成黄色细小的Cu2O晶粒,洗涤备用。
H2、Cu2O和Cu是怎样生成的?推测:甲醛在浓NaOH溶液作用下,发生康尼查罗反应生成甲醇和甲酸钠。甲醇在催化剂作用下发生脱氢反应生成H2和甲醛。甲醛还原Cu(OH)2生成Cu2O,过量甲醛进一步还原Cu2O生成Cu。Cu(OH)2氧化甲醛生成甲酸钠还是Na2CO3?为此设计七个实验,探究反应机理。多次实验,记录生成H2体积的范围。实验结果见表1。
[实验1]反应物初始温度以及混合均匀程度对生成H2的量影响较大。固体物质中单质Cu质量百分含量在98%以上。由于CuSO4用量较多,生成Cu(OH)2悬浊液,有比较少的Cu2O未被甲醛还原生成Cu。另外各反应物用量减少一半直接用酒精灯加热实验,也能收集到40~46mL的H2。
[实验2]生成的紫黑色非常细小颗粒不溶于浓氨水,是单质Cu。由于CuSO4用量较少,生成Na2[Cu(OH)4]被过量甲醛还原生成Cu。
[实验3]不同的水浴温度可生成黄色、红色等颜色的细小颗粒。生成的细小颗粒溶于氨水,是Cu2O晶粒。由于CuSO4用量较少,生成Na2[Cu(OH)4]被适量甲醛还原生成Cu2O晶粒。
[实验4]用实验2生成的Cu粉实验,无氢气生成,Cu没有催化作用,
[实验5]用实验3生成的Cu2O晶粒实验,无氢气生成,Cu2O没有催化作用。
[实验6]用制备的黄色细小的Cu2O晶粒实验,可观察到以下实验现象:试管底部黄色的Cu2O晶粒由上至下逐渐转化为紫红色蓬松Cu,蓬松Cu表面产生大量微小的气泡,当蓬松Cu上浮到液面时就没有产生气泡。Cu2O被甲醛还原生成Cu,刚生成的Cu有催化作用,但很快失去催化能力,称之为活性Cu。
[实验7]实验无明显现象。从水浴中取出小试管,向小试管中加入碎瓷片,直接用酒精灯加热试管,煮沸二十分钟只是溶液被浓缩、蓝色变深。因此在通常情况下,Cu(OH)2与甲酸钠不反应,Cu(OH)2氧化甲醛只能生成甲酸钠。
5 实验结论
6 实验探究的思考
文献[1]作者又有文章指出:甲醛与新制Cu(OH)2反应生成CO、Cu和H2O的反应是化学中“个性”[9]。事实上是作者把副反应的产物H2误认为是CO,又将CO当成甲醛与新制Cu(OH)2反应的产物,甲醛与新制Cu(OH)2反应生成CO的机理是无法考证的。因此在研究化学反应原理时,对产物检测要注意严密性,对产物判断要注意科学性。

我们知道,乙醛与新制Cu(OH)2反应主要产物是Cu2O和乙酸钠,由此推知甲醛与新制Cu(OH)2反应主要产物是Cu2O和甲酸钠。由于甲醛还原性较强,过量甲醛能还原Cu2O生成Cu;甲酸钠还原性较弱,甲酸钠与Cu(OH)2不反应,因此过量甲醛与新制Cu(OH)2反应主要产物是Cu和甲酸钠。由于同类物质的化学性质相似,因此对同类物质发生的化学反应进行类推是非常必要的,否定它就可能导致错误。然而也要注意同类物质化学性质存在差异,忽略它也可能导致错误。虽然研究者在实验探究过程中出现这样那样的错误,但为甲醛与新制Cu(OH)2反应主要产物的检测将成为教学的典型素材奠定了基础。
参考文献:
[1]夏立先.对甲醛与新制氢氧化铜反应的实验研究[J].中学化学教学参考,2011,(6):46~47.
[2]陈廷俊.探究甲醛与新制氢氧化铜的反应[J].中学化学教学参考,2012,(12):62~63.
[3][5][6]北京师范大学等.无机化学(第4版,下册)[M].北京:高等教育出版社,2003:564,704,704.
[4]陆燕海.银氨溶液检验CO气体[J].化学教学,2012,(1):48~49.
[7][8]邢其毅等.基础有机化学(第3版,上册)[M].北京:高等教育出版社,2005:550,553.
[9]夏立先.学生在化学学习中形成错误认识的原因分析及对策[J].化学教育,2013,(12):46~47.

