芦苇生物炭对亚甲基蓝的吸附特性研究❋
张明月, 李锋民, 卢 伦, 顾书瑞
(中国海洋大学环境科学与工程学院,山东 青岛266100)
芦苇生物炭对亚甲基蓝的吸附特性研究❋
张明月, 李锋民❋❋, 卢 伦, 顾书瑞
(中国海洋大学环境科学与工程学院,山东 青岛266100)
本文选取湿地植物芦苇作为原材料,在不同热解温度下(300~600 ℃),利用限氧升温炭化法制备成生物炭,通过元素分析、比表面积测定、红外光谱分析、X射线衍射分析、Zeta电位等方法研究其物理化学特征以及对亚甲基蓝的吸附特性。研究发现,当固液比为6 g·L-1时,芦苇生物炭吸附亚甲基蓝的平衡时间为24h,其中,500 ℃下热解制备的生物炭吸附能力最强,其最大吸附量达到了5.030 mg·g-1;当溶液的初始pH升高时,芦苇生物炭对亚甲基蓝的平衡吸附量随之增加并最终趋向稳定,其最佳pH为8~9;当背景溶液中的离子强度增加时,芦苇生物炭对亚甲基蓝的平衡吸附量略有减少,降幅范围为5%~22%;Langmuir等温线模型对吸附数据具有很好的拟合水平(R2> 0.99),说明芦苇生物炭对亚甲基蓝的吸附为单分子层吸附。
芦苇生物炭;亚甲基蓝;吸附
染料工业在国民经济中占有重要的地位,其产品涵盖了纺织、油墨、涂料、橡胶、皮革、医药以及食品等各大领域,这些染料大多数具有生物致毒效应、环境生态系统危害性等特点,一旦处理不当甚至直接投入到受纳水体,必将破坏当地水体环境,导致严重的污染,尤其在现代染料的化学性质朝着抗生化、抗光化、抗氧化方向的发展环境下,印染废水污染量不断增大,处理过程复杂,处理难度增加,对环境造成十分严重的威胁[1]。亚甲基蓝(Methylene Blue, MB)作为一种典型的印染废水污染物,可与氯化锌形成复盐,对纸张、纤维、棉麻织物甚至生物、细菌组织等进行染色,广泛存在于染料、药物、化学指示剂等领域,进入水体后会改变水体的透光性,不利于水体的生态系统进行光合作用,同时,它也具有一定的毒性,可在人体接触的短时间内引起人眼的灼伤,并使人体出现呼吸困难和有灼烧感的反应,甚至会引起恶心、干呕、大量出汗、精神混乱以及高铁血红蛋白症等症状[2],因此,在印染废水排放之前对其进行亚甲基蓝的去除是十分必要的。印染废水的常用处理方法主要包括物理法、化学法与生物法三类。其中,物理法中的吸附法由于其具有能够实现废物的再利用性和操作简单等优点,在去除难降解污染物的过程中起着重要作用,近年来受到越来越多国内外学者的关注。众多研究已经证实,活性炭吸附法对直接染料、阳离子染料、酸性染料、活性染料等水溶性染料的废水具有良好的吸附性能(对硫化染料、还原染料等不溶性染料的废水处理效果不明显)[3],但价格较高且再生能力弱,应用面较窄,因此广泛的应用于染料废水的治理仍然是非常困难的。所以国内外学者正在积极寻找廉价而且吸附能力较强的吸附剂。
近年来,研究人员用天然矿物质、农林废弃物以及真菌、藻类等生物吸附材料来吸附对废水中的亚甲基蓝,也取得了一定的成果。张佳等人[4]通过山茶籽粉对亚甲基蓝的吸附实验发现,山茶籽粉在中性溶液中可达到9.50 mg·g-1的平衡吸附量;Sikaily等人[5]在石莼吸附亚甲基蓝的实验中发现,当溶液中石莼浓度为2.5 g·L-1时,可吸附约40.2 mg·g-1的亚甲基蓝,去除率高达65%。
生物炭是有机材料在无氧或者缺氧条件下,在封闭容器中通过热化学转化形成的多孔碳质固体[3]。生物炭本身具有有机碳含量高,可作为土壤改良剂有效改善土壤环境等众多优良的性质,此外更能产生显著的或者潜在的农业、经济、环境效应[6],因此近年来越来越多的受到国内外科学家的重视。制备生物炭的原料种类丰富来源广泛,包括农林废物(如作物秸秆、木屑、畜禽粪便等)、有机废弃物、其他废弃的生物物质等,涵盖了作物秸秆生物炭、芦竹生物炭、柚子皮生物炭等各种类型的吸附剂炭材料[7]。
生物炭主要由C、H、O三种元素构成,同时也存在N、P、S、Na、K、Ca、Mg等少量元素,其灰分组分含量通常较高[8],多数呈碱性。总的来说,生物炭是一种表面含有大量的含氧官能团(如羟基、羧基、醛基、酮基、酯基等)和多环芳烃的多碳物质[9],具有比较发达的孔隙结构,相对较大的比表面积,表面带有较多负电荷,电荷密度较高,因此对多环芳烃、多氯联苯和其他疏水性有机污染物以及Cu2+、Pb2+、Hg2+、Cr4+等重金属离子拥有较强的吸附能力[10-15]。
由于在生物炭的制备过程中存在不同的原料,不同的热解工艺,不同的热解温度,使得不同生物炭间的物理化学性质(如生物炭孔隙结构、元素含量、物理化学组成、机械强度及稳定性、pH等)也不会完全相同,进而造成了不同生物炭具有不同的吸附能力[16-19]。其中,热解温度是影响生物炭性状的重要因素。Liu等人[20]用小麦秸秆在550℃下热解制备成生物炭并研究其吸附亚甲基蓝的特性,发现生物炭的表面具有—OH等含氧官能团,并且在pH=7.8时,小麦秸秆生物炭对亚甲基蓝的平衡吸附量达到最大值(10.23 mg·g-1)。此外,Sun 等[21]用厌氧消化残渣、棕榈树皮、桉树等材料分别制备成生物炭,发现这些生物炭都有着良好的孔隙通道和较大的比表面积,对于pH为7初始浓度为5 mg·g-1的亚甲基蓝溶液的去除率分别是99.5%, 99.3%和86.1%。
针对目前大量经济价值低或无价值的湿地植物无法及时去除而重新释放营养和污染物质到土壤中形成二次污染的问题,采用将这些湿地植物(芦苇、芦竹等)在无氧或限氧条件下热解形成生物炭的办法,既可以解决这些植物在土壤里腐烂分解形成二次污染的问题,又可以作为吸附剂去除水体和土壤中的污染物质,实现了“以废制废”的目的。本文选择芦苇作为湿地植物的典型代表,研究了不同热解温度下芦苇生物炭的制备、表征及其对亚甲基蓝吸附特性,揭示了湿地植物生物炭广泛应用于对亚甲基蓝及其他难降解有机污染物的吸附的诸多优势和良好前景,也对全面了解生物炭的吸附性能为其作为人工湿地填料的应用提供了有力的科学依据和技术支持。
1 材料与方法
1.1 生物炭的制备与表征
1.1.1 生物炭原料 本实验选用山东齐河的湿地植物芦苇(Phragmitesaustralis)为生物炭原材料,将其用自来水洗净去除表面附着的颗粒物后,切成2~5 cm的小段,在65~70 ℃的烘箱中烘干至少72 h,储存于实验室内备用。
1.1.2 不同热解温度下芦苇生物炭的制备 准确称取1.0 kg干燥后的芦苇小段装入炉中,通入氮气并将流速控制在500 mL·min-1,利用真空管式炉(KBF-11Q型,南大仪器厂制造)作为热解设备,通过限氧慢速热解法制取芦苇生物炭。热解管的温度由室温持续升温至300、400、500和600 ℃,并在相应的温度下保持恒定温度2 h。热解结束后,继续通入氮气直至生物炭自然冷却至室温后取出,将制备的生物炭粉碎、过滤、洗净、烘干、过筛(0.125 mm),置于干燥器中备用。将制备好的不同温度梯度的芦苇生物炭分别编号为CR300、CR400、CR500、CR600,CR之后的数字代表制备芦苇生物炭的热解温度。
1.1.3 芦苇生物炭的表征 通过元素分析仪(Vario EL III,Elementa,德国)分别对4种芦苇生物炭中的C、H、O、N、S等元素的百分含量进行测定。通过全自动物理吸附仪(安塔公司Adsorption-1)在液氮温度(77 K)利用高纯氮气测定生物炭的比表面积和孔径分布情况。采用傅里叶红外光谱仪(Tensor 27,Bruker,德国)分析测定生物炭,扫描区域为4 000~500 cm-1,分辨率4 cm-1。采用激光粒度及Zeta电位分析仪(Zetasizer Nano ZS90,Malvern)上测定溶液的电移动性,得到生物碳表面电荷(Zeta电位)[19]。
1.2 吸附实验
1.2.1 芦苇生物炭吸附亚甲基蓝动力学实验 称取0.09 g芦苇生物炭(CR300、CR400、CR500、CR600),分别加入15mL浓度为50mg·L-1的亚甲基蓝溶液,滴加少量浓度为0.01~0.1 mol/L的HCl或者NaOH溶液调节溶液pH至7.0±0.1,且含有0.01mol·L-1NaCl和200mg·L-1NaN3作为背景电解质。将其置于温度为20℃转速为150r·min-1的恒温震荡箱中震荡,分别于1~24h间取样。震荡结束后,静置一段时间,使用针头过滤器过0.45μm聚醚砜滤膜过滤,对滤液取样,使用紫外可见分光光度计在665nm处测得其溶液吸光度,通过以下方程计算对应亚甲基蓝浓度:
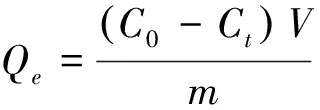
式中:Qe为生物炭对亚甲基蓝的单位吸附量(mg·g-1);C0为亚甲基蓝溶液初始浓度(mg·L-1);Ct为t时刻的亚甲基蓝浓度(mg·L-1);m为加入的生物炭质量(g);V为溶液体积(L)。
1.2.2 pH对生物炭吸附亚甲基蓝的影响 按6 g·L-1的固液比,分别称取0.09g芦苇生物炭(CR300、CR400、CR500、CR600),加入15mL浓度为50 mg·L-1的亚甲基蓝溶液。用HCl或者NaOH溶液调节溶液的pH值达到设定值(3.0~10.0),置于恒温震荡箱中震荡24 h后取样测定。
1.2.3 背景溶液离子强度对生物炭吸附亚甲基蓝的影响 称取0.09g芦苇生物炭(CR300、CR400、CR500、CR600),分别加入15 mL浓度为50mg·L-1的亚甲基蓝溶液,调节溶液pH为8.5±0.1(经2.2.2实验结果证明,pH在8.5附近时,生物炭对亚甲基蓝的吸附效果最好),用含有200mg·L-1NaN3作为背景电解质,并分别添加浓度为0~0.40mol·L-1的NaCl溶液为其提供离子强度支持,置于恒温震荡箱中震荡24 h后取样测定。
1.2.4 芦苇生物炭对于亚甲基蓝的吸附等温线 分别称取0.09g不同热解温度下制备的芦苇生物炭放入20 mL具塞玻璃瓶中,分别加入15mL浓度为20~200mg·L-1的亚甲基蓝溶液,调节溶液pH为7.0左右,置于恒温震荡箱中震荡24 h后取样测定。
1.3 数据分析
利用软件Excel 2010和Origin 8.6统计实验数据并绘制相关图表,采用软件 SPSS 19.0中的Pearson相关系数检验(P=0.05)对相关实验数据进行相关性分析,采用软件SPSS 19.0中的Duncan检验(P=0.05) 进行显著性差异分析。
2 结果与讨论
2.1 芦苇生物炭的物理化学性质
芦苇生物炭的基本物理化学性质列于表1中。随着热解温度的升高,生物炭的内部结构也逐渐发生了相应的变化。芦苇生物炭中C元素的含量逐渐从65.75%增加到了81.64%,而H元素和O元素的含量分别从4.65%、22.15%逐渐下降到了2.49%、6.17%,表明了生物炭的碳化程度随热解温度的升高而升高。同时,随着热解温度的升高,H/C原子比的减少说明高温生物炭具有更高的芳香化程度,O/C和(O+N)/C原子比的减少表示高温生物炭表面含有更少的含氧官能团。实验同时表明,当生物炭热解温度升高时,芦苇生物炭的比表面积也在逐渐增加,表明热解温度能够显著影响芦苇生物炭的比表面积,与文献报道一致[19,22-23]。热解温度越高,生物质原料的裂解越充分,制备得到的生物炭的孔隙结构越发达,从而使高温生物炭的比表面积大于低温生物炭。此外,当热解温度升高时,生物炭的pH也随之增大。其中,CR600的pH达到了10.01。
4种芦苇生物炭的傅里叶红外谱图如图1所示。当热解温度升高时,芦苇生物炭的表面官能团相应也产生了较大变化。不同热解温度下制备的芦苇生物炭在3413cm-1处(—OH)均出现了较高的羟基吸收峰;CR300、 CR400、CR500在2900和1430cm-1附近都有较高的亚甲基(—CH2)吸收峰,CR600的亚甲基吸收峰已经基本消失,表明随着热解温度的升高,芦苇生物炭的非极性组分呈现逐渐减少的趋势;CR300~CR600在1696cm-1处的酯碳基吸收峰逐渐平缓,并且在1 110cm-1处C—O和C—C吸收峰逐渐消失,这说明芦苇生物炭中的脂肪族组分随着热解温度的升高也在逐渐减少。
在pH为3~10的范围内测定不同pH条件下各芦苇生物炭的Zeta电位,结果如图2所示。在此pH范围内,4种生物炭表面电荷均为负,这是由于生物炭表面带有羧基、羟基等含氧官能团的去质子化而造成的。由图2还发现,随着溶液初始pH的升高,芦苇生物炭的Zeta电位呈现逐渐下降趋势,但是该趋势在pH到达8~9时变得趋于平稳。因此在中性pH水溶液中(pH≈7)时,4种芦苇生物炭的表面均带负电荷。
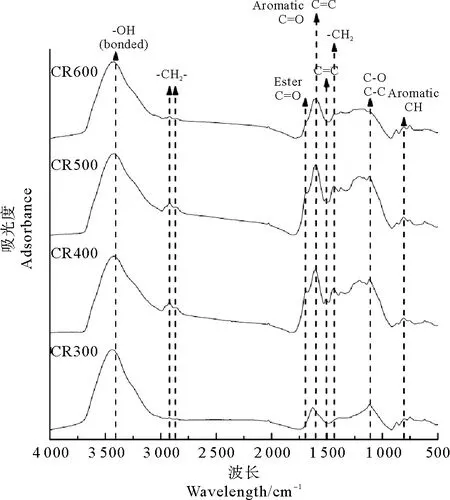
图1 不同热解温度制备的芦苇生物炭的傅立叶红外光谱图
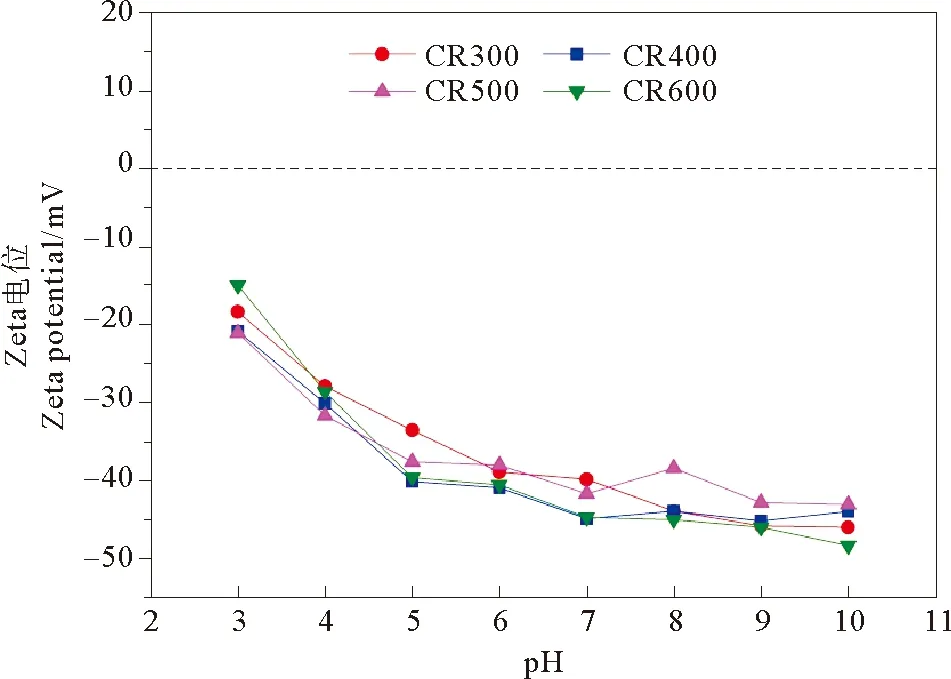
图2 芦苇生物炭在不同pH下的Zeta电位
2.2 芦苇生物炭对亚甲基蓝的吸附动力学
通过吸附动力学可以计算出生物炭的吸附速率和平衡时间,从而估计在实际应用中需要投放生物炭的用量。所以吸附动力学在吸附实验中是必不可少的控制设计和操作步骤。一般而言,吸附剂吸附溶液中吸附质的快慢,主要受到吸附剂本身特性和被吸附的吸附质的特性影响,此外,吸附过程中存在的吸附机理也与其相关。本研究中选择了初始浓度为50mg·L-1的亚甲基蓝溶液,溶液初始pH调节至7.0±0.1,对比不同热解温度下制备的芦苇生物炭在吸附时间和平衡吸附量上的差异。如图3所示,4种不同热解温度下制备的芦苇生物炭达到吸附平衡的时间均为24h左右。其中,CR500的吸附能力最强,24h后平衡吸附量达到,2.70mg·g-1,CR600的吸附能力次之,CR300和CR400的吸附能力最差,平衡吸附量在2.29~2.41mg·g-1之间。这可能由于热解温度由300℃上升到500℃时,生物炭表面的中孔、大孔等孔道增加,平均孔径增大,而热解温度由500℃上升到600℃时,生物炭表面的微孔数量增加,而部分中孔、大孔因为高温而坍塌,导致平均孔径减小[24]。
另外,由图可看出,4种生物炭在吸附初始阶段(0~4h)中对亚甲基蓝的平衡吸附量随着时间的延长而迅速增加,但4h后平衡吸附量随着时间的延长而增加的趋势十分缓慢。这是由于吸附刚开始时,亚甲基蓝与生物炭表面接触,平衡吸附量迅速增加,之后亚甲基蓝通过生物炭的孔通道吸附到介质内部,使介质不能以稳定的速度吸附亚甲基蓝,从而影响了吸附速率[25]。
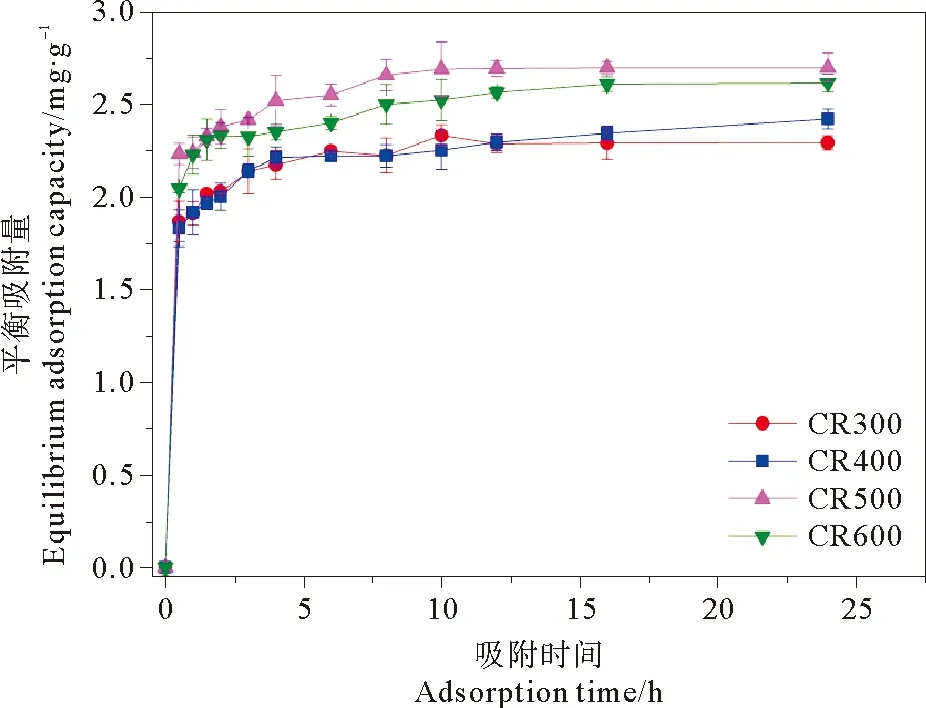
图3 吸附时间对各生物炭吸附亚甲基蓝的影响
同时,拟一级动力学、拟二级动力学模型可以对各生物炭对溶液中亚甲基蓝的吸附过程进行拟合,其动力学拟合参数列于表2中。由动力学模型的拟合参数来看,与伪一级动力学模型相比,伪二级动力学模型对于生物炭对亚甲基蓝的吸附过程具有更准确的拟合性,其拟合相关系数均大于0.999。此外,通过比较实际吸附量(Qe,cal)与吸附模型计算出来的理论吸附量(Qe,cal),发现伪二级动力学在生物炭吸附亚甲基蓝上的结果优于伪一级动力学。因此,伪二级动力学方程可以很好拟合亚甲基蓝在芦苇生物炭上的吸附,即化学吸附在整个吸附过程中占据主要地位,这也与Sun等[21]和Wang 等[26]的研究结果相符。
2.3 pH对生物炭吸附亚甲基蓝的影响
溶液中不同的pH条件可以导致吸附材料的表面构成及染料所带的表面电荷存在差异,从而影响了芦苇生物炭对于亚甲基蓝的吸附。本文研究了pH在3~10之间时芦苇生物炭对于亚甲基蓝的吸附情况,pH对4种不同热解温度下制备的芦苇生物炭对于亚甲基蓝的吸附情况如图4所示。从图中可以看出:在pH = 3时,4种生物炭对亚甲基蓝的吸附量均小于2.64 ± 0.04 mg·g-1,生物炭对亚甲基蓝的平衡吸附量最小;当亚甲基蓝溶液初始pH值增加时,芦苇生物炭对亚甲基蓝的平衡吸附量也迅速增加(pH ≤6),当溶液初始pH继续增加时(pH≥7),平衡吸附量的增加速度减缓趋向稳定。这也说明了亚甲基蓝溶液初始pH的升高有利于生物炭的吸附作用的进行。这是由于溶液中的氢离子比较容易被吸附,从而改变pH条件对染料阳离子的吸附干扰作用较强烈。但pH升至8~9附近时,生物炭对亚甲基蓝的平衡吸附量增加不大,说明生物炭吸附亚甲基蓝并不仅仅通过静电吸附起作用。而Sun等[21]研究pH对桉树制成的生物炭吸附亚甲基蓝的实验发现,当pH从5升高至10时,生物炭对亚甲基蓝的平衡吸附量有轻微的减少。这是由于作为原材料的桉树细胞壁含有一些带正电的表面官能团,当溶液中pH增加时,这些带正电的官能团遭到破坏,从而对亚甲基蓝在生物炭上的吸附产生了轻微抑制作用。
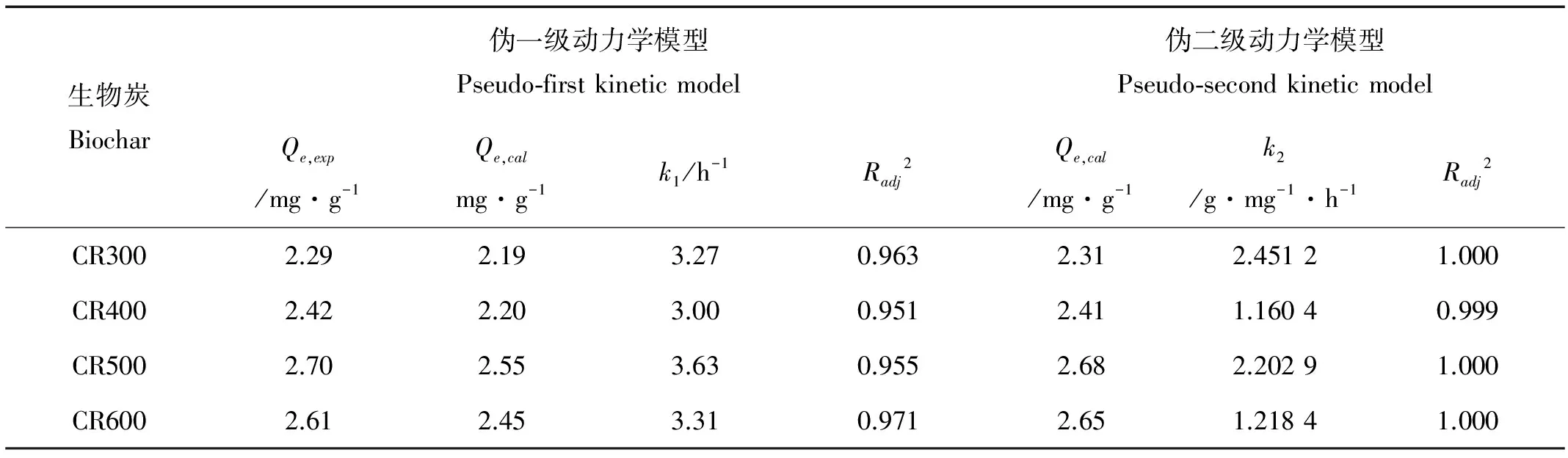
表2 各生物炭对亚甲基蓝吸附的伪一级和伪二级动力学模型的拟合参数
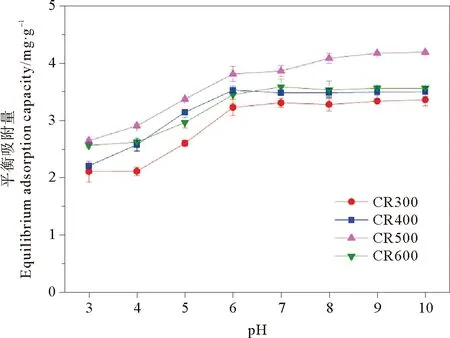
图4 初始pH值对于芦苇生物炭吸附亚甲基蓝的影响
考虑到废水的后期处理和实际应用情况,本研究选择 pH = 8.5 作为研究芦苇生物炭对亚甲基蓝吸附等温线以及其它吸附实验的pH条件。
2.4 背景溶液离子强度对生物炭吸附亚甲基蓝的影响
一般来说,染料废水中通常存在较高的盐浓度,氯化钠的大量存在对于吸附剂应用于染料废水的处理过程有着重大影响。本实验研究了NaCl浓度从0.01~0.4mol·L-1条件下芦苇生物炭对亚甲基蓝的吸附情况(见图5)。当NaCl浓度逐渐增加时,溶液初始pH均调节至8.5±0.1左右,各芦苇生物碳对亚甲基蓝的吸附量都呈现出略微减小的趋势,表明溶液中的NaCl浓度对亚甲基蓝的吸附具有不明显抑制作用。这可能要归因于亚甲基蓝阳离子和钠离子等阳离子之间存在少量竞争吸附作用,从而减少了生物炭表面上的亚甲基蓝吸附。这与Liu等[20]对NaCl浓度的改变对小麦秸秆生物炭吸附亚甲基蓝的结果一致,同时,Liu等人认为当溶液的离子浓度增加时,亚甲基蓝的活性增强,而生物炭表面的吸附位点的活性降低,因而造成了生物炭对亚甲基蓝的平衡吸附量有所减少。
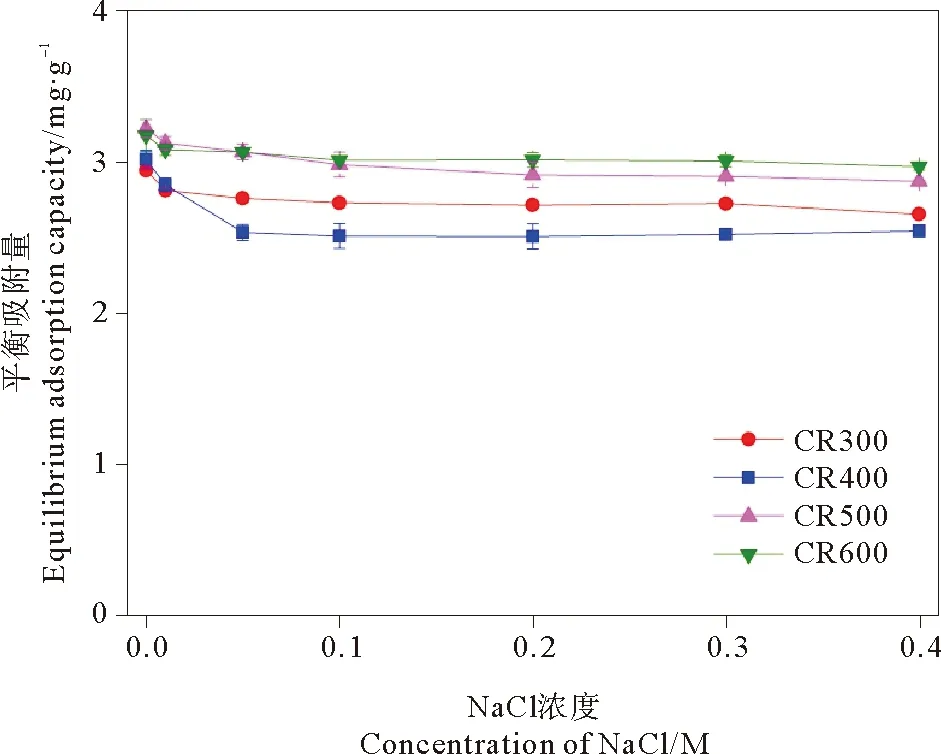
图5 背景溶液离子强度对生物炭吸附亚甲基蓝的影响
2.5 芦苇生物炭对于亚甲基蓝的吸附等温线
吸附等温线是通过测定一系列具有不同初始浓度的溶液相应的平衡吸附量所得到的。吸附等温线可以很好的反映出吸附的基本原理以及吸附剂表面的孔隙分布结构。从图6中可以看出,当亚甲基蓝溶液的平衡浓度由5 mg·L-1增大到120mg·L-1时,高温生物炭对亚甲基蓝的最大吸附量明显高于低温生物炭的平衡吸附量,其中CR500的吸附能力最强,其最大理论吸附量达到了5.076 mg·g-1,而热解温度升至600 ℃时,芦苇生物炭的吸附能力又出现下降趋势,这从表3的拟合参数中也可以很明显的得出结论。对这4种生物炭按照吸附能力大小排序,为CR500>CR600>CR400>CR300。
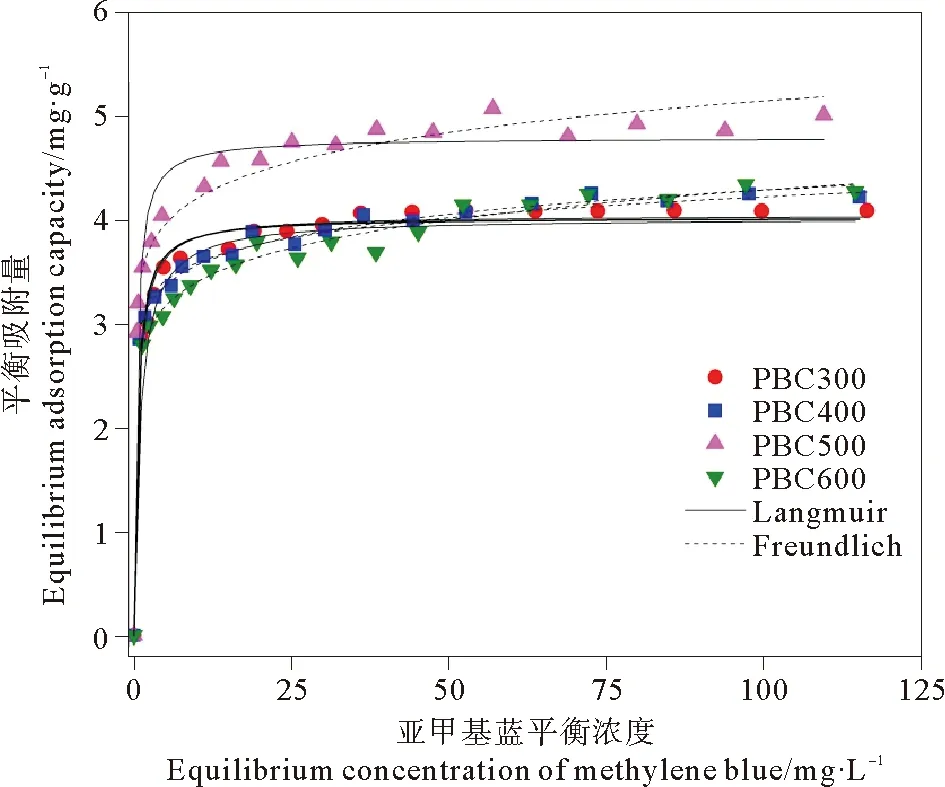
图6 不同热解温度制备的芦苇生物炭对于亚甲基蓝的吸附等温线
表3 列出了Langmuir模型和Freundlich模型对于不同热解温度制备的芦苇生物炭吸附亚甲基蓝情况进行了拟合。从表中可以看出,Langmuir模型对4种芦苇生物炭吸附亚甲基蓝数据的拟合校正相关系数(R2)均大于等于0.990,明显高于Freundlich模型的拟合校正相关系数(0.852~0.973之间),表明相对于Freundlich模型来说,Langmuir模型更适合反应芦苇生物炭对亚甲基蓝的吸附情况,与吴晴雯等人对芦苇生物炭吸附重金属Ni的吸附等温线实验结果相一致。这也反映了芦苇生物炭对于亚甲基蓝的吸附主要是单分子层吸附,而且吸附质材料各分子之间相互影响不大,在吸附平衡时吸附剂的表层位点已达到饱和状态。但郎印海等人[17]在小麦秸秆和花生壳制成的生物炭对五氯酚的吸附性能研究中,发现Freundlich方程更适于描述五氯酚在生物炭上的吸附等温过程(R2>0.960,P<0.01)。这也说明生物炭的吸附性能不仅与自身物化性质、溶液pH等条件有关,生物炭对于不同污染物的吸附机理也是有很大差异的。
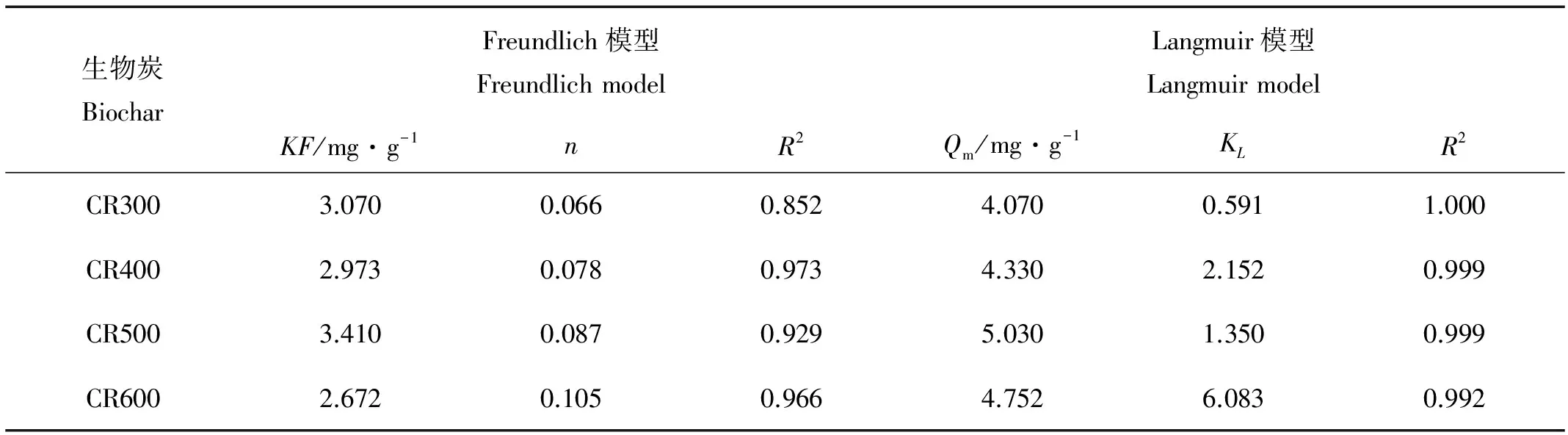
表3 不同热解温度制备的芦苇生物炭对亚甲基蓝吸附的拟合参数
3 结语
高温生物炭具有更高的芳香化程度、更发达的孔隙结构和更大的比表面积,其表面含氧官能团与低温生物体相比较少。与伪一级动力学模型相比,伪二级动力学模型对于生物炭对亚甲基蓝的吸附过程具有更准确的拟合性,化学吸附在整个吸附过程中占据主要地位。当溶液的初始pH增加时,亚甲基蓝在芦苇生物炭上的平衡吸附量逐渐增加,说明碱性环境下更有利于生物炭对于亚甲基蓝的吸附。当溶液的NaCl浓度增加时,亚甲基蓝在芦苇生物炭上的平衡吸附量略有减少,说明溶液中的NaCl浓度对亚甲基蓝的吸附可能存在不明显抑制作用。Langmuir模型能对芦苇生物炭对于亚甲基蓝的等温吸附实验数据进行很好的拟合,说明亚甲基蓝在芦苇生物炭上的吸附基本上是简单的单分子层吸附。
[1] 任南琪,周显娇, 郭婉茜, 等. 染料废水处理技术研究进展[J]. 化工学报, 2013(1): 84-94. Ren N Q, Zhou X J, Guo W X, et al. A review on treatment methods of dye wastewater[J]. Journal of Chemical Industry and Engineering(China), 2013(1): 84-94.
[2] 沈吉利. 竹炭对染料废水的吸附性能试验[J]. 浙江农业科学, 2014(1): 108-111. Shen J L. Adsorption experiment of dye wastewater on bamboo charcoal[J].Journal of Zhejiang Agricultural Sciences, 2014(1): 108-111.
[3] 梁佳, 曹明明. 印染废水特点及其处理技术[J]. 地下水, 2011(2): 67-69. Liang J, Cao M M. Characterization of dyeing effluents and its treatment techniques[J]. Groundwater, 2011(2): 67-69.
[4] 张佳, 任秉雄, 王鹏, 等. 山茶籽粉吸附亚甲基蓝的性能研究[J]. 环境化学, 2013, 32(8): 1539-1545. Zhang J, Ren B X, Wang P, et al. Mechanistic study on adsorption of methylene blue on tea seed powder[J]. Environmental Chemistry, 2013, 32(8): 1539-1545.
[5] El Sikaily A, Khaled A, Nemr A E, et al. Removal of methylene blue from aqueous solution by marine green algaUlvalactuca[J]. Chemistry and Ecology, 2006, 22(2): 149-157.
[6] Ahmad M, Rajapaksha A U, Lim J E, et al. Biochar as a sorbent for contaminant management in soil and water: A review[J]. Chemosphere, 2014, 99: 19-33.
[7] 张阿凤, 潘根兴, 李恋卿. 生物黑炭及其增汇减排与改良土壤意义[J]. 农业环境科学学报, 2009, 28(12): 2459-2463. Zhang A F, Pan G X, Li L Q. Biochar and the effect on C stock enhancement, emission reduction of greenhouse gases and soil reclaimation[J]. Journal of Agro-Environment Science, 2009, 28(12): 2459-2463.
[8] 李际会. 改性生物炭吸附硝酸盐和磷酸盐研究[D]. 北京:中国农业科学院, 2012. Li J H. Adsorption of Nitrate and Phosphate by Modified Biochar[D].Beijing: The Chinese Academy of Agricultural Sciences, 2012.
[9] Lehmann, Joseph. Biochar for Environmental Management: Science and Technology[M]. London: Earthscan, 2009.
[10] Lehmann J, Rondon M. Bio-char soil management on highly weathered soils in the humid tropics[M]. Biological Approaches to Sustainable soil Systems. Boca Raton, FL: CRC Press, 2006: 517-530.
[11] Sun K, Ro K, Guo M, et al. Sorption of bisphenol A, 17α-ethinyl estradiol and phenanthreneon thermally and hydrothermally produced biochars[J]. Bioresource Technology, 2011, 102(10): 5757-5763.
[12] Hale S E, Hanley K, Lehmann J, et al. Effects of chemical, biological, and physical aging as well as soil addition on the sorption of pyrene to activated carbon and biochar[J]. Environmental Science & Technology, 2011, 45(24): 10445-10453.
[13] Tsai W T, Chen H R. Adsorption kinetics of herbicide paraquat in aqueous solution onto a low-cost adsorbent, swine-manure-derived biochar[J]. International Journal of Environmental Science and Technology, 2013, 10(6): 1349-1356.
[14] Dong X, Ma L Q, Li Y. Characteristics and mechanisms of hexavalent chromium removal by biochar from sugar beet tailing[J]. Journal of Hazardous Materials, 2011, 190(1): 909-915.
[15] Van Vinh N, Zafar M, Behera S K, et al. Arsenic (III) removal from aqueous solution by raw and zinc-loaded pine cone biochar: equilibrium, kinetics, and thermodynamics studies[J]. International Journal of Environmental Science and Technology, 2015, 12(4): 1283-1294.
[16] 林雪原, 荆延德, 巩晨, 等. 生物炭吸附重金属的研究进展[J]. 环境污染与防治, 2014(5): 83-87. Lin X Y, Jing Y D, Gong C, et al. Research progress on the sorption of heavy metals by biochar[J].Environmental Pollution & Control, 2014(5): 83-87.
[17] 郎印海, 刘伟, 王慧. 生物炭对水中五氯酚的吸附性能研究[J]. 中国环境科学, 2014(8): 2017-2023. Lang Y H, Liu W, Wang H. Adsorption efficiencies of pentachlorophenol from aqueous solution onto biochars[J]. China Environmental Science, 2014(8): 2017-2023.
[18] 张桂香, 郭文帝, 何秋生, 等. 离子强度, Cd2+和 pH 对生物炭吸附西玛津的影响[J]. 土壤, 2015, 47(4): 733-739. Zhang G X, Guo W D, He Q S, et al. Effects of ionic strength, Cd2+and pH on sorption of simazine to biochars[J]. Soils, 2015, 47(4): 733-739.
[19] Zheng H, Wang Z, Deng X, et al. Characteristics and nutrient values of biochars produced from giant reed at different temperatures[J]. Bioresource Technology, 2013, 130: 463-471.
[20] Liu Y, Zhao X, Li J, et al. Characterization of bio-char from pyrolysis of wheat straw and its evaluation on methylene blue adsorption[J]. Desalination and Water Treatment, 2012, 46(1-3): 115-123.
[21] Sun L, Wan S, Luo W. Biochars prepared from anaerobic digestion residue, palm bark, and eucalyptus for adsorption of cationic methylene blue dye: Characterization, equilibrium, and kinetic studies[J]. Bioresource Technology, 2013, 140: 406-413.
[22] Peng P, Lang Y H, Wang X M. Adsorption behavior and mechanism of pentachlorophenol on reed biochars: pH effect, pyrolysis temperature, hydrochloric acid treatment and isotherms[J]. Ecological Engineering, 2016, 90: 225-233.
[23] 陈宝梁, 周丹丹, 朱利中, 等. 生物碳质吸附剂对水中有机污染物的吸附作用及机理[J]. 中国科学(B辑: 化学), 2008(6): 530-537. Chen B L, Zhou D D, Zhu L Z, et al. Adsorption and mechanism of organic pollutants in water on biological carbon adsorbents[J].Science in China(Series B), 2008(6): 530-537.
[24] 安增莉, 侯艳伟, 蔡超, 等. 水稻秸秆生物炭对Pb(Ⅱ)的吸附特性[J]. 环境化学, 2011, 30(11): 1851-1857. An Z L, Hou Y W, Cai C, et al. Lead (Ⅱ) adsorption characteristics on different biochars derived from rice straw[J]. Environmental Chemistry, 2011, 30(11): 1851-1857.
[25] Jalali M, Moradi F. Competitive sorption of Cd, Cu, Mn, Ni, Pb and Zn in polluted and unpolluted calcareous soils[J]. Environmental Monitoring and Assessment, 2013, 185(11): 8831-8846.
[26] Wang F, Yao J, Sun K, et al. Adsorption of dialkyl phthalate esters on carbon nanotubes[J]. Environmental Science & Technology, 2010; 44: 6985-6991.
[27] 吴晴雯, 孟梁, 张志豪, 等. 芦苇秸秆生物炭对水体中重金属 Ni2+的吸附特性[J]. 环境化学, 2015, 34(9): 1703-1709. WU Qingwen, MENG Liang, ZHANG Zhihao, et al. Adsorption behaviors of Ni2+onto reed straw biochar in the aquatic solutions[J]. Environmental Chemistry, 2015, 34(9): 1703-1709.
责任编辑 庞 旻
The Adsorption Research of Biochars Prepared from Common Reed on Methylene Blue
ZHANG Ming-Yue, LI Feng-Min, LU Lun, GU Shu-Rui
(College of Environmental Science and Engineering, Ocean University of China, Qingdao 266100, China)
In order to study the adsorption properties of biochars on methylene blue(MB), common reed is selected from wetland plants to be pyrolyzed into biochars under different temperatures (300~600 ℃). Physical and chemicalpropertieswere characterized by elemental analysis, specific surface area, Fourier transform infrared spectrum, X-ray diffraction and Zeta potential analysis.And adsorption properties on MBwere detected continuously. In this study, the equilibrium time of MB adsorption was 24 h for the biochars (the ratio of solid of biochars to absorb MB is 6 g·L-1), while the adsorption capacity of 500℃ common reed biochar is the strongest which reached the largest equilibrium adsorption capacity of 5.030 mg·g-1. The adsorption capacity of biochars on the removal of MB increased with the initial pH value and it was tending towards balance, while the best initial pH value of solution is 8~9.Besides, the equilibrium adsorption capacity was slightly declining with the increase of ionic strength with the decline range of 5%~22%.The Langmuir isotherm can fit theequilibrium data well (R2>0.99), and it describes the absorption of biochars on MB belongs to the monolayer adsorption.
common reed biochar; methylene blue; adsorption
国家自然科学基金项目(51378480);国家水体污染控制与治理重大科技专项(2012ZX07203004)资助 Supported by National Nature Science Foundation of China(51378480); National Science and Technology Major Project on Water Pollution Control and Treatment(2012ZX07203004)
2016-02-24;
2016-04-02
张明月(1993-),女,硕士生,主要研究方向为生物炭吸附。E-mail: 18765950812@163.com
X52
A
1672-5174(2016)12-096-08
10.16441/j.cnki.hdxb.20160043
张明月, 李锋民, 卢伦, 等. 芦苇生物炭对亚甲基蓝的吸附特性研究[J]. 中国海洋大学学报(自然科学版), 2016, 46(12): 96-103.
ZHANG Ming-Yue, LI Feng-Min, LU Lun, et al. The adsorption research of biochars prepared from common reed on methylene blue[J]. Periodical of Ocean University of China, 2016, 46(12): 96-103.
❋❋ 通讯作者:lifengmin@ouc.edu.cn

