CO2加氢合成清洁能源DME催化剂的研究
杜 杰,张雅静,李德豹,王康军,李春艳,吴 静
(沈阳化工大学化学工程学院,辽宁 沈阳 110142)
由于国民经济的高速发展,中国已成为世界上能源消耗大国。目前我国的能源结构以不可再生的化石燃料为主,其燃烧后排放大量的CO2,引发了温室效应等一系列环境问题[1]。节能减排势在必行,因此将CO2进行转化利用成为研究的热点[2]。目前,CO2利用的主要方法是将廉价的CO2转化为高附加值化学品,如甲烷[3]、甲醇[4-5]、二甲醚(DME)[6-9]、低碳烃[10]、碳酸酯类[11]、醋酸等[12]。 DME 具有无毒、无腐蚀、易压缩性等优点,可以应用在化工、制冷和燃料等方面[13]。DME具有较高的十六烷值(大于55),碳烟排放和微粒排放为零,没有加速烟尘,发动机氮氧化物、微粒、一氧化碳、非甲烷碳氢和醛类等有害物排放量都低于世界上最严格的美国加州排放标准[14],符合绿色能源的要求,国际上称之为21世纪洁净燃料[15]。因而CO2加氢制DME近年来成为研究热点。
CO2合成DME可以分为两步法和一步法,其中一步法具有较大的优势。CO2加氢一步法合成DME双功能催化剂由甲醇合成催化剂和甲醇脱水催化剂两部分组成。CO2加氢生成甲醇主要使用Cu基催化剂,甲醇脱水生成DME则用如HZSM-5分子筛类固体酸催化剂[16]。催化剂制备方法对催化剂结构与性能具有非常重要的影响。文献报道制备方法主要有共沉淀法[6-9]、浸渍法[17-18]、溶胶-凝胶法[19]、燃烧合成法[20]等,其中共沉淀法为最常用的方法。对于共沉淀法,常用的沉淀剂有草酸、氨水、氢氧化钠、草酸钠和碳酸钠[21-22],沉淀剂的选择会对制备催化剂的晶粒尺寸、比表面积、还原性能、对反应物气体的吸附性能等物化性质产生影响[23]。本文以尿素作为沉淀剂[23-24],利用其水溶液在一定温度下发生水解反应后缓慢均匀地释放出来的OH-来沉淀金属离子,获得催化剂前驱体,再经焙烧制备出CuO-ZnOZrO2/HZSM-5催化剂,本文主要研究沉淀剂的量对催化剂结构及性能的影响。
1 实验部分
1.1 催化剂的制备
将称量好的一定量的 Cu、Zn、Zr硝酸盐按照m(CuO):m(ZnO)=5:4,m(ZrO2)/m(CuO+ZnO+ZrO2)=2%配制成水溶液,室温下搅拌10min左右直至得到蓝色透明溶液A,在搅拌过程中将一定量的尿素加到溶液A中,直至溶液混合均匀。将溶液A转移到三口烧瓶中,同时将分子筛HZSM-5(n(SiO2)/n(Al2O3)=38)加入三口烧瓶中,其与氧化物总量的质量比为1:8,将三口烧瓶置于水浴95℃搅拌老化12h;产物经过滤、洗涤后在干燥箱中120℃下干燥12h;然后在马弗炉中400℃下焙烧4h,得到催化剂粉末B。将所得粉末B压片,过筛选取20~40目的催化剂,得到CuO-ZnO-ZrO2/HZSM-5双功能催化剂,简称为CZZH-X(C、Z、Z、H 分别代表组分 CuO、ZnO、ZrO2、HZSM-5,X代表尿素添加量占化学计量比的倍数)。按这种方法制成尿素用量分别为200%、300%、400%、500%的双功能催化剂,分别记为CZZH-2、CZZH-3、CZZH-4、CZZH-5。
1.2 催化剂的活性评价
催化剂的评价在高压固定床管式反应器中进行,取1.0mL催化剂装入反应管正中部,常压下通入体积流量1:9的氢氮混合气对催化剂进行还原(30mL/min),在 300℃下还原 3h。 还原完成后,切换为体积比为3:9:1的CO2/H2/N2反应气,空速为1500h-1,压力为3.0MPa。反应产物和尾气分析采用北分瑞利公司SP-3420型气相色谱仪,CO、CO2的检测采用TCD检测器 (GDX-101串联Porapak T色谱柱),C2H4、CH3OH 和 CH3OCH3的检测采用 FID 检测器(Porapak Q色谱柱)。
1.3 催化剂表征
X射线衍射 (XRD)测量采用Rigaku D/max 2500pc型X射线衍射仪,Cu靶,Kα射线,管电压50kV,管电流300mA。比表面积 (BET)测定在QuantachromeAutosorb 1-C全自动物理化学吸附仪上进行,吸附质为N2,吸附温度为液氮温度。采用Multi-BET方法(相对压力0.05~0.30的吸附数据)计算比表面积,用BJH方法算出孔径分布,用T-Plot方法算出样品的微孔孔容,总孔容与微孔孔容的差值为介孔孔容。氢气程序升温还原(H2-TPR)在康塔公司化学吸附仪上进行,称取0.03g催化剂样品装入石英玻璃管中,400℃下通入 He(30mL/min)吹扫30min,降至室温后切换成体积比1∶9的H2/N2标准混合气(30mL/min),以 10℃/min升温至 400℃。氨气程序升温脱附(NH3-TPD)在康塔公司化学吸附仪上进行,称取0.10g催化剂样品装入石英玻璃管中,通入He(30mL/min),在400℃条件下吹扫1h,降至50℃,连续通入φ(NH3)为8%的氨氦混合气吸附30min,切换成 He(30mL/min)吹扫 1h,然后以 10℃/min升温至800℃。扫描电镜(SEM)采用JEOLJSM-6360型扫描电子显微镜观察催化剂颗粒表面的形貌,加速电压10kV。
2 结果与讨论
2.1 催化剂的物相
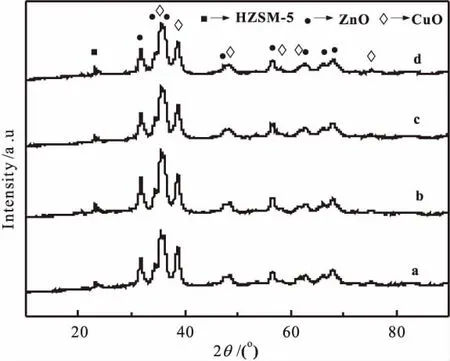
图1 采用不同尿素用量制备催化剂焙烧后的XRD谱图Fig.1 XRD patterns of catalysts prepared with different amount of urea
图1是在不同尿素用量条件下制备的CZZH-X催化剂经焙烧后的XRD谱图。从谱图中可以看出,四组催化剂中均存在 CuO (2θ=35.5°、38.7°、48.4°、58.2°、61.7°、75.3°) 和 ZnO (2θ=31.7°、34.4°、36.1°、47.9°、56.6°、62.8°、66.3°、68.1°)的特征衍射峰;在图中没有出现ZrO2的衍射峰,说明其高度分散在催化剂中或以无定形的形态存在。HZSM-5分子筛的特征峰在2θ=23.3°附近均出现,说明在催化剂制备过程中,HZSM-5分子筛晶体结构保持完好。通过Scherrer公式计算了催化剂中 CuO(111)(2θ=35.5°的衍射峰对应的晶面)和ZnO(100)(2θ=31.7°的衍射峰对应的晶面)的晶粒大小(见表1),结合XRD谱图的衍射峰和表1结果可以看出,当尿素用量从化学计量比的200%增加至400%时,CuO的衍射峰强度变小,峰宽变宽,至400%时,CuO的衍射峰强度变小至最低,CuO的晶粒尺寸达最小;当尿素用量增至500%时,其衍射峰强度基本相同。ZnO的衍射峰强度逐渐变低、衍射峰逐渐变宽。这说明:随着尿素用量的增加,ZnO晶粒尺寸越来越小,而CuO晶粒则先减小后增大。当尿素量为其化学计量比的400%时,CuO晶粒的尺寸最小,说明催化剂中活性组分的分散性最好。
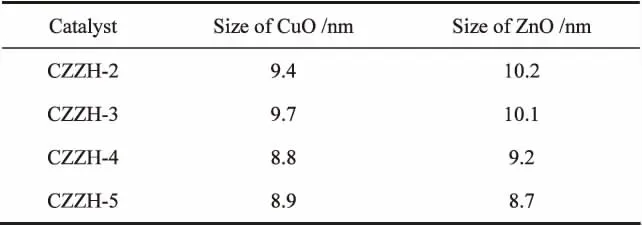
表1 不同尿素量制备催化剂晶粒尺寸Table 1 Crystal grain sizes of catalysts prepared with different amount of urea
2.2 不同尿素用量催化剂的比表面积、孔容和孔径
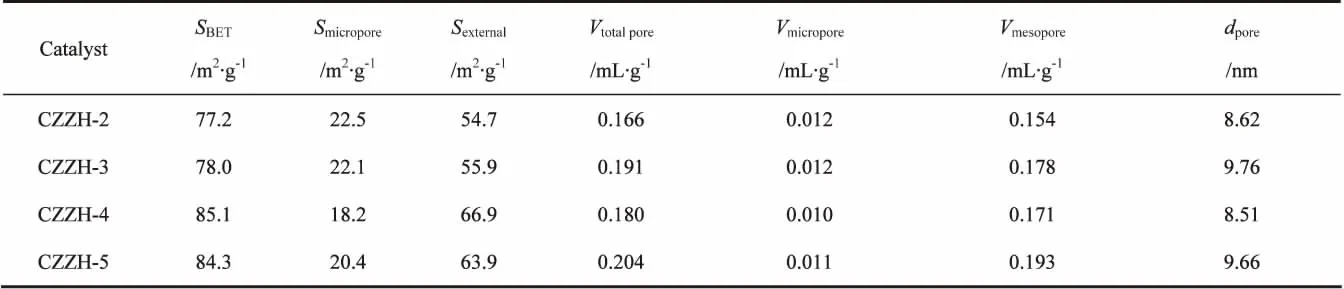
表2 催化剂的BET比表面积、孔容和孔径Table 2 Specific surface areas,pore volumes and average pore diameters of the catalysts
表2给出了不同尿素含量的CuO-ZnO-ZrO2/HZSM-5催化剂的BET比表面积、孔容和平均孔径数据。从表中可以看出,随着尿素量的增加,双功能催化剂的比表面积先增加后减小,CZZH-4催化剂的比表面积最大,达到85.1m2/g,但总体来说差别不是很大。而且可以看到CZZH-4催化剂的孔容较小,平均孔径较小。双功能催化剂比表面积的增加,有助于活性组分的分散,使催化剂的活性位数目增加,从而有助于提高CO2的转化率。
2.3 催化剂的H2-TPR
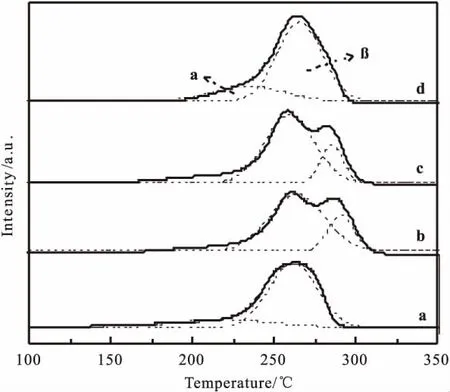
图2 催化剂的H2-TPRFig.2 H2-TPR profiles of catalysts
图2是加入不同尿素量催化剂的H2-TPR图,由图可以看出,催化剂均存在α、β两个还原峰,说明催化剂中存在两种不同状态的CuO。对于两种还原峰,一些研究者认为低温峰(α)归属于表相高度分散的CuO的还原,这部分CuO与ZnO之间有较强相互作用,而高温峰(β)则归属于体相CuO的还原[26-27];还有一些学者认为低温峰(α)对应着Cu2+→Cu+的还原过程,而高温峰(β)对应着 Cu+→Cu的还原过程[28]。此外尿素用量由200%至500%催化剂的还原温度及峰面积分布见表3,尿素用量为200%时还原温度最低,但用量增加到300%时还原温度骤然增大到极值,而后随着制备过程中尿素量的增加,催化剂的还原温度逐渐降低,表明CuO变得容易被还原。当尿素用量从200%增加到400%时,低温还原峰(α)峰面积逐渐增大到最大值,相应高温还原峰(β)逐渐减小到最小值;α峰面积的增加,说明有更多的表相CuO被还原,这就使得在反应时有更多的活性中心参与催化反应。但是当尿素用量增加至化学计量比为500%时,还原峰(α)峰面积突然减小,而高温还原峰(β)峰面积急剧增加,这说明随着尿素用量的增加,体相中的CuO量逐渐增多,催化剂的还原性和加入400%尿素相比,虽还原性较好,但表相中CuO的比例急剧下降这就造成活性大幅下降。
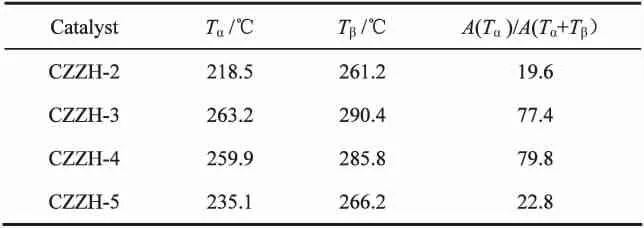
表3 催化剂的还原温度及峰面积分布比例Table 3 Reduction temperature and peak area distribution ratio of catalysts
2.4 不同尿素用量催化剂的表面酸性
催化剂的酸性位是甲醇脱水的活性中心,CuOZnO-ZrO2/HZSM-5双功催化剂的酸性主要由HZSM-5分子筛提供。从图3中可以看出,纯HZSM-5分子筛具有两种酸性位,其中225℃的脱附峰对应着弱酸中心,467℃的脱附峰对应着强酸中心。相对于纯HZSM-5分子筛而言不同尿素含量的双功能催化剂均出现三个脱附峰,分别为弱酸性位、中强酸性位和强酸性位,其中弱酸性位和强酸性位都向低温方向移动。这说明制备催化剂过程中,加入尿素作为沉淀剂,在水解的过程中产生一定OH-,从而使得HZSM-5的表面强酸中心变弱,所以复合催化剂出现了中强酸中心,同时强酸中心减弱。在双功能催化剂中甲醇脱水主要在中强酸性位上进行,强酸会进一步脱水生成烃类,弱酸没有脱水效果,因而中强酸的数量越多,分布越分散,甲醇脱水效果越好。这说明采用尿素作为沉淀剂,可以改变固体酸的酸性中心。
对比双功能催化剂的四条NH3脱附曲线,可以发现随着尿素用量的增加,弱酸性位、中强酸性位和强酸性位的位置和面积基本相同,说明尿素沉淀剂的用量对酸性位强弱的影响不大,这可能和尿素水解过程pH比较稳定有关。
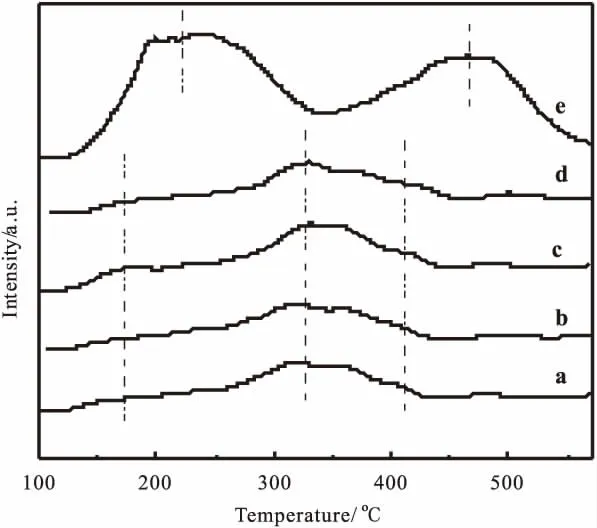
图3 催化剂的NH3-TPD图Fig.3 NH3-TPD spectra of catalysts
2.5 不同尿素用量催化剂的形貌

图4 催化剂的SEM图Fig.4 SEM images of catalysts
图4给出了不同尿素用量的CuO-ZnO-ZrO2/HZSM-5双功能催化剂的SEM图。由图4可以看出:加入尿素量较少时,催化剂呈现不规则形状,颗粒较大(如图中a、b所示);随着尿素用量的不断增加,催化剂颗粒有减小的趋势,颗粒大小分布也变得更加均匀(如图c、d所示)。当尿素用量的化学计量比从400%增加至500%时,催化剂表面形貌变化不明显。SEM图的结果也从侧面印证了催化剂比表面积的变化规律。
2.6 催化剂的催化性能
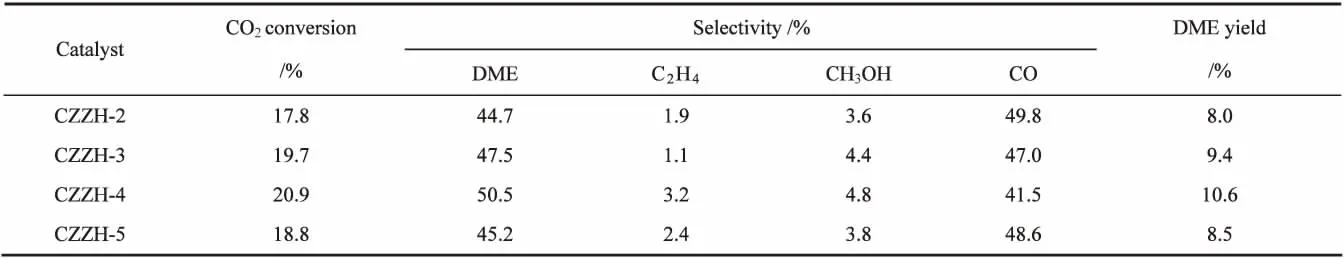
表4 催化剂的催化性能Table 4 Catalytic performances of the catalysts
不同尿素用量条件下制备的CuO-ZnO-ZrO2/HZSM-5催化剂的催化性能见表4。从表中可知,加入适当尿素可以提高催化剂的催化性能。随着尿素量的增加,催化剂的催化活性呈现峰型变化趋势,当尿素从化学计量比为200%增加到400%时,CO2的转化率、DME的选择性以及DME和甲醇的总选择性不断增加,副产物CO的选择性呈下降趋势,当尿素含量到达400%时,CO2转化率、DME选择性达到峰值,分别为20.9%和50.5%。进一步增加尿素的量至化学计量比的500%时,CO2的转化率呈现降低的趋势,DME、甲醇选择性出现下降趋势,副产物CO的选择性呈上升趋势。由此可知,适量的尿素能够使催化剂具有较好的催化性能,这可能是由于沉淀剂的用量影响催化剂的比表面积、晶粒尺寸、还原性和表面酸性所致。
3 结论
(1)在尿素均匀沉淀过程中,沉淀剂尿素的用量对催化剂的结构有着重要的影响,适量的沉淀剂可减小活性组分CuO的晶粒尺寸,加强氧化物之间的相互作用,提高催化剂的比表面积,使活性组分变得更分散,降低催化剂的还原温度,同时也改变了催化剂的酸性中心的强度。
(2)对于该催化体系而言,当尿素用量为其化学计量比的400%时,所制备的催化剂效果最好,在反应温度为260℃,压力为3.0MPa,空速1500h-1下,CO2的转化率、DME的选择性和收率均达最大值,分别为20.9%、50.5%和10.6%。
[1] 许红星.我国能源利用现状与对策[J].中外能源,2010,15(1):3-14.
[2] 杨烽,王睿.温室气体CO2资源化催化转化研究进展[J].煤炭学报,2013,38(6):1060-1071.
[3] Perkas N,Amirian G,Zhong ZY,et al.Methanation of carbon dioxide on Ni catalysts on mesoporous ZrO2doped with rare earth oxides[J].Catal Lett,2009,130:455-462.
[4] 高成广,范凤兰,贾丽华,等.助剂对CuO-ZnO-Al2O3催化CO2加氢合成甲醇性能的影响 [J].天然气化工—C1化学与化工,2013,38(4):42-46.
[5] Li Y N,Ma R,He L N,et al.Homogeneous hydrogenation of carbon dioxide to methanol[J].Catal Sci Technol,2014,4(6):1498-1512.
[6] 邓据磊,吴静,张雅静,等.CO2加氢合成二甲醚催化剂双组份复合方法研究[J].天然气化工—C1化学与化工,2013,38(2):1-4.
[7] 杜杰,张雅静,张宇,等.SiO2助剂对CuO-ZnO/HZSM-5催化CO2加氢制DME性能的影响[J].分子催化,2016,30(4):346-353.
[8] Zhang Y,Li D B,Zhang Y J,et al.V-modified CuO-ZnOZrO2/HZSM-5 catalyst for efficient direct synthesis of DME from CO2hydrogenation catalysis communications[J].Catal Commun,2014,55(19):49-52.
[9] Zhou X H,SuT M,Jiang Y X,et al.CuO-Fe2O3-CeO2/HZSM-5 bifunctionalcatalysthydrogenated CO2for enhanced dimethyl ether synthesis[J].Chem Eng Sci,2016,153:10-20.
[10] Suo Z H,Kou Y.Synthesis of ligth hydrocarbons from carbon dioxide and hydrogen over Fe/TiO2or Fe/ZrO2catalyst[J].J Nat Gas Chem,2000,9(4):283-340.
[11] 崔艳宏,王超,王安杰,等.二氧化碳和甲醇氢等离子体催化反应合成碳酸二甲酯[J].天然气化工—C1化学与化工,2016,41(3):48-51.
[12] Wang J G,Liu C J,Zhang Y P,et al.A DFT study of synthesis of acetic acid form methane and carbon dioxide[J].Chem Phy Lett,2003,368:313-318.
[13] 李伟,张希良.国内二甲醚研究述评 [J].煤炭转化,2007,30(3):88-95.
[14] Sardesai A,Gunda A,Lee S,et al.Carbon dioxide tonerance in the single-stage liquid-phase synthesis of dimethyl ether[J].Energy Sources,2000,22:77-82.
[15] 胡益之,李洪晋,韩冬青.21世纪洁净燃料-二甲醚[J].煤化工,2006,34(5):10-14.
[16] Wang W,Wang S P,Ma X B,et al.Recent advances in catalytic hydrogenation of carbon dioxide[J].Chem Soc Rev,2011,40:3703-3727.
[17] Zhuang H D,Bai S F,Liu X M,et al.Structure and performance of Cu/ZrO2catalystfor the synthesis of methanol from CO2hydrogenation [J].J Fuel Chem Technol,2010,38:462-467.
[18] 解红娟,谭猗生,牛玉琴.CuO/SiO2催化剂用于CO2加氢合成甲醇的研究[J].煤炭转化,2000,23(3):92-96.
[19] 张晓阳,胡志彪,凌华招,等.二氧化碳加氢合成甲醇催化剂及工艺研究开发[J].天然气化工—C1化学与化工,2011,36(6):41-45.
[20] 张素娟,吴静,冯小兵,等.固态研磨-燃烧法制 CuOZnO-ZrO2/HZSM-5二甲醚合成催化剂 [J].分子催化,2013,27(5):445-451.
[21] 张雅静,邓据磊,吴静,等.沉淀剂对悬浮共沉淀法制备二甲醚催化剂的影响[J].分子催化,2013,27(1):43-48.
[22] 张建祥,赵彦巧,陈吉祥,等.二氧化碳加氢直接合成二甲醚催化剂的研究Ⅰ.沉淀剂对催化剂结构和性能的影响[J].燃料化学学报,2003,31(5):444-448.
[23] Zha F,Ding J,Chang Y,et al.Cu-Zn-Al oxide cores packed by metal-doped amorphous silica-alumina membrane for catalyzing the hydrogenation of carbon dioxide to dimethyl ether[J].Ind Eng Chem Res,2012,51:345-352.
[24]Frusteri F,Cordaro M,Cannilla C,et al.Multifunctionality of Cu-ZnO-ZrO2/H-ZSM5 catalysts for the one-step CO2-to-DME hydrogenation reaction[J].Appl Catal B,2015,162:57-65.
[25] Nie R F,Lei H,Pan S Y,et al.Core-shell structured CuO-ZnO@H-ZSM-5 catalysts for CO hydrogenation to dimethyl ether[J].Fuel,2012,96:419-425.
[26] Robinson W,Mol J.Support effects in methanol synthesis over copper-containing catalysts[J].Appl Catal,1991,76:117-129.
[27] Arena F,Barbera K,Italiano G,et al.Synthesis,haracterization and activity pattern ofCu-ZnO/ZrO2catalysts in the hydrogenation of carbon dioxide to methanol[J].J Catal,2007,249:185-194.
[28] Tu M,Davis R J.Cycloaddition of CO2to epoxides over solid base catalysts[J].J Catal,2001,199:85-91.

