纯牛乳中硫氰酸钠高通量快速检测方法的建立
穆洪涛,贺帆丽,王 宇,刘凤银,曾思敏,梁 岳,李晓珺,邹红丽,冯丽娜
(1.广东第二师范学院生物与食品工程学院,广东广州 510303; 2.广州市食品检验所,广东广州 511400)
硫氰酸钠(NaSCN,Sodium thiocyanate)是一种化工原料,常被用于医药、印染等多种行业,同时具有一定的防腐功能,在牛乳中添加一定量的硫氰酸钠可达到抑菌、保鲜及延长牛乳保质期的目的[1-2]。但硫氰酸钠对人体有一定的毒害作用,过量摄入可引起急性毒性,主要表现有恶心、呕吐、昏迷、器官功能衰竭等症状;少量摄取可妨碍人体对碘的吸收和利用,引起甲状腺疾病,尤其对胎儿和婴儿的智力和神经发育存在较大的危害[3]。
2008年12月,我国卫生部发布的《食品中可能违法添加的非食用物质和易滥用的食品添加剂品种名单(第一批)》中明确规定,硫氰酸钠在乳及乳制品中属于违法添加物质[4]。国际食品法典委员会规定生乳中硫氰酸钠的最高限量值为14 mg/kg。我国食品药品监督管理总局将液态乳品中硫氰酸钠的风险监测参考值设定为10 mg/kg[5],国家食药监总局一直将乳品中的硫氰酸钠作为一个监测项目[5]。因此,发展高通量、高灵敏度的硫氰酸钠快速检测方法对于监测和筛查乳及乳制品中的硫氰酸钠残留具有重要意义。
目前,对牛乳中硫氰酸钠进行检测常用的方法主要有两大类:一类是采用高精确度的仪器进行检测,如离子色谱法[6-7]、高效液相色谱法[8]、气相色谱法[9]、扫描拉曼高光谱法[10]等。但是使用这些方法处理样品时间较长、步骤较复杂,对操作人员要求较高,难以满足我国当前养殖业和流通环节的现场高通量快速检测。另一类是基于显色的原理对硫氰酸钠进行检测,比较常用的是铁盐法,其原理是硫氰酸钠在水溶液中可解离出硫氰酸根(SCN-),在酸性条件下可与三价铁离子(Fe3+)反应生成血红色的络合物硫氰酸铁(Fe(SCN)3),利用分光光度法进行定性定量检测[2]或利用目视比色法进行半定量检测[11]。
微孔板法通常用于酶联免疫吸附法分析目标物的含量,具有快速、简便、通量高等特点。因微孔板法优点显著,故被用于总黄酮含量测定[12]、藻类细胞培养[13]、亚硝酸盐含量测定[14]等领域。
本研究基于SCN-与 Fe3+反应生成血红色络合物的原理,以微孔板作为显色载体,通过显色剂筛选、显色条件优化、方法评价等步骤开发出一种准确、快速、简便和高通量的纯牛乳中硫氰酸钠含量测定方法。
1 材料与方法
1.1 材料与仪器
盐酸、硝酸、硫酸、高氯酸、氯化铁、硝酸铁、硫酸铁、高氯酸铁、硫酸铁铵、硫氰酸钠、甲醇、醋酸铅、三氯乙酸 均为分析纯,上海阿拉丁试剂公司;96孔酶标板 厦门怡佳美实验器材有限公司;实验用水 为三级去离子水;全脂灭菌纯牛乳硫氰酸钠阴性样品(经SN/T 3927-2014离子色谱法[15]确认) 由广州市食品检验所提供。
JA2603B型分析天平(0.1 mg) 上海精科科学仪器有限公司;SP-Max 2300A2型光吸收型全波长酶标仪 上海闪谱生物科技有限公司。
1.2 实验方法
1.2.1 溶液的配制 硫氰酸根标准储备溶液(1000 mg/L):将硫氰酸钠固体置于烘箱中60 ℃烘干24 h,并称取1.000 g硫氰酸钠固体,溶解至1 L纯水中,4 ℃保存备用。
硫氰酸钠标准使用液:临用前,准确移取0、0.25、0.5、1、1.5、2、2.5、3 mL硫氰酸钠标准储备液于100 mL容量瓶中,加水稀释至刻度。硫氰酸钠质量浓度分别为0、2.5、5、10、15、20、25、30 mg/L。
显色剂:选取5种常见的铁盐:高氯酸铁(Fe(ClO4)3)、硫酸铁(Fe2(SO4)3)、硝酸铁(Fe(NO3)3)、三氯化铁、硫酸铁铵(NH4Fe(SO4)2)。用其对应酸根阴离子所对应的1.5 mol/L的酸溶液溶解配制成1 mol/L的铁盐溶液作为显色液。
1.2.2 最佳波长的确定 使用1.2.1配制的5种1 mol/L的铁盐溶液0.5 mL与1.5 mL的1.0 g/L硫氰酸钠溶液进行显色,用紫外可见分光光度计在200~800 nm波段对溶液进行扫描,确定显色物质的最佳吸收波长。
1.2.3 显色剂种类筛选 取上述5种1 mol/L铁盐溶液10 μL分别与0、2.5、5、10、15、20、25 mg/L的硫氰酸钠标准使用液200 μL在96孔微孔板中进行显色,调整酶标仪至最佳吸收波长,测定每个微孔的吸光值,选取本底值低且拟合曲线斜率大的铁盐溶液作为最佳显色剂。选取较优的2种1 mol/L铁盐溶液10 μL分别与0、1、1.5、2、2.5、3、3.5、4、4.5、5、6、7、8、9、10 mg/L的硫氰酸钠标准使用液200 μL在96孔微孔板中进行显色,进一步确定最优显色剂。
1.2.4 显色剂浓度筛选 若无特殊说明以下显色均在96孔微孔板中进行,显色剂与硫氰酸钠标准使用液的用量分别为10和200 μL。
将1.2.3筛选到的最优显色剂配制成0.5、1.0、1.5、2.0、2.5 mol/L的溶液(溶剂为最佳显色剂的酸根阴离子所对应的1.5 mol/L的酸溶液),将不同浓度的显色剂溶液分别于30 mg/L硫氰酸钠标准使用液显色5 min,于最佳吸收波长测定反应体系吸光值,确定显色剂工作浓度。为进一步确认显色剂工作浓度,用系列浓度梯度为0.5、1.0、1.5、2.0、2.5 mol/L的高氯酸铁溶液对浓度范围为0~60 mg/L的硫氰酸钠溶液进行显色,测定465 nm的吸光值,建立硫氰酸钠浓度与吸光度间的线性关系。
1.2.5 显色剂酸度优化 用浓度梯度为0.5、1.0、1.5、2.0、2.5、3.0 mol/L的最佳显色剂酸根阴离子所对应的酸溶液作为溶剂,配制显色剂最佳工作浓度溶液。并与30 mg/L硫氰酸钠使用液进行显色,于最佳吸收波长处测定吸光值,选取吸光值变化趋于稳定时对应的酸度为最佳显色剂酸度。
1.2.6 显色时间优化 向200 μL的30 mg/L硫氰酸钠标准使用液中加入10 μL上述步骤优化的显色剂(1.5 mol/L的高氯酸铁溶液(用2.0 mol/L高氯酸溶液配制))后混匀,立即用酶标仪在最佳吸收波长下进行30 min动力学扫描,频率为5 s采集一次。选取吸光值趋于稳定时对应的时间为最佳显色时间。
1.2.7 显色温度优化 用最优显色剂(1.5 mol/L的高氯酸铁溶液(用2.0 mol/L高氯酸溶液配制))分别在温度为4、25、37、50、60 ℃的环境下对浓度为0~30 mg/L的硫氰酸钠标准使用液进行显色,选取显色灵敏度高的温度为最佳显色温度。
1.2.8 标准曲线的绘制 采用优化后的最佳测试条件,分别测定0、0.5、1、5、10、20、30、40、50、60、70和80 mg/kg硫氰酸钠系列标准溶液的吸光值。以硫氰酸钠浓度为0的标准溶液调零,以硫氰酸钠的浓度为横坐标,以465 nm下酶标仪的读数为纵坐标绘制标准曲线。
1.2.9 样品前处理优化 取4份10 mL纯牛乳样品,分别加入1 mL处理液(甲醇、50%三氯乙酸、配制最佳显色剂所用的酸溶液(2 mol/L高氯酸)、饱和醋酸铅溶液)进行前处理,然后10000 r/min离心 5 min,选取离心液最澄清且对显色体系无干扰者为最佳样品前处理剂。
1.2.10 加标回收实验 使用全脂灭菌纯牛乳经样品前处理后,用本研究建立的检测方法进行加标回收实验[16],硫氰酸钠添加量分别为:1.0、5.0、10.0、20.0和80.0 mg/kg。加标回收率的计算公式为:
加标回收率(%)=(加标样品=测得目标物总量-基质中目标物的量)/添加硫氰酸钠的量×100
1.2.11 精密度检验 精密度是指在规定条件下对同一被测对象重复测量所得示值或被测量的量值间的一致程度[17]。向牛乳样品中分别添加1.0、5.0、10.0、20.0和80.0 mg/kg的硫氰酸钠标准品,用本研究确定的方法进行20次重复测定用以验证本方法的精密度。
1.3 数据处理
本研究中数据无特殊说明均重复3次或以上,纯牛乳中硫氰酸钠数据采用SPSS 19.0软件进行显著性差异分析,数据绘图软件选用Origin 8.0。
2 结果与分析
2.1 最佳波长的确定
对5种铁盐(高氯酸铁、硝酸铁、硫酸铁、三氯化铁、硫酸铁铵)与硫氰酸钠的反应溶液进行200~800 nm全波长扫描,扫描结果见图1。由图1可知,各显色体系在200~800 nm波长下均出现三个明显的吸收峰:230、249和465 nm。其中230和249 nm处的两个峰很可能为硫氰酸根离子中碳氮三键(S-C≡N)-的紫外吸收引起的,但因其峰强度与浓度变化之间的线性关系不明显,故不用此二峰进行硫氰酸铁的定量分析。另外波长位于465 nm处的峰强与浓度变化呈明显的线性关系,为硫氰酸铁络合物的特征峰[2]。即硫氰酸铁络合物的最佳吸收波长为465 nm。
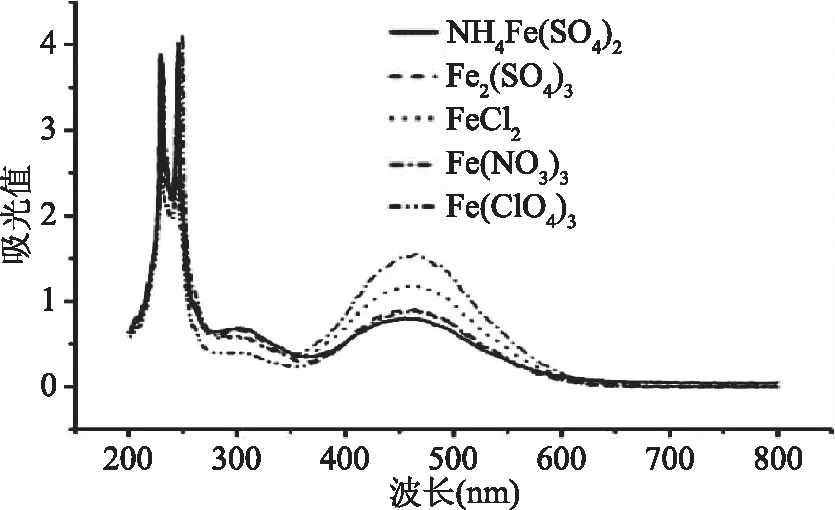
图1 5种不同显色体系全波长扫描结果Fig.1 Full wavelength scanning result of chromogenic solution
2.2 显色剂种类筛选
用5种铁盐溶液分别与0~25 mg/L的硫氰酸钠标准使用液进行显色,于465 nm的波长下测定吸光值,结果如图2所示。由图2可知,各种显色剂拟合曲线的回归系数(R2)无显著差异(硝酸铁0.99677、高氯酸铁0.99767、三氯化铁0.99845、硫酸铁铵0.99691、硫酸铁0.99534)。在分光光度分析方法中,标准曲线的斜率表示的意义为单位浓度变化所引起的吸光值的变化。由此可知,相同条件下,斜率值越大说明此方法单位浓度的吸光值变化越灵敏。显色剂本身的本底值越低,试剂本底值对显色的影响就越小。故选择斜率值较大本底值较低的显色剂作为工作显色剂。5种显色体系标准曲线斜率由高到低依次为:硝酸铁(0.038)、高氯酸铁(0.036)、三氯化铁(0.025)、硫酸铁铵(0.012)、硫酸铁(0.010)。其中硝酸铁体系与高氯酸铁体系的斜率接近,信号响应最为灵敏。各显色剂的本底吸光度分别为:硝酸铁0.15、高氯酸铁0.11、三氯化铁0.17、硫酸铁铵0.10、硫酸铁0.09,其中以高氯酸铁、硫酸铁铵和硫酸铁的本底值最低。经初步筛选,将硝酸铁体系与高氯酸铁体系作为进一步实验对象。
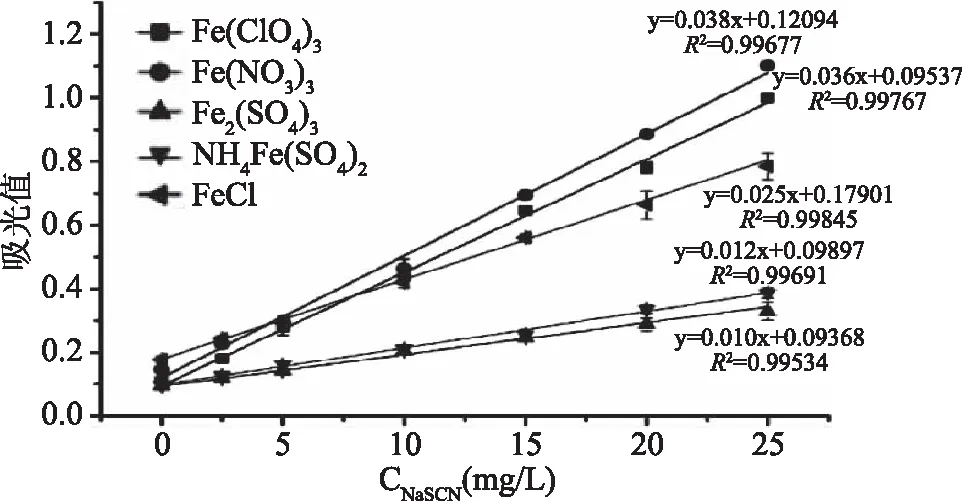
图2 不同显色体系显色拟合曲线Fig.2 Fitting curves of different chromogenic agents’reactions
为了进一步了解硝酸铁与高氯酸铁的显色效果差异,使用两者分别对0~10 mg/L 的硫氰酸钠标准使用液进行显色,于最佳波长下测定吸光值,结果见图3。在0~10 mg/L的硫氰酸钠质量浓度范围内,高氯酸铁体系拟合曲线斜率为0.0328,硝酸铁体系曲线斜率为0.0292,高氯酸铁的信号响应灵敏度稍高于硝酸铁,但两者无显著性差异(P>0.05)。高氯酸铁体系的本底吸光值(0.0964)极显著小于硝酸铁体系本底吸光值(0.1560)(P<0.01),为了最大地减少显色剂本身的颜色对显色体系的影响,本研究选取高氯酸铁为最佳显色剂。
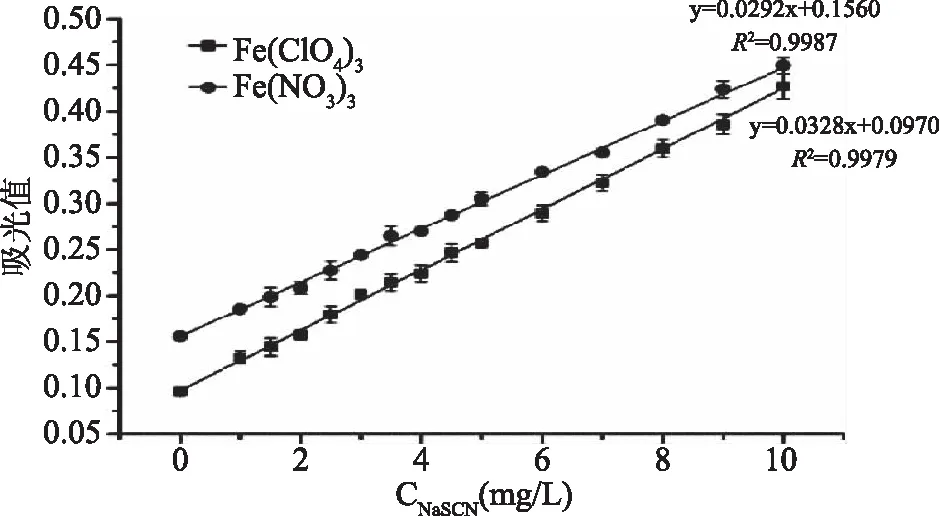
图3 显色剂高氯酸铁、硝酸铁与硫氰酸钠显色拟合曲线(n=3)Fig.3 Fitting curves of ferric perchlorate, iron nitrate color reactions(n=3)
2.3 显色剂浓度筛选
选取高氯酸铁为显色试剂,其与硫氰酸钠反应的浓度与吸光值的关系见图4。随高氯酸铁浓度的增加吸光值(A465 nm)呈缓慢上升趋势,在浓度达到1.5 mol/L时吸光值变化趋于平缓,浓度为1.0、1.5和2.0 mol/L时A465 nm分别为1.130、1.233和1.268,经显著性分析得浓度为1.0、1.5 mol/L时吸光值差异显著(P<0.05),浓度为1.5、2.0 mol/L时吸光值差异不显著(P>0.05),故初步选择1.5 mol/L为高氯酸铁工作浓度。造成此趋势的原因为:高氯酸铁浓度在0.5~1.5 mol/L时,30 mg/L硫氰酸钠是相对过量的,在此范围内增加高氯酸铁的浓度会使吸光值上升。当高氯酸铁浓度达到1.5 mol/L后,高氯酸铁相对过量,此时硫氰酸钠的含量成为吸光值提高的制约因素,故吸光值变化趋势不明显。由此表明高氯酸铁浓度在1.5 mol/L时对30 mg/L的硫氰酸钠充分显色。
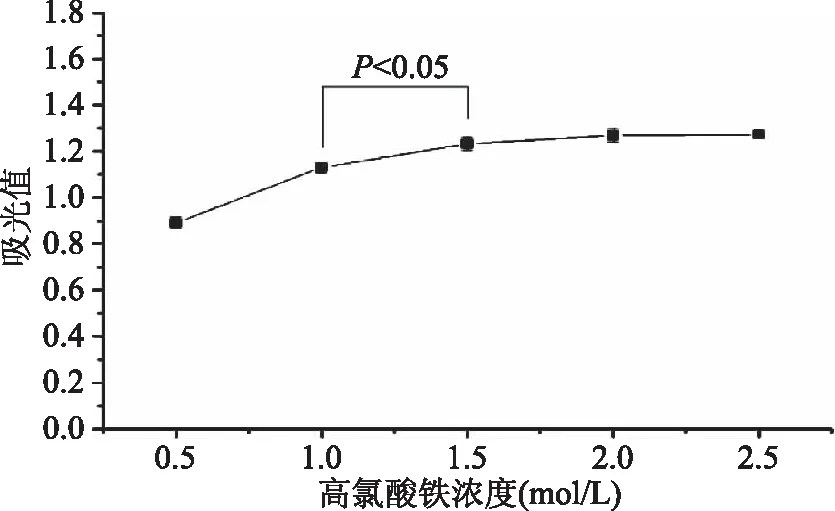
图4 不同浓度高氯酸铁溶液与30 mg/L硫氰酸钠反应的吸光值影响(n=3)Fig.4 Chromogenic absorbance of 30 mg/L sodium thiocyanate with different concentration chromogenic agents(n=3)
为保证选取的高氯酸铁浓度为最佳,用系列浓度梯度为0.5、1.0、1.5、2.0、2.5 mol/L的高氯酸铁溶液对浓度范围为0~60 mg/L的硫氰酸钠溶液进行显色,于465 nm下测定,结果如图5。随高氯酸铁溶液浓度增加,其与硫氰酸钠的拟合曲线斜率和空白本底值都所增加(0.5 mol/L的斜率和空白本地值分别为0.0321、0.0625;1.0 mol/L的分别为0.0337、0.0747;1.5 mol/L的分别为0.0350、0.1034;2.0 mol/L的分别为0.0354、0.1316;2.5 mol/L的分别为0.0357、0.2063)。高氯酸铁溶液浓度选择原则为在稳定性和拟合斜率较高,空白本底值较低为最佳。另外考虑到高氯酸铁浓度越高试剂成本也越高,故选择1.5 mol/L为高氯酸铁工作浓度。
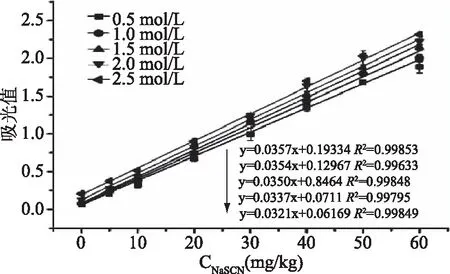
图5 不同浓度高氯酸铁溶液对拟合曲线斜率的影响Fig.5 Effects of different concentrations of ferric perchlorate solution on the slope of fitting curves
2.4 显色剂酸度优化
SCN-与 Fe3+的反应为可逆反应,Fe3+极易发生水解,从而增加显色本底值的影响。0.5、1.0、1.5、2.0、2.5、3.0 mol/L的高氯酸对吸光值的影响如图6。由图可知在2.0 mol/L高氯酸浓度时(即d点)显色吸光值达到峰值(1.2152±0.0228)。高氯酸浓度2.0 mol/L时的吸光值(1.2152±0.0228)与相邻浓度2.5 mol/L时的(1.0991±0.0287)和1.0 mol/L时的(1.1043±0.0409)差异均显著(P<0.05),与浓度为1.5 mol/L时的(1.1693±0.0414)相比,2.0 mol/L时的吸光值稍高,但差异未达到显著水平(P>0.05)。综合考虑选择高氯酸浓度2.0 mol/L为其工作浓度。
图6所示,吸光值随着酸度的增大而增大,在 2.0 mol/L 高氯酸浓度时显色吸光值达到峰值,之后有所下降。吸光值下降的可能原因是:当反应溶液过酸,溶液中有大量的H+,会使可逆反应中:Fe3++3SCN-Fe(SCN)3的SCN-形成HSCN分子,导致SCN-减少,使可逆反应向生成SCN-的方向移动,而导致Fe(SCN)3减少,反应体系颜色变浅,吸光值减小。
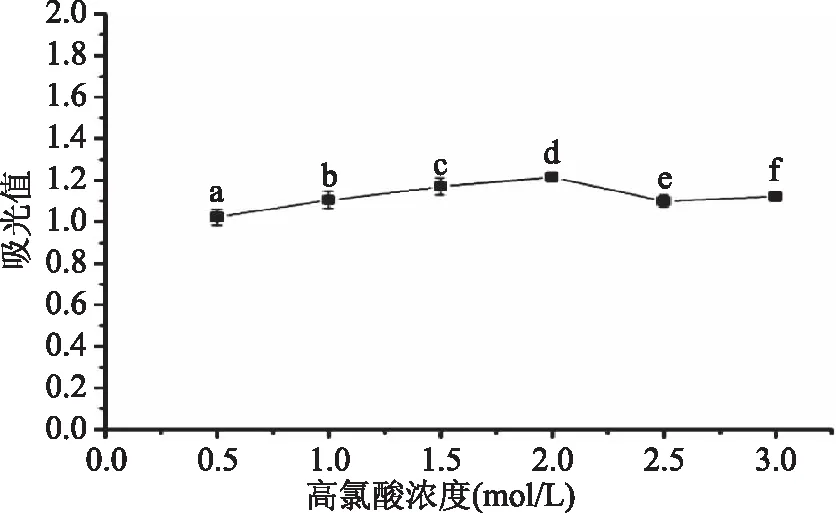
图6 不同酸度对吸光值的影响(n=3)Fig.6 Influence of different acidity on color rendering effect(n=3)
2.5 显色时间优化
显色时间过短,会导致显色不充分,从而影响检测结果,显色时间过长,会降低检测的效率。本研究对30 mg/L 硫氰酸钠标准使用液显色后用酶标仪在465 nm波长下以每5 s间隔记录一个吸光值数据,获得1800 s(30 min)内的动力学扫描图,结果如图7。由图7可知显色反应在30 min内呈直线型缓慢上升,显色开始和显色1800 s吸光值分别为1.1578和1.2721,差异显著(P<0.05)。延长显示反应时间虽然能提高吸光值,但需要耗费大量的测试时间。由于吸光值随反应时间变化匀速且缓慢,从快速测定方法的时间因素考虑,本研究选择反应300 s(即5 min)作为显色反应时间。
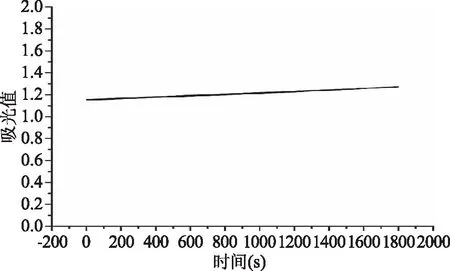
图7 吸光值与时间的关系Fig.7 Relationship between absorption and time
2.6 显色温度优化
本研究分别以2.5、5、10、15、20、25、30 mg/L的硫氰酸钠标准使用液考察了在4、25、37、50、60 ℃五种温度环境对显色体系的影响,用酶标仪在465 nm波长下进行3次平行测定,结果如图8。不同显色温度下的吸光值变化曲线基本重合,显色温度对显色结果影响不显著(P>0.05)。可能原因是本体系的显色反应速率在较低的温度下即可正常进行,实验中选用的温度梯度均在其高速反应的阶段。为了使检测方便易操作,本方法选择反应温度为室温25 ℃。
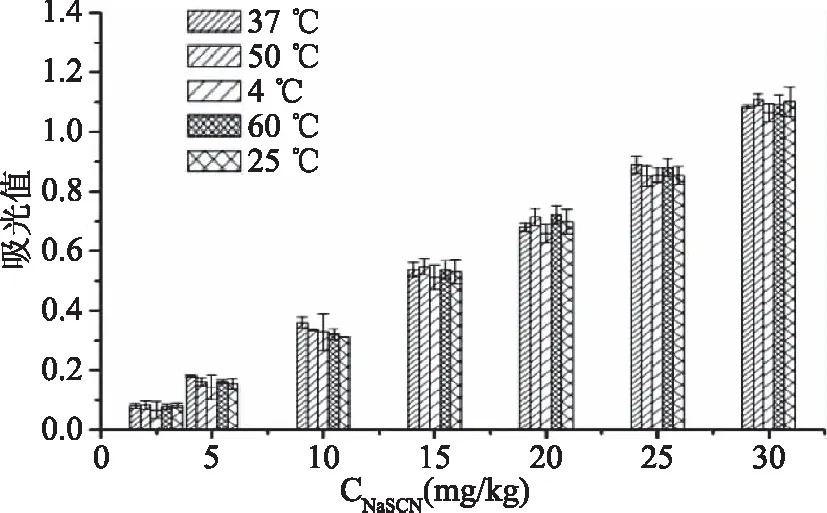
图8 温度对吸光值的影响Fig.8 The effect of temperature on light absorption
2.7 标准曲线的绘制
根据以上优化试验获得方法最佳工作条件为:1.5 mol/L的高氯酸铁溶液(用2.0 mol/L高氯酸溶液配制)作为最佳显色剂,室温25 ℃下反应5 min,用酶标仪读取465 nm波长下的吸收值,标准曲线绘制结果如图9。由线性拟合得标准曲线方程为y=0.00945x+0.00099,R2=0.9997。此方法能够满足国标GB/T 27404-2008“实验室质量控制规范食品理化检测”中对相关系数的要求,能够满足当前对纯牛乳中硫氰酸钠残留的日常快速检测方法的要求。
通过测定20个标准零浓度,计算所有标准零浓度的标准偏差,以3倍(S/N=3)标准零浓度的标准偏差作为最低检出限,为0.27 mg/kg。用10倍标准零浓度的标准偏差作为最低定量限,为0.9 mg/kg。如图9所示,曲线在硫氰酸钠量浓度为80 mg/L时弯曲开始出现平台,故本方法线性范围的最大值为80 mg/kg。方法的检测线性范围为0.9~80 mg/kg。此方法的检测灵敏度和线性范围能够满足生鲜牛乳市场对硫氰酸钠的筛查要求。
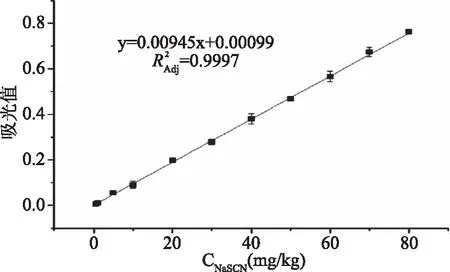
图9 硫氰酸钠标准曲线Fig.9 Sodium thiocyanate standard curve
2.8 样品空白前处理优化
取10 mL纯牛乳样品加入1 mL处理液,振荡后以10000 r/min速度离心5 min。甲醇处理纯牛乳无法离心得到澄清液,50%三氯乙酸、2 mol/L高氯酸、饱和醋酸铅溶液处理后的纯牛乳均可在离心后得到澄清液,但在澄清液液面会形成一层蛋白薄膜,较难取出中间的澄清液。故本实验采用过滤方法获得处理样澄清液。
采用过滤方法,甲醇处理样品仍无法获得澄清液。用50%三氯乙酸处理剂、1.5 mol/L高氯酸铁与2 mol/L高氯酸处理剂、饱和醋酸铅处理剂进行显色反应,结果显示饱和醋酸铅会对本体系显色呈棕红色,从而造成显色干扰;高氯酸处理剂、50%三氯乙酸处理剂与显色剂不发生任何颜色变化,不会对本体系显色造成干扰(图10)。为了更好的保证显色体系的准确性,因2 mol/L高氯酸为显色剂中的成分,无需另外添加其他试剂,故样品前处理使用2 mol/L高氯酸进行。

图10 不同澄清剂对显色体系的影响Fig.10 Effects of different clarifying agents on the color developing system
2.9 样品加标回收实验
加标回收实验所采用的样本为全脂灭菌纯牛乳,其本身所含有的硫氰酸钠含量经《SN/T 3927-2014出口乳制品中硫氰酸钠含量的测定》[15]中的离子色谱法确定为阴性样品。加标回收实验中硫氰酸钠的添加量分别为:1.0、5.0、10.0、20.0和80.0 mg/kg五组,经样品前处理及测定得实验结果见表1。由表1可知,本方法的加标回收率范围在83%~99%之间,本方法对高中低各添加浓度均有较好的回收率。
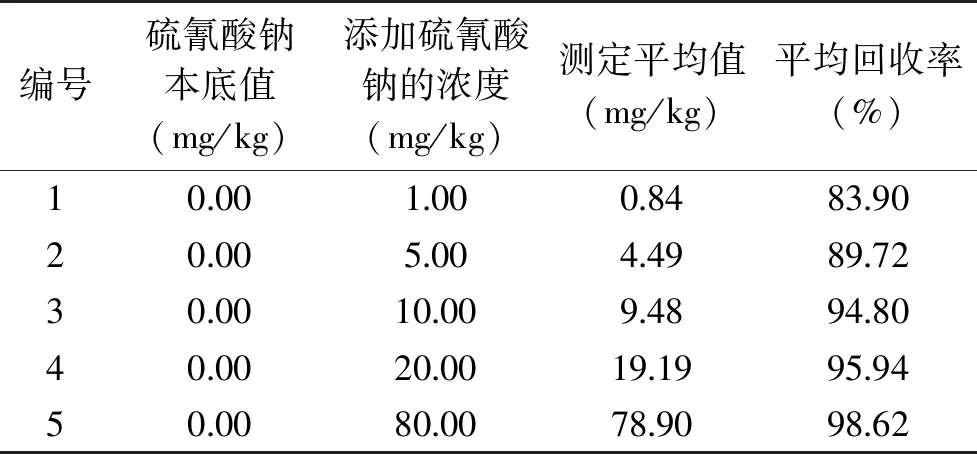
表1 样品加标回收实验结果(n=6)Table 1 The results of the adding recovery experiment(n=6)
2.10 精密度检验
向全脂灭菌纯牛乳阴性样品中分别添加1.0、5.0、10.0、20.0和80.0 mg/kg的硫氰酸钠标准品,用本研究建立的方法进行20次重复测定,结果见表2。从测定平均值分析,表2和表1结果一致,方法具有较好的加标回收率,测定结果可靠。纯牛乳样品中分别添加1.0、5.0、10.0、20.0和80.0 mg/kg的硫氰酸钠标准品测定,相对标准偏差分别为7.892、5.426、4.899、4.177和1.046,相对标准偏差均小于10.0%,说明该体系精密度良好。
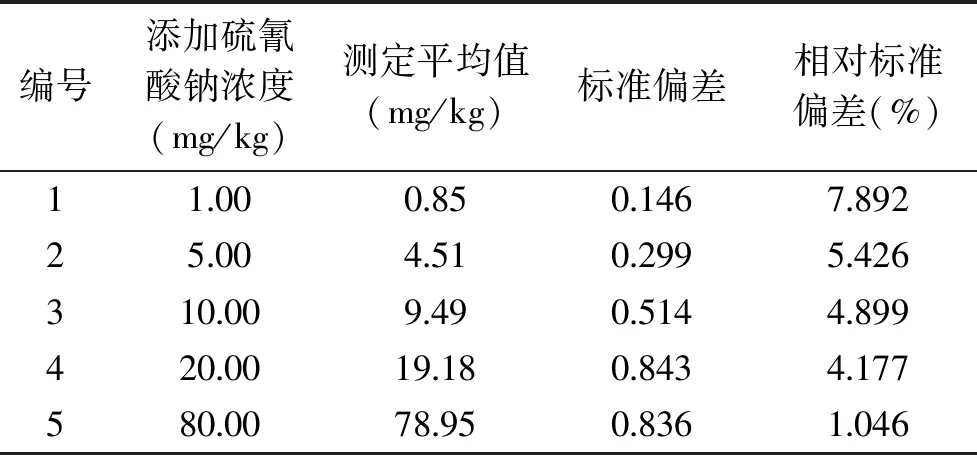
表2 精密度试验(n=20)Table 2 Precision test(n=20)
3 讨论
目前,硫氰酸钠作为违法添加物已列入《食品中可能违法添加的非食用物质和易滥用的食品添加剂品种名单(第一批)》,对其风险监控具有重要意义。内蒙古地区生鲜乳中硫氰酸钠含量的风险监测结果显示,2013-2017年生鲜乳中硫氰酸钠含量平均值为2.75 mg/kg,硫氰酸钠的平均检出率为78.14%[18]。故研究者开发硫氰酸钠高通量快速方法具有较好的应用前景。本研究基于铁盐的显色原理开发了微孔板显色定量方法,与现有检测方法对比如表3。
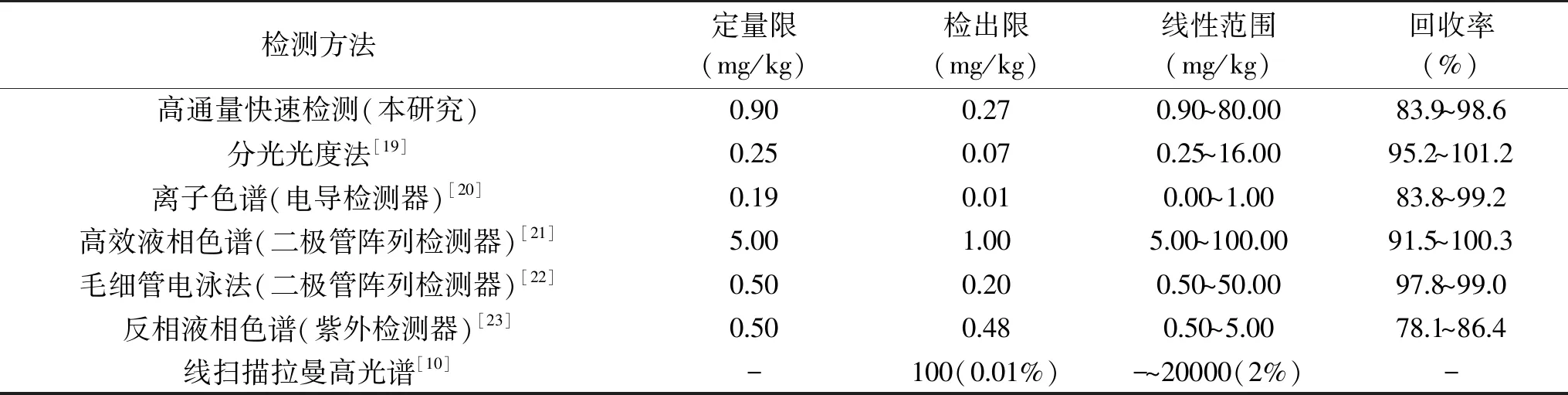
表3 硫氰酸钠检测方法的性能比较Table 3 Comparison of the performance of detection methods for sodium thiocyanate
何瑛等[19]利用分光光度计对乳中的硫氰酸钠含量进行检测,其检测线性范围为0.25~16.00 mg/kg,相比本研究的线性范围0.90~80.00 mg/kg,本方法的定量限0.90 mg/kg虽然不及分光度法,但因生鲜乳中硫氰酸钠含量平均值为2.75 mg/kg[18],此定量限能够满足实际的检测需要。仪器方法如离子色谱法和液相色谱法,为标准确证方法,往往具有更高的灵敏度和稳定性,为硫氰酸钠检测的首选方法,特别是离子色谱法[6]。但考虑到现场快速筛查的客观条件因素,本研究开发的方法无论在定量限和加标回收率方面都能够满足实际检测的需要,特别是本方法基于微孔板显色比传统仪器方法和分光光度法具有更高的通量,检测快速,适合对批量奶样进行快速筛查。
4 结论
本研究基于SCN-与Fe3+反应生成血红色络合物的原理,经系统优化选取1.5 mol/L的高氯酸铁溶液(用2.0 mol/L高氯酸溶液配制)作为最佳显色剂,室温25 ℃下反应5 min,用酶标仪读取465 nm波长下的吸收值。高氯酸铁显色剂与传统的硝酸铁显色剂相比具有更低的本底值(P<0.01)。建立了一种纯牛乳中硫氰酸钠高通量快速检测的方法,其检出限为0.27 mg/kg,定量限为0.90 mg/kg,线性范围为0.90~80.00 mg/kg,加标回收率范围在83.9%~98.6%之间,测试精密度较高,相对标准偏差均小于10.0%。本方法具有准确度高、通量高、试剂用量小、环保、快速等优点,能够满足纯牛乳中硫氰酸钠的检测,适合于大批量纯牛乳中硫氰酸钠残留的快速筛查。

