117例贝伐珠单抗注射液致药品不良反应的特点分析Δ
王明媚,马建丽,王心慧,卫晋菲,李 莎,许玉莲
(解放军总医院第四医学中心药剂药理科,北京 100048)
贝伐珠单抗注射液是目前临床应用较成熟的单克隆抗体抗肿瘤药,该药通过特异性结合血管内皮生长因子(vascular endothelial growth factor,VEGF),抑制VEGF活性,使肿瘤血管生成受阻[1]。目前,贝伐珠单抗注射液多采用联合用药的形式用于治疗结直肠癌、非鳞状细胞非小细胞肺癌及胃癌、乳腺癌等[2]。贝伐珠单抗注射液毒性较低,虽为靶向药物但作用靶点多,应用面相对于其他抗体类靶向药物更广,但需要引起重视的是,其作用易影响正常血管内皮细胞的生长和增殖,应用过多、滥用会导致药品不良反应(adverse drug reaction,ADR)。近年来,贝伐珠单抗注射液致ADR的报道日趋增多。为深入分析贝伐珠单抗注射液致ADR发生的规律和特点,本研究收集解放军总医院第四医学中心(以下简称“我院”)贝伐珠单抗注射液致ADR的临床资料进行归纳总结,为合理用药提供参考。
1 资料与方法
1.1 资料来源
收集2016年9月至2019年12月我院使用贝伐珠单抗注射液治疗的患者。贝伐珠单抗注射液,罗氏制药公司生产,规格100 mg(4 ml),使用时以0.9%氯化钠注射液稀释至所需给药容积,常用剂量范围为4~7.5 mg/kg。
1.2 方法
首先,依据美国东部肿瘤协作组织(eastern cooperative oncology group,ECOG)体能状态评分标准,对患者治疗前的体能状态进行评分,体能状态较好即ECOG评分≤2分的患者纳入收集范围。第二,调取ECOG评分≤2分患者的全部病历,ADR信息记录完整的纳入本次归纳分析。第三,对患者性别、年龄、原患疾病、ADR发生率、ADR种类以及ADR严重程度分级等进行归纳分析,并将ADR种类区分为两大类:(1)贝伐珠单抗注射液药品说明书中提及的所有ADR;(2)剔除其他合用化疗药因素,高度怀疑与贝伐珠单抗注射液相关的ADR,包括血管毒性中的出血、血栓和高血压,肾脏和泌尿系统毒性中的蛋白尿,胃肠道毒性中的胃肠道穿孔、腹痛、便秘腹泻以及其他毒性中的过敏和伤口愈合困难等。ADR严重程度分级按照《美国国家癌症研究所不良事件常用术语评定标准4.0》(national cancer institute common terminology criteria for adverse events,NCI-CTCAE)v4.0版本进行评价。
1.3 统计学方法
相关需要统计的数据采用SPSS 18.0统计学软件进行分析,不同性别患者间ADR发生率差异比较,采用χ2检验,P<0.05表示差异有统计学意义。
2 结果
2.1 患者的基本资料
纳入本次归纳分析的患者共117例,其中男性患者65例,女性患者52例;均根据患者病情制订了相应的贝伐珠单抗注射液用药方案;根据患者实际情况,107例的给药途径为静脉滴注,7例为腹腔灌注,3例为胸腔灌注;患者年龄为10~86岁,中位年龄为60.4岁;患者原患疾病以肺癌和结直肠癌为主,分别为40例和21例,见表1。
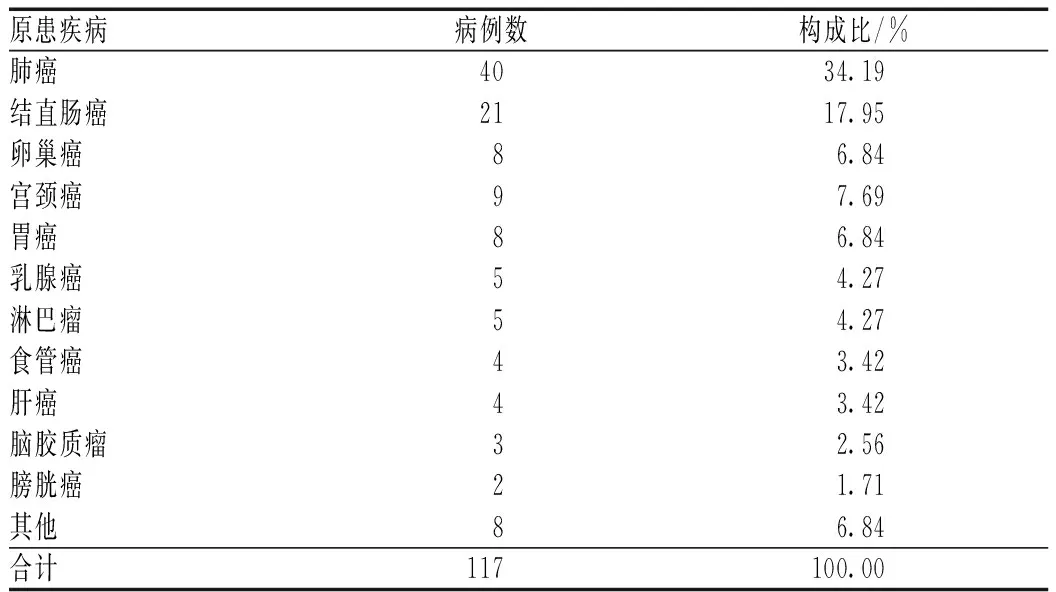
表1 患者原患疾病分布Tab 1 Distribution of primary disease
2.2 患者年龄、性别与ADR的关系
117例患者中,发生贝伐珠单抗注射液药品说明书中提及的所有ADR的患者共75例,发生率为64.10%,年龄主要集中于>50岁。其中,男性患者40例,药品说明书中提及ADR发生率为61.54%(40例/65例);女性患者35例,药品说明书中提及ADR发生率为67.31%(35例/52例),不同性别患者间药品说明书中提及ADR发生率的差异无统计学意义(χ2=0.418,P>0.05)。发生药品说明书中提及ADR的患者年龄、性别分布见表2。
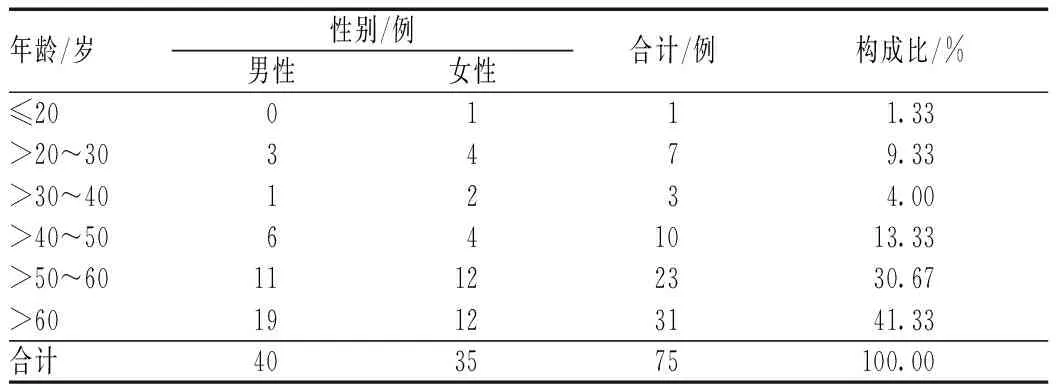
表2 发生药品说明书中提及ADR的患者年龄、性别分布Tab 2 Distribution of gender and age of patients with ADR mentioned in the instructions
发生高度怀疑与贝伐珠单抗注射液相关ADR的患者共39例,其中男性患者21例,高度怀疑与贝伐珠单抗注射液相关ADR发生率为32.31%(21例/65例);女性患者18例,高度怀疑与贝伐珠单抗注射液相关ADR发生率为34.62%(18例/52例),不同性别患者间高度怀疑与贝伐珠单抗注射液相关ADR发生率的差异无统计学意义(χ2=0.069,P>0.05)。高度怀疑与贝伐珠单抗注射液相关的ADR中患者年龄、性别分布见表3。
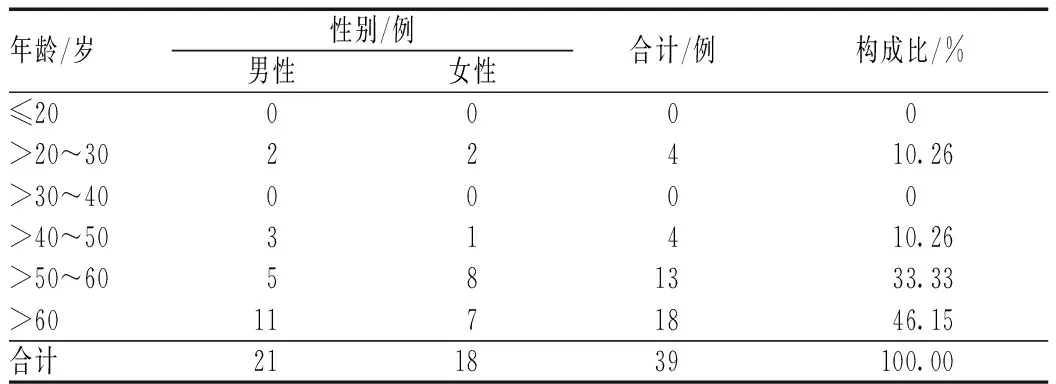
表3 高度怀疑与贝伐珠单抗注射液相关的ADR中患者年龄、性别分布Tab 3 Distribution of gender and age of patients with highly suspected ADR induced by bevacizumab injection
2.3 ADR的分类与分级
根据NCI-CTCAE v4.0的分类与分级,117例患者中,高度怀疑与贝伐珠单抗注射液相关的ADR主要有高血压(18例,发生率为15.38%)、胃肠道毒性(15例,发生率为12.82%)、免疫系统毒性(7例,发生率为5.98%)、出血(6例,发生率为5.13%)和蛋白尿(2例,发生率为1.71%),见表4。
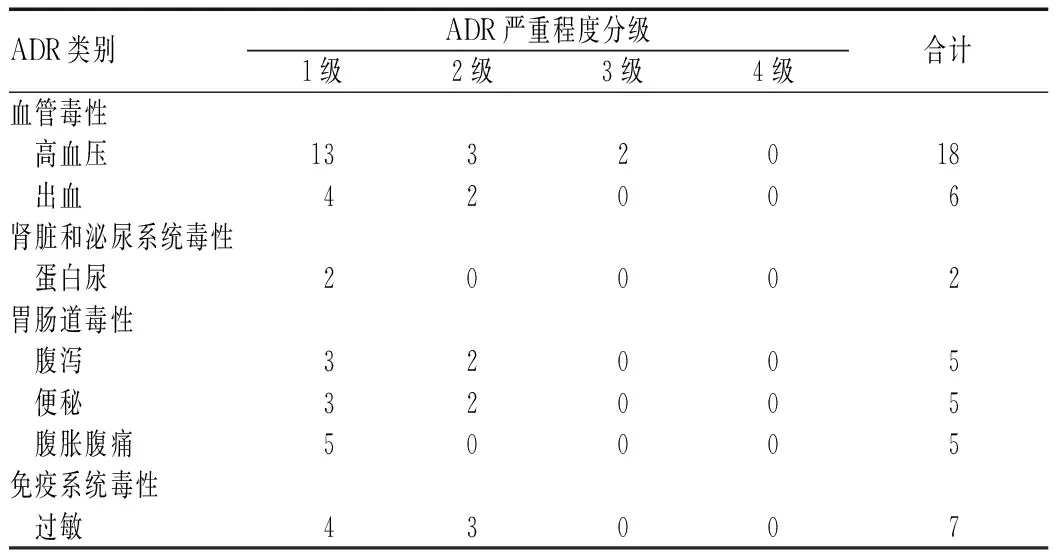
表4 高度怀疑与贝伐珠单抗注射液相关的ADR发生情况(例)Tab 4 Occurrence of highly suspected ADR induced by bevacizumab injection(cases)
药品说明书中提及的其他ADR以血液系统毒性最为常见,其次为胃肠道毒性和神经系统毒性,见表5。
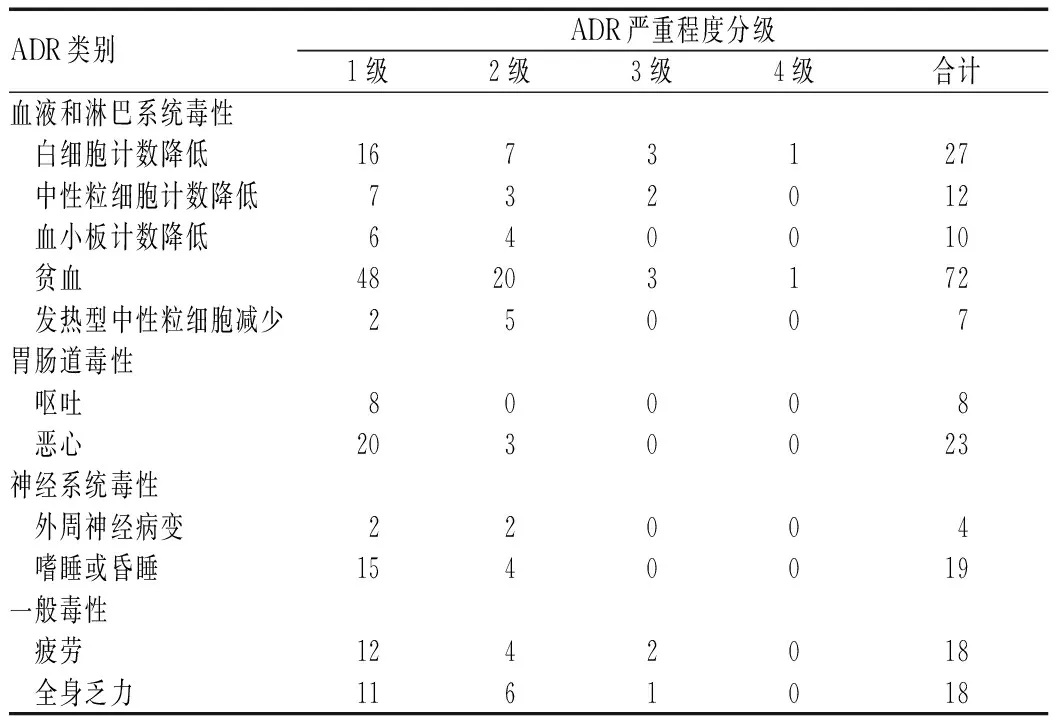
表5 药品说明书中提及的其他ADR发生情况(例)Tab 5 Occurrence of other ADR mentioned in the instructions(cases)
3 讨论
2010年,贝伐珠单抗注射液在我国上市,其在我院主要用于肺癌(非小细胞肺癌)和结直肠癌的治疗,用于其他实体瘤的治疗多见于宫颈癌、乳腺癌及胶质瘤等,在我国还有用于胃癌的相关研究[3]。但因上市时间不长,临床上对其ADR的了解较为有限。
3.1 高度怀疑与贝伐珠单抗注射液相关ADR的分析
3.1.1 高血压:高血压是贝伐珠单抗注射液常见的ADR,有报道其发生率约为8%~29%[4],也有荟萃分析报道其发生率约为2.7%~32%[5]。其中3级以上严重高血压的发生率约为11%,在贝伐珠单抗注射液联合化疗治疗非小细胞肺癌的研究中,3级以上高血压发生率为3%[6]。本研究中,共18例患者发生了高血压,发生率与文献报道基本相符。第1次发生高血压的患者13例,另外5例患者(1级1例,2级3例,3级1例)有高血压病史,治疗前已采取降压措施。发生3级高血压的患者分别予以厄贝沙坦氢氯噻嗪、硝苯地平治疗,血压可控。未观察到明显剂量、疗程相关性及年龄相关性,且所有患者均密切监测血压,处置合理及时,说明临床上已充分重视该类ADR。贝伐珠单抗注射液引起高血压的机制尚未完全明确,高血压的发生可能具有剂量依赖性。有研究报道,VEGF可促进前列环素(PGI2)及一氧化氮(NO)的产生,贝伐珠单抗注射液抑制VEGF的活性,导致PGI2和NO产生减少。PGI2和NO是血管舒张剂,有稳定血压的作用,其减少会引发高血压[7]。另有报道称,贝伐珠单抗注射液可引起微循环的异常改变,导致高血压[8]。临床用药期间应密切监测,若患者发生2级以上的高血压,应暂停贝伐珠单抗注射液并给予降压治疗,直至血压(舒张压/收缩压)恢复至治疗前水平或<150/100 mm Hg(1 mm Hg=0.133 kPa)[9];对于贝伐珠单抗注射液致高血压的患者,临床上采取常规方法降压治疗即可,若治疗1个月后降压效果不佳,或发生高血压危象,须永久停用贝伐珠单抗注射液[10]。
3.1.2 出血:贝伐珠单抗注射液导致的出血主要有2类。一类为皮肤黏膜出血,常见的有1级鼻黏膜出血以及牙龈、阴道出血等[11]。Ⅲ期临床研究(E4599研究)结果显示,使用贝伐珠单抗注射液联合铂类药物化疗的患者3级以上鼻出血发生率为0.7%[12]。另一类为肿瘤性出血,常见的有结直肠癌患者的胃肠道出血(直肠出血、黑便)和非小细胞肺癌患者的咯血、肺出血。针对晚期非小细胞肺癌患者的Ⅳ期临床研究(SAiL研究)结果显示,使用贝伐珠单抗注射液联合一线化疗药治疗的患者咯血、肺出血发生率为7.9%,其中3级以上出血的发生率为0.6%[13]。本研究中,共有6例患者在治疗过程中发生了出血,均为1、2级出血,皆为结直肠癌患者且皆有胃肠道出血,多数为便潜血阳性,不排除为肠道黏膜出血。其中,1例患者同时伴有口腔黏膜出血,但考虑治疗前即有口腔溃疡,可能与贝伐珠单抗注射液关系不大;另有1例患者鼻腔出血。贝伐珠单抗注射液致出血的机制同样与其抑制VEGF的活性有关,如导致内皮细胞功能紊乱或发生血小板功能障碍等,这都会使血管易出血且干扰正常止血功能[3]。贝伐珠单抗注射液不可用于既往有出血史的肿瘤患者,正在使用抗凝血药、抗炎药及凝血功能障碍的患者慎用,用药过程应密切检测血常规、凝血功能,如发生3、4级出血,须立即终止并永久停用贝伐珠单抗注射液。
3.1.3 蛋白尿:多数患者无症状表现,有文献报道,贝伐珠单抗注射液致蛋白尿的总发生率约为0.7%~38%,3级蛋白尿发生率<3%,4级蛋白尿发生率<1%[13]。本研究中,仅2例患者出现1级蛋白尿检测阳性,且均同时伴有高血压,提示有可能是患者体质较差、肾功能不全所致。贝伐珠单抗注射液致蛋白尿的机制可能为用药期间,肾小球脏层上皮细胞中VEGF活性降低致肾小球滤过膜通透性增加,从而产生蛋白尿。一般根据24 h尿蛋白定量检测结果,<2 g的患者定期检测即可,无需停药;>2 g的患者需暂停贝伐珠单抗注射液,下个疗程前复查24 h尿蛋白定量;出现4级蛋白尿的患者,即认为发生肾病综合征,须立即终止使用并永久停用贝伐珠单抗注射液。
3.1.4 胃肠道穿孔:胃肠道穿孔是使用贝伐珠单抗注射液患者少见的ADR,贝伐珠单抗注射液联合化疗治疗各类实体瘤时胃肠道穿孔的发生率为0.3%~11.4%[3]。本研究中未发现胃肠道穿孔现象,共有5例患者出现了腹部胀痛,已予以奥美拉唑抑酸护胃治疗;另有5例患者出现腹泻,5例患者便秘,均为较轻微的胃肠道毒性。但需要高度重视该类ADR,胃肠道穿孔一旦发生,后果严重,死亡率较高,其机制可能与贝伐珠单抗注射液对微循环的抑制有关,尤其是部分结直肠癌患者本身易发生器质性病变,贝伐珠单抗注射液抑制病变的恢复,进而导致胃肠道穿孔的发生,穿孔可发生于胃、小肠或结肠的任何一个部位。在贝伐珠单抗注射液治疗期间,应密切监测患者的胃肠道反应,高龄、腹腔炎症、有胃肠道梗阻或穿孔史的患者,须慎用[13]。
3.1.5 其他与贝伐珠单抗注射液相关的ADR:其他与贝伐珠单抗注射液相关的ADR包括血栓、伤口愈合困难及过敏等。(1)肿瘤患者易发生血栓,药品说明书中指出,贝伐珠单抗注射液治疗组患者的动脉血栓栓塞事件(arterial thromboembolic events,ATE)发生率为3.8%,相比较而言,化疗对照组患者的ATE发生率为1.7%;贝伐珠单抗注射液治疗组患者的静脉血栓栓塞事件(venous thromboembolic events,VTE)总发生率为2.8%~17.3%,化疗对照组的VTE总发生率为3.2%~15.6%,提示贝伐珠单抗注射液有增加血栓的风险。一项贝伐珠单抗注射液治疗非小细胞肺癌的研究结果显示,血栓发生率为11.3%[14]。本研究中,有4例患者发生了VTE,但其入院时皆已表现为深静脉血栓,无法判断是否与贝伐珠单抗注射液有关。(2)VEGF参与组织修复和伤口愈合,贝伐珠单抗注射液影响VEGF活性,导致伤口愈合困难(主要指伤口裂开或延迟愈合)。药品说明书中指出,使用贝伐珠单抗注射液联合化疗的结直肠癌患者,若疗程中进行了手术,其伤口愈合困难发生率显著高于对照组。一般需使用贝伐珠单抗注射液治疗的手术患者,应在伤口完全愈合后使用该药,若疗程中必须手术,应密切监测伤口愈合情况[15]。本研究中并未有患者出现伤口愈合困难。(3)贝伐珠单抗注射液存在潜在免疫原性,引起输注过敏反应发生率<3%[4]。药品说明书提醒,应注意贝伐珠单抗注射液输注时间的把握,发生过敏应立即停止输注。本研究中,疑似7例患者发生了过敏反应,均为1—2级,表现为输注中或结束后发热,部分伴有寒颤,予以异丙嗪及地塞米松治疗后好转,过敏发生率略高。
3.2 药品说明书中提及的其他ADR
其他ADR如胃肠反应(恶心、呕吐)、外周感觉神经病变、血液和淋巴系统毒性、嗜睡及乏力等,部分可能与贝伐珠单抗注射液相关,但多数属于化疗药常见的或共有的ADR[16]。本研究中未发现呼吸系统紊乱、充血性心力衰竭以及可逆性后部白质脑病综合征等ADR。
4 结论
综上分析,如处理得当,绝大部分贝伐珠单抗注射液所致ADR是可逆、可控的,严重程度多为1—2级,且与常规化疗药的ADR重合度较低,联合用药较为安全。虽与某些化疗药比较,贝伐珠单抗注射液致高血压、出血、蛋白尿、血栓和过敏的发生率更高,但权衡利弊后认为,对于多数患者而言,使用贝伐珠单抗注射液的益处大于风险。
本研究中发现的不足是部分医师对于出血和蛋白尿的重视程度不够,便(尿)常规检查数据有部分缺失。提示临床医师应熟知和重视贝伐珠单抗注射液常见的ADR,充分了解不同患者的病史及健康状况,提倡个体化用药,有效规避及监测ADR,预防可能会带来严重后果的ADR[17-18]。临床药师应发挥自身作用,积极深入临床一线,配合医师查错补漏,并进行有效监管,提高贝伐珠单抗注射液的合理应用水平,做好患者的用药教育及心理护理,使患者获益[19]。

