拟除虫菊酯类农药在NCI源和EI源中的质谱行为
连增维,倪建成,龚小丽,朱宏斌,胡银凤
(1.漳州市农业检验监测中心,福建 漳州 363000;2.吉克检测技术 (福建) 有限公司,福建 漳州 363005; 3.宁德师范学院生命科学学院,福建 宁德 352100)
拟除虫菊酯类农药(pyrethroid pesticides, PyPs)是以天然除虫菊素化学结构为模板,人工合成的一系列具有高效、低毒、广谱等优点的农药[1-2]。自烯丙菊酯上市以来,截至2020年7月1日,在我国登记上市的含有拟除虫菊酯类农药成分的产品共有5 340种,已广泛用于农业和卫生害虫防治[3]。有研究表明,PyPs具有神经毒性、生殖毒性、免疫毒性[4-6],大范围、大规模地使用PyPs,使得人类接触风险越来越高。对PyPs的检测主要以气相色谱分离为基础,采用电子捕获检测器(ECD)或质量分析器(MSD)检测。如贝峰等[7]采用气相色谱-负化学源质谱法(GC-NCI/MS)测定牛肉中10种PyPs,定量限为0.1~2 μg/kg;沈伟健等[8]采用气相色谱-负化学源质谱法测定蔬菜中17种PyPs,其定量限为0.02~5 μg/kg。这些研究的定量限均达到0.01 mg/kg以下,符合GB 2763—2019的限量要求[9]。然而以液相色谱分离为基础,采用MSD或其他检测器的灵敏度较低,因此很少应用于实际检测中[10-12]。
有机物分子在负化学源中裂解机理的研究兴起于20世纪70年代后期,一般认为其质谱裂解规律是由于捕获的热电子能量不同,发生了不同程度的化学反应:1) 有机物分子捕获1个热电子形成分子离子,即M+e-→M-;2) 捕获的热电子能量超过分子内少部分化学键的解离能,发生分子内化学键的断裂,并生成中性分子,即M+e-→(M-X)-+X;3) 捕获的热电子能量很高,大多数化学键发生断裂,无分子离子生成[13]。有机磷农药在NCI源中易形成磷酸酯基负离子[(RO)2P(=O)O]-或[(RO)2P(=S)S]-(其中R=CH3或C2H5),如敌敌畏形成的碎片离子[(CH3O)2P(=O)O]-(m/z125)、甲拌磷形成的碎片离子[(RO)2P(=S)S]-(m/z185);若含有邻对位取代的苯基硫代磷酸酯,则会发生重排反应,生成(R—C6H4—S)-,如对硫磷的分子结构(C2H5)2P(=S)O—C6H4NO2,形成基峰碎片离子(O2N—C6H4)-(m/z122);硫丹、六六六等氯代烷烃类农药因C-Cl极易断裂,分子离子峰较弱,易形成Cl-(m/z35)和(HCl2)-(m/z71);而对于滴滴涕等芳香有机氯农药,其分子离子峰比氯代烷烃类更强[14]。除虫菊酯类农药易在酯基处发生断裂,形成带环丙烷结构的羧酸碎片离子,易形成碎片离子[M—HCl]- [8]。醚类除草剂大部分易形成分子离子,碎片离子峰通常是由醚键左右两侧发生断裂形成,但含有硝基苯类除草剂不易产生分子离子峰,如三氟硝草醚和喹氧灵[15]。其他农药(如三唑酮、己唑醇、氟虫腈等)在NCI源上有响应,主要是因为其结构上含有卤代苯环[16]。
Raina等[17]对比了大气样品中二硝基苯胺类除草剂(氟乐灵等3种)、有机磷农药(毒死蜱等20种)和有机氯农药(六六六、滴滴涕等27种)在负化学源-单离子检测扫描(NCI-SIM)、负化学源-选择反应监测扫描(NCI-SRM)、电子轰击源-单离子检测扫描(EI-SIM)和电子轰击源-选择反应监测扫描(EI-SRM)模式下的灵敏度,认为NCI-SIM的检测限最低(2.5~10 μg/L),且大部分小于NCI-SRM,但NCI-SRM适用于这些农药的定性分析。对于大多数农药,EI-SRM的检测限低于100 μg/L时不适用,EI-SIM比NCI-SIM更易受到干扰,但对于NCI模式下响应小的农药,其在EI-SIM模式下的检测限也能达到1~10 μg/L,故没有一种方法能够在检测多种农药的同时还能获得最低的检测限。Húsková等[18]比较了23种农药(如溴氰菊酯、联苯菊酯)在NCI-SIM和EI-SIM的灵敏度,发现在同等检测浓度下,NCI-SIM的检测限低于EI-SIM。
李娇等[19-20]对PyPs在EI源中的质谱裂解规律做了系统性分类和研究,但未见PyPs在NCI源中质谱裂解规律的报道。为此,本工作拟利用现有的仪器设备对19种PyPs在NCI源上得到的全扫描质谱图和二级裂解扫描质谱图进行归纳整理,希望为PyPs农药残留日常检测时监测离子的选择提供依据,为假阳性的确证提供方法参考。
1 实验部分
1.1 仪器与设备
TQ8040三重四极杆气相色谱-质谱联用仪:日本岛津公司产品,配有EI源和NCI源。
1.2 标准品和试剂
19种拟除虫菊酯类农药标准品:德国Dr. Ehrensorfer公司产品;正己烷:色谱纯,德国Meker公司产品。
1.3 实验条件
1.3.1色谱条件 SH-RxiTM-5ms石英毛细管柱(30 m×0.25 mm×0.25 μm);进样口温度260 ℃;进样模式:不分流;进样量1 μL;载气:氦气;柱流量1.2 mL/min;升温程序:200 ℃保持2 min,以20 ℃/min升至300 ℃,保持5 min;传输线温度280 ℃。
1.3.2质谱条件 EI模式:离子源温度230 ℃,四极杆温度150 ℃,Q1为离子全通过模式,Q3为离子全扫描模式。
NCI模式1:离子源温度150 ℃,四极杆温度150 ℃,Q1为离子全通过模式,Q3为离子全扫描模式,反应气为甲烷。
NCI模式2:离子源温度150 ℃,四极杆温度150 ℃,Q1为离子选择模式,Q3为全扫描模式,反应气为甲烷,碰撞气为氩气,碰撞电压(CE)15 V。
1.4 实验方法
称取适量的农药标准品,用正己烷配制成1.0 mg/L或10.0 mg/L的上机测试液。上机测试条件参照1.3节。
2 结果与讨论
2.1 通用参数的选择
PyPs属于弱极性农药,能够溶解于正己烷中,按“相似相溶”原理,可以选择固定相为100%聚甲基硅氧烷或95%聚甲基-5%聚苯基硅氧烷的弱极性毛细管色谱柱,依现有实验条件,最终选择SH-RxiTM-5ms色谱柱。
进样口温度:进样口温度太低不利于相对分子质量数较高的有机物汽化,进样口温度太高不利于热不稳定农药的测定。由于PyPs的相对分子质量数均大于300且热稳定性良好,考虑到高温会缩短隔垫寿命,加快色谱柱前端的柱流失,最终选择进样口温度260 ℃。在EI-SIM模式下,以溴氰菊酯的碎片离子m/z181为定量离子,进样量1 μL,浓度1.0 mg/L,进样品温度260 ℃时的峰面积是200 ℃时的1.5倍。
升温程序:为了节约时间,并使PyPs在6~10 min内出峰,经测试,最终确定的色谱条件如1.3.1节。
传输线温度:直接采用岛津公司推荐的默认参数280 ℃。
2.2 EI模式下的参数选择
直接采用岛津仪器使用说明书推荐的默认参数,离子源温度230 ℃,四极杆温度150 ℃,电子能量70 eV,发射电流35 μA。
EI-SCAN模式:设置Q1为全通过模式,Q3为SCAN模式。此种模式相比于Q1为SCAN模式,Q3为全通过模式的灵敏度更优。
EI-SIM-SCAN模式:设置Q1为选择离子模式,Q3为SCAN模式,打开碰撞气,碰撞电压20 V。
EI-SIM(单离子选择)模式:设置Q1为全通过模式,Q3为选择离子模式。
EI-SRM(多离子选择)模式:设置Q1为选择母离子模式,Q3为选择子离子模式。母离子、子离子和碰撞电压直接采用厂家提供的优化参数。
2.3 NCI模式下的参数选择
离子源温度:设置Q1为全通过模式,Q3为SCAN模式,同时分别设置NCI模式下的离子源温度为120、150、180、210、240 ℃。联苯菊酯随着温度的升高,其m/z386的丰度越来越低,而m/z241、205的丰度越来越高,可见低温条件的离子源有利于分子离子峰的稳定存在,但120 ℃离子源温度低于四极杆的工作温度,显然是不合适的,故选择离子源温度为150 ℃。
反应气的设置:反应气的流路没有配置流量控制器,只能通过减压阀调节,厂家推荐的压强是0.1~0.4 MPa。反应气压强过低,不利于热电子的形成;反应气压强过高,背景噪音太大。经调试,最终确定PyPs的甲烷气压强为0.2 MPa。
碰撞电压:为了明确负离子模式下分子离子峰可以产生的碎片离子,故设定碰撞电压均为15 V,碰撞气为氩气。
NCI-SCAN、NCI-SIM-SCAN、NCI-SIM和NCI-SRM模式Q1和Q3的设置与EI源一致。
2.4 联苯菊酯在不同采集模式下的质谱图
在NCI-SCAN模式下,联苯菊酯的全扫描质谱图示于图1a。在NCI-SIM-SCAN模式下,不同母离子在碰撞池与氩气发生碰撞后,形成的碎片离子峰示于图1b~1d。可以看出,在碰撞电压15 V条件下,所得的碎片离子是有差异的。m/z205在氩气的碰撞下,通过不断脱去中性分子HF,得到碎片离子m/z121、141、161(图b);m/z241在氩气的碰撞下,通过脱去中性分子HCl,形成碎片离子m/z205,后脱去HF得到m/z185、165,脱去HCF3得到m/z135(图c);m/z386在氩气的碰撞下,形成4个主要碎片离子是m/z205、185、161、141(图d)。
2.5 不同拟除虫菊酯类农药在NCI源中的质谱裂解过程
2.5.1含有环丙烷酸结构的PyPs 联苯菊酯(bifenthrin)得到1个热电子,形成分子离子m/z422,其不稳定、易裂解,裂解途径示于图2。裂解途径1:分子离子发生热裂解,先脱去1个中性分子HCl,形成碎片离子C23H21F3O2-(m/z386),然后与酯基相连的C—O键发生α-断裂,形成带环丙羧酸根结构的碎片离子C9H8F3O2-(m/z205),之后脱去不同的中性分子(HCF3、CO2、HF)形成不同的碎片离子;裂解途径2:在与酯基相连的C—O键发生α-断裂,形成带环丙羧酸根的碎片离子C9H9ClF3O2-(m/z241),然后脱去1个中性分子HCl,形成碎片离子m/z205,之后同裂解途径1。
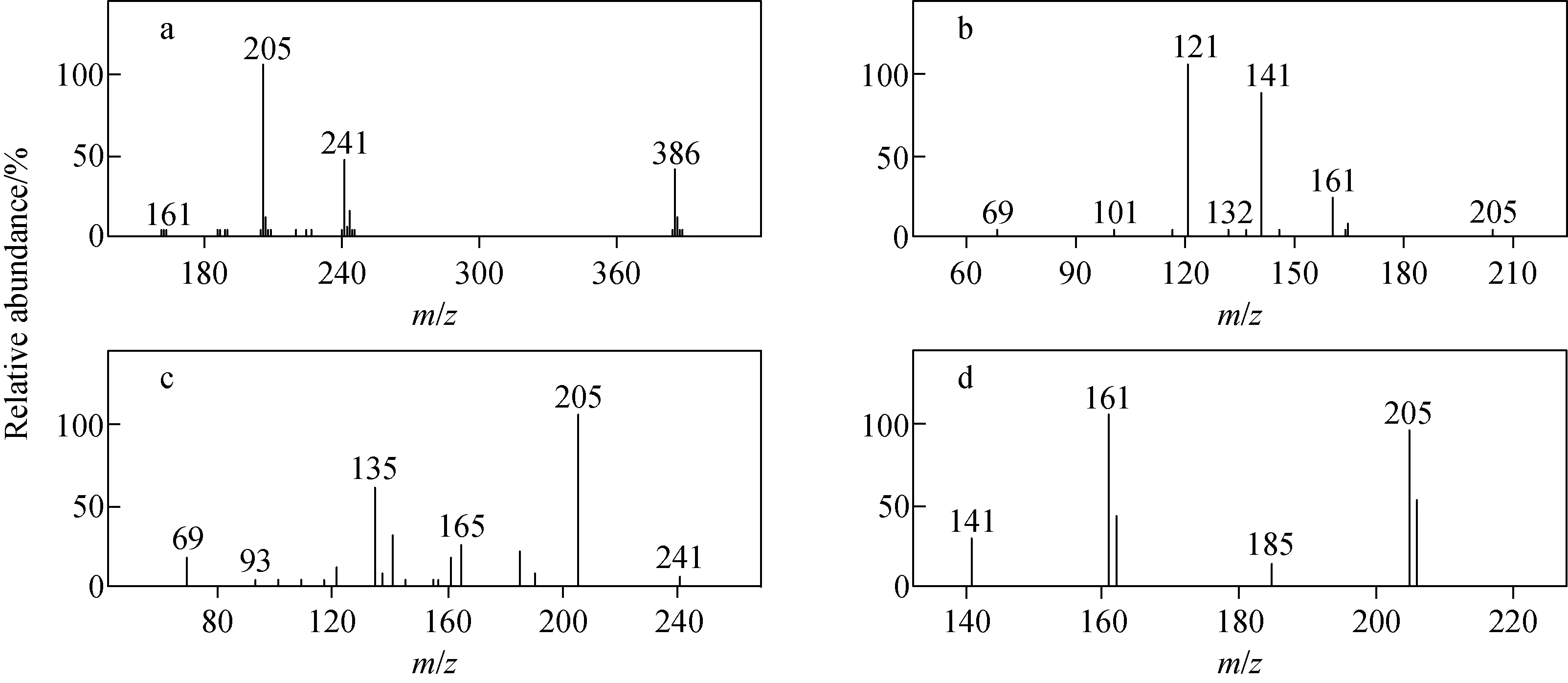
图1 NCI-SCAN模式(a)和母离子m/z 205(b)、241(c)、386(d)的NCI-SIM-SCAN模式下,联苯菊酯的质谱图Fig.1 Mass spectra of bifenthrin in NCI-SCAN mode (a) and NCI-SIM-SCAN mode for precursor ion m/z 205 (b), 241 (c), 386 (d)
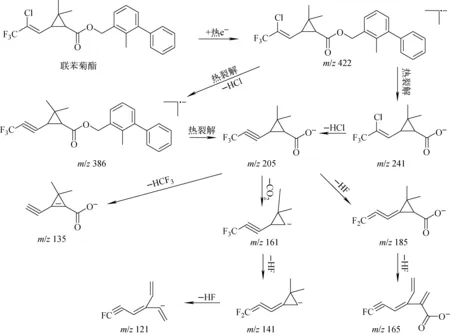
图2 联苯菊酯在NCI源中主要碎片离子可能的裂解过程Fig.2 Possible fragment pathways of the main ion fragments of bifenthrin in NCI source

图3 氯氰菊酯在NCI源中主要碎片离子可能的裂解过程Fig.3 Possible fragment pathways of the main ion fragments of cypermethrin in NCI source
氯氰菊酯(cypermethrin)得到1个热电子发生热裂解,形成C8H9Cl2O2-(m/z207);脱去1个中性分子HCl,得到C8H8ClO2-(m/z171),脱去1分子CO2,得到C7H8Cl-(m/z127);或者先脱去1分子CO2,得到C7H9Cl2-(m/z163),再脱去1分子HCl,得到C7H8Cl-(m/z127),其裂解途径示于图3。
2.5.2不含环丙烷结构的PyPs 氟氰戊菊酯(flucythrinate)得到1个热电子产生热裂解,形成C12H13F2O3-(m/z243),脱去1分子CO2得到C11H13F2O-(m/z199),脱去CH4得C10H9F2O-(m/z183),其裂解途径示于图4。
氟胺氰菊酯(fluvalinate)得到1个热电子发生热裂解,形成C12H12ClF3NO2-(m/z294),脱去1分子CO2得到C11H12ClF3N-(m/z250),脱去1分子HCl得到C11H11F3N-(m/z214),脱去1分子HF得到C11H10F2N-(m/z194),脱去1个自由基CH3·得到C10H7F2N-(m/z179),其裂解途径示于图5。

图4 氟氰戊菊酯在NCI源中主要碎片离子可能的裂解过程Fig.4 Possible fragment pathways of the main ion fragments of flucythrinate in NCI source

图5 氟胺氰菊酯在NCI源中主要碎片离子可能的裂解过程Fig.5 Possible fragment pathways of the main ion fragments of fluvalinate in NCI source
2.5.3不含卤原子的PyPs 不含卤原子的PyPs在NCI源中很难捕获1个热电子而发生热裂解,所以这些农药(如醚菊酯、氟硅菊酯)在进样量1.0 μL,浓度10 mg/L的气相色谱-质谱条件下,其质谱图上不能获得可辨认的碎片离子峰。在相同条件下,烯丙菊酯和苄呋菊酯的质谱图上能够获得可辨认的碎片离子峰,但峰强度不高,其能够有响应的主要原因是含有共轭结构。
2.6 不同拟除虫菊酯类农药在EI源中的质谱裂解过程

氯氰菊酯在EI源中失去1个电子,形成分子离子C22H19Cl2NO3·+(m/z415)。裂解途径1:分子内重排,形成碎片离子C8H9Cl2O2+(m/z207);裂解途径2:与环丙烷上相邻的甲基上的氢迁移至与羰基相连的氧上,形成羟基,同时在氰基的吸电子作用下发生断裂,生成分子C14H11NO(m/z209),失去1个电子,得到C14H11NO·+(m/z209),脱去1个苯酚,得到C8H5N·+(m/z115),或脱去C8H6N·(m/z116),得到C6H5O+(m/z93);裂解途径3:羰基上氧的电荷诱导,发生裂解得到C14H10NO+(m/z208),再脱去1个HCN,得到C13H9O+(m/z181),裂解途径示于图7。
2.6.2不含环丙烷结构的PyPs 氟氰戊菊酯在EI源中失去1个电子,形成分子离子C26H23F2NO4·+(m/z451)。裂解途径1:分子内重排得到分子C14H11NO2(m/z225),失去1个电子再脱去1个羟基,得到C14H10NO+(m/z208),脱去1个HCN得到C13H9O+(m/z181);裂解途径2:羰基上氧的诱导,酯基发生α裂解,得到C12H13F2O2+(m/z227),脱去1个CO得到C11H13F2O+(m/z199),脱去1个CH3·得到C10H10F2O·+(m/z184),脱去1个C2H3·得到C8H7F2O·+(m/z157),裂解途径示于图8。

图6 联苯菊酯在EI源上主要碎片离子可能的裂解过程Fig.6 Possible fragment pathways of the main ion fragments of bifenthrin in EI source
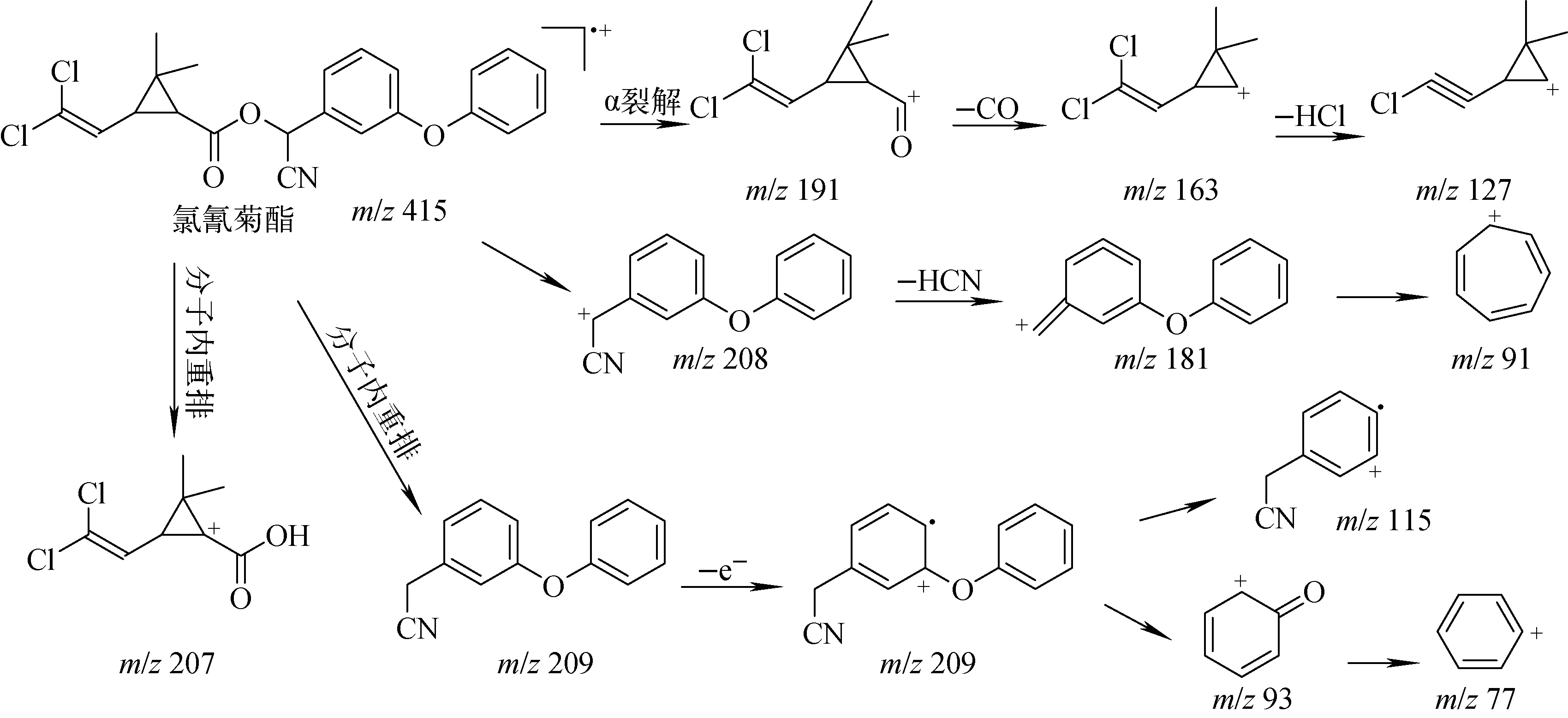
图7 氯氰菊酯在EI源上主要碎片离子可能的裂解过程Fig.7 Possible fragment pathways of the main ion fragments of cypermethrin in EI source

图8 氟氰戊菊酯在EI源上主要碎片离子可能的裂解过程Fig.8 Possible fragment pathways of the main ion fragments of flucythrinate in EI source
氟胺氰菊酯在EI源中失去1个电子,形成分子离子C26H22ClF3N2O3·+(m/z502)。裂解途径1:分子内重排形成分子C14H11NO2(m/z225),脱去1个羟基,得到C14H10NO+(m/z208),脱去1个HCN得到C13H9O+(m/z181);裂解途径2:羰基上氧的诱导,酯基发生α裂解,得到C12H12ClF3NO+(m/z278),脱去1个CO,得到C11H12ClF3N+(m/z250),脱去1个CH4,得到C10H8ClF3N+(m/z234),裂解途径示于图9。
2.6.3不含卤原子的PyPs 烯丙菊酯在EI源中失去1个电子,形成分子离子C19H26O3·+(m/z302)。裂解途径1:分子内重排形成分子C10H16O2,失去1个电子得到C10H16O2+(m/z168),脱去1个甲酸,得到C10H14+(m/z107);裂解途径2:羰基上氧的诱导,酯基发生α裂解,得到C10H15O+(m/z151),脱去1个CO,得到C9H15+(m/z123),裂解途径示于图10。

图9 氟胺氰菊酯在EI源上主要碎片离子可能的裂解过程Fig.9 Possible fragment pathways of the main ion fragments of fluvalinate in EI source

图10 烯丙菊酯在EI源上主要碎片离子可能的裂解过程Fig.10 Possible fragment pathways of the main ion fragments of S-bioallethrin in EI source
苄呋菊酯在EI源中失去1个电子,得分子离子C22H26O3·+(m/z338)。裂解途径1:羰基上氧的诱导,酯基发生α裂解,得到C10H15O+(m/z151),脱去1个CO得到C9H15+(m/z123);裂解途径2:σ键发生电离得到C12H11O+(m/z171),脱去1个CO得到C11H11+(m/z143),脱去1个CH3·得到C10H8·+(m/z128),裂解途径示于图11。
2.7 拟除虫菊酯类农药在NCI源和EI源中碎片离子的比较
PyPs在NCI源中易发生热裂解,主要是与酯基相连的碳氧键断裂形成带负电的羧酸根离子(图12 Path 1)。在含有环丙烷的结构中,与环丙烷相连的官能团电负性越强,其离子强度越强,且易失去1个卤化氢形成次级离子,如联苯菊酯、氯氰菊酯;不含环丙烷结构的PyPs则易失去1个CO2,形成次级离子,如氟氰戊菊酯、氟胺氰菊酯。各菊酯类农药的典型碎片离子列于表1,以这些碎片离子为母离子,脱去中性分子,如HBr、HCl、HF、CO2、HCF3等(图12 Path 2),从而形成各种不同的次级碎片离子,PyPs在NCI源中常见的碎片离子结构示于图12。
在EI源模式下,PyPs的酯基或苄基位易发生断裂。在酯基位发生断裂时,有些PyPs会产生羧酸酯类常见的碎片离子RCO+,如苄呋菊酯、联苯菊酯,但是大部分PyPs在质谱图上只出现碎片离子R+,并未见到碎片离子RCO+,如氟氯氰菊酯、氟氰戊菊酯(图13 Path 3);含有苄基苯基醚类结构的PyPs当甲基位上有氰基取代时易形成特征碎片离子m/z181、208,如氯氰菊酯、氟氰戊菊酯、氟胺氰菊酯(图13 Path 1);当甲基位上无取代基时,形成特征离子m/z183,如氯菊酯、醚菊酯、苯醚菊酯(图13 Path 2)[20],常见的特征碎片离子结构示于图13。

图11 苄呋菊酯在EI源上主要碎片离子可能的裂解过程Fig.11 Possible fragment pathways of the main ion fragments of chrysron in EI source

图12 NCI源模式下不同菊酯类农药产生的主要碎片离子及其裂解通式Fig.12 Main ion fragments produced by different pyrethroids and its general formula in NCI source
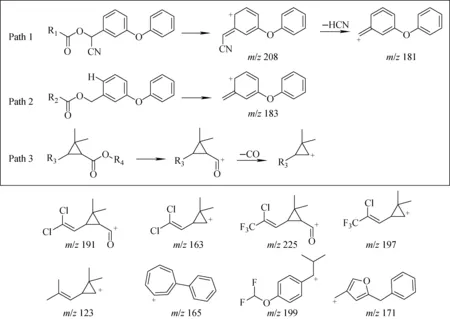
图13 EI源模式下,拟除虫菊酯类农药产生的主要碎片离子及其裂解通式Fig.13 Main ion fragments produced by different pyrethroids and its general formula in EI source

表1 拟除虫菊酯类农药在不同离子源中的主要碎片离子Table 1 Main ion fragments of pyrethroid pesticides in different ion sources
3 结论
本文系统性地对比了19种拟除虫菊酯类农药在NCI源和EI源中碎片离子的差异,给出了PyPs在不同离子源中形成的常见碎片离子,明确了裂解规律,为采用NCI源测定PyPs时的离子选择提供了理论依据。

