阿西美辛治疗强直性脊柱炎在真实世界研究中的疗效和安全性评价
张家鑫,胡立冬,冀肖健,王一雯,宋 川,朱 剑,黄 烽
1 解放军医学院,北京 100853;2 解放军总医院第一医学中心 风湿免疫科,北京 100853
强直性脊柱炎(ankylosing spondylitis,AS)是一种慢性自身炎症性疾病,主要累及骶髂关节、脊柱、椎旁组织等中轴结构[1-2]。AS 的患病率各国报道不一,西方国家AS 患病率为0.1%~0.5%[3],我国AS 患病率为0.3%[4]。AS 可导致脊柱关节活动受限甚至残疾,严重影响患者心理健康和生活质量。非甾体抗炎药(non-steroidal anti-inflammatory drugs,NSAIDs),在短期内即可有效缓解AS 患者腰背部疼痛和晨僵等症状,改善关节活动,是治疗AS 的一线用药[5]。有研究表明NSAIDs 可减缓AS 新骨形成,可能改善AS 患者的远期预后[6]。2016 年欧洲抗风湿病联盟在AS 管理推荐意见中明确指出:NSAIDs 是治疗有症状的AS 患者的首选药,病情持续活动的患者需要持续使用NSAIDs 治疗[5]。目前NSAIDs 种类繁多,其中哪一种更有效,证据相对不足,故有必要进一步探索不同NSAIDs 之间的疗效的差异。阿西美辛于1980 年上市,是目前广泛应用于治疗风湿病的乙酸类NSAIDs。但美国Thomson Healthcare MICROMEDEX 数据库无阿西美辛治疗AS 的相关评价[7]。本研究旨在评价在真实世界中阿西美辛治疗AS 的有效性及安全性。
对象与方法
1 研究对象 基于中国强直性脊柱炎前瞻性影像队列,通过SpA 智能移动管理系统(smart-phone spondyloarthritis management system,SpAMS)收集2016 年6 月-2019 年9 月就诊于解放军总医院风湿科门诊的AS 患者[8]。纳入标准:1)符合1984年修订的纽约AS 分类诊断标准;2)能理解并独立应用手机填写资料的患者;3)正在规律使用NSAIDs 药物治疗。 排除标准:拒绝通过电子化收录信息或不能独立应用手机填写资料的患者。本研究通过解放军总医院伦理委员会审查(批文号:S2016-049-02),所有受试者均签署知情同意书。
2 分组及治疗 根据风湿科医生医嘱及患者应用NSAIDs 种类不同,分为阿西美辛组(石药集团欧意药业,批号:H19990358)和其他NSAIDs 组,阿西美辛组的患者口服阿西美辛治疗(90 mg/d,90 mg/粒),其他NSAIDs 包括塞来昔布(200 mg/d,200 mg/粒)、美洛昔康(15 mg/d,7.5 mg/片)、洛索洛芬钠(60 mg/d,60 mg/片)、布洛芬(100 mg/6 h,100 mg/片)、双氯芬酸(75 mg/d,75 mg/粒)。两组患者均在风湿免疫专科医师指导下调整药物剂量。
3 疗效评估 在基线期、3 个月和6 个月时观察两组患者以下指标:1)患者整体评分(patient general assessment,PGA)、总体背痛、夜间背痛、C 反应蛋白(C reactive protein,CRP)、Bath AS 功能指数(Bath ankylosing spondylitis functional index,BASFI)、AS疾病活动评分(ankylosing spondylitis disease activity score,ASDAS)。2)疗效评估:①以ASDAS 作为主要疗效指标,统计阿西美辛组各疾病活动度百分比。ASDAS<1.3 为疾病缓解(inactive disease,ID),1.3≤ASDAS<2.1为疾病低度活动(low disease activity,LDA),2.1≤ASDAS<3.5 为疾病高度活动(high disease activity,HDA),ASDAS>3.5 为疾病极高度活动(very high disease activity,VHDA)。②次要疗效指标包括PGA、总体背痛、夜间背痛、BASFI 和CRP。③药物安全性评估,确定和记录每次随访中的不良反应。
4 统计学方法 采用SPSS21.0 软件进行统计学分析。正态分布且方差齐性资料的计量资料以±s表示。非正态、方差不齐的资料以Md(IQR)表示,组内比较采用t检验,组间比较采用广义加性混合模型。分类变量以例数和百分比表示,组间比较采用χ2检验或Fisher 确切概率法。P<0.05为差异有统计学意义。
结果
1 纳入患者临床资料 本研究共纳入1115 例AS 患者,其中阿西美辛组992 例,其他NSAID组123 例。两组基线期的PGA、总体背痛、夜间背痛、BASFI、CRP、ASDAS 等差异无统计学意义,在阿西美辛组患者男性占比(84.1%)高于其他NSAIDs 组(63.4%)。见表1。

表1 两组AS 患者基线的临床资料比较Tab.1 Comparison of baseline data between the two groups
2 疗效比较 阿西美辛组治疗后第3 个月、第6 个月ASDAS 整体呈下降趋势(P均<0.001),见图1。并且处于ID 和ID+LDA 患者的百分比逐步升高(P均<0.001),见图2。除CRP 外,其他次要疗效指标PGA、总体背痛、夜间背痛、BASFI在观察期间整体呈下降趋势(P均<0.001),见图3。其他NSAIDs 组治疗后第3 个月与治疗前各项指标差异无统计学意义(P>0.05),治疗后第6 个月BASFI 改善明显(P=0.045),其他指标差异无统计学意义(P>0.05),见图4。ASDAS 在基线期和治疗第3 个月时两组差异无统计学意义(P>0.05),但在第6 个月,阿西美辛组ASDAS 水平显著低于其他NSAIDs 组(P=0.007)。次要疗效指标基线期时两组差异无统计学意义(P>0.05)。在第3 个月时阿西美辛组总体背痛和BASFI 改善较其他NSAIDs组更明显(P<0.05)。治疗第6 个月时阿西美辛组的PGA、总体背痛、夜间背痛、BASFI、CRP 的水平较其他NSAIDs 组更低(P均<0.05),见表2。

表2 两组疗效指标比较Tab.2 Comparation of efficacy between the two groups
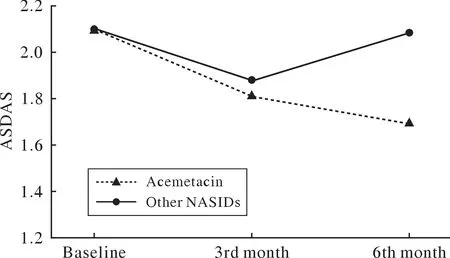
图1 两组ASDAS 随时间变化Fig.1 Changes of ASDAS over time in the two groups

图2 两组疾病活动度百分比随时间变化Fig.2 Changes of disease activity over time in the two groups
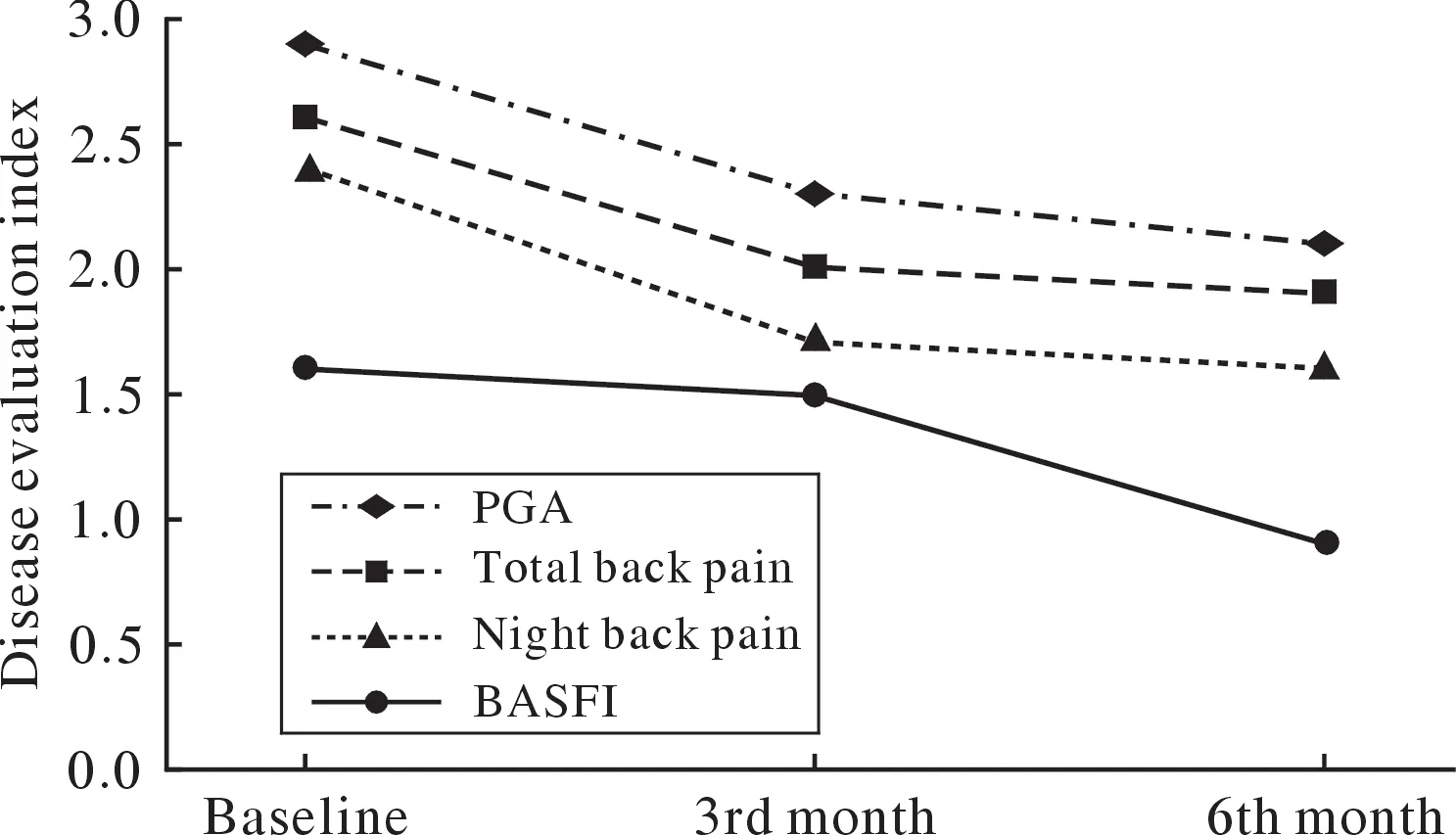
图3 阿西美辛组次要指标随时间变化Fig.3 Changes of the secondary indexes in the Acemetacin group over time

图4 其他NSAIDs 组次要指标随时间变化Fig.4 Changes of the secondary indexes of other NSAIDs group over time
3 两组应用其他药物情况 阿西美辛组14.7%的患者同时应用生物制剂治疗,其他NSAIDs 组26.6%的患者同时应用生物制剂,两组差异有统计学意义(P<0.001)。阿西美辛组47.8%的患者同时应用改善病情的抗风湿药(disease-modifying antirheumatic drugs,DMARDs),其他NSAIDs 组42.7%的患者同时应用DMARDs,但两组差异无统计学意义(P=0.352)。见表3。

表3 两组生物制剂、DMARDs 应用情况比较(n, %)Tab.3 Comparison of application of biological agents and DMARDs between the two groups (n, %)
4 两组不良反应发生率比较 在本研究观察期内,两组均仅观察到肝功能不全,阿西美辛组9 例(0.91%)出现肝功能异常;其他NSAIDs 组6 例(4.88%)出现肝功能异常。两组不良反应均表现为肝酶的轻度升高,未观察到严重不良反应。
讨论
AS 是一种以中轴结构受累为主的慢性自身炎症性疾病,通常中青年时发病,随着病情进展可导致患者骶髂关节强直、韧带骨赘形成和脊柱融合[9-10]。许多患者青年时期即出现关节畸形和功能受限,生存质量严重下降[11]。本研究观察AS 患者应用阿西美辛或其他NSAIDs 的疗效及安全性。
阿西美辛是一种乙酸类的非选择性NSAIDs,由德国Tropon 公司在20 世纪70 年代研制的吲哚美辛的前体药,该药口服后首先不显示药理作用,需经肝转化为吲哚美辛才显示其疗效[12]。阿西美辛主要作为一种缓激肽和环氧合酶抑制剂,可以通过抑制前列腺素合成、组胺释放、补体活性、透明质酸酶和蛋白水解酶释放,从而抑制炎症的多个过程[13]。它具有较强的抗炎、镇痛和退热作用。除AS 外,阿西美辛还广泛用于治疗类风湿关节炎、骨关节炎等其他风湿病[12]。
2016年欧洲抗风湿病联盟(EULAR)在AS 推荐指南支持达标治疗(T2T)在AS 患者中应用[5]。T2T 的实质是改善患者的生活质量,其目标设定是T2T 的关键[14]。一项瑞士的AS 患者脊柱影像学表明ASDAS 是预测脊柱影像学进展的危险因素[15]。而关节和脊柱结构损伤后致残是影响AS 患者生活质量的主要原因。所以ASDAS 被推荐为AS 患者T2T 的主要指标。故本研究以ASDAS 为主要疗效指标。在阿西美辛组组内比较中发现,与基线期相比,第 3个月时即可以观察到ASDAS 显著下降,且在阿西美辛治疗的6 个月期间,该指标得到持续改善。在达标率方面,阿西美辛组在基线期、第3 个月、第6个月ID 的百分比分别为22.8%、32.1%、39.0%。ID+LDA 的百分比分别为55.2%、67.3%、74.2%。尽管阿西美辛组有14.7%和47.8%的患者应用生物制剂和DMARDs,但阿西美辛作为该组患者的治疗基石,其帮助AS 患者达标的作用不可忽视,证明了阿西美辛的疗效。本研究达标率与其他相关研究相似。英国的DESIR 队列AS 患者的治疗5 年的ID 百分比为25%[16],而西班牙SPA-PAZ队列AS 患者治疗2 年的ID+LDA 百分比为80%[17]。差异的原因可能是由于随访时间和随访频率的不同。次要疗效指标,如PGA、总体背痛、夜间背痛和BASFI 也观察到类似的结果,进一步说明阿西美辛可改善AS 患者症状和其他相关临床指标。在阿西美辛组和其他NSAIDs 组的组间比较中发现,ASDAS 在第6 个月时,阿西美辛组的改善程度优于其他NSAIDs 组。次要疗效指标中总体背痛和BASFI在第3 个月时即观察到两组的差异性,阿西美辛组优于其他NSAIDs 组。本研究观察到阿西美辛的有效性与其他研究一致。德国一项多中心临床研究评估了阿西美辛治疗760 例不同种风湿病患者的疗效(其中AS 有243 例)[18]。其记录医生对治疗效果的评估,并将其作为疗效观察指标。包括“很有效、较有效、疗效中等和无效”4 个等级。该研究结果显示,55.3%的患者应用阿西美辛治疗后被医生评估为“很有效”,28.5%患者被评估为“较有效”,33.3%患者被评估为“疗效中等”。共97%的患者可从阿西美辛治疗中获益。此外英国一项为期1 年的阿西美辛治疗类风湿关节炎的研究表明,阿西美辛治疗的第1 个月,Ritchie 关节指数和晨僵明显改善(P均<0.0001)[19]。并在12 个月的治疗期间内,晨僵和患者疼痛视觉模拟评分持续改善。在第12 个月时患者左手和右手的握力也较基线期明显增加(P值分别为0.032 和0.043)。表明阿西美辛治疗可改善风湿病患者症状。本研究证实了我国AS 患者应用阿西美辛的疗效,但由于研究仅6 个月,而治疗AS 是一个长期的过程,故阿西美辛治疗AS 的长期疗效与不良反应需进一步验证。
本研究发现,阿西美辛具有良好的安全性。研究期间仅观察到肝功能不全。在服用阿西美辛的992 例患者中,有9 例患者出现肝功能异常,其他NSAIDs 组有6 例出现肝功能异常。均为未达到停药程度一过性的肝功能异常。未观察到其他不良反应。相比于NSAIDs 不良反应中更常见的胃肠道不良反应,医生容易忽视其导致的肝功能损伤。2017 年意大利一项研究表明,NSAIDs所致的药物性肝损伤约占所有药物的35.5%[20]。该研究显示NSAIDs 所致肝损伤57.8%为肝细胞型,18.3%为胆汁淤积型,23.2%为混合型。多数NSAIDs 致肝损害机制为特异体质反应,依赖个体易感性[21]。NSAIDs 经肝代谢,发挥作用同时导致的肝损害很难避免。但部分研究者认为NSAIDs 在用药过程中的肝功能指标异常多数为一过性的,患者停药后可恢复正常[22]。与本研究结果一致。
随着生物制剂时代的到来,治疗AS 可选择的方法越来越多,但NSAIDs 仍是AS 的治疗基石[23]。阿西美辛作为经典的NSAIDs,其疗效在本研究中得到证实。疼痛既是AS 的常见症状,也是NSAIDs 的适应证,常被用来评估NSAIDs 治疗AS 的疗效[23];BASFI 主要作为躯体功能指标,也常用来评估AS 的治疗效果[24]。本研究观察到以上指标的改善均具有临床意义,说明了阿西美辛治疗AS 的有效性。另外本研究应用SpAMS系统记录患者的临床数据,SpAMS 是SpA 患者移动医疗数据管理平台,数据的收集与记录过程严谨科学,减少了真实世界研究过程中的信息偏倚。
本研究中其他NSAIDs 组的样本含量较少,可能会产生偏倚。并且研究未排除同时应用生物制剂或其他药物治疗的患者。我们比较了两组同时应用其他药物治疗的情况,发现阿西美辛组DMARDs 应用率稍高,但差异无统计学意义。而阿西美辛组的生物制剂应用率低于其他NSAIDs组,但由于本研究未考虑社会经济学等因素,由此并不能说明阿西美辛优于其他NSAIDs。由于其他NSAIDs 组的患者数目较少,我们未进行具体的再分类,所以本研究并不能说明阿西美辛的疗效优于具体哪一种NSAIDs。本研究观察时间相对较短,治疗AS 需要长期的管理。但在本研究期间内,观察到有临床意义的统计学差异,表明阿西美辛起效较快,在短期内可改善患者临床症状。因为观察期间较短,本研究未把AS 患者的影像学变化纳入疗效指标。药物治疗和影像学进展的关系是近些年来AS 的研究热点之一。Wanders 等[25]研究发现,长期持续应用NSAIDs 相比按需使用NSAIDs 抑制影像学进展更有效。因此有研究认为NSAIDs 有潜在的DMARDs 作用[26]。时间更长的研究将有助于观察阿西美辛与其他NSAIDs 治疗AS 的不同和NSAIDs 治疗AS 的影像学变化。本研究患者的随访期间不固定,导致观察节点的数据脱漏,可能会导致偏倚。所以我们纳入了较多的患者,并运用广义估计方程的方法进行统计分析,减小数据缺失所导致的误差。
本文表明,阿西美辛能够改善AS 患者临床症状、躯体功能和客观的实验室炎性活动指标,可以提高患者的生活质量。在真实世界研究中,阿西美辛治疗AS 能够取得较好的疗效,安全性好。

