三种铝合金化铣槽液中硫化钠含量分析方法的对比
陈庆龙,余 辉
(1.中国航空工业集团公司金城南京机电液压工程研究中心,南京 211106;2.江西洪都航空工业集团有限责任公司,南昌 330024)
0 前言
化学铣切,简称化铣,也叫做化学加工、湿腐蚀等,是一种相当古老的非传统加工方法。化铣是将金属材料要加工的部位暴露在化学介质中进行腐蚀,不需加工的部位则保护起来,从而获得零件所需要的形状与尺寸[1]。化学铣切与一般的机械加工有着本质的区别,它是利用化学或电化学腐蚀原理加工工件,通过对化学溶液有效的控制,从工件上预先确定的部位、范围与深度上除去基体材料,获得所需的加工尺寸和尺寸精度[2-4]。化学铣切加工具有不产生机械切削应力、易加工复杂零件形状等优点,在航空制造业有很广泛的应用。化学铣切加工是对机械加工的补充和发展,弥补了机械加工所不及的范围,值得在实践上广泛应用[5]。
铝合金化学铣切是现代航空材料加工方法中一种必不可少的加工方法,对成型零件的加工可靠又有效,以其加工无应力的特点,应用越来越广,在铝合金零部件加工中占比很高[6]。我国从20世纪80年代中期开始吸收国外铝合金的先进化学铣切技术,并陆续出现了一些关于铝合金化学铣切工艺研究的报道[7-10]。在铝合金化铣中,硫化钠是必不可少的,它的加入主要是提高表面粗糙度。但硫化钠稳定性差,在空气中易氧化,所以在化铣过程中,硫化钠需不断补加。因此,必须定时分析和补加硫化钠,以便及时精准地指导Na2S的添加,确保化铣槽中硫化钠含量在有效范围内,既能节约药品的使用量,又能最大限度地控制化铣粗糙度。
铝合金化铣中硫化钠的分析较复杂,存在杂质离子的干扰。目前使用比较普遍的硫化钠测量方法主要有碘量法、重铬酸钾和沉淀法。本文就这3种分析方法对铝合金化铣槽液中Na2S含量的分析精度进行了对比,以便更好地指导化铣操作。
1 分析试剂
本研究所采用的分析试剂主要包括:硫代硫酸钠标准溶液0.1 moL/L;碘标准溶液0.1 moL/L;盐酸溶液1+1;淀粉指示剂0.5%;重铬酸钾标准滴定溶液c(1/6K2Cr2O7)=0.1 mol/L;碘化钾溶液100 g/L;硫代硫酸钠标准滴定溶液0.1 mol/L(HB/Z 5083-2001 6.5);淀粉指示剂5 g/L;氯化钡10%;硝酸36%~38%;盐酸65%~68%。
2 分析方法
2.1 碘量法
原理:在弱酸性介质中,加过量碘与二价硫离子反应,剩余的碘,以淀粉为指示剂,用硫代硫酸钠标准滴定溶液滴定。
分析步骤:移取离心后的试液10 mL于100 mL容量瓶中,加水稀释至刻度,摇匀。移取碘标准溶液15.0 mL于100 mL烧杯中,在搅拌状态下加入盐酸5 mL,然后移取稀释后的试液10.00 mL,在搅拌状态下逐滴加入烧杯中,放置15 min后加入2 mL淀粉指示剂,用硫代硫酸钠标准溶液滴定至碘的颜色消失为终点,记下体积(V)。
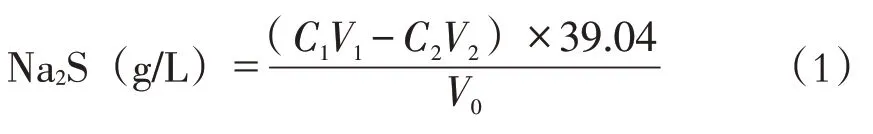
式中:C1为碘标准溶液的浓度,mol/L;V1为移取碘标准溶液的体积,mL;C2为硫代硫酸钠标准溶液的浓度,mol/L;V2为滴定时消耗硫代硫酸钠标准溶液的体积,mL;V0为滴定时移取槽液的体积,mL。
2.2 重铬酸钾法
原理:在弱酸性介质中,加过量的碘化钾与重铬酸钾反应生成碘,过量的碘将二价硫离子氧化成硫析出,剩余的碘,以淀粉为指示剂,用硫代硫酸钠标准滴定溶液滴定。
分析步骤:移取过滤后的试液10 mL于100 mL容量瓶中,以水稀释至刻度,摇匀;分取10.00 mL稀释后的试液于250 mL容量瓶中,加25 mL水,准确加入20.00 mL重铬酸钾标准滴定溶液、20 mL碘化钾溶液和20 mL盐酸溶液,放置暗处5~10 min。用硫代硫酸钠标准滴定溶液滴定,轻轻摇动至接近终点时,加2 mL淀粉指示剂,继续滴定至蓝色消失为终点。
按下列公式计算硫化钠的含量Wa:
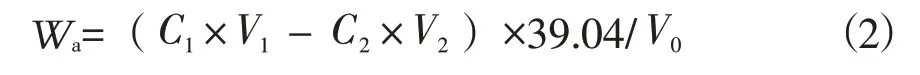
式中:C1为重铬酸钾标准滴定溶液浓度的标准数值,mol/L;C2为硫代硫酸钠标准滴定溶液浓度的准确数值,mol/L;V1为耗用重铬酸钾标准滴定溶液的体积的数值,mL;V2为滴定终点时耗用硫代硫酸钠标准滴定液的体积数,mL;V0为滴定时试验溶液的体积的数值,mL。
2.3 沉淀法
原理:用硝酸将槽液中的S2-转化成SO42-,用氯化钡沉淀SO42-,再称量硫酸钡的质量。
分析步骤:
(1)取样处理:移取20 mL HCl于250 mL锥形瓶中,再移取5 mL HNO3于锥形瓶中并摇匀,移取10 mL澄清试液缓慢滴入锥形瓶中并不断摇匀。
(2)煮沸:为保证S2-全部转化成SO42-,将溶液加热煮沸2~3 min。
(3)沉淀:待锥形瓶中溶液冷却至室温时,用定性分析滤纸过滤,过滤完后并冲洗滤纸5~6次,加热溶液至沸腾,滴加10%BaCl2溶液30 mL,煮沸4~5 min。
(4)过滤:待溶液冷却至室温时,采用双层定量分析滤纸过滤,过滤前滤纸经过干燥(80℃,4~5 h),过滤完后应冲洗滤纸8~10次。
(5)烘干沉淀:将滤纸放置于80℃烘箱中2~3 h,待烘箱温度降到室温时称量滤纸和沉淀的质量。
溶液中硫化钠计算公式如下:
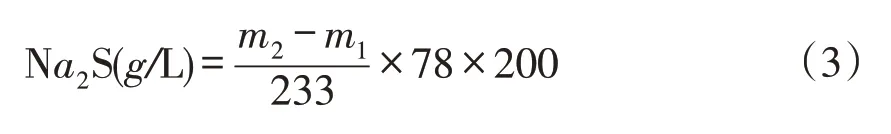
式中:m1为经烘干后硫酸钡和滤纸的质量;m2为滤纸过滤前经烘干的质量。
为了比较3种方法的分析精度,配制含有已知浓度分析纯Na2S的化铣液,其中:NaOH 180 g/L;三乙醇胺(TEA)45 g/L;Na2S(分析纯)10~30 g/L;Al3+30 g/L。
3 结果与讨论
表1是3种分析方法对不同Na2S浓度的分析结果。从表1可以看出,碘量法分析的相对误差随Na2S浓度的增加而减小,在Na2S浓度为10.03 g/L时,相对误差达61.03%,而当Na2S浓度为30.00g/L时,相对误差为1.28%,说明碘量法在Na2S浓度高时比较准确;重铬酸钾法的分析相对误差稳定在20%左右。因此,对于化铣槽液中浓度不断变化的Na2S,这两种分析方法的误差比较大。此外,用硫代硫酸钠滴定剩余的碘时,溶液的pH会影响滴定结果,pH对碘量法、重铬酸钾法分析结果的影响见图1。Na2S理论浓度为20.00 g/L,NaOH 180 g/L,TEA 45 g/L,Al3+20 g/L,RH101 0.3 g/L。
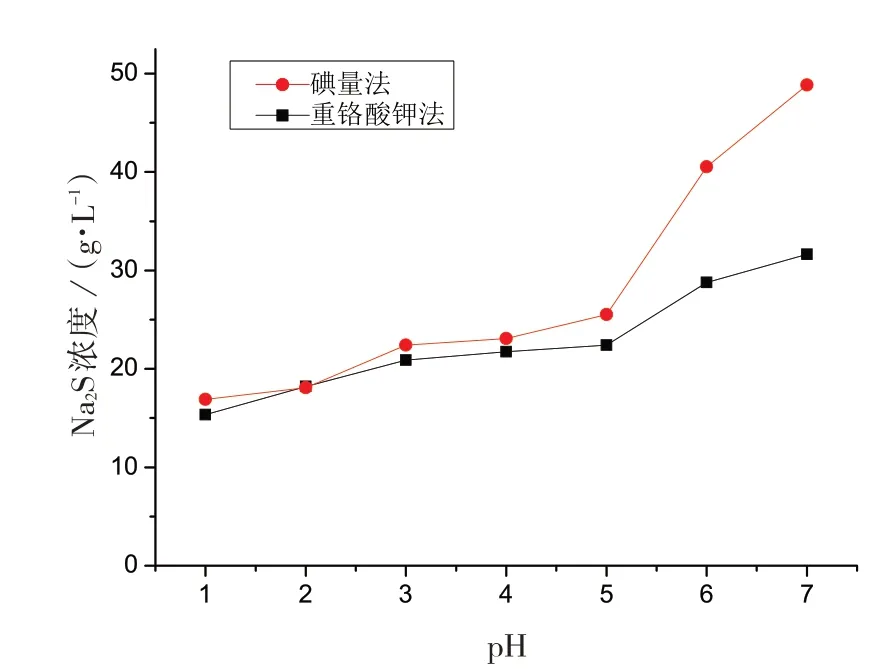
图1 pH对碘量法、重铬酸钾法分析结果的影响
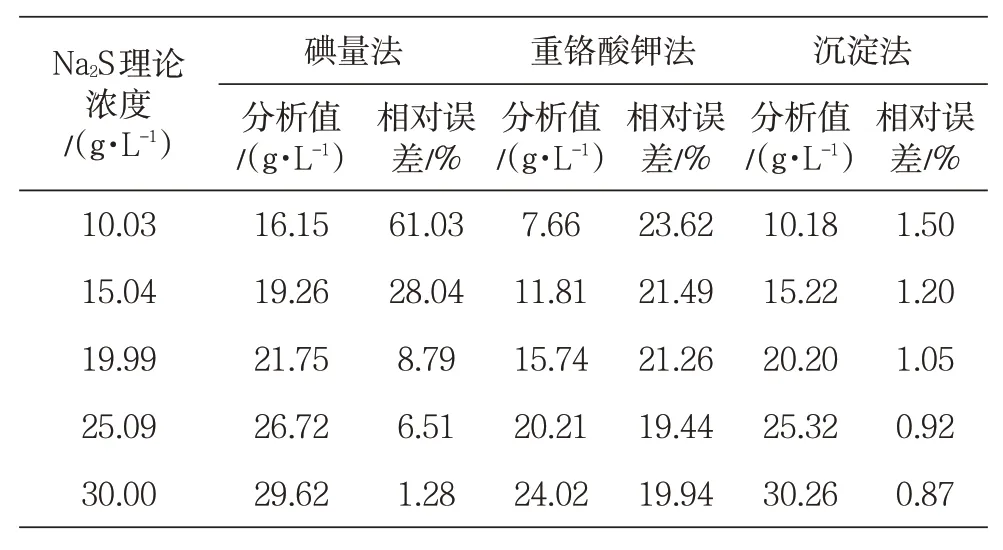
表1 三种分析方法对不同Na2S浓度的分析结果
从图1可以看出,滴定时的pH会影响碘量法和重铬酸钾的分析结果,碘量法和重铬酸钾法的分析误差随pH的增大而增加。这2种分析方法在pH为3~5时较稳定,二者的相对误差分别为8.42%和18.32%。
基本反应如下:
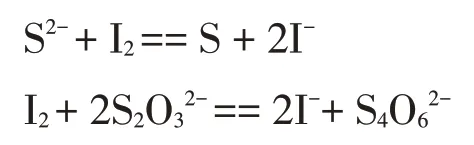
强酸性溶液中进行如下反应:

强碱性溶液中反应为:
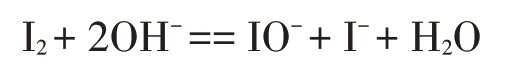
从以上反应可以看出,在强酸性条件下,溶液中的S2-与H+反应生成H2S气体而消耗,因而实际分析浓度比理论浓度小。在强碱性条件下,I2与OH-反应消耗I2,在计算时是以S2-消耗I2的方式计算的,因而实际分析值比理论值大。从表1可以看出,在Na2S浓度范围为10.03~30.00 g/L的槽液中,沉淀法的相对误差小于1.5%。
沉淀法是测定化铣槽液中S元素的含量,不受槽液中其它成分的影响,当然化铣槽液中的其它成分不含硫元素。沉淀法的分析误差随槽液中Na2S浓度的升高而略微降低。
4 结论
(1)在碘量法、重铬酸钾法、沉淀法这3种分析方法中,前二者的分析误差较大,分别为8.42%和18.32%,沉淀法分析精度最高,相对误差小于1.5%。
(2)3种分析方法的分析误差受Na2S浓度的影响,碘量法和沉淀法的分析误差随Na2S浓度的升高而降低,重铬酸钾法则相反。
(3)碘量法和重铬酸钾法的分析误差受滴定时的pH影响,在pH为3~5时较稳定。
(4)为了准确分析化铣槽液中Na2S含量,精确指导Na2S的添加,推荐使用沉淀法。

