UPLC-QqQ/MS法检测阿胶强骨口服液阿胶及杂皮源成分
陈伟 范文玺 王晓敏 马芹

基金项目:
十四五重大科技专项“阿胶强骨口服液”等特色大品种培育及中药民族药新药创制研究(2022A03107-2);第二师铁门关市中青年科技创新领军人才(2020RCTD03)。
作者简介:
陈伟(1986—),男,汉族,硕士,高级工程师,研究方向为药物药理。E-mail:285239579@qq.com
通信作者:
马芹(1974—),女,汉族,硕士,正高级工程师,研究方向为中药民族药。E-mail: 468020596@qq.com
【摘 要】
目的:建立阿胶强骨口服液中阿胶及掺杂皮源成分的专属性检测方法。方法:用序列分析用胰蛋白酶对阿胶强骨口服液及掺入不同杂皮胶的伪品中胶类成分进行酶解,采用超高效液相色谱-三重四极杆质谱(UPLC-QqQ/MS),选择阿胶特征分子离子峰m/z 539.8→612.4及牛皮源特征肽A特征离子对m/z 641.3→726.2作为检测离子对,离子化模式为ESI+,进行多反应监测。同时,建立阿胶强骨口服液中马皮胶成分红外谱检测法,结合质谱法鉴别掺伪马皮胶样品。结果:3批购买的阿胶强骨口服液保留时间均与阿胶对照药材一致,在7.7 min出峰,未出现与牛皮胶溶液对应的牛皮特征色谱峰。6批掺入不同杂皮胶(牛皮胶、猪皮胶和马皮胶)中2批马皮胶自制口服液检测出阿胶对照特征峰;2批牛皮胶口服液样品检测出牛皮源特征峰。红外光谱结果显示马皮胶自制口服液在1400~1700 cm-1处吸收峰较特异,可与其它胶质进行区别,補充阿胶强骨口服液对马皮源成分的鉴别。结论:该检测方法专属性强,可用于阿胶强骨口服液中阿胶及杂皮源成分的检测,为阿胶强骨口服液质量标准提升提供了新的思路和方法。
【关键词】
阿胶强骨口服液;超高效液相色谱-三重四级杆质谱;红外光谱;阿胶
【中图分类号】R284.1 【文献标志码】 A 【文章编号】1007-8517(2023)24-0028-05
DOI:10.3969/j.issn.1007-8517.2023.24.zgmzmjyyzz202324006
UPLC-QqQ-MS/MS Analysis of Donkey-hide Gelatin and Different Animal Skin Gelatin in Ejiao Qianggu Oral Liquid
CHEN Wei1 FAN Wenxi1 WANG Xiaomin1 MA Qin1*
1. Xinjiang Hua Shidan Pharmaceutical Reaearch CO. LT,Urumqi 830011, China;
2. Key Laboratory of Bone Health Traditional Chinese Medicine Research and
Development in Xinjiang Production and Construction Corps,Urumqi 830011, China
Abstract:
Objective To establish an exclusive analytical method to identify donkey-hide gelatin and other source gelatin in Ejiao Qianggu Oral Liquid. Methods Identification of donkey-hide gelatin and others source gelatin in Ejiao Qianggu Oral Liquid was performed by the Multiple Reaction Monitoring of rapid resolution liquid chromatography (UPLC) coupled to triple quadruple mass spectrometry (QqQ), and quantitative ion pair of 539.8 → 612.4 (m/z, Da), 641.3 →762.2 (m/z, Da) were respective used for the detection of the cow skin origin and Ejiao control ingredients. Further, the horse hide glue and donkey-hide gelatin was distinguished by FT- IR. Results Characteristic molecular peaks of donkey-hide gelatin were detected in the three batches of commercially available Ejiao Qianggu Oral Liquid samples, of which three batches of cowhide source were not detected. Meanwhile, two batches of characteristic peaks of horse-hide gelatin were detected in six batches of homemade oral liquid samples and two batch contained elements of cowhide source, either component of donkey-hide gelatin was not detected in the six batches. It must be added, the IR absorption peaks in 400~1700 cm-1 of horse hide glue was more specific than others gelatin, that compensate for the identification of horse-hide gelatin. Conclusion Methodological verification shows that the established method is specific, and suitable for the identification of donkey-hide gelatin and others source in Ejiao Qianggu Oral Liquid. This research has provided theoretical support for the optimizing of Ejiao identification methods, and quality evaluation.
Keywords:
Ejiao Qianggu Oral Liquid;UPLC-QqQ-MS/MS;IR;Donkey-hide Gelatin
阿胶强骨口服液是治疗原发性骨质疏松症的复方制剂,由熟地黄、黄芪、党参、枸杞、阿胶、牡蛎等6味药材组成,是国家3类新药。目前本品种标准收载于新药转正标准第76册,尚未包含原料阿胶的含量检测方法[1]。随着阿胶价格逐年走高,原料阿胶掺伪造假的情况也不断增多,多以牛皮胶、猪皮胶和马皮胶等伪造阿胶产品进行售卖,杂皮胶入药将严重影响药物治疗效果,延误患者的治疗效果,降低民众对中药信赖。为了保证药品的质量及提高检测的专属性,国家药品监管部门连续颁布了一系列胶类原料和制剂的检测方法[2-3],补充了牛皮特征肽A作为检测牛皮胶掺假的指标,但是对马皮胶和猪皮胶的检测尚未给出指导方法。为保证阿胶强骨口服液药品质量,本研究参照相关文献采用超高效液相色谱-三重四级杆质谱(UPLC-QqQ/MS)联合红外光谱同时对药物进行牛皮源成分特征肽A和阿胶特征多肽[4-5]检测,检测效率更高,专属性的和适用性较强。
1 仪器与材料
1.1 仪器 Waters ACQUITY UPLC超高效液相色谱仪- TQ-D三重四级杆质谱系统(沃特世科技(上海)有限公司);傅里叶变换红外光谱仪(美国PerkinElmer公司);电子分析天平(CPA225D,赛多利斯科学仪器有限公司);紫外可见分光光度计(UV-2600,岛津仪器有限公司);台式高速离心机(TGL-16M,上海卢湘仪离心机仪器有限公司);Waters ACQUITY UPLCBEH C18(2.1mm×100mm,1.7μm)。
1.2 材料 阿胶强骨口服液(批号19010801、19100601、19011001,新疆华世丹药业股份有限公司);猪皮胶强骨口服液自制品(实验室自制190212和190214);牛皮胶强骨口服液自制品(实验室自制190227和190228);马皮胶(实验室自制 190302和190304);序列分析用胰蛋白酶(美国Promega);阿胶对照品(批号:121274-201703,中国食品药品检定研究院);牛皮特征肽A(批号:111941-201804,中国食品药品检定研究院);Milli-Q纯水;碳酸氢铵(分析纯,上海国药集团)。
2 实验方法与结果
2.1 超高效液相质谱
2.1.1 样品的前处理 取样品溶液2mL,加1%碳酸氢铵溶液50mL,超声处理30 min,用0.22 μm微孔滤膜滤过,取续滤液100μL,置微量进样瓶中,加胰蛋白酶溶液10μL(取序列分析用胰蛋白酶,加1%碳酸氢铵溶液制成每1mL中含1mg溶液,临用时配制),摇匀,37℃ 恒温酶解12 h,作为供试品溶液。
2.1.2 对照溶液的制备 取牛皮特征肽A对照品粉末5.4mg,阿胶对照药材 0.1095g,分别加1%碳酸氢铵溶液50mL,超声理(功率180 W,频率50 kHz)处理30 min,用0.22μm微孔滤膜滤过,取续滤液100μL,置微量进样瓶中,加胰蛋白酶溶液10μL,摇匀,37℃恒温酶解12 h,作为对照药材溶液。
2.1.3 陰性样品溶液制备 取处方中缺胶类药材的其他药味,制成阴性样品溶液。取阴性样品2mL,照“2.1.1”项下的方法制成阴性样品溶液。
2.1.4 液相色谱条件 采用Waters ACQUITY UPLCBEH C18(2.1mm×100mm,1.7μm)色谱柱,以0.1%甲酸水溶液为流动相A,以乙腈为流动相B,按下表进行梯度洗脱,流速为0.3mL/min。柱温为40℃,进样量为10μL。
2.1.5 质谱条件 离子化模式ESi+,进行多反应监测,选择m/z 539.8→612.4作为阿胶特征分子峰检测离子对m/z 641.3→726.2为牛皮源成分的特征离子对。毛细管电压为3.00 KV,锥孔电压为30 V,离子源温度为120℃,除溶剂温度为450℃,除溶剂气体为500L/hr,锥孔气体为50L/hr。碰撞能量为20 V,碰撞气流速为0.18mL/min[6-7]。
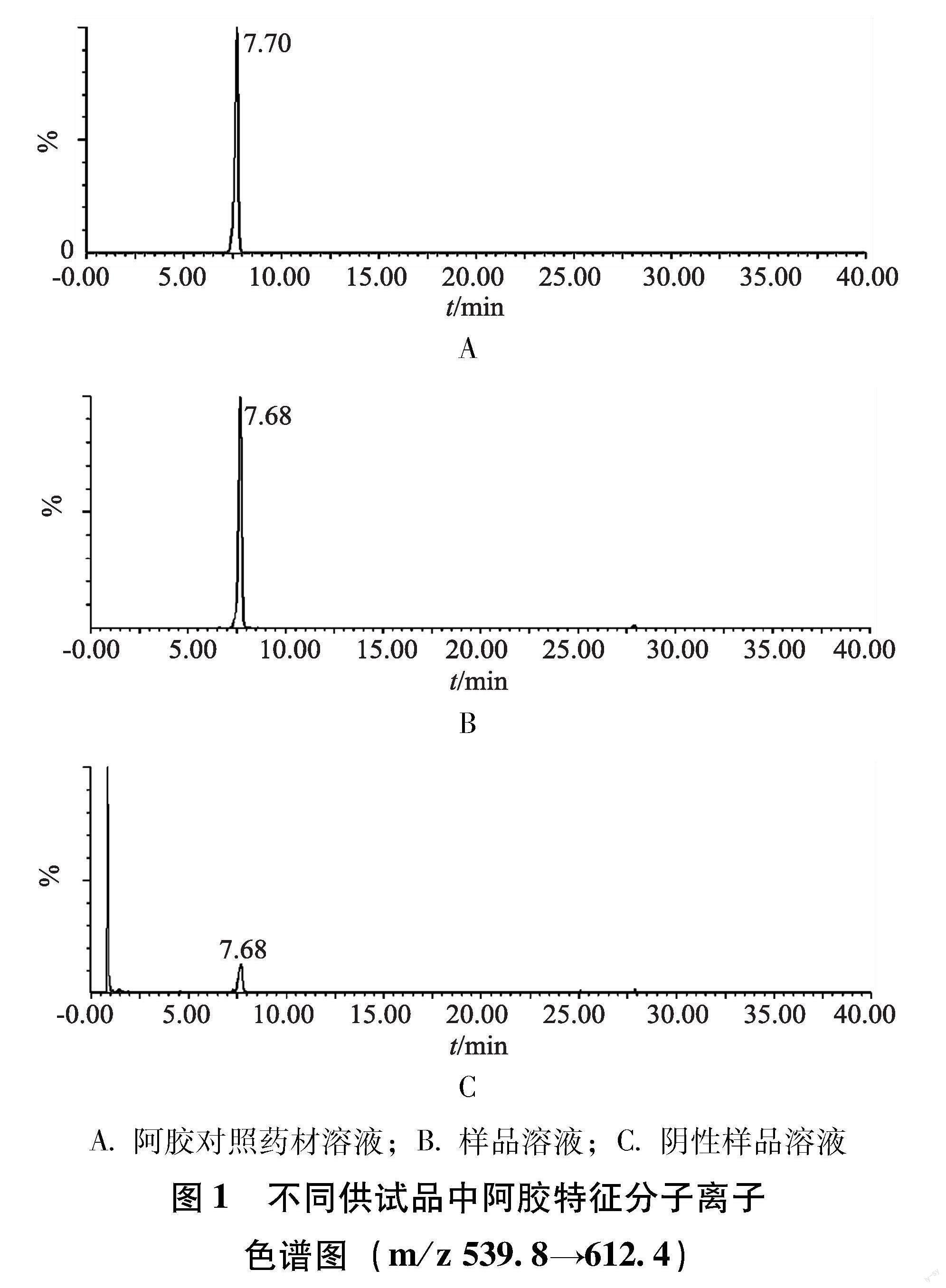
2.1.6 专属性试验 以阴性样品、阿胶对照药材、三批阿胶强骨口服液市售样品为阳性样品,选择阿胶特征分子离子峰m/z 539.8→612.4作为检测离子对进行测定。结果显示阴性样品中其它五个药味且都含有微量的阿胶特征氨基酸多肽成分,但因样品中相应离子流峰面积低于阿胶对照药材溶液相应峰面积,均视为未检出,方法专属性强。如图1所示。
2.1.6 精密度试验 取阿胶对照药材供试溶液,经样品前处理后,连续进样6针,进样量10μL,以阿胶特征分子离子峰m/z 539.8→612.4作为检测离子对进行测定,结果离子对峰面积RSD为0.83%精密度良好。
2.1.7 稳定性试验 取同一批次阿胶强骨口服液供试品(19100601)溶液,于制备后的0 h、4 h、8 h、12 h、18 h、24 h进行前处理,按照液相质谱方法进行检测,以阿胶特征分子离子峰进行测定,峰面积RSD为1.77%,RSD均小于5%,表明供试品溶液在制备后的24 h内稳定。
2.1.8 重复性试验 按“样品前处理方法制备阿胶强骨口服液供试品溶液6份,以阿胶特征分子离子对作为检测离子对进行测定,进样量10 μL,结果6份溶液峰面积RSD为2.44%,重复性良好。
2.1.9 样品检测 以所建立的方法对3批阿胶强骨口服液(19010801、19100601、19011001)进行检测,均检出阿胶特征分子离子峰(图1)。
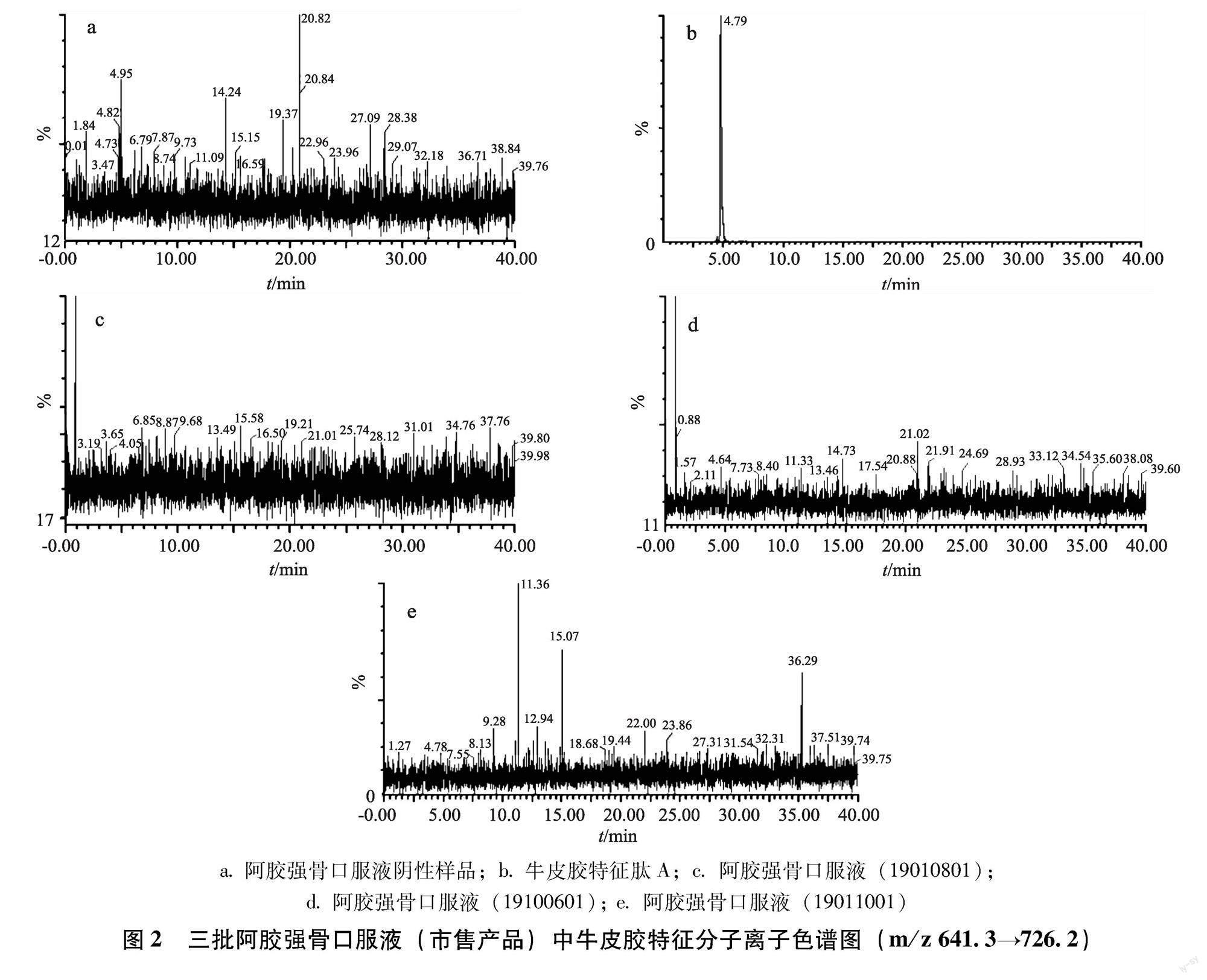
2.1.10 牛皮源成分检测 对3批购买的阿胶强骨口服液检测结果表明阿胶特征峰保留时间均与阿胶对照药材一致,在7.7~7.8 min出峰,未出现与牛皮胶特征肽A对照对应的牛皮特征色谱峰(图2)。6批掺假口服液中2批牛皮胶口服液和2批牛皮胶样品均检测出了牛皮源特征峰,未出现阿胶特征离子峰;但是,2批马皮胶自制口服液检测出阿胶对照特征峰,新建方法对马皮胶掺假检测敏感度低,需结合其它方法进行检测(图3)。
2.2 红外光谱分析 以BKr粉末3.0mg,红外光灯下研匀,并均匀放入压片磨具内,施压制片,制得均匀透明的空白片,取出后,分别精密吸取样品溶液约0.1mL,做红外指纹对比分析。设定扫描次数16次,分辨率4cm-1,取样品压片在4000~400cm-1下进行测定[8]。由红外光谱分析结果可观察到胶质氨基酸在1400~1700cm-1及3400~3600cm-1 处有显著的特征吸收峰,前者为C=O基和芳香环基团所在,后者为-NH-基团所在,图谱结果可知马皮胶口服液在两个频率范围内,吸收频率,强度及峰型均与阿胶强骨口服液有显著的差异。
3 讨论
阿胶为马科动物驴Equus asinus L.的干燥皮或鲜皮经煎煮、浓缩制成的固体胶。《本草纲目》载:“古方用者,多牛皮,后世乃贵驴皮,当以黄透如玻珀色,或光黑如漆者为真”[8]。现代药理学研究[9]表明阿胶主要含有胶原蛋白α1和α2 (64.65% )、蛋白质多肽、糖胺聚糖类物质及其它微量元素组成,具有治疗贫血,增强免疫力,抗休克,增强血管通透性,改善骨质钙代谢和抗疲劳等诸多作用。阿胶强骨口服液是以阿胶为主药的治疗骨质疏松性中成药,其阿胶质量标准研究对原料甄选,产品质量控制具有重要意义。
阿胶的鉴别方法已由传统简单的性状鉴别,发展为现代生物标记物法,DNA标签、液相色谱法等,但是这些方法均有缺点。如阿胶强骨口服液已采用高效液相法对阿胶L-脯氨酸、丙氨酸、甘氨酸等进行含量控制,但对比研究发现该方法对控制杂皮胶缺乏专属性[10]。在阿胶强骨口服液阿胶成分超高效液相色谱-三重四极杆质谱法方法建立上本试验参考了陈佳等[11]建立的方法,在前处理方法上改用序列分析用胰蛋白酶,以提高样品处理外源引入杂质;在液相方法上提高进样量为10μL,毛细管电压由4 kV调整为3 kV,锥孔电压由40 kV修改为30 kV,除溶剂气体为由600L/hr 降为500L/hr,在该条件下不同胶质峰形和强度都有所提高。从试验结果看,阿胶强骨口服液中阿胶成分的质谱检测方法对同为马科奇蹄目的马皮胶专属性不高,因此本试验补充了红外光谱法对阿胶强骨口服液掺马皮胶进行鉴别。在红外谱分析中,与以往报道[12]结果对比,本研究发现在1400~1700cm-1和3400~3600cm-1 频率范围,马皮胶口服液吸收频率,强度及峰型与阿胶强骨口服液相比均有显著的差异,此处为羰基和亚氨基伸缩震动区域,采用红外光谱技术可以有效的区别阿胶强骨口服液和伪阿胶强骨口服液[13],可推测马皮胶经裂解后的肽键分裂程度与驴皮胶完全不同。此外,阿胶在3000cm-1附近频率段出现高震现象,其中2926cm-1频率处的红外吸收峰归属于CH2 不对称伸缩振动模式,而 2855cm-1频率处的红外吸收峰则归属于 CH2对称伸缩振动模式[14]。推测为阿胶中苯丙氨酸芳环上的C—H键(σAr-H)及骨架中的(σC=C)伸缩震动引起,这可能和阿胶气味芳香强于其它胶质的原因有关。
参考文献
[1]国家食品药品监督管理局国家药品标准新药转正(中药)頒布件 [J]. 中国药品标准, 2010, 76: 68-69.
[2]国家食品药品监督管理总局.阿胶中牛皮源的补充检验方法[Z].国家食品药品监督管理局补充检验方法和检验项目批准件,编号2012001,2012.
[3] 国家食品药品监督管理总局.鹿角胶补充检验方法[Z].国家食品药品监督管理局补充检验方法和检验项目批准件,编号2014014,2014.
[4]黄飞燕,李晓君,张国昌,等.超高效液相色谱-质谱法检测妇舒丸中阿胶特征肽及牛皮源成分[J].云南化工,2022,49(7):54-57.
[5]陈佳,程显隆,魏锋,等.超高效液相色谱-三重四极杆质谱法检测复方阿胶浆中阿胶[J].药物分析杂志,2015,35(2):328-332.
[6]张静娴,胡青,董洪霜,等.超高效液相色谱-三重四级杆质谱法用于阿胶糕类食品中阿胶的鉴别及马、牛、羊、猪皮源成分的检测[J].世界中医药,2019,14(4):828-832.
[7]国家药典委员会.中华人民共和国药典(一部) [S].北京:中国医药科技出版社.2020:197.
[8]李时珍.本草纲目(下) [M].北京:人民卫生出版社,1982,兽部:319.
[9]郭中坤,王可洲,籍国霞,等. 阿胶的成分、鉴别方法及药理作用研究进展[J]. 辽宁中医药大学学报,2015,17(4):71-74.
[10]林晓伊,李亘,王冯宇,等.阿胶及其制品质量检测方法研究进展[J].食品与机械,2021,37(7):207-212.
[11]程丽,汪婷,武嘉林.HPLC法同时测定阿胶强骨口服液中4种氨基酸[J].中成药,2017,39(3):636-639.
[12]许长华,周群,孙素琴,等. 二维相关红外光谱法与阿胶的真伪鉴别[J]. 分析化学, 2005,33(2):221-224.
[13]陈丽云,甄璐静,纪硕,等.东阿阿胶红外光谱研究[J].山东化工,2019,48(4):75-78.
[14]LI W L, HAN H F, ZHANG L, et al. Manufacturer identification and storage time determination of “Donge Ejiao” using near infrared spectroscopy and chemometrics[J]. J Zhejiang Univ Sci B. 2016,17(5):382-390.
(收稿日期:2023-03-23 编辑:刘 斌)

