碳热法制备生物炭负载纳米零价铁材料去除对氯苯胺*
徐玉明,袁向娟,孙 磊,夏东升,2
(1 武汉纺织大学环境工程学院,湖北 武汉 430200;2 武汉纺织大学,纺织印染清洁生产教育部工程中心,湖北 武汉 430200)
对氯苯胺(PCA)是一种重要的有机中间体和化工原料,被广泛用于农药和染料的生产和医药制药等过程中[1-2],所以在工业废水和土壤中广泛存在。PCA的氯苯和苯胺结构使其具有较高的毒性,且容易被皮肤吸入并在生物体内累积,影响人体免疫和内分泌系统,具有致畸、致癌、致突变作用[3-4],因此PCA的去除受到了广泛的关注。
生物质炭可以作为一种较为理想的吸附材料吸附环境中的污染物,但是大多数原始生物质炭对污染物吸附选择性较差及吸附量有限[5]。nZVI具有较大的比表面积和较多的反应活性位点,能有效去除水中的氯代有机物,实现脱卤效果[6-7],但是存在易发生团聚和易被氧化的问题,将nZVI负载在生物质炭上不仅可以提高铁的分散性和稳定性,而且可以制得具有较高吸附性和还原性的Fe/Cx复合材料。在nZVI的制备方法中,高温碳热法可以将Fe(II)或Fe(III)还原为零价铁,制备成本低、操作简便,且在制备过程中不会生成有害的副产物。Qiu[8]将花生壳和Fe2O3按一定比例混合后在400 ℃下热解生成以Fe2O3、Fe3O4、FeO和Fe0为主的铁物种,用于偶氮染料AO7的吸附和降解,去除率可达到92%;Li等[9]将玉米秸秆粉末和FeCl3·6H2O混合浸渍后,通过一步碳热法合成了nZVI/BC复合材料去除水中的Cr(VI),反应过程中nZVI发生了氧化,Cr(VI)被还原为Cr(III);Ma[10]通过K2FeO4和竹粉共热解制备了具有较高孔隙结构和较大的比表面积(1 086 m2/g)的nZVI/BC,将其作为活化过硫酸盐降解抗生素的有效催化剂,反应10 min后可以将磺胺嘧啶完全去除。
基于上述研究的可行性,本研究以花生壳生物质为碳源,Fe(NO3)3·9H2O为铁源,按一定比例混合浸渍后在高温条件下热解制备Fe/Cx复合材料,对其进行SEM、XRD、FTIR、XPS等表征分析,探讨了铁掺杂量、溶液初始浓度、pH、共存离子等对PCA吸附效果的影响以及PCA的吸附行为与机理,为水中PCA的去除提供了理论依据。
1 材料与方法
1.1 主要试剂
实验所用九水合硝酸铁(Fe(NO3)3·9H2O),PCA(≥98.5%),碳酸钠(Na2CO3)、碳酸氢钠(NaHCO3)、硫酸钠(Na2SO4),氯化钙(CaCl2),氯化镁(MgCl2),氯化钾(KCl)均为分析纯。
1.2 材料的制备
BC的制备:将花生壳原料洗净烘干,用破碎机破碎成粉末状,过100目筛后置于管式炉中热解,条件为以5 ℃/min速率升温至700 ℃,在加热开始前通入氩气30 min排出空气,热解时间为2 h。
Fe/Cx复合材料的制备:分别称取50 g Fe(NO3)3·9H2O固体和5 g BC于烧杯中,加入200 mL去离子水搅拌混合均匀,置于磁力搅拌器上搅拌过夜。分离上清液后将得到的铁炭混合物在60 ℃条件下烘干,研磨后在管式炉中热解,条件为以5 ℃/min速率升温至800 ℃,并且在加热开始前通入氩气驱气1 h,热解3 h。分别称取10 g、30 g、60 g Fe(NO3)3·9H2O固体与5 g BC混合,以相同的步骤制备不同铁掺杂量的Fe/Cx复合材料(其中x=10,30,50,60)。
1.3 表征方法
利用全自动比表面积和孔径分析仪(BET)表征材料的比表面积和孔隙结构;采用扫描电子显微镜(SEM)和透射电子显微镜(TEM)观察复合材料表面的微观形貌;采用X射线衍射仪(XRD)对复合材料的晶体结构进行表征;利用傅里叶红外光谱分析仪(FTIR)研究材料的表面官能团;X射线光电子能谱(XPS)分析材料表面元素和价态。
1.4 吸附实验方法
Fe/Cx复合材料对PCA的等温吸附实验:在150 mL锥形瓶中加入100 mL不同浓度(50,75,100,150,200 mg/L)的PCA溶液,加入75 mg Fe/C50复合材料,分别在288、298和308 K恒温水浴搅拌器中反应120 min;在不同间隔时间内取样后过0.45 μm滤膜,测定吸附后溶液中PCA的浓度。
Fe/Cx复合材料吸附PCA的动力学实验:称取75 mg Fe/C50复合材料于150 mL锥形瓶中,加入100 mL,75 mg/L的PCA溶液,在298 K温度下反应;在不同间隔时间内取样后过0.45 μm滤膜,测定吸附后溶液中PCA的浓度。
Fe/Cx复合材料对PCA的去除率(%):
(1)
吸附量(mg/g):
(2)
式中:A0、Ae分别为PCA原液和吸附平衡后的吸光度;C0、Ct分别为PCA初始和t(min)时刻的浓度,mg/L;V为PCA溶液的体积,mL;m为加入反应体系的Fe/Cx复合材料的质量,g;qt为t(min)时刻的吸附量,mg/g。
2 结果与讨论
2.1 Fe/Cx复合材料的表征

图1 BC和Fe/Cx复合材料的XRD谱图(a),红外光谱图(b),N2吸附-脱附等温线(c)和孔径分布图(d)
图1(a)所示,在2θ为22°和43°附近为炭的无定型结构特征峰[11],Fe/Cx在2θ=44.6°处明显的衍射峰为体心立方α-Fe0(110),2θ=43.3°和50.6°分别对应γ-Fe0的111和200晶面[12],2θ=35.3°和56.8°为Fe3O4的衍射峰[13-14],说明nZVI以α-Fe0和γ-Fe0的形式存在。随着铁掺杂量的增大,Fe0的衍射峰强度逐渐增大,越有利于Fe0的生成。吸附PCA后,α-Fe0和γ-Fe0的衍射射峰强度明显减弱,说明Fe0对PCA的去除发挥了重要的作用。
如图1(b)所示,在BC和Fe/Cx复合材料中,3 450 cm-1处的宽峰是由-OH的伸缩振动产生的,表明Fe/Cx复合材料有以羟基为主的含氧官能团存在;在1 627 cm-1和1 750 cm-1处为C=O的特征峰,2 920 cm-1和2 850 cm-1处的吸收峰为脂肪族中-CH2的不对称和对称拉伸,1 080 cm-1处为C-O-C或C-O的伸缩振动[15-18]。随着铁掺杂量的升高,C=O官能团数量在一定程度上有所减少,脂肪族中-CH2官能团消失,材料的芳香化程度增强,稳定性提高。
N2吸附-脱附等温线及孔径分布图如图1c、图1d所示,根据IUPAC的分类,BC及Fe/Cx复合材料均呈现出IV型吸附等温线,Fe/C50呈现较明显的吸脱附曲线滞后现象,表明材料中存在微孔和介孔结构;并且在较高压力下N2的吸附量进一步增大,说明少量大孔结构的存在[19-20]。Fe/Cx复合材料的孔径分布集中在15~20 nm,比表面积远大于BC,其中Fe/C50具有最大的比表面积(538.9 m2/g)和孔容积(0.317 2 cm3/g),能够为PCA的吸附提供更多的活性位点,展现出优良的吸附潜力。

图2 不同铁掺杂量的Fe/Cx复合材料扫描电镜图和Fe/C50的TEM图
由图2(a~d)可以看到nZVI负载在BC上,Fe3O4颗粒均匀地覆盖在BC的表面,与XRD结果相符。由EDS分析可知,随着铁掺杂量的升高,生物炭上负载的铁元素含量逐渐增多,其中Fe/C50的铁含量最多,具有较高的反应活性。由图2(e~f)可见Fe/Cx复合材料表面粗糙多孔,可以清晰地看到铁的晶格条纹,Fe0的条纹间距d(110)为0.27 nm,d(111)为0.30 nm。

表1 不同铁掺杂量Fe/Cx复合材料的EDS分析
利用XPS对吸附PCA前后的Fe/Cx复合材料进行表征,Fe/C50在吸附PCA前后均存在C 1s、O 1s和Fe 2p的特征峰。图3(a)存在283.84、285.14和288.65 eV三个特征峰,分别代表着C-C、C-O和C=O;O 1s谱图可以分为三个不同的峰,分别代表Fe-O(530.85 eV)、C-O(531.44 eV)和C=O(532.56 eV)[16,21-22]。如图3(c)所示,在710.17和725.53 eV处为Fe(III)的特征峰,712.97 eV处对应Fe(II),证明了铁氧化物的存在[23-25]。反应后Fe-O、Fe(III)和Fe(II)的峰都发生了偏移,说明Fe0参与反应后生成了铁氧化物。XPS没有检测到Fe0,可能是因为XPS对样品的探测深度小[26-27],且nZVI表面被氧化,铁的氧化物颗粒覆盖在材料的表面,与SEM分析得出的结论一致。

图3 Fe/Cx复合材料吸附PCA前后的XPS谱图
2.2 不同影响因素对PCA吸附效果的影响
由图4(a)知,Fe/Cx复合材料对PCA的去除效果远高于BC,在反应达到平衡时PCA的整体去除率从39.13%提高到98.56%。Fe/Cx复合材料比表面积较大,孔隙结构增多,为PCA提供了更多的吸附位点;随着铁负载比例的增加,PCA的去除率逐渐增大,当m(Fe/C)=50∶5(g)时去除效果最好。
如图4(b)所示,随着投加量的增加,活性位点增多,PCA的去除效果逐渐提升。投加量为1 g/L和0.75 g/L的Fe/C50均在60 min左右对PCA的去除能力达到最大,因此后续实验选定Fe/C50的投加量为75 mg。
设置PCA溶液初始浓度为50、75、100、150、200 mg/L,Fe/C50投加量为0.75 g/L,由图4(c),PCA的去除率随着溶液初始浓度的增大而逐渐降低。当PCA浓度太高时,吸附剂无法为其提供充足的活性位点,说明初始浓度是影响去除效果的因素之一。
图4(d)为初始溶液pH对Fe/C50对PCA吸附效果的影响,在强酸性条件下,生物炭上负载的铁颗粒与H+发生反应,使活性铁物种数量减少,PCA去除率下降。pH在5~11范围内对PCA的去除率均无明显影响,说明Fe/Cx复合材料具有较高的稳定性。
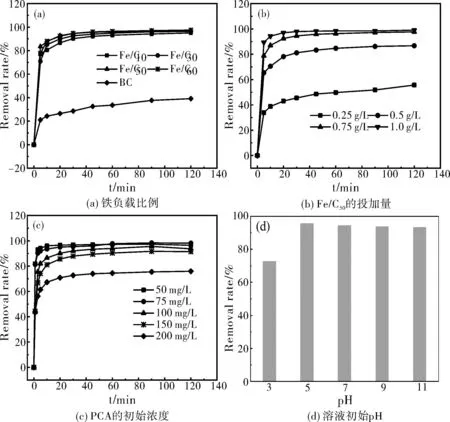
图4 不同影响因素对PCA吸附效果的影响Fig.4 Effect of different influencing factors on the adsorption effect of PCA
实验中控制溶液的离子浓度为5mM,在反应开始前称取相应质量的NaHCO3、Na2CO3、NaCl、MgCl2、CaCl2固体加入到PCA溶液中[28]。如图5(a)所示,HCO3-在一定程度上促进了PCA的吸附效果,其他离子对PCA的促进或抑制作用很微弱,其去除率始终保持在97%以上,说明Fe/Cx复合材料具有较好的抗离子干扰能力。

图5 水中共存阴、阳离子对PCA吸附效果的影响(a)和 Fe/Cx复合材料的重复使用性能(b)Fig.5 Influence of coexisting anions and cations in water on PCA adsorption(a),reusability of Fe/Cx composites(b)
当吸附达到平衡后,采用加热再生的方法将分离后的Fe/C50在管式炉中800 ℃下进行脱附,吸附到生物炭上的PCA在较高温度下挥发[29-30]。由图5(b)可以发现经高温热脱附循环两次后的Fe/C50对PCA的去除效率几乎与原材料相同,经过第三次循环实验后Fe/C50仍对PCA有较高的去除率(90.18%)。说明通过碳热还原法制备的Fe/Cx材料性能稳定,生物炭和铁物种之间的结合力强。
2.3 Fe/C50对PCA的等温吸附、动力学和热力学的研究
2.3.1 Fe/C50对PCA的等温吸附模型
采用Langmuir和Freundlich两种等温吸附模型对Fe/C50复合材料吸附PCA的实验数据进行拟合[31],在288 K、298 K、308 K下考察反应体系温度对PCA去除性能的研究,拟合结果如表2所示。

表2 Fe/C50吸附PCA的Langmuir和Freundlich模型拟合参数Table 2 Langmuir and Freundlich model fitting parameters for PCA adsorption on Fe/C50
(3)
Freundlich:qe=kF×ce1/n
(4)
式中:qe和qm分别为平衡吸附量和最大吸附量(mg·g-1);Ce为吸附平衡时溶液的浓度(mg·L-1);kL为Langmuir吸附平衡常数;kF为Freundlich吸附常数;n为吸附常数。由图6a、图6b和表2可知,Fe/C50对PCA的吸附容量显著(214.12 mg/g),且Langmuir模型的拟合相关系数R2均高于Freundlich模型,说明Fe/C50对PCA的吸附符合Langmuir模型,属于单分子层吸附[32]。
2.3.2 Fe/C50对PCA的吸附动力学模型
采用伪一级动力学模型和伪二级动力学模型研究Fe/Cx复合材料对PCA的吸附动力学,模型相关的参数如表3所示[33]:
伪一级动力学模型:
qt=qe×(1-e-k1t)
(5)
伪二级动力学模型:
(6)

表3 Fe/C50吸附PCA的吸附动力学模型拟合参数Table 3 Kinetic model fitting parameters for PCA adsorption on Fe/C50
式中:K1,K2为速率常数。伪一级和伪二级动力学模型拟合的R2值分别为0.806 2和0.991 9,表明Fe/C50对PCA的吸附更符合伪二级动力学模型,以化学吸附为主,平衡吸附容量为95.62 mg/g,与Chang等[34]研究Fe3O4/石墨烯纳米复合材料对苯胺和对氯苯胺吸附的动力学模型得出的结论一致。
2.3.3 Fe/C50对PCA的吸附热力学

ΔG0=-RTlnK0
(7)
ΔG0=ΔH0-TΔS0
(8)
(9)

表4 Fe/C50对PCA吸附的热力学参数Table 4 Thermodynamic parameters for PCA adsorption on Fe/C50
式中:R为气体常数,R=8.314 J·(mol·K)-1;K0为标准平衡常数;KL为Langmuir吸附平衡常数(L·mg-1)。如表5所示,ΔH0为负值,说明PCA在Fe/C50上的吸附为放热反应,ΔG0分别为-26.50,-25.98,-25.80 kJ/mol,ΔG0为负值表示吸附反应可以自发地进行,标准熵变ΔS0小于零表明Fe/C50对PCA的吸附过程中固液界面的自由度降低。

图6 Fe/C50吸附PCA的拟合曲线Fig.6 Fitting curves of Fe/C50 adsorption of PCA
2.4 Fe/Cx复合材料对PCA吸附机理的探讨
PCA的去除机制主要包括Fe/Cx复合材料的吸附作用和Fe0的还原作用。改性后,Fe/Cx复合材料的比表面积和孔容积都明显增大,可以通过孔隙填充和表面吸附等机制吸附PCA分子,其表面含有的-OH官能团可以与PCA分子中的N原子之间形成氢键[31,37]。此外,Fe/Cx复合材料上的含氧官能团可作为电子供体,含苯环的PCA分子可作为电子受体,可能发生π-π相互作用[31]。在800 ℃高温缺氧条件下硝酸铁很不稳定,受热分解生成Fe2O3,与具有较大比表面积的BC充分接触生成Fe0和Fe3O4,Fe3O4继续与碳反应生成Fe0,具有较强还原性的Fe0可将PCA分子还原成小分子物质而去除,具体反应方程式如(10)~式(13)所示[14,38]。
4Fe(NO3)3·9H2O=2Fe2O3+12NO2+3O2+9H2O
(10)
2Fe2O3+3C=4Fe0+3CO2
(11)
6Fe2O3+C=4Fe3O4+CO2
(12)
Fe3O4+2C=3Fe0+2CO2
(13)

图7 Fe/Cx复合材料对PCA的去除原理图Fig.7 The schematic diagram of PCA removal of Fe/Cx composites
3 结 论
本研究采用一步碳热法制备了Fe/Cx复合材料,并探究了其对PCA的吸附性能,主要结论如下:
(1)通过碳热法在生物质炭上负载了nZVI和Fe3O4颗粒,Fe/Cx复合材料的比表面积和孔容积都明显提高,经热脱附再生后仍对PCA保持较高的去除率,是一种理想的吸附材料。
(2)Fe/Cx复合材料对PCA的吸附过程以单分子层吸附为主,吸附热力学研究表明PCA的吸附过程为放热反应,且反应可以自发地进行。当铁负载比例为m(Fe/C)=50∶5(g),投加量为0.75 g/L,PCA浓度为75 mg/L时,在30min内对PCA的去除率可达到96%。
(3)PCA的去除机制主要包括Fe/Cx复合材料的吸附作用和Fe0的还原作用,Fe/Cx复合材料可以通过表面吸附-孔隙填充作用,氢键作用,π-π相互作用实现PCA的去除。

