超声分层应变技术评估糖耐量异常患者左心室收缩功能及同步性
吴婷,章春泉,龚良庚
1.南昌大学第二附属医院超声科,江西 南昌 330000;2.南昌大学第二附属医院影像中心,江西 南昌 330000;*通信作者龚良庚 gong111999@163.com
2型糖尿病是心血管不良事件的独立危险因素,常导致左心室结构和功能改变。2013年,我国约10.9%的成年人患有糖尿病,糖耐量异常患病率达35.7%[1]。糖尿病相关的心肌损害早期属于可逆性的[2],因此,早期诊断糖耐量异常患者心肌功能受损对于临床工作具有非常重要的价值。基于二维斑点追踪技术的分层应变技术可通过追踪分析心动周期中心肌散在的斑点回声,生成各层心肌的应变及同步化信息,既往研究也证实其评估左心室收缩功能的价值[3-4]。本研究拟通过分析糖耐量异常患者左心室心内膜下、中层、心外膜下及整体收缩期纵向峰值应变和同步性的变化,以早期检出糖耐量异常对心脏的损害,为临床干预提供参考依据。
1 资料与方法
1.1 研究对象 选取2019年1月—2020年12月于南昌大学第二附属医院就诊的53例糖耐量异常患者,其中3例因图像质量差、部分节段显示不满意被排除,最终纳入50例患者为糖耐量异常组,男29例,女21例,年龄30~66岁,平均(51.9±11.1)岁。选取50名年龄、性别相匹配的健康人作为对照组,男27例,女23例,年龄35~68岁,平均(51.1±12.2)岁。糖耐量异常的诊断标准[5]:空腹血糖<7.0 mmol/L,口服葡萄糖耐量试验在7.8~11.1 mmol/L。所有受试者左心室射血分数(left ventricular ejection fraction,LVEF)≥50%。排除标准:心力衰竭、心肌梗死、高血压、原发性心肌病、心脏瓣膜病、先天性心脏病、严重心律失常、肥胖(体质量指数≥30 kg/m2)、肿瘤及其他严重肝肾功能异常等全身性疾病。收集所有受检者的年龄、性别、身高、体质量、心率、空腹血糖、2 h餐后血糖。本研究经本院伦理委员会审核通过(20190305-05),所有受试者均知情同意并签署知情同意书。
1.2 仪器与方法
1.2.1 仪器 采用GE Vivid E95型超声诊断仪,配备二维探头M5S,频率2.0~5.0 MHz,帧频50~70帧/s。配备EchoPAC脱机分析软件。
1.2.2 图像采集 受试者取左侧卧位,平静呼吸,同步记录胸导联心电图,待呼吸和心律平稳时行常规超声心动图测量。于左心室长轴切面测量左心房前后径(left atrium anteroposterior diameter,LAD)、左心室舒张末期内径(left ventricular end-diastolic diameter,LVEDd)、左心室收缩末期内径(left ventricular endsystolic diameter,LVESd)、室间隔舒张末期厚度(interventricular-diastolic septal thickness,IVSd)、左心室后壁舒张末期厚度(left ventricular-diastolic posterior wall,LVPWd),计算LVEF,测量心尖四腔观二尖瓣口舒张期血流速度E值及室间隔组织多普勒数值e',计算E/e'。全部数据测量3次取平均值。分别采集连续3个心动周期的左心室心尖四腔观、三腔观及两腔观二维动态图像。
1.2.3 图像分析 将采集的图像传输到EchoPAC工作站,选择Q-analysis,点击2DStrain,依次分析左心室心尖三腔观、四腔观、两腔观图像,手动描记采集的3个切面的心内膜边界,适当调整感兴趣区宽度使其刚好覆盖左心室心肌全层,软件自动将左心室壁分为内层、中层及外层,自动生成左心室各节段收缩期纵向应变及应变曲线,当有2个及以上节段追踪不满意时,应手动调节重新分析结果。3个切面分析完成后,软件自动计算出左心室各节段心肌纵向应变达峰时间(time to peak,TTP)牛眼图、应变达峰时间离散度(peak strain dispersion,PSD)、左心室心肌整体收缩期纵向应变(global longitudinal strain,GLS)及左心室心内膜下心肌整体纵向应变(endocardial myocardial global longitudinal strain,GLSendo)、中层心肌整体纵向应变(mid-myocardial global longitudinal strain,GLSmid)、心外膜下心肌整体纵向应变(epicardial myocardial global longitudinal,GLSepi)。
1.2.4 重复性检验 用简单随机抽样法抽取20例研究对象,由2名具有分析经验的超声主治医师按照上述分析方法获取左心室应变相关参数,验证观察者之间的重复可靠性,其中1位医师于不同时间进行2次分析获取上述数据,验证观察者内的重复可靠性。
1.3 统计学方法 采用SPSS 20.0软件,所有参数均进行正态检验及方差齐性检验,符合正态分布的计量资料以±s表示,组间比较采用独立样本t检验;不符合正态分布的计量资料以M(Qr)表示,采用Wilcoxon秩和检验。用Pearson相关分析PSD与GLS的相关性。用组内相关系数(ICC)评价观察者间和观察者内多次测量的可信度。以P<0.05为差异有统计学意义。
2 结果
2.1 一般资料比较 糖耐量异常组2 h餐后血糖明显高于对照组(P<0.05)。两组性别、年龄、体质量指数、心率、空腹血糖比较,差异均无统计学意义(P>0.05),见表1。
2.2 各组常规二维超声心动图参数比较 糖耐量异常组E/e'明显高于对照组(P<0.05),LAD、LVEDd、IVSd、LVPWd、LVEF与对照组比较,差异均无统计学意义(P>0.05),见表1。
2.3 分层应变参数比较 对照组、糖耐量异常组心肌各层纵向应变绝对值逐渐降低。糖耐量异常组GLSendo、GLS绝对值低于对照组(P<0.01),GLSmid、GLSepi与对照组比较,差异无统计学意义(P>0.05),见表1、图1。

图1 左心室心内膜下、中层、心外膜下心肌纵向应变。A.男,47岁,糖耐量异常,左心室心内膜下、中层、心外膜下心肌纵向应变值分别为23.2%、20.5%、18.1%;B.男,45岁,健康对照,左心室心内膜下、中层、心外膜下心肌纵向应变值分别为28.0%、25.2%、22.6%
表1 两组一般临床资料及超声心动图参数比较(±s)

表1 两组一般临床资料及超声心动图参数比较(±s)
注:BMI为体质量指数,LAD为左心房前后径,LVEDd为左心室舒张末期内径,IVSd为室间隔舒张末期厚度,LVPWd为左心室后壁舒张末期厚度,LVEF为左心室射血分数,E/e'为二尖瓣舒张早期血流速度与室间隔瓣环舒张早期峰值速度比值,GLSendo为心内膜下心肌纵向应变,GLSmid为心内膜中层心肌纵向应变,GLSepi为心外膜下心肌纵向应变,GLS为左心室整体心肌收缩期纵向应变
项目对照组(n=50)糖耐量异常组(n=50)t值P值一般资料年龄(岁)51.1±12.2 51.9±11.1 0.881>0.05男/女(例) 27/23 29/21 0.632 >0.05 BMI(kg/m2)22.64±2.66 23.26±2.58 0.932>0.05心率(次/min) 73±5 72±6 1.016 >0.05空腹血糖(mmol/L)4.6±0.7 4.8±1.1 1.839>0.05餐后2 h血糖(mmol/L) 5.9±0.8 9.2±2.3 3.829 <0.05常规超声心动图参数LAD(mm) 32.5±2.7 33.2±3.2 0.744 >0.05 LVEDd(mm)48.1±3.2 49.1±3.3 0.653>0.05 IVSd(mm) 9.5±0.7 9.7±0.4 0.853 >0.05 LVPWd(mm)8.9±0.9 9.0±0.7 0.921>0.05 LVEF(%) 63.3±3.2 64.2±4.2 1.083 >0.05<0.05二维应变参数E/e'8.6±3.0 13.1±3.7 4.442 GLSendo(%)24.4±2.1 23.4±1.6 2.896<0.01 GLSmid(%) 22.7±1.9 22.3±1.5 1.265 >0.05 GLSepi(%)21.2±1.8 21.0±1.6 0.595>0.05 GLS(%) 24.3±2.3 22.1±1.8 5.303 <0.01
2.4 两组左心室同步性比较 糖耐量异常组在前间隔、左心室前壁、下壁、后壁基底段TTP较对照组明显延迟(P均<0.01),糖耐量异常组PSD明显高于对照组(P<0.01)。糖耐量异常组PSD与GLS绝对值呈负相关(r=-0.612,P<0.01),见表2及图2、3。

图2 左心室17节段达峰时间牛眼图。A.男,47岁,糖耐量异常,牛眼图中各节段颜色差异较大,TTP较长,PSD为42 ms;B.男,45岁,对照组,牛眼图中各节段颜色均匀一致,TTP短,PSD为21 ms
表2 两组左心室心肌17节段TTP比较(ms,±s)

表2 两组左心室心肌17节段TTP比较(ms,±s)
注:TTP为达峰时间
节段对照组糖耐量异常组t值P值基底段前间隔 346.4±20.3 360.2±26.4 2.916 0.004前壁 347.1±20.5 362.6±25.2 3.376 0.001侧壁 349.8±18.5 353.6±23.6 0.883 0.379后壁 347.0±20.2 360.6±24.9 3.003 0.003下壁 348.6±19.8 361.3±23.5 2.927 0.008间隔 350.0±18.3 354.0±23.4 0.997 0.332中间段前间隔348.6±17.4 351.7±21.2 0.804 0.423前壁347.2±18.2 352.3±22.3 1.256 0.212侧壁349.0±17.9 352.2±21.8 0.321 0.609后壁346.0±17.3 348.9±21.4 0.752 0.454下壁344.4±18.3 350.3±21.5 1.483 0.141 0.117心尖段间隔345.6±17.0 351.7±21.5 1.582前壁 339.0±16.6 342.7±17.6 1.070 0.287侧壁 334.4±14.7 337.9±17.1 1.086 0.280下壁 331.4±14.2 337.2±16.4 1.881 0.063间隔 334.0±15.0 340.0±16.4 1.903 0.060心尖帽 332.4±15.6 337.0±14.9 1.508 0.135
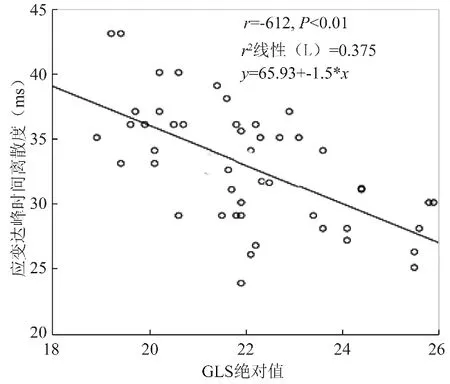
图3 糖耐量异常组左心室GLS绝对值与PSD的相关性
2.5 重复性检验 左心室GLSendo、GLSmid、GLSepi、GLS、PSD在观察者内(ICC=0.93、0.92、0.85、0.94、0.98)和观察者间(ICC=0.91、0.92、0.81、0.91、0.98)的一致性均较好,表明应变数据重复性和可信度较好。
3 讨论
糖耐量异常是处于糖尿病前期的一种病理状态,血糖升高造成的代谢紊乱可触发一系列病理变化,如心肌脂质沉积、氧化应激和炎症反应促使心脏重构、心肌纤维化,从而影响心肌的收缩功能[6-7]。有研究发现糖耐量异常患者左心室心肌质量明显高于健康人,并在妊娠期糖尿病胎儿心脏中得到证实[8-9],王一洒等[10]研究发现,糖耐量异常患者左心室心肌收缩期峰值圆周应变明显降低,因此认为在糖耐量异常时,早期的心血管病变进程已经启动。
本研究显示,正常的左心室3层心肌分层应变存在梯度变化,心内膜下心肌纵向应变最高,其次为中层心肌,心外膜下心肌最低,与以往研究结果一致[11]。本研究发现,糖耐量异常时左心室整体收缩期纵向应变及心内膜下心肌的纵向应变下降,与对照组有显著差异,与乔英艳等[12]研究糖尿病动物模型左心功能演变过程相同,其原因可能是左心室心内膜下心肌主要是纵行肌纤维,对缺血、室壁应力增加等损伤最为敏感[13],微循环障碍是糖代谢异常的主要病理表现之一,血糖升高易导致冠状动脉微循环异常,冠状动脉自上而下、自外而内走行,最终在心内膜下呈毛细血管网,因此心内膜下层心肌血管网最易受累[14-15]。
心脏正常收缩运动表现为从心内膜到心外膜,从基底段到心尖段传导,室壁同步顺序收缩,从而保持各节段心肌应变TTP一致完成左心室一次正常有效做功,如果TTP不一致将导致左心室无效做功或做功相互抵消,PSD是基于二维斑点追踪技术衍生出来的一个新参数,是指左心室17节段心肌纵向应变TTP的标准差,PSD低反映各节段同步性好,应变TTP比较一致[16-17]。本研究表明,糖耐量异常患者左心室收缩同步性异常,基底段的心肌最先受到影响,原因可能是心肌细胞代谢异常,心肌纤维化使心肌的兴奋-收缩偶联机制失调,导致左心室收缩不同步,左心室基底段收缩力高于中间段和心尖段,心肌对氧和能量的需求较大,因此最先受到影响。本研究中糖耐量异常组PSD与整体纵向应变绝对值呈负相关,整体纵向应变绝对值越低,PSD越大,同步性越差,表明随着血糖水平升高,左心室机械-电传导逐渐变差,心肌收缩功能受损加重。
总之,当糖耐量异常患者常规超声心动图LVEF正常时,仍可能存在心肌收缩功能障碍。以往的超声技术均侧重评估左心室整体和局部功能,分层应变技术能够对心内膜下、中层以及心外膜下心肌应变逐层分析,加深对与糖代谢相关心肌损害的病理生理机制的认识,并早期发现糖耐量异常患者轻微的左心室收缩功能减低,分层应变技术还可以定量评价左心室收缩不同步运动,为临床早期诊断、早期干预提供客观依据,具有临床推广应用价值。

