中学化学课堂教学的新思路
——小组协作在高三化学复习中的作用
沙 静
(江苏省如皋市第一中学 江苏 如皋 226500)
一、设计思考
新课程背景下高效课堂教学的要求应运而生,而各种新课堂教学模式也不断推陈出新。 课堂改革的核心环节是课程实施,而课程实施的基本途径是课堂教学。 进入高三一轮复习阶段后, 知识点学生往往已经了解,缺乏去探究新知识的好奇心,课堂容易缺少生机。 基于这样的考虑,笔者通过氧化还原反应专题复习(1) “活动单导学”小组协作模式的教学来改善这种状况。 在教学设计中设计者要根据学习要求设计出可操作性的 “活动单”,根据问题的不同,“活动单”可以由单个人或者协作小组来完成。 不论是哪一种情况,设计都是动态的、创造的过程,大大激发了学生积极参与的热情。 每次展示活动满分计10 分,抢答活动计5 分。 每堂课由课代表记录课堂记录单,记录各小组的表现得分(附表1)。记录单每两周左右总结一次。 记录的不仅是分数,还要有典型、客观、真实的实例,便于展示,便于表扬与批评。 学期将结束时,老师对每个学生进行期末终结性评价。 不仅是素质报告单上的分数,还有对学生的文字评价,一并记入学生的成长记录袋。
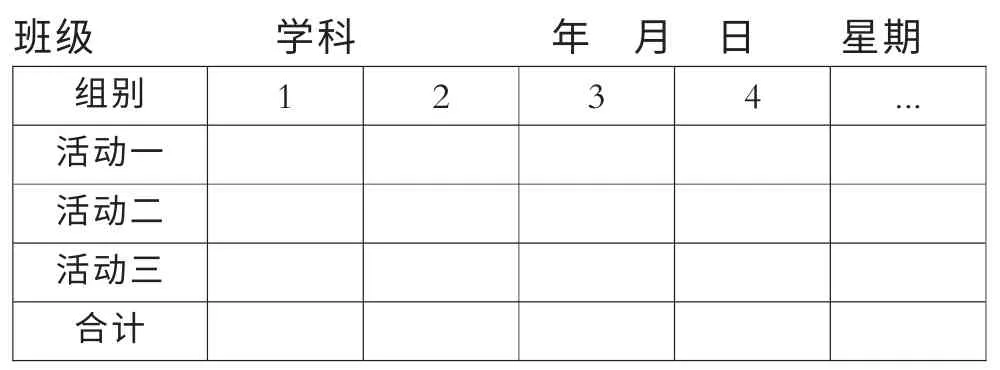
课堂记录单(附表1)
每周小组内评价每个成员的全面表现,由组长组织填写学习小组记录单(附表2)。由小组内成员进行自评、互评。 自评和互评的结合,有助于小组内部进行反思,有利于各小组内成员相互取长补短,不断改进和提高。
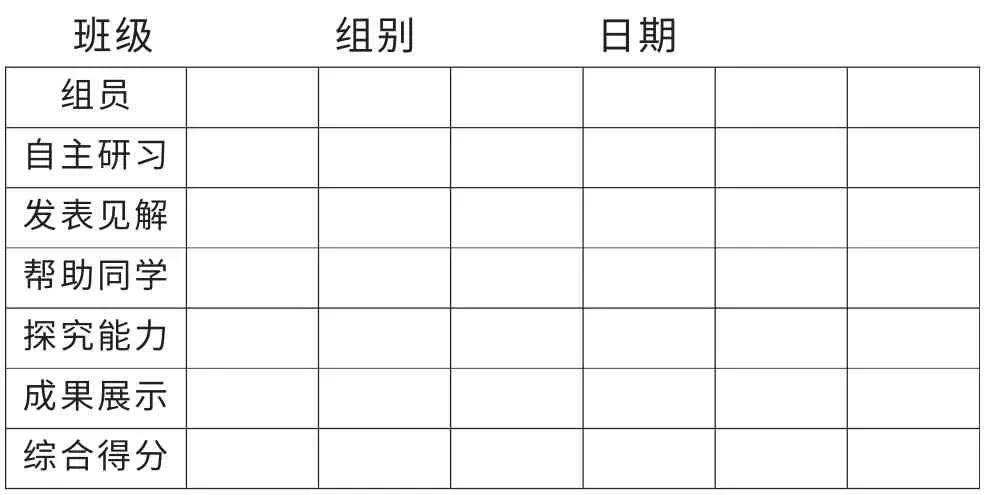
学习小组记录单(附表2)
二、活动目标
1.知道氧化还原反应的本质是电子的转移,理解物质被氧化、被还原的概念。
2.能判断氧化剂、还原剂、氧化产物、还原产物,并通过化合价变化规律, 判断某些陌生氧化还原反应的产物。
3.能用单线桥、双线桥表示电子转移的方向和数目。
4.通过小组协作增强学生合作的意识,通过小组间相互纠错培养学生严谨求实的科学作风。
三、活动过程
活动一 氧化还原反应的本质: 判断下列反应是否为氧化还原反应(请在后面的括号中用“■”或“×”表示)。 若为氧化还原反应,任选一个指出氧化剂、还原剂、氧化产物、还原产物,并用单线桥或双线桥标出电子转移的方向和数目。
(1)Cu2S+O2=2Cu+SO2( )
(2)Fe3O4+8HCl=FeCl2+2FeCl3+4H2O( )
(3)2NO2+Na2CO3=NaNO2+NaNO3+CO2↑( )
(4)CaH2+2H2O=Ca(OH)2+2H2↑( )
通过上述分析, 你认为氧化还原反应的本质是什么? 判断氧化还原反应的最佳判据是什么?
自主研习,小组展示(略):每班有8~10 个学习小组,一半为展示组,一半为评价组,两组依次轮换,相互之间为互助组。每次展示活动两组共计20 分。评价组对展示组的展示成果进行评价, 若发现展示组的错误,则展示组所扣分加到评价组上。 通过这样的激励,每组的各位同学都非常积极的思考并纠错。 活动结束后,教师对共性问题进行点评。
教师:回忆所学元素化合物知识,将常见氧化剂、还原剂按下列标准进行分类。
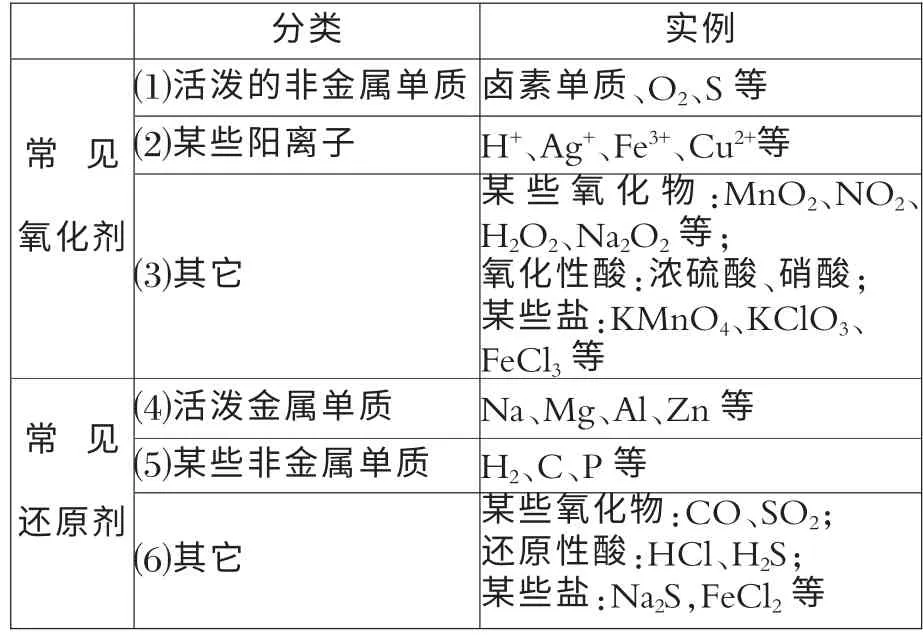
?
根据上表分析,氧化剂、还原剂中所含元素化合价有什么特征?
自主研习,学生抢答(略):每次抢答,满分5 分,记入小组总积分,同时也作为该同学的个人表现得分。 其他同学可对该同学评价或纠错并适当给分。
活动二 物质氧化性、 还原性强弱比较: 物质氧化性、还原性强弱的实质是物质得失电子的难易。 请对有关物质氧化性、还原性的强弱进行判断(用“>”、“<”表示或连接),并分别归纳出你判断的依据。
⑴还原性:Mg___Fe、Ag___Cu。 氧化性:Cu2+___Fe2+、H+___Zn2+。 依据_____________________判断。
⑵①还原性:Mg___Ba、Al___K。 氧化性:Na+___H+。
②氧化性:F2___O2、Cl2___I2。 还原性:Cl-___Br-。
依据____________判断。
⑶已知下列反应:2FeCl3+2KI=2FeCl2+2KCl+I22FeCl2+Cl2=2FeCl3I2+SO2+2H2O=H2SO4+2HI
判 断Fe2+、I-、Cl-、SO2还 原 能 力 由 强 到 弱 的 顺序:____________,依据____________判断。
自主研习,小组合作,展示时由互助组选择对应组任意同学进行展示。 为使本组加分,互助组之间通常都会选择学习滞后生展示,同时为保证展示加分,展示组各成员也都不会懈怠,保证每个成员都不掉队,并不断加强他们的集体意识。
(4)根据电解池中电极放电顺序判断
①比较通常条件的下列物质的还原性强弱。 (在阳极发生氧化反应的顺序)Cl-、SO42-、OH-、Pt、Cu
②比较通常条件下的下列物质的氧化性强弱。 (在阴极发生还原反应的顺序)H+、Cu2+、Zn2+、Na+
从①②可总结出一般规律:_______________。
③已知:用铂做阳极、石墨做阴极电解硫酸和硫酸铵的混合溶液得到过二硫酸铵[(NH4)2S2O8]和氢气。 试比较在该条件下SO42-与OH-还原性的强弱。
④工业上在铁制品上镀锌,采用锌作阳极,镀件作阴极,电解质溶液中含有锌离子。 试比较在该条件下H+与Zn2+氧化性强弱。
从③④可知, 物质氧化性、 还原性强弱还与_________有关。
自主研习,小组合作,本活动留给本节课积分后三名的小组展示:略。其他同学评价得分。对滞后组进行激励。
四、教学反思
学生学习知识的目的不只是为了储存知识,而是应用知识来解决实际问题。 其实,用的过程,也是学的继续。 通过“用”使学生学得更具体、更深刻、更有效。 新课程化学教材的宗旨在于引导学生运用实验探究、调查访问、查阅资料、交流讨论等方式,进一步学习化学科学的基础知识、基本技能和研究方法,更深刻地了解化学与人类生活、科学技术进步和社会发展的关系,以提高化学科学素养,为具有不同潜能和特长的学生未来的发展打下良好基础。 应用“活动单导学”小组协作模式,并通过各种活动方式,启发学生的思维,增加互动,充分发挥学生的自主作用,让学生在自主研习、相互质疑和评价中得到提升和完善。 充分发挥小组作用必须建立一套有效的、长期的评价机制并贯穿于整个学习过程。 积极倡导评价目标多元化和评价方式的多样化,坚持终结性评价与过程性评价相结合、 定性评价与定量评价相结合、学生自评互评与他人评价相结合,努力将评价贯穿于化学学习的全过程。 活动表现评价的对象可以是个人或团体,评价的内容既包括学生的活动过程又包括学生的活动结果,从而让评价的功能发挥最大的催化效率,真正实现高效课堂的理念。
[1] 中华人民共和国教育部. 普通高中化学课程标准 (实验)[M].北京:人民教育出版社,2003.
[2] 缪建新.高效课堂:模式与案例.化学[C].南京:南京大学出版社,2009.12
[3] 丁非.“活动单导学”模式下的课堂筹划与设计[M].天津:新蕾出版社,2009.11
[4] 吴书林.名师面对面[Z].广州:羊城晚报出版社,2008.2

