注射用羟基红花黄色素A对大鼠脑神经元线粒体的保护作用研究
徐 露,董 志(重庆医科大学重庆市生化与分子药理重点实验室,重庆 400016)
注射用羟基红花黄色素A对大鼠脑神经元线粒体的保护作用研究
徐 露*,董 志(重庆医科大学重庆市生化与分子药理重点实验室,重庆 400016)
目的:研究注射用羟基红花黄色素A对大鼠脑神经元线粒体的保护作用。方法:采用线栓法复制大鼠脑缺血再灌注模型,实验分为假手术(等容生理盐水)、模型(等容生理盐水)、尼莫地平(1.0mg·kg-1)和羟基红花黄色素A高、中、低剂量(10.24、5.12、2.56mg·kg-1)组。尾iv给药,每天1次,连续3 d。测定大鼠血清中血小板活化因子(PAF)含量、脑海马组织Na+-K+-ATP酶、Ca2+-ATP酶和Mg2+-ATP酶活性;观察电镜下灰质部位神经元线粒体超微结构。结果:与模型组比较,羟基红花黄色素A高、中、低剂量组大鼠血清中PAF的含量显著降低,海马组织Na+-K+-ATP酶、Ca2+-ATP酶和Mg2+-ATP酶含量显著提高(P<0.01);神经元线粒体结构较完整,线粒体的破坏明显比模型组轻。结论:注射用羟基红花黄色素A具有明显的脑线粒体保护作用。
羟基红花黄色素A;线粒体;血小板活化因子
红花是我国传统的活血化瘀良药,主要有效成分是羟基红花黄色素A(Hydroxysafflor yellow A,HSYA),其不仅是一种药物,也是一种食品和染料。羟基红花黄色素A只能通过静脉给药,在临床上治疗各种缺血性心脑血管疾病,效果良好,但作用机制不甚明确。本文拟将注射用羟基红花黄色素A的神经保护作用机制做一个初步分析,旨在为临床应用提供理论依据。
1 仪器与材料
1.1 仪器
Hitachi-7500透射电镜(日本日立公司);722型分光光度计(中国科技研究院)。
1.2 试药
注射用羟基红花黄色素A(浙江永宁药业股份有限公司,批号:20100305,含量:每瓶含量为85%);尼莫地平注射液(天津药业集团新郑股份有限公司,批号:20100118);三磷酸腺苷(ATP)酶试剂盒(南京建成生物工程研究所);血小板活化因子(PAF)Elisa试剂盒(武汉中美科技有限公司,批号:20100319)。
1.3 动物
清洁级SD大鼠,♀♂兼用,体重200~250 g,由重庆医科大学实验动物中心提供(动物使用合格证号:SCXK(渝)20020001)。
2 方法
2.1 复制模型
采用线栓法复制大脑中动脉闭塞(MCAO)模型。10%水合氯醛,按1m L·100 g-1ip麻醉大鼠。颈部正中切口,分离右颈总动脉与颈内、颈外动脉。在距颈动脉分叉5mm处,双线结扎颈外动脉,颈内动脉穿线备用,结扎右颈总动脉的近心端。在靠近动脉分叉的颈总动脉壁上剪一小口,插入一直径为0.2mm的尼龙线(尼龙线头端用石蜡薄薄地包裹),经颈内动脉进入大脑中动脉起始部,以阻断大脑中动脉的血流。插入线长约16mm时,有明显阻力感。结扎颈内动脉与尼龙线,防止插线脱落。假手术组除不插入尼龙线外其他手术步骤同手术组。缺血30m in后,缓慢拔出栓子约10mm,剪断线栓外露部分,扎紧活结,使血流恢复成再灌注状态。
2.2 分组与给药
将60只大鼠随机分为6组,即假手术(等容量生理盐水)、模型(等容量生理盐水)、尼莫地平(1.0mg·kg-1)和羟基红花黄色素A高、中、低剂量(10.24、5.12、2.56mg·kg-1)组。各组均于缺血再灌注后2 h尾iv给药,每天1次,连续3 d。
2.3 PAF含量检测
手术前大鼠颈动脉取血0.5m L,最后一次给药后12 h,大鼠眼眶取血0.5m L,室温放置1 h后取血清,严格按照试剂盒步骤检测PAF含量水平。
2.4 ATP酶含量检测
将海马组织制成10%的匀浆,2 000 r·m in-1离心10m in,取上清液,1 000 r·min-1离心15min,沉淀物即为线粒体。用Low ry法进行蛋白定量,经检测证实制备的线粒体纯度较高。将分离的线粒体用冰冷的匀浆介质制成混悬液,超声波粉碎法破碎线粒体,测定Na+-K+-ATP酶、Ca2+-ATP酶和Mg2+-ATP酶含量。
2.5 电镜样品的制备
将各组大鼠用4%的戊二醛心脏灌流固定,快速取出缺血侧大脑皮层,切成1mm3小块,置于4%的戊二醛电镜液中固定,按照电镜样品制备程序漂洗、脱水、浸透与环氧树脂包埋,超薄切片后,将切片捞至铜网上,干燥后进行铅铀双染。透射电镜下观察网孔中细胞形态及其超微结构的改变并摄片。
2.6 统计学方法
3 结果
3.1 PAF含量检测结果
与假手术组比较,模型组大鼠血清中PAF含量显著升高(P<0.01);与模型组比较,羟基红花黄色素A高、中、低剂量组大鼠血清中PAF含量显著降低(P<0.01或P<0.05)。PAF含量检测结果见表1。
表1 PAF含量检测结果(±s,n=10)Tab 1 Resultsof content determ ination of PAF(±s,n=10)
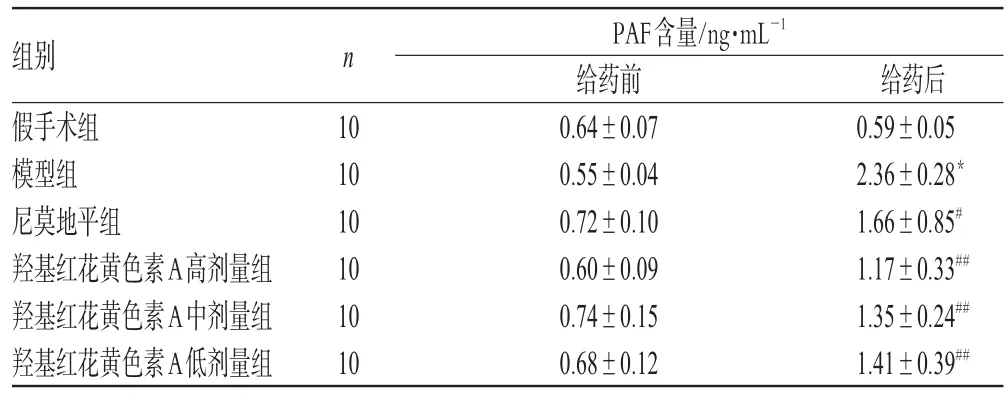
表1 PAF含量检测结果(±s,n=10)Tab 1 Resultsof content determ ination of PAF(±s,n=10)
与假手术组比较:*P<0.01;与模型组比较:#P<0.05,##P<0.01vs.sham operation group:*P<0.01;vs.model group:#P<0.05,##P<0.01
给药后0.59±0.05 2.36±0.28*1.66±0.85# 1.17±0.33## 1.35±0.24## 1.41±0.39## n组别假手术组模型组尼莫地平组羟基红花黄色素A高剂量组羟基红花黄色素A中剂量组羟基红花黄色素A低剂量组10 10 10 10 10 10 PAF含量/ng·mL-1给药前0.64±0.07 0.55±0.04 0.72±0.10 0.60±0.09 0.74±0.15 0.68±0.12
3.2 ATP酶活力比较
与假手术组比较,模型组大鼠海马线粒体的Na+-K+-ATP酶、Ca2+-ATP酶和Mg2+-ATP酶活性显著减弱(P<0.01);与模型组比较,羟基红花黄色素A高、中、低剂量组大鼠海马线粒体的Na+-K+-ATP酶、Ca2+-ATP酶和Mg2+-ATP酶活性显著增强(P<0.01)。ATP酶活力检测结果见表2。
表2 ATP酶活力检测结果(±s,n=10)Tab 2 Resultsof theactivity of ATPenzyme(±s,n=10)
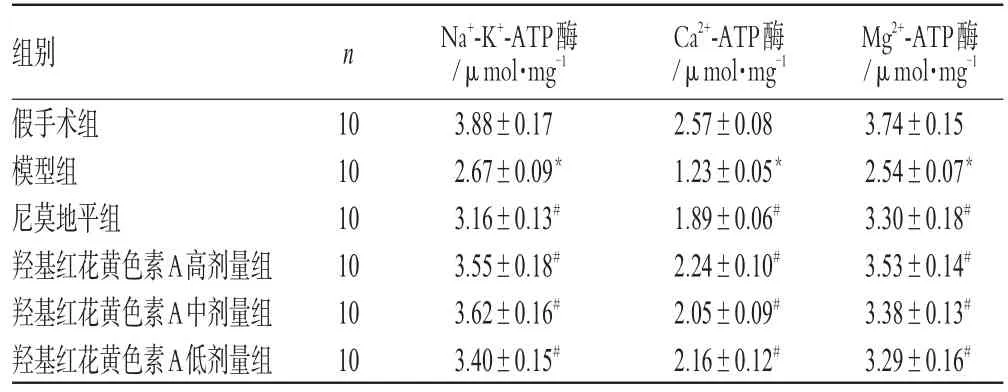
表2 ATP酶活力检测结果(±s,n=10)Tab 2 Resultsof theactivity of ATPenzyme(±s,n=10)
与假手术组比较:*P<0.01;与模型组比较:#P<0.01vs.sham operation group:*P<0.01;vs.modelgroup:#P<0.01
组别假手术组模型组尼莫地平组羟基红花黄色素A高剂量组羟基红花黄色素A中剂量组羟基红花黄色素A低剂量组Mg2+-ATP酶/μmol·mg-1 3.74±0.15 2.54±0.07*3.30±0.18# 3.53±0.14# 3.38±0.13# 3.29±0.16# n 10 10 10 10 10 10 Na+-K+-ATP酶/μmol·mg-1 3.88±0.17 2.67±0.09*3.16±0.13# 3.55±0.18# 3.62±0.16# 3.40±0.15# Ca2+-ATP酶/μmol·mg-1 2.57±0.08 1.23±0.05*1.89±0.06# 2.24±0.10# 2.05±0.09# 2.16±0.12#
3.3 电镜观察结果
假手术组可见正常的杆状线粒体,椭圆形,结构完整,形态均匀,分布有序,嵴丰富;模型组可见神经元坏死,线粒体数量减少,明显肿胀、空泡化,嵴排列不规则甚至断裂;羟基红花黄色素A高、中、低剂量组线粒体损伤较模型组明显减轻,线粒体结构较为清晰,肿胀或变形较不明显,基质中无空泡,内膜较为完整。电镜观察结果见图1。
4 讨论
PAF是一种炎症因子,许多炎性细胞如肥大细胞、碱性粒细胞、中性粒细胞与血小板等均可合成和释放PAF。目前,国内、外已经有大量文献报道,在各种缺血性心脑血管疾病、哮喘、溃疡等患者当中,血清PAF含量较正常人有显著升高,尤其在疾病发生的急性期,PAF含量升高最快。本研究发现,与模型组比较,高、中、低剂量注射用羟基红花黄色素A均能降低MCAO模型大鼠手术后血清PAF含量,提示其具有一定的抗炎作用[1,2]。

图1 电镜观察结果(20 000×)A.假手术组;B.模型组;C.尼莫地平组;D.羟基红花黄色素A高剂量组;E.羟基红花黄色素A中剂量组;F.羟基红花黄色素A低剂量组Fig 1 resultsof electronm icroscope(20 000×)A.sham operation group;B.model group;C.nimodipine group;D. HSYA high-dose group;E.HSYA medium-dose group;F.HSYA low-dosegroup
ATP酶存在于组织细胞与细胞器膜上,是生物膜上的蛋白酶,在物质运输、能量转换以及信息传递方面具有重要作用。机体在缺氧与一些疾病状态下,此酶活力会发生一系列改变,膜上各种离子泵(Na+-K+-ATP酶、Ca2+-ATP酶和Mg2+-ATP酶)的泵功能失调,细胞内、外离子失衡,造成细胞内Na+、Ca2+大量聚集,细胞水肿,甚至死亡。注射用羟基红花黄色素A能够显著提高海马区域的线粒体ATP酶含量,改善线粒体ATP酶活性,保障能量代谢的顺利进行,从而减轻神经元的损伤。从线粒体的超微结构上来看,羟基红花黄色素A可改善MCAO模型大鼠脑组织线粒体的超微结构,可能与线粒体ATP酶活性的提高从而更好地维持细胞结构有关[3,4]。
综上所述,注射用羟基红花黄色素A能够有效减少MCAO模型大鼠的炎症因子PAF含量水平,减轻炎症,提高线粒体ATP酶活性,维持正常的线粒体结构,从而达到神经保护效果。
[1] Jiang X,ShiE,Nakajima Y,etal.Posteonditioning,aseries of brief intem iptions of early reperfusion,prevents neurologic injury after spinal cord ischem ia[J].Ann Surg,2006,244(1):145.
[2] Blecharz-Klin K,Piechal A,Joniec I,et al.Pharmacological and biochem ical effects ofGinkgo bilobaextract on learning,memory consolidation and motor activity in old rats[J].Acta Neurobiol Exp(Wars),2009,69(2):217.
[3] Nishida Y,Ito S,OhtsukiS,etal.Depletion of vitamin E increases abeta accumulation by decreasing its clearances from brain and blood in amousemodel of A lzheimer disease[J].JBiolChem,2009,284(48):33 400.
[4] 赵淑敏,刘 胜,杨宏光,等.黄芩叶总黄酮预处理对缺血再灌注心肌脂质过氧化损伤的保护作用[J].解剖学杂志,2006,29(4):450.
Protective Effect of HSYA Freeze-dried Powder on Brain Neuronal M itochondria of Rats
XU Lu,DONG Zhi(Chongqing Key Laboratory of Biochem istry and Molecular Pharmacology,Chongqing Medical University,Chongqing 400016,China)
OBJECTIVE:To study the protective effect of HSYA freeze-dried powder on brain neuronalmitochondria of rats. METHODS:Cerebral ischemia-reperfusion modelwas induced by suturemethod.Model rats were divided into 5 groups,i.e.sham operation group(constant volume normal saline),model group(constant volume normal saline),nimodipine group(1.0mg·kg-1),HSYA high-dose,medium-dose and low-dose groups(10.24 mg·kg-1,5.12 mg·kg-1,2.56 mg·kg-1).They were given relevant drugs intravenously via tail once a day for consecutive 3 days.The content of PAF in serum and the activity of Na+-K+-ATP enzyme,Ca2+-ATP enzyme and Mg2+-ATP enzyeme in hippocampus were all determined.We observed ultrastructure of mitochondrial in gray area w ith electron m icroscope.RESULTS:Compared w ith model group,the content of PAF in serum of HSYA high-dose,medium-dose and low-dose groups could decrease significantly,and the activity of Na+-K+-ATP enzyme,Ca2+-ATP enzyme and Mg2+-ATP enzyme in hippocampus could increase significantly(P<0.01).M itochondrial structure wasmore complete and mitochondrial damaging in HSYA groups was slighter than that in model group.CONCLUSION:HSYA freeze-dried powder has a significant protective effect on brain m itochondria.
HSYA;M itochondria;PAF
R285.5;R97
A
1001-0408(2012)23-2127-03
DOI 10.6039/j.issn.1001-0408.2012.23.06
*助理研究员,硕士。研究方向:新药研发。E-mail:xulu62@163. com
2011-06-19
2011-10-28)

