蔗糖与浓硫酸反应实验的改进及反应产物的定性检测
何婧+乔金锁+刘延华
摘要:人教版高中化学教材中,浓硫酸与蔗糖反应实验存在不足之处,反应过程有污染室内环境的有毒气体排出及无法检验蔗糖炭化后的产物。为改进该演示实验,进行了实验探究。把该实验设计在相对封闭的体系中进行,并可对实验中产生的有毒气体及水蒸气进行定性检测。结果表明,该反应产物有C、CO、CO2、SO2和水蒸气,且产物炭经洗涤、干燥与研磨后,可作为还原CuO的原料,也可用于吸附气体或有色溶液中的色素。
关键词:浓硫酸与蔗糖反应;实验改进;产物检测;实验探究
文章编号:1005–6629(2017)6–0060–03 中图分类号:G633.8 文献标识码:B
1 问题的提出
浓硫酸与蔗糖反应是现行高中化学教材中的一个演示实验。按照人教版教材上的做法:在200mL的烧杯中放入20g蔗糖,加入几滴水,搅拌均匀,然后再加入15mL质量分数为98%的浓硫酸,迅速搅拌,观察实验现象。实验时,很容易出现教材中所描述的现象:蔗糖逐渐变黑,体积膨胀,变成疏松多孔的海绵状的炭,并放出有刺激性气味的气体。但该实验是一个开放体系,蔗糖与浓硫酸反应过程中会产生有毒的二氧化硫与一氧化碳气体,污染室内环境,危害师生健康,不利于培养学生的环保意识,也无法检验蔗糖炭化后的产物,不适合作为课堂演示实验。为此,近年来一些化学教师对该实验进行了改进。改进主要集中在三个方面:一是针对实验中产生的SO2气体污染问题,用NaOH溶液吸收[1],或把该实验设计在一个封闭体系内达到减少或消除污染的目的[2]。二是认为该实验中仅产生CO2和SO2的混合气体,于是用NaOH吸收SO2和CO2,用KMnO4溶液和品红溶液验证SO2,用澄清石灰水验证CO2[3,4]。三是认为该实验中不仅产生CO2、SO2,还会产生CO,并用尾气点燃法(或还原CuO),验证并除去CO。事实上,把CO直接点燃烧掉,存在巨大的爆炸隐患;用气球收集CO后,若处理不当又会造成二次污染;用CO还原CuO,需要加热,浪费能源、增加成本。因此,以上处理CO尾气的方法都是不可取的。我们从有利于化学教学、节约环保、知识的整体性角度出发,把浓硫酸与蔗糖反应实验设计在相对封闭的体系中进行,同时对实验中产生的有毒气体及水蒸气进行定性检测,取得了较好的效果。
2 实验用品
仪器与材料:分液漏斗、10mL注射器、100mL烧杯、30×200mm试管、20×150mm试管、18×140mm玻璃管、玻璃棒、胶塞、胶管、玻璃弯曲导管、镊子、棉花、凡士林
试剂:蔗糖、浓硫酸、品红、0.03%酸性高锰酸钾溶液、无水硫酸铜、澄清石灰水、2%硝酸银、2%氨水、氢氧化钠溶液
3 实验装置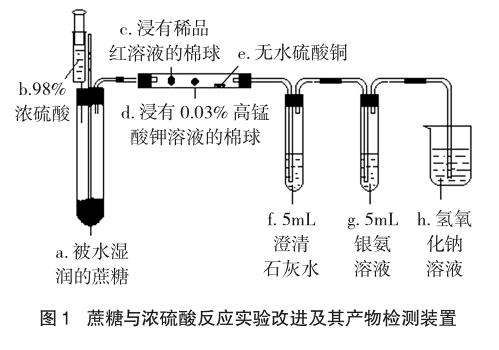
实验装置见图1。该实验装置可以把浓硫酸与蔗糖反应相对封闭在30×200mm试管中进行。该装置所用试管直径不能小于30mm,否则试管中所留空间不够10g蔗糖与水混合物和浓硫酸反应所产生的黑色物质体积膨胀所占用,使实验失败。插玻璃棒的孔的直径应稍大于玻璃棒的直径,以利于搅拌和玻璃棒上升,如果太紧,可用圆锉加工一下。在胶塞扎注射器针头的适当位置,用锥子或铁钉扎一个孔,便于注射器吸上浓硫酸后能顺利插入胶塞中。
当注射器中的硫酸注入蔗糖中后,可以明显地观察到反应混合物发生由白色→黄色→褐色→黑色的变化,同时可看到黑色物质体积膨胀推动玻璃棒缓缓上升,反应产生的气体使c、d、e、f、g等部位发生明显变化。该装置需要蔗糖与浓硫酸的量仅是教材实验装置的一半。用该装置实验产生的有毒气体经与各物质反应,并经氢氧化钠溶液吸收后已减少了许多(从h中玻璃管口气泡冒出的速度较慢可以看出),显著降低了对环境的污染。
4 实验步骤及现象
依据文献“‘半定量法制‘黑面包实验浅探”[6]采用30×200mm规格试管,药品最佳用量:10g蔗糖、7.5mL浓硫酸、30滴水。
实验步骤如下:
(1)检查装置的气密性。按照图1组装好仪器,把30×200mm试管的底部放置在热水中,观察烧杯中玻璃管口是否有气泡冒出。保证装置有良好的气密性。
(2)在30×200mm试管中加入10g蔗糖,用滴管向蔗糖中加入30滴水,用玻璃棒搅拌均匀,并用玻璃棒把蔗糖与水的混合物表面整平。
(3)用10mL注射器吸入7.5mL浓硫酸,把注射器针头插入胶塞中,用胶塞塞紧试管口。把玻璃棒插入胶塞上的孔中,用凡士林密封玻璃棒所在孔处,防止漏气。
(4)把注射器中的7.5mL硫酸全部注入蔗糖中,然后用玻璃棒搅拌,使蔗糖与水的混合物充分与浓硫酸接触,观察并记录发生的现象。
现象:注入浓硫酸后,混合物由白色→黄色→褐色→黑色,而后黑色物质体积膨胀推动玻璃棒上升(由原来2.5cm上升至13.5~14cm);c中红色逐渐褪去;d的浅紫红色褪去;e由白色变为蓝色;f中稍有白色浑浊产生(说明产物中CO2较少);g中有大量黑色沉淀产生(说明产物中CO量较多); h中的玻璃管口有气泡冒出,但溶液没有明显变化;用手小心触摸30×200mm试管,有烫的感觉(说明实验放出大量的热)。
5 实验说明与注意事项
(1)该实验系统中不能有漏气的地方。该实验装置如果不漏气,可在几分钟内顺利完成。如有漏气的地方必须用凡士林密封,不然,实验难以做成功。
(2)用该装置进行实验,蔗糖不能少于8~10g。若蔗糖量过少会使得c、d、e、f、g等处发生的变化不够明显;但蔗糖量若多于10g,则注入浓硫酸后,混合物形成的黑色物质体积膨胀会冲开胶塞,甚至胀裂试管(即试管中所留空间不够黑色物质体积膨胀所占用)。
(3)反应混合物由白色变为褐色再变为黑色,是缘于浓硫酸的脱水性。

(11)产物炭的利用。实验完成后,取出炭放在烧杯中,用自来水冲洗干净炭中残留的浓硫酸,放在铁质平底盘上压碎、干燥,即制得炭。把该“炭”研磨后,做还原CuO的实验,反应速度快,实验成功率高,效果好[8]。也可作为活性炭用于吸附气体或有色溶液中的色素。
(12)该实验中加水是使浓硫酸与水作用放出大量热,提高反应混合物温度,加快脱水炭化反应速率,并为后续碳与浓硫酸、CO2的反应及水的汽化提供热量。
参考文献:
[1]靳建华,朱楠.利用手持技术探究“黑面包实验”[J].化学教学,2014,(8):64~66.
[2]张桂芹.黑面包创新实验[J].中学化学教学参考,2014,(3):59.
[3]劉子越.浓硫酸脱水性实验的研究与改进[J].考试周刊,2016,(35):141.
[4]曾华,唐元会.浓硫酸的脱水性——“黑面包”实验的改进[J].中学化学教学参考,2016,(6):22.
[5]冀向飞.浅谈浓硫酸与蔗糖反应实验中忽视的问题及实验改进[J].中国校外教育上旬刊,2012,(10):53.
[6]张霞.“半定量法”制“黑面包”实验浅探[J].化学教与学,2014,(12):91~92.
[7]北京师范大学,华中师范大学,南京师范大学.无机化学(下)(第4版)[M].北京:高等教育出版社,2003:564.
[8]张玉敏,李海建.用新“黑面包”的产物还原氧化铜的实验研究[J].教学仪器与实验,2006,22(8):28~29.

